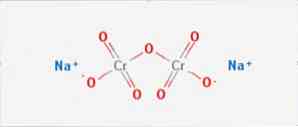
Дихромат натрия
| Дихромат натрия | |
 | |
 | |
| Общие | |
|---|---|
| Традиционные названия | динатриевая соль дихромовой кислоты, динатрий дихромат(VI) |
| Химическая формула | Na2Cr2O7 |
| Физические свойства | |
| Состояние (ст. усл.) | красные до оранжевых гигроскопичные кристаллы |
| Молярная масса | (ангидрид) 261.968 г/моль |
(дигидрат) около 100 °C
Дихрома́т на́трия (бихромат натрия, натриевый хромпик) — неорганическое химическое соединение, натриевая соль дихромовой кислоты. Существует дигидрат дихромата натрия( Na2Cr2O7·2H2O) и безводная соль.
Полупродукт в производстве хрома, практически вся хромовая руда перерабатывается в дихромат натрия.
Содержание
Свойства
Химические
С точки зрения реакционной способности и внешнего вида дихромат натрия и дихромат калия очень похожи. Соль натрия, однако, в двадцать раз лучше растворяется в воде, чем соль калия (49 г/л при 0 °C) и ее эквивалентная масса также меньше — поэтому она является наиболее часто используемым веществом.
Схожестью хромовой кислоты и дихромата натрия является их общее свойство — они являются окислителями. По отношению к калийной соли, основным преимуществом бихромата натрия является его большая растворимость в воде и в полярных растворителях, например таких как уксусная кислота.
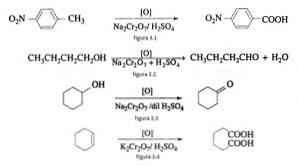
В области органического синтеза это соединение окисляет бензилы и аллильную группу C—H соединений до карбонильных производных. Так, например, 2,4,6-тринитротолуол окисляется до соответствующих карбоновых солей. Кроме того, 2,3-диметинаптален (англ. 2,3-dimethylnaphthalene ) окисляется в присутствии Na2Cr2O7 до 2,3-напталендикарбоксилиновой кислоты (англ. 2,3-naphthalenedicarboxylic acid ).
Получение
Дихромат натрия образуется в больших масштабах из руд содержащих оксид хрома(III).
Сначала руду сплавляют, как правило, с карбонатом натрия при температуре около 1000 °C в присутствии воздуха (источник кислорода):
Использование
Используют при дублении кож и в электрических элементах.
Опасность применения
Как и все соединения шестивалентного хрома, дихромат натрия считается опасным. Кроме того, он известный канцероген. Вещество очень токсично для водных организмов, может вызвать долговременные изменения в водной экосистеме.
См. также
Ссылки
Полезное
Смотреть что такое «Дихромат натрия» в других словарях:
Дихромат аммония — Дихромат аммония … Википедия
Дихромат лития — Общие Систематическое наименование Дихромат лития Традиционные названия Бихромат лития; хромовокислый литий Химическая формула Li2Cr2O7 Физические свойства … Википедия
Дихромат рубидия — Общие Систематическое наименование Дихромат рубидия Традиционные названия Бихромат рубидия; двухромовокислый рубидий Химическая формула Rb2Cr2O7 Физические свойства … Википедия
Дихромат калия — У этого термина существуют и другие значения, см. хромпик. Дихромат калия … Википедия
Натрия фосфаты — Известны следующие фосфаты натрия: Дигидрофосфат натрия NaH2PO4 Гидрофосфат натрия Na2HPO4 Ортофосфат натрия Na3PO4 Применение Употребляются для буферных растворов различного назначения, как эмульгаторы в пищевой промышленности … Википедия
натрия дихромат — natrio dichromatas statusas T sritis chemija formulė Na₂Cr₂O₇ atitikmenys: angl. sodium dichromate rus. натрий двухромовокислый; натрия бихромат; натрия дихромат ryšiai: sinonimas – dinatrio μ okso( )heksaoksodichromatas … Chemijos terminų aiškinamasis žodynas
натрия бихромат — natrio dichromatas statusas T sritis chemija formulė Na₂Cr₂O₇ atitikmenys: angl. sodium dichromate rus. натрий двухромовокислый; натрия бихромат; натрия дихромат ryšiai: sinonimas – dinatrio μ okso( )heksaoksodichromatas … Chemijos terminų aiškinamasis žodynas
НАТРИЯ ХРОМАТ — Na2CrO4, желтые кристаллы; до 423 °С устойчива орторомбич. модификация ( а =0,717 нм, b= =0,924 нм, с= 0,588 нм, z =4, пространств. группа Pnmb), выше 423°С гексагональная; DH перехода 9,62 кДж/моль; т. пл. 794°С; плотн. 2,72 г/см 3;… … Химическая энциклопедия
Гексагидроксохромат (III) натрия — Общие Систематическое наименование Гексагидроксохромат (III) натрия Традиционные названия Гексагидроксохромит (III) натрия Химическая формула Na3[Сr(OH)6] Физические свойства … Википедия
Хромат натрия — Хромат натрия … Википедия
Натрий двухромовокислый — основное сырье для производства хрома
Натрий двухромовокислый — неорганическое соединение, 
Получают бихромат натрия обработкой природного сырья — руды, содержащей окись хрома (III). В процессе производства руду сплавляют с карбонатом натрия, а потом полученное соединение хрома очищают от примесей, содержавшихся в руде. Следующий этап — окисление до соединения хрома (VI) с помощью водного раствора серной кислоты или двуокиси углерода.
Свойства
С точки зрения химии — сильный окислитель. Химические свойства сходны со свойствами калиевого хромпика, но натриевый хромпик гораздо лучше растворяется в воде. Взаимодействует с толуолом и его производными, со многими углеводородами.
 |  |  |
| Костюм «Л-1» с хранением | Натрий двухромовокислый (бихромат натрия) | Перчатки «Неотоп» химостойкие (Ansell) (9,5-10) |
Меры предосторожности
Как и все производные хрома (VI), натрий двухромовокислый очень ядовит как для людей, так и для окружающей среды. Обладает канцерогенным действием, мутаген, влияет на функцию воспроизводства. Особенно опасен для беременных, так как может нанести вред будущему ребенку. Пожаро- и взрывоопасен. Относится к 1-му классу опасности для человека. Вдыхание или проглатывание пыли или аэрозолей вещества вызывают тяжелые отравления, поражение органов дыхания и пищеварения, кожи. Воздействие на кожу или слизистые глаз может привести к химическим ожогам и плохо заживающим язвам.
Пострадавшего от контакта с бихроматом натрия следует вынести на свежий воздух, промыть место поражения, переодеть и тепло укрыть. Дать пить много воды или молока. Вызвать скорую помощь. Вызвать рвоту. Потом дать смесь из молока и яиц, жженую магнезию или активированный уголь.
На производствах, имеющих дело с натриевым хромпиком, следует предоставить работникам средства защиты от токсичной пыли или капель раствора (спецодежда, маслобензостойкие перчатки, защитные очки, противопылевые и противоаэрозольные респираторы/маски). К работе с веществом разрешается допускать только после прохождения инструктажа. Само рабочее помещение должно быть оборудовано принудительной вентиляцией, места пыления — местной вентиляцией; оборудование следует загерметизировать, пыль необходимо регулярно убирать.
Остатки реактива и тару из-под него утилизируют по правилам для опасных отходов. Требуется исключить его попадание в окружающую среду. Очистке должны подвергаться сточные воды и воздух, содержащий пыль и аэрозоли.
Хранят дихромат натрия в прохладных, сухих помещениях, отдельно от горючих материалов и сильных окислителей, вдали от источников тепла, открытого огня, потенциальных источников искр. Емкости для хранения (стальные барабаны, многослойные мешки) должны закрываться герметично.
Применение
• Сырье в химпроме для производства хрома и его производных. Большая часть добываемой хромовой руды перерабатывается в бихромат натрия, так как он является промежуточным продуктом между стадией хромовой руды и чистым хромом.
• Для изготовления минеральных пигментов, катализаторов, пассивирующих составов, антифризов для двигателей.
• В кожевенном деле для дубления кож и мехов.
• В текстильпроме для протравы тканей перед окраской.
• При изготовлении деталей электрических устройств.
• Входит в состав средств для защиты древесины от микроорганизмов и паразитов.
• Для очистки реактивов, ацетилена.
Дихромат натрия свойства, производство, опасности и применение
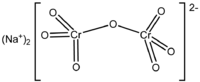
дихромат натрия неорганическое соединение формулы Na2Cr2O7. Это одно из многих соединений шестивалентного хрома (Cr VI). Его структура проиллюстрирована на рисунке 1, хотя обычно соль обрабатывается в дигидратированной форме, формула которой будет Na2Cr2O7 · H2O.
Он имеет две ионные связи между молекулами натрия и отрицательно заряженными атомами кислорода. Хромированная руда извлекается из дихромата натрия. Миллионы килограммов бихромата натрия производятся ежегодно.
Китай является крупнейшим производителем дихромата натрия, однако китайские химические заводы имеют относительно низкое производство, менее 50 000 тонн в год, по сравнению с казахстанским заводом, который производит более 100 000 тонн в год..
Заводы в России, Соединенных Штатах и Великобритании имеют промежуточное производство от 50 000 до 100 000 тонн в год (Kogel, 2006)..
С точки зрения реакционной способности и внешнего вида дихромат натрия обладает свойствами, аналогичными дихромату калия, однако натриевая соль более растворима в воде и имеет весовой эквивалент, меньший, чем у калиевой соли..
При нагревании дихромат натрия образует токсичные пары хрома. Это сильный окислитель и очень агрессивный.
Это соединение можно найти в источниках питьевой воды, загрязненных различными промышленными процессами, такими как гальванизация или гальваника, кожевенное дубление и текстильное производство..
Физико-химические свойства
Дихромат натрия состоит из кристаллов с красно-оранжевой моноклинной структурой в их безводной форме и без запаха. Его молекулярная масса составляет 261,97 г / моль в безводной форме и 298,00 г / моль в его дигидратированной форме..
Он имеет температуру плавления 356,7 градусов по Цельсию, температуру кипения 400 градусов по Цельсию, при которой он разлагается. Он имеет плотность 2,52 г / мл..
Рисунок 2 показывает появление дихромата натрия. Его растворимость в воде составляет 187 г на 100 г при 25 градусах Цельсия, а его растворимость в этаноле составляет 513,2 г / литр при 19,4 градусах Цельсия (Национальный центр биотехнологической информации, s.f.).
Он считается стабильным соединением, если хранится в рекомендуемых условиях, и не воспламеняется. Поскольку это сильный окислитель, он вызывает коррозию, а в растворе это кислота, обладающая способностью снижать рН до 4 в растворе 1% мас. / Об..
Методы производства
Хромат натрия может быть преобразован в дихромат с помощью непрерывного процесса, который обрабатывает серной кислотой, диоксидом углерода или комбинацией этих двух.
Испарение раствора бихромата натрия вызывает осаждение сульфата натрия и / или бикарбоната натрия, и эти соединения удаляются перед окончательной кристаллизацией дихромата натрия..
Дихромат натрия можно сделать в три этапа:
Безводный дихромат натрия можно приготовить путем плавления дигидрата дигидрата натрия, кристаллизации водных растворов дихромата при температуре выше 86 ° C или сушки растворов дихромата натрия в распылительных сушилках..
Растворы дихромата натрия в количестве 69 и 70% мас. / Об. Используются в качестве удобного и экономически эффективного способа отправки количеств, избегая необходимости ручной обработки или растворения кристаллов..
Реактивность и опасности
Это сильный окислитель. Несовместимо с сильными кислотами. Контакт с горючими материалами может привести к пожару. Токсичные пары оксида хрома могут образовываться в присутствии тепла или огня.
Известная «смесь хромовой кислоты» дихромата и серной кислоты с органическими остатками вызывает бурную экзотермическую реакцию. Эта смесь в сочетании с остатками ацетона также приводит к бурной реакции.
Сочетание дихромата и серной кислоты со спиртами, этанолом и 2-пропанолом приводит к бурной экзотермической реакции. В связи со многими инцидентами, связанными со смешением дихромат-серной кислоты с окисляемыми органическими материалами, вероятно, лучше избегать таких взаимодействий..
Комбинация дихромата с гидразином является взрывоопасной, можно ожидать, что реакция с дихроматом в целом будет энергичной с аминами. Добавление обезвоженной дихроматной соли к уксусному ангидриду приводит к окончательной взрывной экзотермической реакции.
Вдыхание пыли или тумана вызывает раздражение дыхательных путей, которое иногда напоминает астму. Может возникнуть перфорация перегородки. Считается ядом.
Проглатывание вызывает рвоту, диарею и, что очень необычно, осложнения со стороны желудка и почек. Контакт с глазами или кожей вызывает местное раздражение. Повторное воздействие на кожу вызывает дерматит.
Дихромат натрия является канцерогеном для человека. Существуют доказательства того, что соединения шестивалентного хрома или Cr (VI) могут вызывать рак легких у людей. Было показано, что дихромат натрия вызывает рак легких у животных.
Хотя дихромат натрия не был идентифицирован как тератогенное соединение или репродуктивный риск, известно, что соединения шестивалентного хрома или Cr (VI) являются тератогенными и вызывают репродуктивное повреждение, такое как снижение фертильности и нарушение менструальных циклов..
Дихромат натрия может вызвать повреждение печени и почек, поэтому с ним следует обращаться с особой осторожностью (Департамент здравоохранения Нью-Джерси, 2009 г.).
В случае проглатывания жертва должна пить воду или молоко; никогда не вызывать рвоту. При попадании на кожу или в глаза его следует рассматривать как кислотные ожоги; Промойте глаза водой не менее 15 минут.
Использование и приложения
Помимо важности в производстве других химических соединений хрома, дихромат натрия также имеет множество прямых применений в качестве ингредиента при производстве:
(Дихромат натрия, строительный блок для практически всех других соединений хрома., 2010-2012)
Дихромат натрия дигидрат, его использование идеально в различных условиях, в том числе при высоких температурах, таких как керамические глазури и цветное стекло.
Оксид хрома, твердее других оксидов металлов, таких как титан или железо, идеально подходит для сред, где температура и условия процесса агрессивны.
Это вещество в основном используется для производства других соединений хрома, но оно также используется в бентонитовых грязях, используемых при производстве нефти, в консервантах для древесины, в производстве органических химикатов и в качестве ингибитора коррозии..
При смешивании с алюминием и дихроматом калия с использованием алюмотермического процесса оксид хрома образует металлический хром высокой чистоты. Это жизненно важный ингредиент в производстве высокоэффективных суперсплавов, используемых в аэрокосмической промышленности..
В органическом синтезе дихромат натрия используется в качестве окислителя в окислительных реакциях восстановления в присутствии серной кислоты.
биохимия
Интратрахеальная инстилляция дихромата натрия (CrVI) и гидроксида ацетата хрома (CrIII) у самцов крыс приводила к повышению концентрации хрома в цельной крови, плазме и моче вплоть до 72 часов после воздействия; Максимальные концентрации были достигнуты через 6 часов после воздействия.
Соотношение между концентрациями хрома в плазме крови и хрома в плазме значительно различалось при лечении Cr (VI) и Cr (III). Поэтому анализ хрома в крови и хрома в плазме следует использовать для оценки воздействия хрома.
Хром был также обнаружен в периферических лимфоцитах. Cr (VI), но не Cr (III), значительно накапливался в лимфоцитах после лечения. Эти клетки потенциально могут быть использованы в качестве биомаркеров при оценке воздействия соединений хрома (Hooth, 2008).
Натрия бихромат купить
| Производитель | Фасовка | Натрия бихромат цена |
| Россия | Мешки по 25 кг | 64 грн/кг |
Натрия бихромат (дихромат натрия, натрий двухромовокислый, натриевый хромпик) — неорганическое химическое соединение, натриевая соль дихромовой кислоты.
Физико-химические свойства.
Химическая формула: Na2Cr2O7. Неслеживающиеся нелетучие кристаллы от светло-оранжевого до темно-красного цвета. Температура плавления 357°С. Температура разложения 400°С. Разлагается на натрия хромат, хрома (III) оксид, кислород. Водные растворы обладают кислой реакцией.
Растворимость натрия бихромата в различных растворителях
Применение.
Области применения натриевого хромпика:
В кожевенной и меховой промышленности для дубления кож и мехов;
В химической промышленности при производстве неорганических пигментов, катализаторов и других хромсодержащих соединений;
В текстильной промышленности при крашении тканей в качестве протравы;
В ряде других отраслей промышленности в составе пассивирующих смесей, антифриза для двигателей, очистки ацетилена и химических реактивов.
Применение бихромата натрия при бурении скважин.
Дихромат натрия используется в качестве ингибитора коррозии, а также как добавка, предотвращающая высокотемпературное застудневание.
Применение дихромата натрия в строительстве деревянных мостов
Дихромат натрия и медный купорос применяют при антисептировании элементов деревянных мостов методом глубокой местной пропитки под давлением.
Консервация древесины препаратом ХМ-5 производится 10-процентным водным раствором под давлением. Древесина, пропитанная препаратом ХМ-5, приобретает светло-зеленую окраску, стойкость к биологическим агентам разрушения, не оказывает значительного действия на коррозирование металлов, контактирующих с пропитанной древесиной, склеивается и окрашивается, не ядовита. Препарат ХМ-5 относится к типу невымываемых антисептиков, фиксируется в древесине в среднем на 84-90%.
Препарат ХМ-5 может быть изготовлен двух вариантов и по физико-химическим показателям должен соответствовать нормам, указанным в таблице
Состав препарата ХМ-5
Для приготовления раствора препарата ХМ-5 в специальную емкость вливается необходимое количество воды, засыпается требуемое количество технического бихромата натрия и полученную смесь тщательно перемешивают до полного растворения, после чего добавляют столько же медного купороса и перемешивают.
Технология проведения глубокой местной пропитки под давлением относится к здоровой, не загнившей древесине.
Применение натрия бихромата при химическом оксидировании алюминия и алюминиевых сплавов.
Оксидирование алюминия заключается в химическом процессе образования на поверхности алюминиевых деталей пленки оксидов алюминия. На оксидированный алюминий хорошо ложится краска. Оксидирование придает алюминиевым деталям красивый товарный вид.
Состав химического раствора: натрия бихромат 1,5 г/л; натрия карбонат (сода кальцинированная) 5 г/л. Температура обработки 80-100 °С. Продолжительность обработки 3-5 мин. Цвет оксидной пленки: светло-серый.
К этому химическому раствору можно прибавить 0,25 части за массой едкого натра, чтобы он глубже проник в металл. После оксидирования деталь погружают на 10-15 мин в 2 %-ной раствор хромового ангидрида температурой 18-20 °С или же промывают ее в воде и кипятят 15-20 мин, чтобы удалить остатки реактивов. Потом деталь сушат. Очень хорошо, если оксидированную поверхность защитить лаком. Оксидируют алюминий до образования пленки с перламутровым блеском так: поверхность изделия очищают от грязи, обезжиривают органическим растворителем и проволочной щеткой (наждачной кожицей № 60 или 80) обрабатывают ее в разных направлениях. Потом деталь нагревают до температуры 80-100°С, покрывают, нагретым до 90—100°С 10%-им раствором едкого натрия и сушат на воздухе. Покрытая прозрачным лаком поверхность не теряет цвета на протяжении трех лет.
Применение бихромата натрия при дублении кожи.
При дублении кожи бихромат натрия используют как минеральное дубящее вещество.
Дубление может происходить однованным или двухванным способом. Однованное дубление выполняют в растворе минеральных хромовых соединений, уже обладающих дубящими свойствами. Этим способом дубят в одну стадию, когда всё дубящее вещество вводят сразу в один раствор, или в две стадии — вначале на растворе с расходом дубящего вещества от 1/3 до 1/2 всего количества, а затем, после ряда промежуточных операций, — на растворе оставшегося количества дубящего вещества. Для двухванного дубления применяют соединения шестивалентного хрома. Вначале полуфабрикат обрабатывают в растворе бихромата и минеральной кислоты. При этом образовавшаяся бихромовая кислота, не обладающая дубящими свойствами, равномерно прокрашивает гольё. Затем полуфабрикат обрабатывают в растворе гипосульфита для восстановления шестивалентного хрома в трёхвалентный и тем самым превращения его в дубящее вещество, которое связывается с белком, вызывая эффект дубления.
Чтобы получить равномерно продубленный полуфабрикат, на первом этапе дубления применяют низкоосновные соли хрома, затем постепенно повышают их основность. Часто трёхвалентные соли получают из бихромата калия или бихромата натрия. При этом все расчёты ведут на содержание в растворе оксида хрома. Для приготовления хромого экстракта в качестве исходных материалов берут калиевый или натриевый хромпик. Приготовление экстракта заключается в превращении шестивалентного хрома в трёхвалентный. Концентрация серной кислоты может быть различной. В качестве востановителей применяют глюкозу, патоку или глицерин. Для приготовления дубильного раствора хромпик мелко дробят и растворяют в горячей воде. Затем медленно добавляют серную кислоту. Необходимое количество её расчитывают по формуле:
n-количество 100%-ой серной кислоты на 100 массовых частей хромпика;
После добавления серной кислоты к кислому раствору хромпика постепенно добавляют при непрерывном помешивании восстановитель (глюкозу или прочее). Раствор сильно разогревается, вспенивается и выделяет большое количество газов, при этом окраска раствора меняется от красновато-оранжевой до зелёной, характерной для солей трёхвалентного хрома. Если зелёный экстракт не окрашивается в синий цвет при добавлении нескольких капель 10%-ого крахмала, то экстракт готов. Если образуется синяя окраска, то реакция не окончена и её надо продолжить. Приготовленный экстракт настаивают в течении суток.
Применение бихромата натрия в качестве ингибитора коррозии для водяного охлаждения дизелей тепловозов.
В дизелях тепловозов, охладительная система которых заполняется обессоленной или дистиллированной водой, несмотря на отсутствие агрессивных солей, наблюдается усиленная коррозия отдельных элементов, в особенности в местах завихрения водяного потока и в щелевых зазорах. Также появляются трещины у отверстий втулок и рубашек двигателей. Обработка воды с применением бихромата натрия способствует удовлетворительной защите охладительной системы дизелей тепловозов от коррозии.
Состав ингибиторной смеси №1. Бихромат натрия Na2Cr2O7 500 мг/л; нитрит натрия NaNO2 500 мг/л; кальцинированная сода Na2CO3 500 мг/л.
Состав ингибиторной смеси №2. Бихромат натрия Na2Cr2O7 1000 мг/л; кальцинированная сода Na2CO3 400 мг/л.
Применение бихромата натрия для чистки двигателей внутреннего сгорания от нагара.
На рабочих поверхностях двигателей внутреннего сгорания образуется нагар, который представляет собой трудноудалимую пленку из асфальтосмолистых веществ. Нагар прочно сцепливается с металлом и сложно удаляется стандартными моющими средствами.
Нагар с поверхности черных металлов удаляют раствором: кальцинированная сода 30 г/л; каустическая сода 25 г/л; жидкое стекло 10 г/л; хозяйственное мыло 8 г/л. натрия бихромат 5 г/л. Температура раствора 80-95 °С. Продолжительность обработки до 3-х часов.
Применение натрия бихромата для производства пигмента «изумрудная зелень».
Пигмент «изумрудная зелень» имеет красивый изумрудно-зеленый цвет. Является термостойким (200°С), светостойким, атмосферостойким, устойчив к сернистым газам, кислотам и щелочам. Применяется для художественных красок и эмалей.
Пигмент «изумрудная зелень» получают из натрия бихромата термическим способом. Шихту, состоящую из натрия бихромата и борной кислоты прокаливают при температуре 650-700°С. В качестве катализатора в шихту вводят алюминиевые квасцы. При прокаливании происходят химические реакции:
Плав, полученный после прокаливания обрабатывают кипящей водой. При этом из него переходит в раствор пироборат натрия, а в осадке остается «изумрудная зелень». Осадок отмывают горячей водой почти до полного удаления борной кислоты, фильтруют, сушат и измельчают.
Средства защиты при использовании бихромата натрия.
Натрий бихромат раздражает и обжигает слизистые оболочки и кожу, вызывая изъязвления; при вдыхании пыли возможно прободение хрящей части носовой перегородки. В случае всасывания бихромата в кровь отмечаются желудочно-кишечные заболевания.
При работах, связанных с образованием пыли, необходимо применять противопылевые респираторы и пользоваться спецодеждой. Для предупреждения раздражения кожи рук при работе с бихроматом натрия рекомендуется смазывать руки перед работой специальной мазью (три части парафина, одна часть ланолина и небольшое количество фенола) и вымыть руки после работы 5%-ным раствором гипосульфита натрия.
Получение.
Дихромат натрия в промышленных масштабах получают из руд, содержащих оксид хрома.