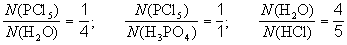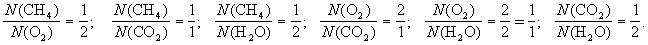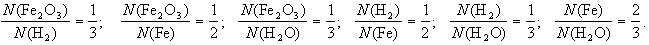Бинарное соединение
Бинарные соединения, несмотря на кажущуюся простоту их химического состава, представляют собой следующий после простых веществ принципиально важный объект изучения природы вещества. С химической точки зрения, этот класс веществ обладает и качественно иными характеристиками, с которыми не приходится сталкиваться при изучении простых веществ. Во-первых, помимо внешних факторов, влияющих на состояние и свойства вещества (температура и давление), здесь появляется и внутренний фактор — состав, и связанная с ним проблема постоянства и переменности состава, имеющая фундаментальное значение в химии. Во-вторых, при описании бинарных соединений впервые формируются такие базисные понятия, как валентность, степень окисления, поляризация химической связи. Здесь, в отличие от простых веществ, появляются гетерополярная составляющая химической связи и все эффекты, связанные с разностью электроотрицательностей компонентов.
Исключительно важную роль играют бинарные соединения с классификационной точки зрения. Многие из них относятся и к так называемым характеристическим соединениям, отражающим типичные степени окисления и их сравнительную стабильность. К таким соединениям относятся прежде всего оксиды, летучие водородные соединения, а также галогениды.
Связанные понятия
Интерметалли́д (интерметаллическое соединение) — химическое соединение двух или более металлов. Интерметаллиды, как и другие химические соединения, имеют фиксированное соотношение между компонентами.
Разница между Ионными и Бинарными соединениями
Ключевое различие между Ионными и Бинарными соединениями состоит в том, что Ионные соединения содержат два заряженных компонента, тогда как Бинарные соединения содержат два разных химических элемента.
Ионные соединения представляют собой бинарные соединения, которые подразделяются на две категории. Ионные соединения входят в категорию ковалентных соединений, когда это химическое соединение анализируют в соответствии с типом химических связей, присутствующих в молекуле. С другой стороны, Бинарные соединения подпадают под классификацию соединений в зависимости от химических элементов, присутствующих в молекуле.
Содержание
Что такое Ионные Соединения?
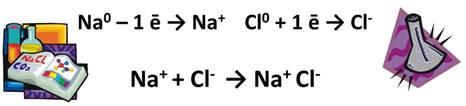
Ионные соединения представляют собой химические соединения, содержащие катионы и анионы, удерживаемые вместе ионными связями. Ионная связь — это электростатическая сила притяжения. Это притяжение происходит между противоположно заряженными ионами (катионы или положительно заряженные ионы и анионы или отрицательно заряженные ионы). Эти соединения образуются в результате того, что атомы стремятся завершить свою электронную конфигурацию, чтобы получить электронную конфигурацию благородного газа, которая является наиболее стабильным способом существования этих атомов. Кроме того, ионные соединения обычно существуют в виде кристаллов, поскольку противоположно заряженные ионные частицы имеют тенденцию к кластеризации.
Что такое Бинарные соединения?
Бинарные соединения — это химические соединения, содержащие два разных химических элемента. Кроме того, тип химической связи между атомами этих двух химических элементов может представлять собой ковалентные связи, ионные связи или даже координационные связи.
Кроме того, независимо от того, каково соотношение между атомами в химической формуле, если есть только два типа атомов, тогда это бинарное соединение.
В чем разница между Ионными и Бинарными соединениями?
Ключевое различие между Ионными и Бинарными соединениями состоит в том, что Ионные соединения содержат два заряженных компонента, тогда как Бинарные соединения содержат два разных химических элемента. Кроме того, ионные соединения имеют ионные связи, но в Бинарных соединениях ионные связи могут присутствовать или не присутствовать.
Содержание — Ионные против Бинарных соединений
Существуют разные классификации химических соединений. Ионные соединения и ковалентные соединения классифицируются в зависимости от химических связей между атомами. Ключевое различие между Ионными и Бинарными соединениями состоит в том, что Ионные соединения содержат два заряженных компонента, тогда как Бинарные соединения содержат два разных химических элемента.
Степень окисления. Бинарные соединения
Урок 18. Химия 8 класс
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобрев в каталоге.
Получите невероятные возможности
Конспект урока «Степень окисления. Бинарные соединения»
Бинарные соединения еще называют двухэлементными соединениями, потому что «би» от лат. – два. Т.е. бинарные соединения – это сложные вещества, состоящие из двух химических элементов.
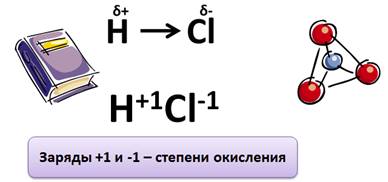
Ковалентная полярная связь
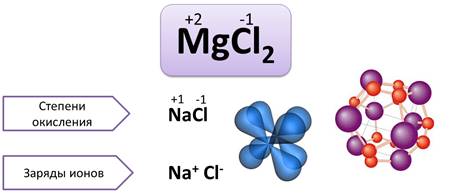
Степень окисления – это условный заряд атомов химического элемента в соединении, если предположить, что оно состоит только из ионов.
Степень окисления может быть положительной, отрицательной и нулевой. Положительную степень окисления имеют как металлы, так и неметаллы, кроме фтора, гелия и неона. Максимальная степень окисления равна номеру группы. Т.е. у N высшая степень окисления равна +5, т.к. он находится в V группе. Отрицательную степень окисления имеют только неметаллы, т.к. они присоединяют электроны до завершения внешнего уровня. Минимальная степень окисления равна № группы – 8. Т.о. у N минимальная степень окисления будет 5 – 8 = –3. Кроме максимальной и минимальной степени окисления есть еще промежуточная степень окисления. Например, у N она равна +3.
Степень окисления F всегда –1, потому что он самый электроотрицательный элемент и принимает электроны при образовании химической связи. Например, в соединении NaF, у F степень окисления (–1).
У кислорода степень окисления –2, потому что он второй элемент по электроотрицательности, исключение cоставляет соединение кислорода с фтором, где его степень окисления +2. Например, в соединении CaO, степень окисления О (–2), а в соединении OF2, степень окисления О (+2).
У металлов степень окисления всегда положительная, т.к. они отдают электроны другим атомам. Степень окисления металлов А групп численно совпадает с валентностью. Например, в соединении Na2O степень окисления Na (+1), т.к. он является металлом, значит, у него только положительная степень окисления, а 1, потому что он является металлом I A группы, значит, и валентность его – единица. Аналогично и в соединении BaS, степень окисления Ва (+2), т.к. он металл II A группы, в соединении Al2O3, степень окисления Al (+3), т.к. это металл III А группы.
Степень окисления Н всегда (+1), за исключением его соединений с металлами, где у него степень окисления (–1). Например, CaH2, KH, LiH, в этих соединениях у водорода степень окисления (–1).
Как было сказано, валентность численно совпадает со степенью окисления. Однако не всегда. Степень окисления имеет знак заряда, а валентность – нет.
Валентность – это число связей, которыми атом связан с другими атомами, а степень окисления – это условный заряд атомов.
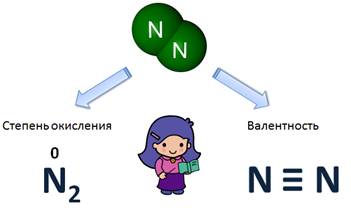
Сравним валентность и степень окисления у азота (N2). Степень окисления равна 0, т.к. это простое вещество, а вот валентность равна III, потому что атом азота связан с другим атомом азота тройной связью.
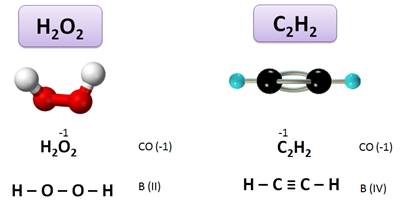
Или в пероксиде (Н2О2) степень окисления О (–1), а валентность равна II, т.к. О связан двумя связями с атомами водорода: Н – О – О – Н.
А в ацетилене (С2Н2) степень окисления С (–1), а валентность IV:
Учитывая, что суммарная степень окисления равна 0, можно найти степени окисления элементов в соединении, а также составить формулу соединения, зная степени окисления.
Определим степени окисления элементов в соединении Fe2O3. Степень окисления О нам известна (–2). Следовательно, три атома О будут иметь общий заряд (–6), т.к. (–2) · 3 = –6. Тогда общий заряд двух атомов железа будет равен (+6), помните, что суммарный заряд равен 0. Значит, степень окисления одного атома Fe будет (+3), т.к. (+6) ׃ 2 = +3.
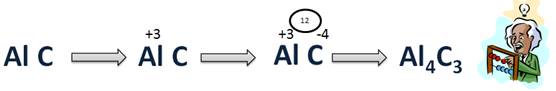
Составим формулу соединения Al с C. Для этого запишем символы элементов Al, C. Углерод на втором месте, потому что он более электроотрицательный. Al – элемент III A группы. Он является металлом, поэтому он отдаст свои 3 электрона и получит степень окисления (+3), а С – элемент IV A, он примет еще 4 электрона для завершения своего внешнего уровня, на котором уже есть 4 электрона, при этом получит степень окисления (–4). Запишем значения степеней окисления в формулу сверху. Теперь найдем наименьшее общее кратное. Оно будет 12. Затем НОК разделим на абсолютные значения степеней окисления и получим соответствующие индексы. 12 : 3 = 4, значит индекс у Al – 4, 12 : 4 = 3, значит индекс у С – 3. Следовательно, формула будет Al4C3.
Чтобы дать название бинарному соединению нужно сделать следующим образом: сначала называют более электроотрицательный элемент – это неметалл. Его латинское название стоит в именительном падеже и употребляется с суффиксом – ид. Например: оксид, хлорид, сульфид, нитрид. Второе слово обозначает элемент менее электроотрицательный, его название стоит в родительном падеже.
Na2S – сульфид натрия, K2O – оксид калия, BaCl2 – хлорид бария, Mg3N2 – нитрид магния. Если элемент имеет переменную степень окисления, то после названия в скобках римскими цифрами указывают степень окисления. Например, назовём следующие соединения: MnO2, CO2, P2O5.
Название бинарного соединения
В некоторых случаях, число атомов элементов обозначают при помощи названий числительных на греческом языке. Т.е. 1 – моно, 2 – ди, 3 – три, 4 – тетра, 5 – пента и т.д. Например, СО – монооксид углерода, или оксид углерода (II); СО2 – диоксид углерода, или оксид углерода (IV).
Для того чтобы химики всего мира понимали друг друга, необходимо было создать единую терминологию и номенклатуру, т.е. названия веществ. Впервые в 1785 г. такими учеными, как А. Лавуазье, А. Фуркруа, Л. Гитоном де Мерво и К. Бертолле, были разработаны принципы номенклатуры. В настоящее время принципы номенклатуры и терминологии разрабатывает Международный союз теоретической и прикладной химии (ИЮПАК).
Что такое бинарные соединения в химии
При химических реакциях одни вещества превращаются в другие. Вспомним известную нам реакцию серы с кислородом. И в ней из одних веществ (исходных веществ или реагентов) образуются другие (конечные вещества или продукты реакции).
Для записи и передачи информации о химических реакциях используются схемы и уравнения реакций.
Схема химической реакции – условная запись,дающая качественнуюинформацию о химической реакции.
Схема реакции показывает, какие вещества вступают в реакцию и какие образуются в результате реакции. И в схемах, и в уравнениях реакций вещества обозначаются их формулами.
Это означает, что при взаимодействии серы с кислородом протекает химическая реакция, в результате которой образуется диоксид серы (сернистый газ). Все вещества здесь молекулярные, поэтому при записи схемы использованы молекулярные формулы этих веществ. То же относится и к схеме другой реакции – реакции горения белого фосфора:
При нагревании до 900 o С карбоната кальция (мела, известняка) протекает химическая реакция: карбонат кальция превращается в оксид кальция (негашеную известь) и диоксид углерода (углекислый газ) по схеме:
CaCO3 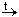
Карбонат кальция и оксид кальция – вещества немолекулярные, поэтому в схеме использованы их простейшие формулы, отражающие состав их формульных единиц. Для молекулярного вещества – углекислого газа – использована молекулярная формула.
Иногда для передачи информации о химической реакции бывает достаточно и краткой схемы этой реакции, например:
Естественно, что краткой схеме может соответствовать и несколько разных реакций.
Уравнение химической реакции – условная запись, дающая качественную и количественную информацию о химической реакции.
Для любой химической реакции справедлив один из важнейших законов химии:
При протекании химических реакций атомы не появляются, не исчезают и не превращаются друг в друга.
При записи уравнений химических реакций, кроме формул веществ, используются коэффициенты. Как и в алгебре, коэффициент «1» в уравнении химической реакции не ставится, но подразумевается. Рассмотренные нами реакции описываются следующими уравнениями:
Знак равенства между правой и левой частью уравнения означает, что число атомов каждого элемента, входящих в состав исходных веществ, равно числу атомов этого элемента, входящих в продукты реакциии.
Коэффициенты в уравнении химической реакции показывают отношение между числом реагирующих и числом образующихся молекул (для немолекулярных веществ – числом формульных единиц) соответствующих веществ. Так, для реакции, протекающей при взаимодействии пентахлорида фосфора с водой
Схема химической реакции показывает, что (1) в реакции, протекающей между метаном и кислородом, образуются углекислый газ и вода.
Уравнение реакции добавляет, что (2) число молекул метана, вступившего в реакцию, относится к числу молекул вступившего в реакцию кислорода, как 1 к 2, и так далее, то есть:
Кроме того, уравнение показывает, что одна молекула метана реагирует с двумя молекулами кислорода, при этом образуется одна молекула углекислого газа и две молекулы воды.
Схема химической реакции показывает, что (1) при взаимодействии оксида железа(Fe2O3) с водородом (которое происходит при нагревании) образуются железо и вода.
Уравнение добавляет к этому, что (2) число формульных единиц оксида железа, вступившего в реакцию, относится к числу вступивших в реакцию молекул водорода, как 1 к 3, и так далее. То есть:
Кроме того уравнение показывает, что одна формульная единица оксида железа реагирует с тремя молекулами водорода, при этом образуется два атома железа и три молекулы воды.
Как вы узнаете в дальнейшем, уравнения реакций дают нам и другую количественную информацию.
| Карбонат кальция – CaCO3. Бесцветное немолекулярное вещество, нерастворимое в воде. Такие широко известные горные породы, как мрамор и известняк, состоят в основном из карбоната кальция. Мел, которым вы пишете на доске, – тоже карбонат кальция: многие морские организмы (радиолярии и др.) строят свои панцири из этого вещества; за длительное время на дне океана формируются залежи мела, представляющего собой огромные слои спрессованных панцирей этих организмов. Карбонат кальция не обладает способностью плавиться – при нагревании он разлагается. Горные породы, образуемые карбонатом кальция, используются в строительстве в качестве отделочных материалов, строительного камня, а также для производства негашеной извести (CaO). В металлургии карбонат кальция в виде известняка добавляют в руду для лучшего образования шлаков. |
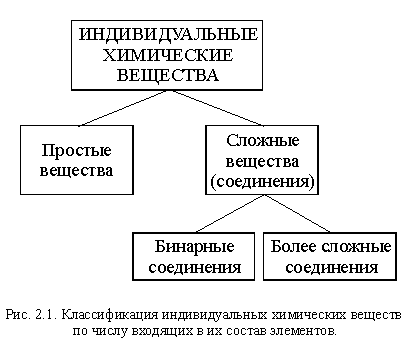
Вы уже познакомились в той или иной степени примерно с пятьюдесятью индивидуальными (чистыми) химическими веществами. Всего же науке известно несколько миллионов таких веществ. Чтобы не утонуть в этом » море» веществ, их необходимо систематизировать и прежде всего классифицировать – классифицировать более подробно, чем мы делали это в параграфе 1.4 (рис. 1.3).
Вещества отличаются друг от друга своими свойствами, а свойства веществ определяются составом и строением. Поэтому важнейшие признаки, по которым классифицируют вещества – состав, строение и свойства.
По составу, а точнее, по числу входящих в их состав элементов, вещества делятся на простые и сложные (это вы уже знаете). Сложных веществ в сотни тысяч раз больше, чем простых, поэтому среди них выделяют бинарные вещества (бинарные соединения).
Бинарные вещества (бинарные соединения) – сложные вещества,в состав которых входят атомы двух элементов.
Схема этой классификации приведена на рисунке 2.1.
Признаком, по которому проводят дальнейшую классификацию веществ, являются их свойства.
Начнем с простых веществ.
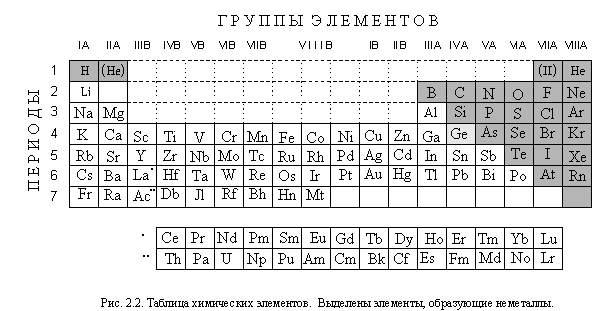
По физическим свойствам простые вещества делятся на металлы и неметаллы.
Характерные физические свойства металлов:
1) высокая электропроводность (способность хорошо проводить электрический ток),
2) высокая теплопроводность (способность хорошо проводить теплоту),
3) высокая пластичность (ковкость, изгибаемость, вытягиваемость).
Кроме того все металлы обладают » металлическим» блеском. Но следует помнить, что таким блеском обладают не только металлы, но и часть неметаллов, и даже некоторые сложные вещества. Блестит кристаллический кремний, одна из полиморфных модификаций мышьяка, теллур, а это всё – неметаллы. Из сложных веществ – пирит FeS2, халькопирит CuFeS2 и некоторые другие.
При комнатной температуре металлы – твердые вещества (исключение – ртуть, ее температура плавления – 39 o С).
В отличие от металлов, неметаллы не обладают каким-либо определенным набором характерных физических характеристик. Даже агрегатное состояние у них может быть разным. При комнатной температуре газообразныдвенадцать простых веществ (Н2, Не, N2, O2, O3, F2, Nе, Cl2, Аr, Кr, Хе, Rn), жидкость одна (Br2), а твердых веществ – более десяти (В, С(алмаз), С(графит), Si, P4, S8, As, Se, Те, I2 и др.). По своим химическим свойствам большинство металлов сильно отличается от большинства неметаллов, но резкой границы между ними нет.
Многие простые вещества при определенных условиях могут вступать в реакции друг с другом, например:
В результате таких реакций образуются бинарные соединения.
В принципе, в состав бинарного соединения могут входить любые элементы (кроме гелия и неона). Но часто один из этих элементов – кислород, водород или один из галогенов (фтор, хлор, бром или йод). Такие вещества называются кислородными соединениями, водородными соединениями или галогенидами. Примеры бинарных соединений: CaO, Al2O3, КН, HCl, АlI3, СаС2.
| Кислородное соединение – бинарное соединение, один из элементов в котором кислород. |
Примеры кислородных соединений: H2O (вода), H2O2 (пероксид водорода), Na2O (оксид натрия), Na2O2 (пероксид натрия), СО2 (диоксид углерода), OF2 (фторид кислорода). Большинство кислородных соединений является оксидами. Чем оксиды отличаются от остальных кислородных соединений, вы узнаете позже.
Примеры оксидов:
Li2O – оксид лития, CO2 – диоксид углерода, CaO – оксид кальция, SiO2 – диоксид кремния, Al2O3 – оксид алюминия, Н2О – вода,
MnO2 – диоксид марганца, SO3 –триоксид серы.
| Водородное соединение – бинарное соединение, один из элементов в котором водород. |
Галогенид (фторид, хлорид, бромид или – бинарное соединение,один из элементов в котором – галоген.
Примеры галогенидов: CaF2 – фторид кальция, BF3 – трифторид бора, NaCl – хлорид натрия,PCl5 – пентахлорид фосфора, КВr – бромид калия, НВr – бромоводород, AlI3 – йодид алюминия, HI – йодоводород.
Примеры названий бинарных соединений приведены в таблице 6.
Бинарные соединения



Обширный тип неорганических сложных веществ бинарные соединения. К ним относятся, в первую очередь все двухэлементные соединения (кроме основных, кислотных и амфотерных оксидов), например H2O, KBr, H2S, Cs2(S2), N2O, NH3, HN3, CaC2, SiH4. Электроположительная и электроотрицательная составляющие формул этих соединений включают отдельные атомы или связанные группы атомов одного элемента.
Многоэлементные вещества, в формулах которых одна из составляющих содержит не связанные между собой атомы нескольких элементов, а также одноэлементные или многоэлементные группы атомов (кроме гидроксидов и солей), рассматривают как бинарные соединения, например CSO, IO2F3, SBrO2F, CrO(O2)2, PSI3, (CaTi)O3, (FeCu)S2, Hg(CN)2, (PF3)2O, VCl2(NH2). Так, CSO можно представить как соединение CS2, в котором один атом серы заменен на атом кислорода.
Названия бинарных соединений строятся по обычным номенклатурным правилам, например:
| OF2 дифторид кислорода | K2O2 пероксид калия |
| HgCl2 хлорид ртути(II) | Na2S сульфид натрия |
| Hg2Cl2 дихлорид диртути | Mg3N2 нитрид магния |
| SBr2O оксид-дибромид серы | NH4Br бромид аммония |
| N2O оксид диазота | Pb(N3)2 азид свинца(II) |
| NO2 диоксид азота | CaC2 ацетиленид кальция |
Для некоторых бинарных соединений используют специальные названия, список которых был приведен ранее.
Такие бинарные соединения, как AgF, KBr, Na2S, Ba(HS)2, NaCN, NH4Cl, и Pb(N3)2, построены, подобно солям, из реальных катионов и анионов, поэтому их называют солеобразными бинарными соединениями (или просто солями). Их можно рассматривать как продукты замещения атомов водорода в соединениях НF, НCl, НBr, Н2S, НCN и НN3. Последние в водном растворе обладают кислотной функцией, и поэтому их растворы называют кислотами, например НF(aqua) фтороводородная кислота, Н2S(aqua) сероводородная кислота. Однако они не принадлежат к типу кислотных гидроксидов, а их производные к солям в рамках классификации неорганических веществ.
Химические свойства веществ выявляются в разнообразных химических реакциях.
Превращения веществ, сопровождающиеся изменением их состава и (или) строения, называются химическими реакциями. Часто встречается и такое определение: химической реакцией называется процесс превращения исходных веществ (реагентов) в конечные вещества (продукты).
Химические реакции записываются посредством химических уравнений и схем, содержащих формулы исходных веществ и продуктов реакции. В химических уравнениях, в отличие от схем, число атомов каждого элемента одинаково в левой и правой частях, что отражает закон сохранения массы.

Химические уравнения могут содержать дополнительные сведения об особенностях протекания реакции. Если химическая реакция протекает под влиянием внешних воздействий (температура, давление, излучение и т.д.), это указывается соответствующим символом, как правило, над (или «под») знаком равенства.
Огромное число химических реакций может быть сгруппировано в несколько типов реакций, которым присущи вполне определенные признаки.
В качестве классификационных признаков могут быть выбраны следующие:
1. Число и состав исходных веществ и продуктов реакции.
2. Агрегатное состояние реагентов и продуктов реакции.
3. Число фаз, в которых находятся участники реакции.
4. Природа переносимых частиц.
5. Возможность протекания реакции в прямом и обратном направлении.
Такие реакции относят к термохимическим.
Рассмотрим более подробно каждый из типов реакций.