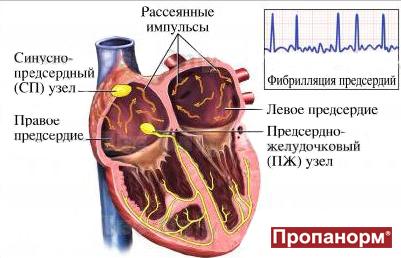
Фибрилляция предсердий: причины, симптомы, лечение
Фибрилляция предсердий (ФП) – синоним более применимого в странах СНГ термина «Мерцательная аритмия».
Фибрилляция предсердий является наиболее распространенным нарушением сердечного ритма. ФП не связана с высоким риском внезапной смерти, поэтому ее не относят к фатальным нарушениям ритма, как, например, желудочковые аритмии.
Фибрилляция предсердий
Один из самых распространенных видов наджелудочковых тахиаритмий – фибрилляция предсердий (ФП). Фибрилляцией называют быстрое нерегулярное сокращение предсердий, при этом частота их сокращений превышает 350 в минуту. Появление ФП характеризуется нерегулярным сокращением желудочков. На долю ФП приходится более 80 % всех пароксизмальных суправентрикулярных тахиаритмий. Фибрилляция предсердий возможна у пациентов всех возрастных категорий, однако у больных пожилого возраста распространенность синдрома увеличивается, что связано с учащением органической патологии сердца.
Причины развития и факторы риска
Возрастные органические изменения. С возрастом структура миокарда предсердий претерпевает изменения. Развитие мелкоочагового кардиосклероза предсердий может стать причиной фибрилляции в пожилом возрасте.
Классификация фибрилляции предсердий
По продолжительности клинических проявлений. Различают следующие формы ФП:
Типы мерцательной аритмии (МА)
Термин «мерцательная аритмия» может обозначать два следующих вида суправентрикулярной тахиаритмии.
Фибрилляция (мерцание предсердий). В норме электрический импульс возникает в синусовом узле (в стенке правого предсердия), распространяется по миокарду предсердий и желудочков, вызывая их последовательное сокращение и выброс крови. При ФП электрический импульс распространяется хаотично, заставляя предсердия «мерцать», когда волокна миокарда сокращаются несогласованно и очень быстро. В результате хаотичной передачи возбуждения на желудочки, они сокращаются неритмично и, как правило, недостаточно эффективно.
Трепетание предсердий. В этом случае сокращение волокон миокарда происходит в более медленном темпе (200–400 уд./мин.). В отличие от ФП, при трепетании предсердия все-таки сокращаются. Как правило, за счет периода рефрактерности атриовентрикулярного узла на желудочки передается не каждый электрический импульс, поэтому они сокращаются не в столь быстром темпе. Однако, как и при фибрилляции, при трепетании насосная функция сердца нарушается, а миокард испытывает дополнительную нагрузку.
Осложнения мерцательной аритмии
По последним данным, пациенты с мерцательной аритмией попадают в группу риска не только по развитию тромбоэмболического инсульта, но и инфаркта миокарда. Механизмы поражения таковы: при фибрилляции предсердий невозможно полноценное сокращение предсердий, поэтому кровь в них застаивается и в пристеночном пространстве предсердий образуются тромбы. Если такой тромб с током крови попадает в аорту и в менее крупные артерии, то возникает тромбоэмболия артерии, питающей какой-либо орган: головной мозг, сердце, почки, кишечник, нижние конечности. Прекращение кровоснабжения вызывает инфаркт (некроз) участка этого органа. Инфаркт мозга называется ишемическим инсультом. Наиболее часто встречаются осложнения:
Медикаментозная терапия
Выделяют следующие направления лекарственной терапии фибрилляции предсердий: кардиоверсия (восстановление нормального синусового ритма), профилактика повторных пароксизмов (эпизодов) наджелудочковых аритмий, контроль нормальной частоты сокращений желудочков сердца. Также важная цель медикаментозного лечения при МА – предотвращение осложнений – различных тромбоэмболий. Лекарственная терапия ведется по четырем направлениям.
Лечение антиаритмиками. Применяется, если принято решение о попытке медикаментозной кардиоверсии (восстановления ритма с помощью лекарств). Препараты выбора – пропафенон, амиодарон.
Пропафенон – один из наиболее эффективных и безопасных лекарственных препаратов, который используется для лечения наджелудочковых и желудочковых нарушений сердечного ритма. Действие пропафенона начинается через 1 ч после приема внутрь, максимальная концентрация в плазме крови достигается через 2–3 ч и длится 8–12 ч.
Контроль ЧСС. В случае невозможности восстановить нормальный ритм необходимо привести мерцательную аритмию в нормоформу. Для этой цели применяют бета-адреноблокаторы, антагонисты кальция недигидропиридинового ряда (группы верапамила), сердечные гликозиды и др.
Бета-адреноблокаторы. Препараты выбора для контроля работы сердца (частоты и силы сокращений) и артериального давления. Группа блокирует бета-адренергические рецепторы в миокарде, вызывая выраженный антиаритмический (урежение ЧСС), а также гипотензивный (снижение АД) эффект. Доказано, что бета-блокаторы статистически увеличивают продолжительность жизни при сердечной недостаточности. Среди противопоказаний к приему – бронхиальная астма (так как блокировка бета 2-рецепторов в бронхах вызывает бронхоспазм).
Антикоагулянтная терапия. Для снижения риска тромбообразования при персистирующей и хронической формах ФП обязательно назначают препараты, разжижающие кровь. Назначают антикоагулянты прямого (гепарин, фраксипарин, фондапаринукс и пр.) и непрямого (варфарин) действия. Существуют схемы приема непрямых (варфарин) и так называемых новых антикоагулянтов – антагонистов факторов свертывания крови (прадакса, ксарелто). Лечение варфарином сопровождается обязательным контролем показателей свертываемости и, при необходимости, тщательной коррекцией дозировки препарата.
Метаболическая терапия. К метаболическим препаратам относятся лекарственные средства, улучшающие питание и обменные процессы в сердечной мышце. Эти препараты якобы оказывают кардиопротективное действие, защищая миокард от воздействия ишемии. Метаболическая терапия при МА считается дополнительным и необязательным лечением. По последним данным, эффективность многих препаратов сравнима с плацебо. К таким лекарственным средствам относятся:
Диагностика и лечение любого вида аритмии требует немалого клинического опыта, а во многих случаях – высокотехнологичного аппаратного оснащения. При фибрилляции и трепетании предсердий главная задача врача – по возможности устранить причину, приведшую к развитию патологии, сохранить функцию сердца и предотвратить осложнения.
Симптомы ФП
В зависимости от формы аритмии (постоянная или приступообразная) и восприимчивости больного клиническая картина ФП варьирует от отсутствия симптомов до наличия признаков сердечной недостаточности. Больные могут жаловаться на:
Фибрилляция предсердий и трепетание предсердий может сопровождаться учащенным мочеиспусканием, вызванным повышенной выработкой натрийуретического пептида. Приступы, длящиеся несколько часов или суток и не проходящие самостоятельно, требуют медицинского вмешательства.
Патогенез и общая клиническая картина
Основное проявление фибрилляции предсердий – аритмичный пульс. При высокой частоте сердечных сокращений в момент приступа ФП может возникнуть дефицит пульса, когда число сердечных сокращений превышает частоту пульса.
Причины ФП и факторы риска
Заболевания различного генеза
Наиболее часто ФП возникает у пациентов с заболеваниями сердечно-сосудистой системы – артериальной гипертензией, ИБС, хронической сердечной недостаточностью, пороками сердца – врожденными и приобретенными, воспалительными процессами (перикардит, миокардит), опухоли сердца. Среди острых и хронических заболеваний, не связанных с патологией сердца, но влияющих на возникновение фибрилляции предсердий, выделяют нарушения функций щитовидной железы, сахарный диабет, хроническую обструктивную болезнь легких, синдром сонного апноэ, болезни почек и др.
Возрастные изменения
Фибрилляцию предсердий называют «аритмией дедушек», так как заболеваемость этой аритмией резко увеличивается с возрастом. Развитию данного нарушения сердечного ритма могут способствовать электрические и структурные изменения предсердий,. Однако специалисты отмечают, что мерцательная аритмия может возникнуть у молодых людей, не имеющих патологии сердца: до 45 % случаев пароксизмальной и до 25 % случаев персистирующей фибрилляции.
Другие факторы риска
Фибрилляция предсердий может развиваться на фоне употребления алкоголя, после удара электрического тока и операций на открытом сердце. Пароксизмы могут спровоцировать такие факторы, как физическая нагрузка, стрессовые состояния, жаркая погода, обильное питье. В редких случаях имеется наследственная предрасположенность возникновения ФП.
Методы диагностики
Сначала требуется определить индивидуальный риск инсульта:
Определение риска инсульта при первичной * (если инсультов ранее не было) профилактике (J Am Coll Cardiol 2001;38:1266i-1xx).
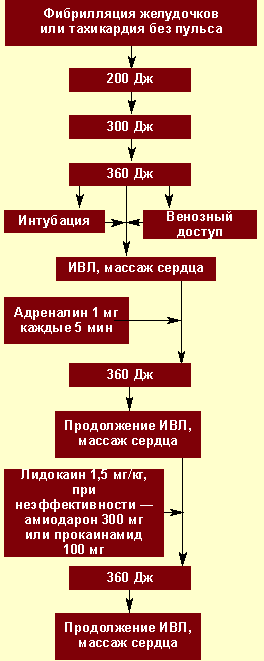 |
| Рисунок 2. Алгоритм неотложной помощи при фибрилляции желудочков |
Электрическая дефибрилляция сердца (ЭДС). Это важнейший компонент СРЛ. ЭДС эффективна только при сохранности энергетического ресурса миокарда, т. е. при регистрации на ЭКГ крупноволновых осцилляций от 0,5 до 1 мВ и более (рис. 2). Если же отмечаются низкие, аритмичные, полиморфные осцилляции, а также асистолия, то начинают с ИВЛ, непрямого массажа и медикаментозной терапии (рис. 3), добиваются перехода асистолии или мелковолновой фибрилляции желудочков в крупноволновую фибрилляцию и применяют ЭДС.
Первый разряд для ЭДС — 200 Дж, при неэффективности второй — 300 Дж, при неэффективности третий — 360 Дж. Перерыв между разрядами минимальный — для контроля ритма. Непрямой массаж сердца и ИВЛ прерываются только на момент разряда. Если первая серия из трех разрядов оказывается неэффективной, то на фоне продолжающейся ИВЛ, непрямого массажа сердца, медикаментозной терапии проводится вторая серия разрядов в той же последовательности.
В настоящее время на догоспитальном этапе применяются автоматические наружные дефибрилляторы, в этом случае ЭКГ регистрируется с электродов дефибриллятора, приложенных к грудной клетке. Дефибриллятор регистрирует ритм сердца и производит его автоматический анализ; при выявлении желудочковой тахикардии или фибрилляции желудочков конденсаторы автоматически заряжаются, и прибор дает разряд. Эффективность автоматических дефибрилляторов очень высока. Кроме автоматических, используются полуавтоматические наружные дефибрилляторы.
Медикаментозная терапия при сердечно-легочной реанимации. Медикаменты при СЛР могут вводиться: в периферическую вену; в центральную вену; в трахею.
По понятным причинам внутримышечный путь введения не показан. При наличии возможности катетеризируется периферическая вена. Если реаниматолог опытный и хорошо владеет методикой пункции центральной вены, можно использовать этот способ. Проблема в том, что в этом случае приходится прерывать реанимационные мероприятия, а перерыв больше, чем на 5–10 с нежелателен. Внутритрахеальный путь удобен, если выполнена интубация трахеи, в крайнем случае можно ввести препараты в трахею через перстнещитовидную мембрану. Эндотрахеально допустимо вводить адреналин, атропин, лидокаин. Препараты лучше развести в 10–20 мл 0,9% раствора натрия хлорида.
Адреналин остается средством выбора при остановке кровообращения. При асистолии и электромеханической диссоциации он «тонизирует» миокард и помогает «запустить» сердце, мелковолновую фибрилляцию переводит в крупноволновую, что облегчает ЭДС. Дозы: по 1–2 мг внутривенно струйно с интервалом 5 мин, суммарно обычно — до 10-15 мг.
М-холинолитик атропин снижает тормозящее влияние ацетилхолина на синусовый узел и атриовентрикулярную проводимость и, возможно, способствует высвобождению катехоламинов из мозгового слоя надпочечников. Он показан при брадисистолии и асистолии. Дозы — 1 мг, можно повторить через 5 мин, но не более 3 мг за время реанимации.
Все антиаритмические препараты оказывают депрессивное действие на миокард и небезвредны для организма пациента. При развившейся фибрилляции желудочков их следует вводить лишь в случае нескольких неудачных попыток ЭДС, поскольку они, подавляя желудочковую эктопию затрудняют восстановление самостоятельного ритма. Лидокаин считается одним из наиболее эффективных средств при рефрактерной фибрилляции желудочков, устойчивой желудочковой тахикардии и тахикардиях неясной этиологии с широким комплексом QRS. Доза для насыщающего внутривенного введения — 1,5 мг/кг струйно (обычно — 75–100 мг). Одновременно начинается введение поддерживающей дозы 2–4 мг в мин. Для этого 1 г лидокаина разводится в 250 мл 5% раствора глюкозы.
Показанием к введению гидрокарбоната натрия можно считать затянувшуюся более чем на 15 мин реанимацию, если остановке сердца предшествовали выраженный метаболический ацидоз или гиперкалиемия. Доза — 1 ммоль/кг, внутривенно однократно, при повторном введении она уменьшается вдвое. Некоторые авторы считают, что при адекватных реанимационных мероприятиях гидрокарбонат натрия следует вводить только под контролем кислотно-основного состояния, поскольку организм значительно хуже адаптируется к алкалозу, чем к ацидозу.
В качестве инфузионных растворов целесообразно использовать 0, 9% раствор хлорида натрия, но наиболее эффективен раствор лактата Рингера по Хартману, а из коллоидов — растворы со средней молекулярной массой, содержащие гидроксиэтилкрахмал — волювен или венофундин.
Во всех случаях показана экстренная госпитализация по витальным показаниям в отделение реанимации и интенсивной терапии.
И. Г. Труханова, доктор медицинских наук, доцент
Е. В. Двойникова, кандидат медицинских наук, доцент
Самарский государственный медицинский университет, Самара