Очаги демиелинизации на МР-томограммах: рассеянный склероз или нет?
Наша задача – в этом разобраться.
Очаги демиелинизации на МРТ: что это может быть
Очаг демиелинизации в веществе головного или спинного мозга – это участок, где когда-то был, или в настоящее время идёт воспалительный процесс с разрушением миелина – оболочки проводящих нервных путей. Подробнее о демиелинизации
Если найдены очаги демиелинизации в головном или спинном мозге – первое, что нужно сделать, это выяснить природу очагов, степень их опасности и наличие/отсутствие потребности в лечении. Для уточнения диагноза мы предложим Вам осмотр неврологом и исследования на предмет нейроинфекций, аутоиммунного процесса (рассеянный склероз, аутоиммунный энцефаломиелит), ревматических заболеваний с вовлечением головного и/или спинного мозга. Результаты этих исследований внесут ясность в ситуацию и помогут правильно построить лечение, если оно потребуется.
Какие находки возможны:
 |  |
| Очаги демиелинизации на МРТ до и после лечения. Через 4 месяца от начала лечения видно уменьшение очагов – ремиелинизация (диагноз – рассеянный склероз, протекавший на фоне инфекции вирусом Эпштейн-Барр, микоплазмой и хламиией). Чем раньше начато лечение – тем лучше прогноз на восстановление. | |
 |
| Очаг демиелинизации в веществе спинного мозга |
Активны очаги демиелинизации или нет? МРТ головного мозга с контрастом, олигоклональный IgG в ликворе и крови
Наличие/отсутствие активности очагов демиелинизации в текущий момент времени может много прояснить в диагнозе и указывает на срочность лечения. Что такое активный очаг демиелинизации: это участок в головном или спинном мозге, где в настоящее время идет активный процесс разрушения миелина (обострение или дебют демиелинизирующего заболевания).
Ответ о происхождении и активности очагов демиелинизации в веществе головного мозга может дать МРТ с гадолиниевым контрастированием. Очаги, в которых демиелинизация идёт прямо сейчас, накапливают контрастное вещество, и это видно при МР-томографии.
Однако, очаги демиелинизации накапливают контраст только в период активного воспаления, и в стадии ремиссии (временной остановки заболевания) возможен ложноотрицательный результат. В этом случае диагноз можно уточнить с путем исследования олигоклонального IgG в ликворе и крови. Олигоклональный IgG дает информацию о наличии/отсутствии повышенной активности иммунной системы в головном и спинном мозге.
С достаточной степенью достоверности результаты исследования олигоклонального IgG и МРТ с контрастом трактуются так:
Как будет построено обследование при обнаружении очагов демиелинизации в головном или спинного мозге
 |  |
| Клинический осмотр неврологом при подозрении на рассеянный склероз. Проверка рефлексов, чувствительности, координации и т.д. | |
Если очаги демиелинизации активны (накапливают контраст), если нарастает неврологическая симптоматика – мы предложим лечение немедленно. В этой ситуации нужно срочно остановить разрушение головного и/или спинного мозга. В процессе лечения будем уточнять диагноз, и как только диагноз будет ясен – предложим Вам плановое лечение, исходя из результатов диагностики. Если на текущий момент активной демиелинизации нет – есть время спокойно разобраться в происходящем. Полученные данные исследований помогают понять причину демиелинизации и ложатся в основу схемы лечения.
Имеет ли практический смысл определять содержание основного белка миелина и антитела к миелину? Обычно не имеет. Почему:
Ревматическое заболевание с вовлечением мозга может имитировать картину рассеянного склероза
Хронические аутоиммунные болезни могут протекать длительно, скрыто, и напоминать МРТ-картину рассеянного склероза. В первую очередь следует иметь в виду васкулит и системную красную волчанку.
Васкулит – это атака иммунной системы против кровеносных сосудов собственного же организма. Сопровождается обескровливанием ткани, питаемой пострадавшим сосудом. При васкулите обнаруживаются характерные изменения в анализах крови (антитела к цитоплазме нейтрофилов), а кроме того, иногда можно обнаружить очаги васкулита на коже при простом осмотре. Системная красная волчанка может протекать с аутоиммунным повреждением мозга и периферических нервов. Лечение ревматических болезней, рассеянного склероза и других демиелинизирующих заболевания строится по-разному, поэтому правильно поставленный диагноз здесь очень важен.
Хроническая воспалительная демиелинизирующая полинейропатия (ХВДП) (информация для пациента)
Хроническая воспалительная демиелинизирующая полинейропатия (ХВДП)
Что означают эти термины?
Каковы причины развития заболевания?
Причины развития ХВДП до сих пор полностью не изучены. Однако результаты многочисленных исследований и эффективность иммуномодулирующей терапии указывают на нарушение работы иммунной системы, как ключевой причины развития заболевания. Иммунная система представляет собой очень сложный и гармоничный механизм. Ключевыми звеньями иммунной системы являются антитела, ряд белков сыворотки крови и белые клетки крови, лейкоциты. В норме иммунная система борется с чужеродными агентами (белки, вирусы, бактерии). Однако при ряде заболеваний (аутоиммунные заболевания) компоненты иммунной системы по ошибке начинают работать против собственного организма. К одним из таких заболеваний и относится ХВДП. В данном случае развивается реакция против компонентов оболочки периферических нервов, что проявляется в виде специфических симптомов, характерных для ХВДП.
В качестве триггерных факторов описаны респираторно-вирусные заболевания, оперативные вмешательства, беременность, вакцинация и другие причины, тем не менее прямая связь вышеуказанных факторов с развитием заболевания пока не доказана.
Возможна ли передача заболевания по наследству?
Нет. Существует ряд исследований, в которых выявлены гены, предполагаемые в развитии заболевания. Тем не менее, пока не доказано их участие в риске развития заболевания у потомков.
Как проявляется ХВДП и в чем особенности этого заболевания?
Точный механизм ХВДП до конца не раскрыт ввиду комплексности иммунных реакций, а потому симптоматика и характер течения заболевания могут варьировать. Отсюда выделены так называемые атипичные формы ХВДП, которые несколько отличаются от классического течения заболевания и могут иметь особенности прогноза и лечения. Диагностика таких форм может быть затруднена. К атипичным формам ХВДП относят:
На основании чего мне установили диагноз ХВДП?
Ключевым в постановке диагноза является клинический осмотр неврологом. Существуют критерии заболевания, предложенные Европейской федерацией неврологических сообществ в 2010 г. Для подтверждения диагноза и исключения альтернативных причин полинейропатии обычно проводится ряд лабораторных анализов, а также инструментальные методы исследования. К сожалению, до сих пор нет “золотого” стандарта диагностики, который с высокой точностью мог бы указывать на «ХВДП». Поэтому диагноз зачастую ставится на основании клинической картины и результатов исследования.
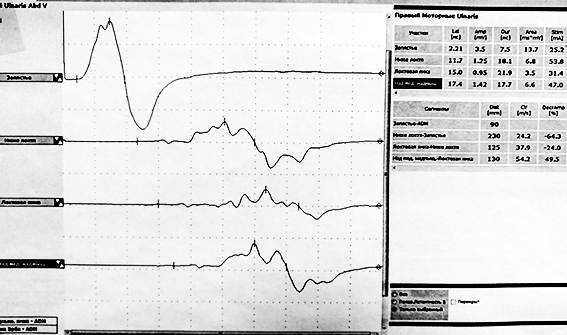
Ключевым инструментальным методом диагностики ХВДП, как и любой полинейропатии, является электронейромиография. Это исследование проводимости периферических нервов при помощи коротких электрических импульсов, передающихся по ходу нерва. Стимуляция приводит к сокращению мышцы, иннервируемой исследуемым нервом, которое регистрируется электродом.
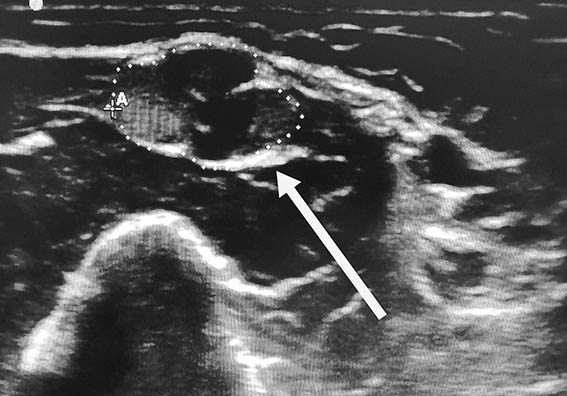
Если данных для установки диагноза окажется недостаточно, могут дополнительно проводиться МРТ сплетений, анализ спинномозговой жидкости, УЗИ периферических нервов и в редких случаях биопсия нерва. К одним из критериев правильности установленного диагноза относится улучшение состояния, либо приостановление прогрессирования заболевания на фоне патогенетической терапии.
Какие варианты лечения ХВДП существуют?
До 80% пациентов с ХВДП имеют эффект от терапии, модулирующей работу иммунной системы. На основании крупных исследований в лечении ХВДП доказанную эффективность имеют следующие варианты лечения:
Ни один из известных на сегодняшний день препаратов не излечивает ХВДП, только позволяет снизить активность заболевания, предупредить от дальнейшего ухудшения или обострения, а также уменьшить выраженность симптомов. Кроме того, ответ на лечение у разных людей может различаться.
Каждый способ лечения имеет свои плюсы и минусы, которые обговариваются врачом, учитывая все индивидуальные особенности?
Аналогичными по эффективности глюкокортикостероидам являются препараты человеческого иммуноглобулина, однако последние гораздо реже сопряжены с развитием побочных эффектов, а потому более безопасны. Пожалуй, главным недостатком такого лечения является его высокая стоимость. Препараты человеческого иммуноглобулина получают путем очистки большого количества (>10,000 л) человеческой плазмы (>1000 доноров), что обуславливает их дороговизну. Лечение заключается в ежемесячном курсовом внутривенном введении препарата. Курс обычно занимает 4-5 дней. В дальнейшем частота введения препарата может варьироваться в зависимости от его эффективности. Важным моментом является выбор препарата. Необходимо обратить внимание на его основные характеристики: препарат должен подходить для проведения высокодозной внутривенной иммунотерапии, содержание IgG должно быть не менее 95%, количества IgA и IgM должны быть следовыми. При этом количество IgA должно быть четко обозначено в инструкции, так как именно с этим классом иммуноглобулинов ассоциировано развитие аллергических реакций.
Третьим вариантом лечения является высокообъемный плазмаферез. Данный способ терапии представляет собой забор плазмы с патогенными антителами через катетер и восполнение ее стерильными растворами, белковыми растворами и/или донорской плазмой. Процедура повторяется около 5 раз, обычно с интервалом через день. Эффект от такого лечения сохраняется на протяжении 3-4 недель. Учитывая его сложность, такой способ терапии не используется для длительного лечения и часто бывает полезен в случае стремительного и\или тяжелого обострения.
У некоторых больных, несмотря на грамотное лечение, заболевание всё равно может прогрессировать или не поддаваться контролю. В этих случаях назначаются иммунодепрессанты (микофенолата мофетил, азатиоприн, циклоспорин, циклофосфамид) или моноклональные антитела (ритуксимаб). Назначение данных препаратов должно исходить от врача, имеющего опыт их применения, учитывая все показания и противопоказания, с последующим тщательным контролем эффективности и безопасности терапии.
Нужно ли вносить какие-либо изменения в привычный образ жизни?
Да. Существуют ряд рекомендаций для больных с диагнозом ХВДП:
Каковы прогнозы при данном заболевании?
Если у вас есть симптомы полинейропатии или вам поставлен диагноз «Полинейропатия» или «ХВДП», вы можете пройти комплексное обследование в Центре заболеваний периферической нервной системы ФГБНУ НЦН, где вам помогут уточнить диагноз, выявить причины поражения периферических нервов и назначат терапию с позиций доказательной медицины.
Сотрудники центра заболеваний периферической нервной системы консультируют пациентов амбулаторно в рамках ОМС и на коммерческой основе.
ЗАПИСЬ НА ПРИЕМ И ЭНМГ/иЭМГ ПО МНОГОКАНАЛЬНОМУ ТЕЛЕФОНУ
+7 (495) 374-77-76
+7 (985) 931-60-24
Демиелинизирующие заболевания
Демиелинизирующие заболевания
Связь между отдельными функциональными нервными клетками (нейронами) осуществляется через сложнейшую систему тонких проводниковых выростов, их ответвлений и сплетений (соотв., аксоны и дендриты, а также синапсы как точки коммутации). Эти микроскопические «соединительные кабели» нервной системы покрыты снаружи особой разновидностью мембраны – миелиновой оболочкой. Миелин примерно на 25-30% состоит из белка; остальная доля приходится на липидные (жировые) соединения. Насколько известно на сегодняшний день, миелиновая оболочка выполняет несколько функций: обеспечение механической прочности проводника, защита от разрушительных внешних воздействий на клеточном и молекулярном уровнях, питание аксона, его электрохимическая изоляция и ускорение трансляции нервного импульса. В будущем, вероятно, представления о предназначении миелиновой оболочки будут расширяться; сегодня принято считать, что две последние функции, – изоляционная и ускорительная, – являются важнейшими. Известно также, что по степени миелинизации аксонов центральной и периферической нервной системы (соотв., ЦНС и ПНС), организм человека превосходит организм любого другого вида живых существ, включая высших приматов. Возможно, именно этот биохимический механизм, случайно появившийся благодаря бесконечным спонтанным мутациям, а затем закрепленный и развившийся в ходе эволюции, обеспечил виду Homo Sapiens не только надежное выживание, но и доминирующее положение в биосфере планеты.
В норме процессы демиелинизации (естественный распад миелинового слоя) и ремиелинизации (его восстановление) уравновешены и продолжаются, по-видимому, в течение всей жизни. Однако в силу ряда неблагоприятных условий, внешних и/или внутренних, процесс разрушения миелиновых оболочек может оказаться форсированным. Вообще, пробой или деструкция миелинового слоя является наиболее типичным вариантом повреждения нервных клеток. Если же демиелинизация обретает прогредиентный характер, т.е. неуклонно прогрессирует, то при поражении 40-60% всех миелиновых оболочек развиваются полиморфные или, реже, моносимптомные неврологические синдромы, совокупность которых обобщается термином «демиелинизирующие заболевания».
Таким образом, демиелинизирующие заболевания – это обширная группа патологических процессов, основу которых составляет разрушение миелиновых оболочек аксонов. При этом могут преимущественно страдать различные участки ЦНС или ПНС, – что неизбежно сказывается на функциональной состоятельности этих зон и проявляется соответствующей клиникой, – либо вовлекаться нервная система в целом, что приводит к генерализации симптоматики.
Причины
По патогенетическому критерию в группе демиелинизирующих заболеваний условно различают миелинопатии и миелинокластии. Первый термин подразумевает аномальную, нестойкую биохимическую структуру самого миелина (обычно вследствие генетических нарушений), второй – разрушение оболочек какими-либо факторами. Условность же такой классификации заключается в том, что генетически обусловленная миелинопатия может запускаться внешними причинами, и наоборот, – у больных с приобретенными миелинокластиями в анамнезе нередко обнаруживается наследственная предрасположенность.
Демиелинизирующими являются наследственные болезни Тея-Сакса, Лебера, Ниманна-Пика, Канавана, Александера, некоторые лейкодистрофии и ферментопатии.
К приобретенным миелинокластиям с воспалительным компонентом относятся некоторые процессы, обусловленные хронической гипоксией или локальной ишемией (дефицитом кровоснабжения), алиментарными факторами (бедный витаминами рацион, недостаток питательных веществ), вирусной инфекцией, иммунопатологическим откликом на введение вакцин, а также интоксикациями, в т.ч. алкогольными.
Симптоматика
Учитывая вышесказанное, нетрудно представить себе многообразие клинической картины демиелинизирующих заболеваний: она зависит от преимущественной локализации (или генерализации) очагов разрушения миелина, то есть может включать в себя фактически любые психоневрологические симптомы и синдромы: моторные, перцептивные, когнитивные (деменция), атактические (нарушения равновесия и координации), речевые, тазовые, аффективные, экстрапирамидные и т.д. Вместе с тем, сама по себе демиелинизация не имеет собственной симптоматики, – по крайней мере, патогномоничные ее признаки на сегодняшний день неизвестны.
Очень различаются такие заболевания и в части прогноза: от медленного плавного прогрессирования в течение десятилетий до быстрого неостановимого нарастания с летальным исходом через несколько месяцев.
Диагностика
Во многих случаях прижизненная диагностика демиелинизирующих заболеваний весьма сложна и проблематична. Необходимо глубокое изучение всех доступных анамнестических сведений в сопоставлении с клиникой и данными объективизирующих исследований. Из инструментальных методов наиболее информативными являются МРТ и электронейромиография, из лабораторных – различные иммунологические анализы.
Лечение
Основными направлениями терапии демиелинизирующих заболеваний выступают, как правило, назначение противовоспалительных гормонов, иммуносупрессоров, иммунокорректоров и иммуномодуляторов, а также ноотропов, нейропротекторов и других средств по показаниям. Как правило, необходим пересмотр образа жизни, категорический отказ от вредных привычек, соблюдение особого щадящего режима нагрузок и отдыха. Единой этиопатогенетической схемы лечения пока нет, терапия чаще всего носит паллиативный, симптоматический характер. Ведутся активные исследования в поисках способов интенсивной ремиелинизации; наиболее перспективными считаются разработки в области генной и гормональной терапии.
Что такое демиелинизирующий процесс
Кафедра неврологии и нейрохирургии Ярославской государственной медицинской академии
Демиелинизирующий процесс при системных ревматических заболеваниях (обзор литературы)
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2012;112(9-2): 64-72
Пизова Н. В. Демиелинизирующий процесс при системных ревматических заболеваниях (обзор литературы). Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2012;112(9-2):64-72.
Pizova N V. Demyelinating process in systemic rheumatoid diseases (review). Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2012;112(9-2):64-72.
Кафедра неврологии и нейрохирургии Ярославской государственной медицинской академии
Кафедра неврологии и нейрохирургии Ярославской государственной медицинской академии
Системные ревматические заболевания (СРЗ), основные из которых представлены в таблице, являются мультифакториальными болезнями. 
В настоящее время РС считается хроническим воспалительным заболеванием ЦНС, характеризующимся множественными очагами демиелинизации в белом веществе головного и спинного мозга и гибелью аксонов [99]. Причина РС неизвестна, считается, что определенную роль играют вирусная инфекция и аутоиммунные процессы, поэтому РС длительное время принимался за аутоиммунное заболевание. Сегодня диагноз РС может быть поставлен только при наличии всех указанных критериев. Поэтому достоверный диагноз иногда выставляется через длительное время от манифестации заболевания [28, 32, 64, 98, 118, 163]. Признаком РС являются очаги демиелинизации, состоящие из гипоинтенсивных участков с олигодентроцитами и потерей миелина, дегенерацией аксонов, глиотическими изменениями и периваскулярной воспалительной инфильтрацией, состоящей в основном из лимфоцитов и макрофагов [32, 64, 118, 163]. Также показано, что гипоксическое метаболическое повреждение может в некоторых случаях способствовать воспалительному повреждению белого вещества, но формирование мелких сосудистых инфарктов при РС не описано [12, 32]. Существующие данные позволяют считать РС мультифакториальным заболеванием.
КИС представляет не менее сложную диагностическую проблему, так как может быть не только манифестным проявлением РС, но встречаться и при некоторых СРЗ: АФС, СКВ, болезни Бехчета (ББ), синдроме Шегрена (СШ). Иммунологическая природа этих заболеваний, поражаемая популяция, рецидивирующее или ремиттирующее течение, неврологические проявления и наличие множественных очагов в белом веществе на МРТ делают их трудноразличимыми [46, 72, 73, 78, 84, 132, 143, 147].
ОН, ПМ, синдром Девика могут быть первым дебютным проявлением различных аутоиммунных заболеваний. При ошибочной постановке диагноза РС пациентам с ревматическими заболеваниями последствия могут оказаться трагическими, так как назначенное лечение (например, интерферон-β) для предполагаемого РС может вызвать обострение СРЗ [34, 46, 52, 73, 132].
Большинство клинических проявлений при СКВ (головная боль, эпилептические приступы), симптомы поражения периферической нервной системы и психические расстройства встречаются и у пациентов с РС [52]. Поэтому столь важно использование МРТ, которая стала одной из часто выполняемых диагностических процедур. F. Barkhof и соавт. [31] представили МРТ-критерии, специфичные и чувствительные для РС. Важны и нейроморфологические исследования, которые позволяют выявить мелкие множественные очаги демиелинизации. Но они могут определяться как при РС, так и быть результатом мелких инфарктов, которые случаются при СКВ и АФС. При этом в последних случаях они могут быть клинически «немыми». Такие феномены, как «пальцы Доусона» и «черные дыры», наиболее характерны для РС, но не патогномоничны [22, 29, 31, 52]. Поэтому многие исследователи считают, что все пациенты с ПМ должны быть осмотрены для исключения СКВ и/или АФС с учетом анамнеза, клинической картины и наличия антител к фосфолипидам (АФЛ) в крови.
Остановимся более подробно на отдельных системных ревматических заболеваниях.
СКВ входит в группу аутоиммунных ревматических заболеваний. Она развивается на основе генетически обусловленного несовершенства иммунорегуляторных процессов, приводящего к образованию множества антител к собственным клеткам и их компонентам и возникновению иммунокомплексного воспаления, следствием этого является повреждение многих органов и систем [2, 3, 9]. Диагноз СКВ требует клинического и серологического подтверждения, и пациенты должны соответствовать критериям, разработанным Американской коллегией ревматологов [156]. Должно определяться наличие не менее 4 из 11 критериев.
Демиелинизирующие заболевания
1. Что представляет собой группа демиелинизирующих заболеваний?
Термин «демиелинизирующие» применим в отношении любых заболеваний, связанных с повреждением белого мозгового вещества, однако более правильно к демиелинизирующей патологии относить нарушения, непосредственно связанные с поражением миелина. Эта группа заболеваний весьма неоднородна как по этиологии, так и по патогенезу. В последние годы отмечается существенный рост числа пациентов, инвалидизированных вследствие разрушения миелина, поэтому изучение группы демиелинизирующих заболеваний является актуальной проблемой современной неврологии.
Миелин – специфический вид клеточной мембраны, которая окружает аксоны (отростки нервных клеток). Он присутствует как в центральной, так и в периферической нервной системе. Роль миелина довольно существенна (питание, передача нервных импульсов, изоляция, опорно-барьерная функция), поэтому любые изменения в структуре этой оболочки негативно отражаются на работе самих нервных отростков, что вызывается серьёзные прогрессирующие заболевания.
Специфика демиелинизирующей патологии в том, что синтез миелина как таковой у больных не нарушен. Патология заключается в последующем разрушении нормальной миелиновой оболочки.
2. Причины и классификация демиелинизирующих заболеваний
Наличие демиелинизирующих заболеваний у ближайших родственников всегда выступает фактором отнесения к группе риска, поскольку значимость наследственной предрасположенности подтверждена. Семейный анамнез, отягощённый этими заболеваниями, существенно повышает вероятность их развития.
Классификация демиелинизирующих заболеваний основывается на этиологии и локализации процессов демиелинизации.
По зоне, в которой наблюдается разрушению миелина, заболевания делятся на те, что затрагивают ЦНС и ПНС.
3. Симптомы и диагностика демиелинизирующих заболеваний
Клиническая картина различных демиелинизирующих заболеваний сильно варьирует, поскольку зависит от локализации патологического процесса и объёма вовлечённых в него нервных тканей.
Существенным фактором также является характер течения, которое может быть острым монофазным, прогрессирующим или ремитирующим.
Кроме того, степень клинических проявлений находится в зависимости от числа очагов разрушения миелина. Различают монофокальные, мультифокальные и диффузные демиелинизирующие процессы.
Наличие этих нарушений в любом сочетании позволяет предположить наличие демиелинизирующей патологии того или иного типа.
Диагностика ДЗ опирается на МРТ и электромиографию. При поражении центральной нервной системы наиболее информативна магниторезонансная томография, позволяющая выявить очаги разрушения миелина диаметром от 3 мм. Электромиография показательна при периферическом поражении.
Также проводятся иммунологические и генетические исследования с целью оценки роли наследственного фактора в развитии патологии.
4. Лечение
Лечение при демиелинизирующих заболеваниях сочетает патогенетические мероприятия и симптоматическую помощь. Новые препараты и достижения генной инженерии позволили в последние годы достичь существенного прогресса в терапии ДЗ.
Препаратами первого выбора являются бета-интерфероны, которые на 30% снижают частоту обострений при рассеянном склерозе.
Также хорошую эффективность показывает внутривенное введение иммуноглобулинов.
Более 20 лет применяется технология иммунофильтрации ликвора, которая оказывает положительное влияние, замедляя развитие патологического процесса. Эта методика для многих больных остаётся актуальной и по сей день.
Также по показаниям могут быть назначены кортикостероиды, миорелаксанты, цитостатики, нейропротекторы, плазмаферез.