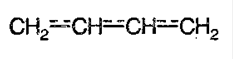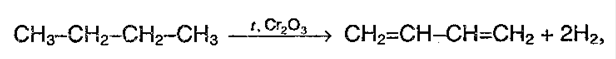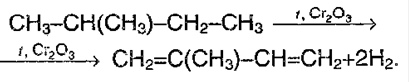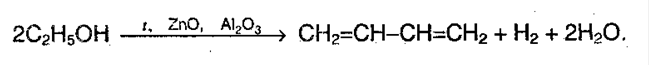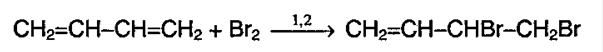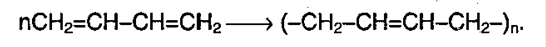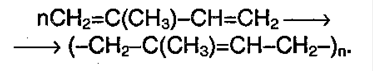Диены — номенклатура, получение, характерные химические свойства
Алкадиены (диены) – непредельные алифатические углеводороды, молекулы которых содержат две двойные связи. Общая формула алкадиенов СnH2n-2.
Свойства алкадиенов в значительной степени зависят от взаимного расположения двойных связей в их молекулах. По этому признаку различают три типа двойных связей в диенах:
1) изолированные двойные связи разделены в цепи двумя или более s-связями:
2) кумулированные двойные связи расположены у одного атома углерода:
СН2=С=СН2 (подобные диены (аллены) менее стабильны, чем другие диены и при нагревании в щелочной среде перегруппировываются в алкины);
3) сопряженные двойные связи разделены одной s-связью:
Перекрывание р-орбиталей молекулы бутадиена имеет место не только между С1 – С2, С3 – С4, но и между С2 – С3. В связи с этим применяют термин: «сопряженная система». Следствием делокализации электронной плотности является то, что длины связей С1 – С2 (С3 – С4) увеличены, по сравнению с длиной двойной связи в этилене (0,132 нм) и составляют 0,137 нм; в свою очередь, длина связи С3 – С4 меньше, чем в этане С – С (0,154 нм) и составляет 0,146 нм. Диены с сопряженной системой двойных связей более энергетически выгодны.
Номенклатура алкадиенов
По правилам IUPAC главная цепь молекулы алкадиена должна включать обе двойные связи. Нумерация атомов углерода в цепи проводится так, чтобы двойные связи получили наименьшие номера. Названия алкадиенов производят от названий соответствующих алканов (с тем же числом атомов углерода) с добавлением окончания –диен.
Виды изомерии алкадиенов:
Структурная изомерия:
1) изомерия положения сопряженных двойных связей;
2) изомерия углеродного скелета;
3) межклассовая (изомерны алкинам)
Пространственная изомерия — диены, имеющие различные заместители при углеродных атомах у двойных связей, подобно алкенам, проявляют цис-транс-изомерию.
Способы получения алкадиенов

Химические свойства алкадиенов

Для сопряженных диенов характерны реакции присоединения (реакции 1, 2). Наличие сопряженной системы p-электронов приводит к особенностям реакций присоединения. Сопряженные диены способны присоединять не только по двойным связям (С1 и С2, С3 и С4), но и к концевым (С1 и С4) атомам углерода сообразованием двойной связи между С2 и С3. Соотношение продуктов 1,2- и 1,4-присоединения зависит от температуры, при которой проводился эксперимент и от полярности применяемого растворителя.
Восстановление (реакция 3) с помощью [Na + C2H5OH] называется восстановлением водородом в момент выделения (при взаимодействии натрия и спирта выделяется водород). Алкены в таких условиях не восстанавливаются, это отличительное свойство сопряженных диенов.
Полимеризация (реакция 4) важнейшее свойство сопряженных диенов, которая происходит под действием различных катализаторов (AlCl3, TiCl4+(C2H5)3Al) или света. В случае применения определенных катализаторов можно получить продукт полимеризации с определенной конфигурацией цепей.
Цис-конфигурацию имеет натуральный каучук. Макромолекулы натурального каучука имеют спиралевидную структуру цепи из-за того, что изопреновые звенья изогнуты, что создает пространственные препятствия упорядоченному расположению цепей. В каучуке длинные молекулы скручены в спутаны друг с другом в спирали. При растяжении каучука спирали растягиваются, а при снятии напряжения они снова скручиваются. В природе существует еще другой полимер изопрена гуттаперча (транс-конфигурация). Гуттаперча обладает стержнеобразной структурой цепи из-за выпрямленности изопреновых звеньев (цепи с транс-конфигурацией двойных связей могут располагаться одна вдоль другой), поэтому гуттаперча твердый, но хрупкий полимер. Натуральный каучук имеют немногие страны и поэтому его заменяют синтетическими каучуками из дивинила, а также из изопрена.
Для практического использования каучуки превращают в резину.
Резина – это вулканизованный каучук с наполнителем (сажа). Суть процесса вулканизации заключается в том, что нагревание смеси каучука и серы приводит к образованию трехмерной сетчатой структуры из линейных макромолекул каучука, придавая ему повышенную прочность. Атомы серы присоединяются по двойным связям макромолекул и образуют между ними сшивающие дисульфидные мостики.
Сетчатый полимер более прочен и проявляет повышенную упругость – высокоэластичность (способность к высоким обратимым деформациям).
В зависимости от количества сшивающего агента (серы) можно получать сетки с различной частотой сшивки. Предельно сшитый натуральный каучук – эбонит – не обладает эластичностью и представляет собой твердый материал.
Диены
Алкадиены — класс углеводородов, содержащих две двойных связи углерод-углерод.
Содержание
Классификация
В зависимости от взаимного расположения двойных связей диены подразделяются на три группы:
Обычно к диенам относят ациклические и циклические 1,3-диены, образующие гомологические ряды общих формул 

Физические свойства
Реакционная способность
Реакции алленов
Центральный sp-гибридизованный атом углерода в алленах является электрофильным центром, поэтому, в отличие от не активированных электронакцепторными заместителями алкенов, аллены реагируют с мягкими нуклеофилами, образуя винильные и аллильные производные:
CH2=C=CH2 + PhSH 
Электрофильность sp-гибридизованного атома алленов повышается электроноакцепторными группами, в этом случае присоединение нуклеофила идет исключительно по этому атому:
CH2=C=CHCOOR + NuH 
Гидратации аллена в условиях кислотного катализа присоединение протона идёт по терминальному углероду, образующийся при этом енол далее таутомеризуется в ацетон:
CH2=С=CH2 + H2O 

Под действием щелочей или кислот аллены могут претерпевать прототропные перегруппировки в 1,3-диены:
RCH2CH=C=CH2 
Реакции 1,3-диенов
Специфика реакционной способности 1,3-диенов обусловлена мезомерией вследствие сопряжения двойных связей:

Результатом является то, что в случае электрофильного присоединения к сопряженным диенам типичны реакции 1,4-присоединения, идушие через промежуточное образование резонансно стабилизированных аллильных карбокатионов:
Х = Hal, H, Y = Hal, OH
Сопряженные диены легко полимеризуются по механизму 1,4-присоединения, реакция полимеризации 1,3-диенов лежат в основе синтеза диеновых каучуков.

Получение
Формально эту реакцию можно представить как дегидратацию двух молекул этилового спирта с одновременным межмолекулярным дегидрированием.
Алкадиены. Свойства алкадиенов.
Алкадиены – непредельные углеводороды, в состав которых входят две двойные связи. Общая формула алкадиенов – CnH2n-2.
Если двойные связи находятся в углеродной цепи между двумя или боле атомов углерода, то такие связи называются изолированными. Химические свойства таких диенов не отличаются от алкенов, только в реакцию вступают 2 связи, а не одна.
Если же диен выглядит так: С=С=С, то такая связь является кумулированной, а диен называется – алленом.
Строение алкадиенов.
π-электронные облака двойных связей перекрываются между собой, образуя единое π-облако. В сопряженной системе электроны делокализованы по всем атомам углерода:
Чем длиннее молекула, тем она более устойчива.
Изомерия алкадиенов.
Для диенов характерна изомерия углеродного скелета, изомерия положения двойных связей и пространственная изомерия.
Физические свойства алкадиенов.
Бутадиен-1,3 – легко сжижающийся газ с неприятным запахом. А изопрен – жидкость.
Получение диенов.
1. Дегидрирование алканов:
2. Реакция Лебедева (одновременное дегидрирование и дегидратация):
Химические свойства алкадиенов.
Химические свойства алкадиенов обусловлены наличием двойных связей. Реакция присоединения может протекать в 2х направлениях: 1,4 и 1,2 – присоединение. Например,
Способность алкадиенов к полимеризации:
Для получения изопренового каучука используют реакцию при воздействии металлоорганических катализаторов:
Применение алкадиенов.
Основная сфера использования диенов и их производных – это производство каучука.
Новости
Диены
Алкадиенами (диенами) называют органические вещества, относящиеся к группе непредельных углеводородов, которые содержат в своей структуре две двойные связи. Диены имеют общую формулу – СnH2n-2.
Номенклатура и изомерия
Названия алкадиенов формируются с помощью добавления к корню соответствующего алкана окончания «диен», при этом указывая положение кратных связей.
Для диенов характерны несколько типов изомерии:
Классификация
По принципу расположения кратных связей различают алкадиены:
Химические свойства
Для диеновых углеводородов характерны реакции, которые протекают по механизмам радикального и электрофильного присоединения. Причём диены с сопряжёнными двойными связями обладают большей реакционной способностью.
Алкадиены способны присоединять к себе галогены, галогенводороды, воду по механизму электрофильного присоединения.
1,2 – присоединение: СН2 = СН – СН = СН2 + Br2 → СН2Br – СНBr – СН = СН2
1,4 – присоединение: СН2 = СН – СН = СН2 + Br2 → СН2Br – СН = СН – СН2Br
СН2 = СН – СН = СН2 + H2O → СН3 – СНOH – СН = СН2
СН2 = СН – СН = СН2 + HCl→ СН3 – СНCl – СН = СН2
В присутствии никелевого или платинового катализатора происходит полное гидрирование с образованием соответствующего алкана. Реакция сопровождается выделением тепла.
n(СН2 = СН – СН = СН2) → ( – СН2– СН = СН –СН –)n
Получение
Существует несколько способов получения алкадиенов:
1) Дегидрирование углеводородов под действием платинового, палладиевого или никелевого катализатора при нагревании:
СН3 – СН2 – СН2 – СН3 → СН2 = СН – СН = СН2 + 2Н2
Метод используется только в промышленности!
2) Дегидратация двухосновных спиртов (протекает при нагревании в присутствии концентрированной серной кислоты):
3) Взаимодействие галогенпроизводных алкенов с металлическим натрием (реакция Вюрца):
2СН2 = СН – СН2Cl + 2Na → СН2 = СН – СН2 – СН2 – СН = СН2 + 2NaCl
4) Дегидрирование и дегидратация этилового спирта (реакция Лебедева):
Данная реакция проходит при действии катализаторов на основе оксидов цинка и алюминия, а также температуре 440˚С.
Применение
Диеновые углеводороды в большинстве своём используют при производстве синтетического каучука.
Каучук — эластомер, который используется для изготовления клея, машинных шин, резин с различными полезными свойствами (эластичность, малая истираемость, термостойкость, кислотостойкость и т.д.).
Еще по этой теме:
Серная кислота
Основные сведения о серной кислоте: свойства, получение, применение.
Теперь «ХиШник» стал полностью бесплатным
Как развивалось приложение все эти годы, и почему мы им так гордимся.
Азотная кислота
Статья содержит основную информацию об азотной кислоте: её свойства, получение и применение.
Правило Марковникова
Правило Марковникова: формулировка, механизм протекания реакций, исключения из правила.
Таблицы для ЕГЭ по химии
В статье представлены таблицы, необходимые при изучении химии и сдаче ЕГЭ.
Внеклассное мероприятие по химии
Идеи интересных внеклассных мероприятий по химии.
Формулы для решения задач по химии
Перечень основных формул, которые используются при решении школьных задач по химии.
Химические профессии
Обзор необычных профессий, связанных с химией.
ЕГЭ по химии 2019
Основная информация о ЕГЭ по химии 2019: структура экзамена, баллы, даты проведения.
Критерии оценивания ОГЭ по химии, баллы 2019
Подробно расскажем о баллах ОГЭ по химии 2019, методах и критериях оценивания заданий и переводе первичных баллов в школьную оценку.
Изменения ОГЭ по химии в 2019 году
Расскажем об изменениях, которые ждут школьников при сдаче ОГЭ по химии в 2019 году.
Подготовка к ОГЭ по химии
Несколько советов и рекомендаций, следуя которым подготовка к ОГЭ по химии будет проходить результативно.
Онлайн тесты по химии
Немного информации о проверке знаний с помощью тестов по химии в режиме онлайн.
Все об ОГЭ по химии в 2019
Основные сведения об ОГЭ по химии 2019: даты, время, баллы, материалы для подготовки.
Тест по химии 11 класс
Рассказываем о тестах по химии, используемых для проверки знаний в 11 классе.
Тест по химии 10 класс
Общие сведения о тестах по химии в 10 классе.
Тест по химии 9 класс
Рассказываем о тестах по химии, используемых для проверки знаний в 9 классе.
Тест по химии 8 класс
Рассказываем в общих чертах о тестах по химии в 8 классе
Ионная связь
Статья, содержащая в себе базовые понятие об ионном виде химической связи.
Водородная связь
Статья о водородном типе химической связи и его особенностях.
Подготовка к ЕГЭ по химии с нуля
В статье дано несколько действенных советов по подготовке к ЕГЭ по химии «с нуля».
Металлическая связь
Продолжаем серию статей про виды химической связи.
Ковалентная связь
Начинаем серию статей про виды химической связи.
Шкала перевода баллов ЕГЭ по химии 2018
Отвечаем на вопросы о системе оценивания и переводе первичных баллов в тестовые.
Учимся на летних каникулах
Размышляем о том, как полезно провести время во время летнего отдыха на каникулах. (в статье есть подарок внимательным читателям)
«ХиШник» приехал на Сахалин!
Этим летом открывается очередная летняя сессия областной профильной школы для одаренных детей «Эврика».
Мой сын увлёкся химией, что делать?
Собрали ТОП-5 полезных материалов для старшеклассника.
Двенадцать сервисов для изучения химии, с которыми ты точно сдашь
Великолепная подборка полезных сайтов для самостоятельного изучения химии.
О правах и обязанностях в школе: почему необходимо сотрудничество учеников и учителей
Что такое право само по себе и откуда оно берется. Как не заработать славу скандалистов, «вечно качающих права», и при этом не переносить безропотно нарушение своих личных границ…
Современный задачник по химии
материал о том, какие виды задачников по химии существуют и как среди них ориентироваться.
Выбираем репетитора по химии: инструкция
Научиться решать задачи по химии легко: следуем инструкции
Учимся решать задачи по химии к ОГЭ, ЕГЭ, инструкция от ХиШника
Изменения в ЕГЭ по химии 2018 года, новая демоверсия, спецификация, кодификаторы ЕГЭ
ФИПИ снова решил усложнить нам жизнь новыми требованиями к ЕГЭ. О том, почему изменения не всегда плохи, и как встретить их с достоинством.
Обновление в демонстрационной версии «ХиШника»
Мы расширили приветственное окно, чтобы при входе в приложение всем новым пользователям были понятны основные принципы работы «ХиШника».
Активация лицензионного ключа и первые шаги в «ХиШнике».
Что такое лицензионный ключ и как происходит его активация в приложении
Современный урок химии по ФГОС
Для чего нужны стандарты, по которым происходит обучение химии в российских школах, и как приложение “ХиШник” поможет соответствовать этим стандартам?
ХиШник в школе: ИКТ на уроках химии
Как наше приложение поможет внедрить ИКТ в уроки
Ура! Новые планы ХиШника и подарочки
Подводим итоги 2017, планируем 2018 и, конечно же, дарим подарки!
Родина приложения «ХиШник» – Новосибирский Академгородок
Почему же родиной «ХиШника» стал Новосибирский Академгородок?
Совпадение не случайное.
Можно ли просматривать историю решения задач учениками в онлайн-режиме?
Итак, «ХиШник» это приложение, в котором могут работать и ученики, и преподаватели. После того, как преподаватель создает в приложении учебную группу
Можно ли заниматься в «ХиШнике» со смартфона/планшета?
Сегодня у нас вопрос, которого мы давно ждали: можно ли заниматься в «ХиШнике» со смартфона/планшета?
Семинар от «ХиШника» на КПК для учителей химии
На прошлой неделе мы провели семинар в рамках масштабных ежегодных курсов повышения квалификации на базе СУНЦ НГУ (Новосибирск, Академгородок).
Команда «ХиШника» провела мастер-класс для преподавателей химии и методистов
Вчера команда «ХиШника» провела мастер-класс для преподавателей химии и методистов программ повышения квалификации из разных регионов России.
Как купить полный доступ к приложению?
Сегодня новый вопрос: что делать, если решать задачи в демо-версии приложения понравилось, как получить полный доступ? Отвечаем!
«ХиШник» представляет два кейса на ярмарке кейсов «Школа реальных дел»
Ярмарка кейсов «Школы реальных дел» – уже в эту пятницу! В этом году «ХиШник» представляет два кейса.
Служба поддержки:
support@hishnik-school.ru
Для СМИ:
onp@alekta.ru
Спасибо!
Настоящее пользовательское (лицензионное) соглашение (далее – «Соглашение») заключается между Обществом с ограниченной ответственностью «АЛЕКТА» (далее – «Лицензиар»), и Пользователем (физическим лицом, выступающем в роли конечного потребителя Продукта) совместно именуемые «Стороны».
Пожалуйста, внимательно ознакомьтесь с текстом настоящего Соглашения. Оно представляет собой публичную оферту и, после его принятия Вами, образует соглашение между Вами (Пользователем) и Лицензиаром о предмете и на условиях, изложенных в тексте Соглашения.
Принимая настоящее Соглашение, Вы соглашаетесь с положениями, принципами, а также соответствующими условиями лицензионного соглашения, изложенными ниже.