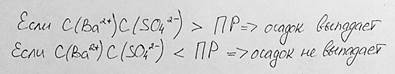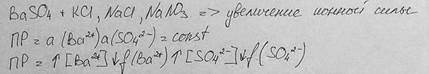Дробное осаждение
Смотреть что такое «Дробное осаждение» в других словарях:
дробное осаждение — frakcinis nusodinimas statusas T sritis chemija apibrėžtis Tirpinio sudedamųjų dalių atskyrimas nusodinimo būdu. atitikmenys: angl. fractional deposition; fractional precipitation rus. дробное осаждение … Chemijos terminų aiškinamasis žodynas
дробное осаждение — фракционное осаждение … Cловарь химических синонимов I
фракционное осаждение — дробное осаждение … Cловарь химических синонимов I
Хлопин, Виталий Григорьевич — В Википедии есть статьи о других людях с такой фамилией, см. Хлопин. Виталий Григорьевич Хлопин Дата рождения … Википедия
Лантаноиды — (от Лантан и греч. еidos образ, вид) лантаниды, семейство из 14 химических элементов с атомным номером от 58 до 71, расположенных в 6 м периоде системы Менделеева вслед за лантаном (табл. 1). Л. и сходные с ними элементы Скандий, Иттрий и … Большая советская энциклопедия
Нефть — (Oil) Нефть это горючая жидкость Добыча и переработка запасов нефти является основой экономики многих стран Содержание >>>>>>>>>>>>>>>>> … Энциклопедия инвестора
fractional deposition — frakcinis nusodinimas statusas T sritis chemija apibrėžtis Tirpinio sudedamųjų dalių atskyrimas nusodinimo būdu. atitikmenys: angl. fractional deposition; fractional precipitation rus. дробное осаждение … Chemijos terminų aiškinamasis žodynas
fractional precipitation — frakcinis nusodinimas statusas T sritis chemija apibrėžtis Tirpinio sudedamųjų dalių atskyrimas nusodinimo būdu. atitikmenys: angl. fractional deposition; fractional precipitation rus. дробное осаждение … Chemijos terminų aiškinamasis žodynas
frakcinis nusodinimas — statusas T sritis chemija apibrėžtis Tirpinio sudedamųjų dalių atskyrimas nusodinimo būdu. atitikmenys: angl. fractional deposition; fractional precipitation rus. дробное осаждение … Chemijos terminų aiškinamasis žodynas
Горная порода — (Rock) Горная порода это совокупнность минералов, образующая самостоятельное тело в земной коре, вследстие природных явлений Группы горных пород, магматические и метаморфические горные породы, осадочные и метасоматические горные породы, строение… … Энциклопедия инвестора
Гетерогенные равновесия в аналитической химии. Способы выражения растворимости малорастворимых электролитов.
Гетерогенное равновесие – равновесие, устанавливающее на границе фаз (два типа: осадок какого-либо вещества, находящийся в равновесии с насыщенным раствором того же вещества и две равновесные жидкие фазы: водный раствор и орг. растворитель)
Способы выражения растворимости малорастворимых электролитов
6. Произведение растворимости малорастворимого сильного электролита– это величина, равна произведению равновесных активностей (или равновесных концентраций) ионов данного электролита в его насыщенном растворе в степенях, равных соответствующим стехиометрическим коэффициентам.
BaSO4 = Ba 2+ + SO4 2- (в растворе)
Условие образования осадков малорастворимых сильных электролитов
Дробное осаждение и дробное растворение осадков
Дробное осаждение – последовательное осаждение ионов из анализируемого раствора при действии какого-либо общего реагента вследствие различной растворимости образующегося в результате реакции малорастворимого соединения.
Дробное растворение – последовательное растворение ионов из осадка.
Перевод одних малорастворимых электролитов в другие
Влияние посторонних электролитов на растворимость малорастворимых сильных электролитов
Влияние добавок электролита с одноименным ионом на растворимость
Растворимость малорастворимого электролита уменьшается при введении в раствор сильных электролитов, содержащих одноименные ионы с осадком.
Влияние добавок постороннего (индифферентного) электролита на растворимость
При увеличении ионной силы, коэффициент активности f уменьшается (по Деббаю-Хюккелю)
Солевой эффект: растворимость осадков увеличивается при введении в раствор сильных электролитов, не имеющих с осадком общих ионов.
11. Влияние различных факторов на полноту осаждения осадков и их растворение:природа осаждаемого вещества, осадителя, растворителя; концентрация реагентов; температура; рН среды; присутствие посторонних веществ, как имеющих, так и не имеющих одноименные ионы с осадком; характер образующегося осадка (аморфный, кристаллический); возможность протекания побочных реакций.
Протолитические равновесия. Понятие о протолитической теории кислот и оснований.
Дата добавления: 2020-04-25 ; просмотров: 589 ; Мы поможем в написании вашей работы!
Факторов на полноту осаждения осадков и их растворение
Гетерогенные равновесия в аналитической химии. Способы выражения
Растворимости малорастворимых электролитов. Произведение
Растворимости малорастворимого сильного электролита. Условие
Образования осадков малорастворимых сильных электролитов. Дробное
Осаждение и дробное растворение осадков. Перевод одних
Малорастворимых электролитов в другие. Влияние посторонних
Электролитов на растворимость малорастворимых сильных электролитов(влияние добавок электролита с одноименным ионом, влияние добавок
Постороннего (индифферентного) электролита). Влияние различных
факторов на полноту осаждения осадков и их растворение.
—————-Гетерогенные равновесия в аналитической химии (в аналитике)————————————
Закон действующих масс применим как к гомогенным равновесиям (например, к равновесиям в жидких растворах), так и к гетерогенным равновесиям, т. е. к равновесиям в гетерогенных системах.
Гетерогенное равновесие˗ это равновесие, устанавливающееся на границе раздела фаз.
В аналитической химии часто встречаются гетерогенные системы и равновесия двух типов: осадок (твердая фаза) какого-либо вещества, находящийся в равновесии с насыщенным раствором того же вещества (жидкая фаза), и две равновесные жидкие фазы, например, водный раствор и органический растворитель, не смешивающиеся друг с другом, между которыми распределено растворенное вещество, находящееся в равновесии с обеими жидкими фазами.
Примером системы первого типа может служить насыщенный водный раствор сульфата бария ВаSO4, находящийся в равновесии с осадком сульфата бария.
Примером системы второго типа может служить экстракционная система, состоящая из слоя жидкого тетрахлорида углерода 

В гетерогенной системе при постоянной температуре рано или поздно самопроизвольно достигается состояние равновесия.
Под растворимостью обычно подразумевают концентрацию насыщенного раствора данного вещества при определенной температуре. Используют различные способы выражения растворимости, например, массовую растворимость вещества 

^ Массовая растворимость вещества ст — это масса растворенного вещества в граммах, содержащаяся в одном литре его насыщенного раствора:

где т ˗ масса растворенного вещества, г; V ˗ объем насыщенного раствора, л. Массовая растворимость вещества выражается в г/л.
^ Молярная растворимость вещества 

где т ˗ масса растворенного вещества, г; М ˗ молярная масса растворенного вещества в г/моль; V ˗ объем насыщенного раствора, л. Молярная растворимость вещества выражается в моль/л.
Применяются и другие способы выражения растворимости и иные обозначения.
Растворимость малорастворимого сильного электролита зависит от его природы и природы растворителя, температуры, давления (обычно зависимость от давления мала, если не поглощаются и не выделяются газообразные вещества), присутствия других электролитов в растворе (как имеющих, так и не имеющих одноименные ионы с рассматриваемым малорастворимым электролитом), а также различных веществ (в том числе нейтральных молекул), способных образовывать комплексные соединения с данным малорастворимым электролитом или вступающих с ним в другие химические реакции.
для любого малорастворимого сильного электролита, мы можем заключить, что произведение растворимости есть постоянная величина при постоянной температуре.
———————Условие образования осадков малорастворимых сильных электролитов——————
Рассмотрим условие образования осадка малорастворимого сильного электролита в частном случае — образование осадка сульфата бария BaSO4 в водной среде. Произведение растворимости этой соли для чистой водной среды


Концентрации ионов бария с(Ва 2+ ) и сульфат-ионов c 
Назовем произведение концентраций ионов c(Ba 2 + )c 
В ненасыщенном растворе сульфата бария концентрации ионов с(Ва 2+ ) и c 
Из ненасыщенного раствора осадок сульфата бария не выпадает.
Если ионное произведение будет больше произведения растворимости, то это означает, что концентрация ионов в растворе выше их молярной растворимости:
с(Ва 2+ ) > S, c 
т. e. раствор — пересыщенный. Осадок будет выпадать до тех пор, пока концентрации ионов станут равными их концентрации в насыщенном растворе, т. е. до тех пор, пока ионное произведение сравняется с произведением растворимости:
с(Ва 2+ ) = S, c 
Таким образом, условием образования осадка сульфата бария и выпадения его из раствора является неравенство
т. е. ионное произведение должно быть больше произведения растворимости.
Аналогично условию (3.4) можно указать условия образования осадков и для других малорастворимых сильных электролитов, например:
т. е. ионное произведение должно быть больше произведения растворимости сильного малорастворимого электролита.
Если ионное произведение меньше произведения растворимости, то осадок не выпадает.
———————Дробное осаждение и дробное растворение осадков———————————
Учет величин 
Действительно, при комнатной температуре произведение растворимости указанных сульфатов уменьшается в последовательности:
Рассуждая аналогичным образом, можно объяснить, почему наблюдается помутнение растворов вследствие образования осадков сульфатов при прибавлении: насыщенного раствора сульфата кальция к растворам солей стронция и свинца (помимо растворов солей бария), насыщенного раствора сульфата стронция к растворам солей свинца и бария; насыщенного раствора сульфата свинца к растворам солей бария.
На основе сопоставления значений 
т. е. в системе протекает гетерогенная реакция
СаSO4(т) + Sr 2+ (раствор) → SrSO4(т)+Са 2+ (раствор)
Объясняется это тем, что растворимость сульфата стронция меньше растворимости сульфата кальция. Сульфаты свинца и бария останутся в осадке, так как их растворимость меньше растворимости сульфата стронция.
Чем больше различие между значениями произведения растворимости однотипных малорастворимых сильных электролитов, тем легче можно провести селективное осаждение или селективное растворение.
———————Перевод одних малорастворимых электролитов в другие—————————-
При проведении анализа иногда возникает необходимость перевести малорастворимые осадки в другие, также малорастворимые осадки.
Так, например, при систематическом анализе катионов для отделения катионов кальция, стронция и бария от остальных катионов их осаждают разбавленной серной кислотой или растворами сульфатов, переводя в малорастворимые осадки сульфатов кальция СаSO4, стронция SrSO4 и бария ВаSO4. Осадок, состоящий из смеси этих сульфатов, отделяют от маточного раствора. Для открытия катионов кальция, стронция и бария в этой смеси ее необходимо перевести в растворимое состояние и в полуденном растворе идентифицировать каждый из указанных катионов с помощью той или иной реакции. Однако сульфаты кальция, стронция и бария не растворяются ни в воде, ни в кислотах, ни в щелочах.
Для перевода катионов кальция, стронция и бария в раствор из осадка смеси их сульфатов эту смесь обрабатывают при нагревании раствором соды Na2СO3. При такой обработке твердые сульфаты переходят в твердые же карбонаты:
Образовавшуюся нерастворимую в воде смесь карбонатов растворяют в какой-либо кислоте (например, в уксусной):
Катионы кальция, стронция и бария при этом переходят в раствор, в котором их затем открывают различными реакциями.
Рассмотрим превращение твердых сульфатов в твердые карбонаты на примере перевода сульфата бария ВаSO4 в карбонат бария:
Поскольку ионное произведение с(Ва 2+ )с 

В равновесном растворе над осадком сульфата бария концентрация ионов бария равна
Следовательно, для образования осадка карбоната бария необходимо, чтобы концентрация карбонат-ионов 
Операцию обработки осадка сульфата бария раствором соды при нагревании (нагревание применяют для повышения скорости процесса) повторяют несколько раз, периодически удаляя раствор, в котором накапливаются сульфат-ионы, поскольку они препятствуют растворению сульфата бария.
Аналогичным образом осуществляется и перевод твердых сульфатов кальция и стронция в твердые карбонаты кальция и стронция.
——————Влияние добавок посторонних электролитов на растворимость малорастворимых сильных электролитов——————————————————————-
1. Влияние добавок электролита с одноименным ионом
Рассмотрим гетерогенное равновесие
BaSО4 (т) = Ва 2+ + 
Это равновесие характеризуется константой равновесия —произведением растворимости 



[Ba 2+ ][ 
Поэтому рост [ 
Аналогичное рассмотрение можно провести для любого другого электролита.
Таким образом, введение в раствор электролита, содержащего одноименные с осадком ионы, не образующие с ним растворимые комплексные соединения, понижает растворимость малорастворимого сильного электролита, т. е. увеличивает полноту осаждения вещества.
К такому же выводу можно прийти и на основе учета принципа смещения подвижного равновесия Ле Шателье—Брауна. Однако этот принцип позволяет сделать лишь качественное заключение о том, в какую сторону смещается равновесие при введении одноименных ионов в раствор, тогда как использование произведения растворимости и концентраций дает возможность получить количественные результаты.
Заметим, однако, что если вводимые одноименные с осадком ионы образуют с ним растворимые комплексные соединения, то при достаточно большом избытке этих ионов наблюдается не понижение растворимости вещества, а, наоборот, растворение осадка.
2. Влияние добавок постороннего (индифферентного) электролита
Рассмотрим то же гетерогенное равновесие
BaSО4 (т) = Ba 2+ + 
Введем в систему какие-то растворимые электролиты, не содержащие одноименных с осадком ионов (например, KCl, NaCl, NaNО3, NH4Br и т. д.). При этом общее число ионов в растворе возрастает, увеличиваются силы электростатического взаимодействия между всеми ионами и повышается ионная сила раствора 
В этом случае коэффициенты активности f(Ва 2+ ) и f( 




Учитывая, что а(Ва 2+ ) =f(Ва 2+ )[Ва 2+ ] и a( 





При не слишком высоких концентрациях растворов с ростом ионной силы раствора Iс коэффициенты активности ионов уменьшаются (становятся меньше единицы) в соответствии с уравнением второго приближения теории сильных электролитов Дебая и Хюккеля

Но величина 



Аналогичные рассуждения справедливы для любого малорастворимого сильного электролита.
Таким образом, введение в гетерогенную систему добавок постороннего (индифферентного) электролита приводит к изменению растворимости малорастворимого сильного электролита вследствие изменения коэффициентов активности ионов.Это явление называется солевым эффектом.
При не очень больших значениях ионной силы раствора (картина, достаточно часто встречающаяся для аналитических систем) введение посторонних электролитов обычно повышает растворимость осадка,так как уменьшаются коэффициенты активности ионов. При больших значениях ионной силы раствора возможно не увеличение, а, наоборот, уменьшение растворимости осадка при введении в систему посторонних электролитов, так как при высоких ионных силах раствора, как было показано выше (см. гл. 3), коэффициенты активности ионов могут быть больше единицы. В общем случае следует говорить об изменении растворимости осадков.
Солевой эффект проявляется всегда, также и при введении в гетерогенную систему таких электролитов, которые имеют с осадком одноименные ионы. Однако солевой эффект в меньшей степени изменяет растворимость осадка (в несколько раз) по сравнению с влиянием одноименных ионов (в несколько десятков и в сотни раз).
Полнота осаждения осадков и их растворимость (а также и чистота) зависят от ряда факторов, важнейшими из которых являются: природа осаждаемого вещества, осадителя, растворителя; концентрация реагентов; температура; pH среды; присутствие посторонних веществ, как имеющих, так и не имеющих одноименные ионы с осадком; условия осаждения (быстрое или медленное образование осадка, осаждение из разбавленных или концентрированных растворов, при перемешивании или без перемешивания и т. д.); характер образующегося осадка (аморфный, кристаллический, мелкозернистый, крупнозернистый, рыхлый, плотный и т. п.); возможность протекания побочных реакций; продолжительность выдерживания осадка с маточником.
Влияние добавок посторонних веществ было рассмотрено в предыдущем разделе.
Процесс электролитической диссоциации — эндотермический, идет с поглощением теплоты, так как для разрыва молекулы (или кристалла) на ионы необходимо затратить определенную энергию. Повышение температуры, следовательно, должно способствовать этому процессу, т. е. приводить к увеличению растворимости. Однако ионы, на которые распадается молекула электролита, в растворе сольватируются (в водных растворах — гидратируются), т. е. окружают себя молекулами растворителя, образуя часто довольно прочные сольватокомплексы. Сольватация — процесс экзотермический, идет с выделением теплоты. Рост температуры затрудняет сольватацию. Оба процесса — распад на ионы и сольватация ионов — по разному, таким образом, зависят от температуры, поэтому суммарно растворимость электролита увеличивается с ростом температуры в меньшей мере, чем это наблюдалось бы при отсутствии сольватации. Бели в энергетическом отношении сольватационные процессы преобладают над процессом ионизации, то возможно даже уменьшение растворимости с ростом температуры.
Во многих аналитически значимых случаях растворимость увеличивается с повышением температуры.
Обычно, особенно в количественном анализе, осадительные аналитические реакции проводят в таких условиях, которые обеспечивают наибольшую полноту выпадения осадка стехиометрического состава, содержащего минимум примесей посторонних веществ, и исключающих протекание побочных процессов.