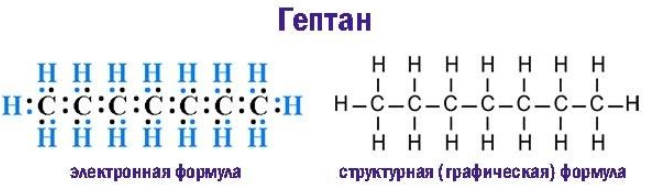
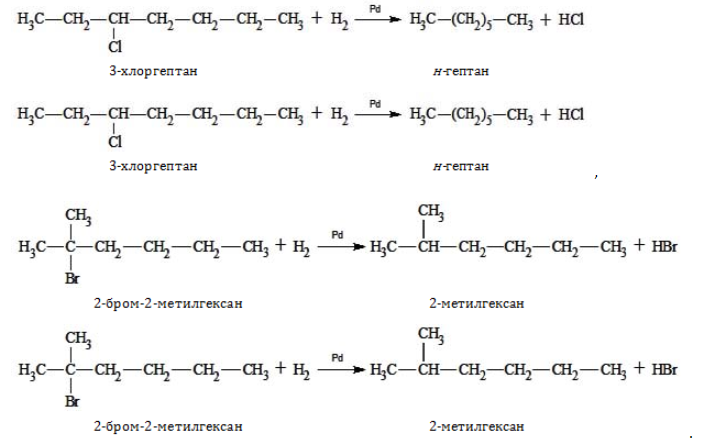
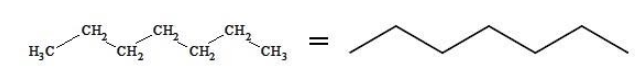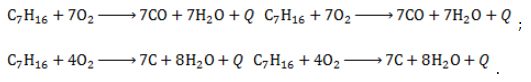Гептан
Гептан (от др.-греч. ἑπτά — семь) СН3(СН2)5СН3 — органическое соединение класса алканов. Гептан и его изомеры — бесцветные жидкости, хорошо растворимые в большинстве органических растворителей, нерастворимые в воде. Обладают всеми химическими свойствами алканов.
Содержание
Физические свойства
Бесцветная подвижная жидкость с резким запахом.
Химические свойства
Аналогичны химическим свойствам других высших алканов.
Получение
Может быть выделен из бензина прямой перегонки путем адсорбционного выделения на цеолитах из соответствующей фракции
Использование
Гептан имеет несколько изомеров; н-гептан применяют при определении детонационной стойкости карбюраторных топлив; его октановое число по определению равно 0.
Изомеры и энантиомеры
Гептан имеет девять изомеров, или одиннадцать, если учитывать оптические изомеры.
| название | формула | температура кипения |
| Гептан (н-гептан) | H3C–CH2–CH2–CH2–CH2–CH2–CH3 | 98.43 °C |
| 2-Метилгексан | H3C–CH(CH3)–CH2–CH2–CH2–CH3 | 90.05 °C |
| 3-Метилгексан | H3C–CH2–C*H(CH3)–CH2–CH2–CH3 | 91.85 °C |
| 2,2-Диметилпентан | (H3C)3–C–CH2–CH2–CH3 | 79.20 °C |
| 2,3-Диметилпентан | (H3C)2–CH–C*H(CH3)–CH2–CH3 | 89.78 °C |
| 2,4-Диметилпентан | (H3C)2–CH–CH2–CH–(CH3)2 | 80.50 °C |
| 3,3-Диметилпентан | H3C–CH2–C(CH3)2–CH2–CH3 | 86.06 °C |
| 3-Этилпентан | H3C–CH2–CH(CH2CH3)–CH2–CH3 | 93.48 °C |
| 2,2,3-Триметилбутан | (H3C)3-C–CH(CH3)–CH3 | 80.88 °C |
(C* обозначает хиральный центр, то есть существование асимметрического центра, относительно которого различают «правые» и «левые» оптические изомеры)
Полезное
Смотреть что такое «Гептан» в других словарях:
гептан — сущ., кол во синонимов: 3 • алкан (37) • парафин (14) • углеводород (77) Словарь синонимов ASIS … Словарь синонимов
гептан — (C7H14) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN heptane … Справочник технического переводчика
Гептан — н гептан, углеводород C7H16; бесцветная подвижная жидкость со слабым запахом: tkип 98,4° С, плотность 0,6838 г/см3 (20°С), показатель преломления nD 1,3876; теплота сгорания жидкого Г. 1167,11 ккал/моль (25°С). Г. нерастворим в воде,… … Большая советская энциклопедия
гептан — СН3(СН2)5СН3, бесцветная жидкость, tкип 98,43ºC. Содержится в нефти. Эталон при определении детонационной стойкости моторных топлив (см Октановое число). * * * ГЕПТАН ГЕПТАН, CH3(CH2)5 CH3, бесцветная жидкость, tкип 98,43 °С. Содержится в нефти.… … Энциклопедический словарь
гептан — (см. гепта. ) органическое соединение, насыщенный углеводород алифатического ряда; бесцветная жидкость; получают фракционной перегонкой нефтяных и синтетических бензинов; нормальный г. примен. в качестве эталона при определении детонационной… … Словарь иностранных слов русского языка
гептан — heptanas statusas T sritis chemija formulė H(CH₂)₇H atitikmenys: angl. heptane rus. гептан … Chemijos terminų aiškinamasis žodynas
ГЕПТАН — С 7 Н 16, мол. м. 100,21. Г. и его изомеры бесцв. жидкости (см. табл.); хорошо раств. в орг. р рителях, не раств. в воде. Обладают всеми хим. св вами насыщенных углеводородов. н Г. содержится в бензиновых фракциях нефтей и газовых конденсатов,… … Химическая энциклопедия
ГЕПТАН — СНз(СН2)5СНз, насыщенный углеводород, бесцв. жидкость, tкип 98,43°С. Содержится в нефти. Эталон при определении детонац. стойкости моторных топлив (см. Октановое число) … Естествознание. Энциклопедический словарь
гептан — гепт ан, а … Русский орфографический словарь
Гептан, свойства, химические реакции
Гептан, свойства, химические реакции.
Гептан, C7H16 – органическое вещество класса алканов. В природе содержится в природном газе, добываемом из газовых и газоконденсатных месторождений, в попутном нефтяном газе, в нефти.
Гептан, формула, характеристики:
Гептан – органическое вещество класса алканов, состоящий из семи атомов углерода и шестнадцати атомов водорода.
Химическая формула гептана C7H16. Имеет одиннадцать изомеров, включая два оптических изомера: н-гептан (нормальный гептан), 2-метилгексан, 3-метилгексан, 2,2-диметилпентан, 2,3-диметилпентан, 2,4-диметилпентан, 3,3-диметилпентан, 3-этилпентан, 2,2,3-триметилбутан.
3-метилгексан и 2,3-диметилпентан имеют правые и левые оптические изомеры.
Строение молекулы н-гептана:
Все изомеры гептана – бесцветная прозрачная горючая жидкость с резким запахом.
Пожаро- и взрывоопасен.
Не растворяется в воде. Растворяется в органических веществах (ацетон, бензол, хлороформ, диэтиловый эфир и другие).
Гептан по токсикологической характеристике относится к веществам 3-го класса опасности (умеренно опасным веществам) по ГОСТ 12.1.007.
Физические свойства гептана:
| Наименование параметра: | Значение: |
| Цвет | без цвета |
| Запах | с резким запахом |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | жидкость |
| Плотность н-гептана (при 20 °C и атмосферном давлении 1 атм.), кг/м 3 | 683,8 |
| Плотность н-гептана (при 0 °C и атмосферном давлении 1 атм.), кг/м 3 | 700,4 |
| Температура плавления н-гептана, °C | -90,61 |
| Температура кипения н-гептана, °C | 98,42 |
| Температура самовоспламенения н-гептана, °C | 223 |
| Температура вспышки н-гептана, °C | -4 |
| Критическая температура н-гептана, °C | 267,01 |
| Критическое давление н-гептана, МПа | 2,74 |
| Взрывоопасные концентрации смеси газа н-гептана с воздухом, % объёмных | от 1,06 до 6,7 |
| Удельная теплота сгорания н-гептана, МДж/кг | 45,105 |
| Молярная масса, г/моль | 100,21 |
Физические свойства изомеров гептана:
| Название: | Температура кипения: | Октановое число: |
| гептан (н-гептан) | 98,42 °C | 0 |
| 2-метилгексан | 90,05 °C | 45 |
| 3-метилгексан | 91,85 °C | 65 |
| 2,2-диметилпентан | 79.20 °C | 93 |
| 2,3-диметилпентан | 89,78 °C | 89 |
| 2,4-диметилпентан | 80.50 °C | 82 |
| 3,3-диметилпентан | 86,06 °C | 84 |
| 3-этилпентан | 93,48 °C | 68 |
| 2,2,3-триметилбутан | 80,88 °C | 106 |
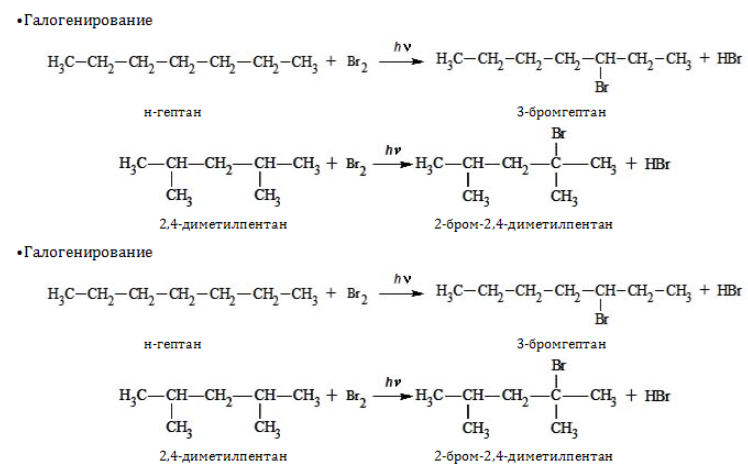
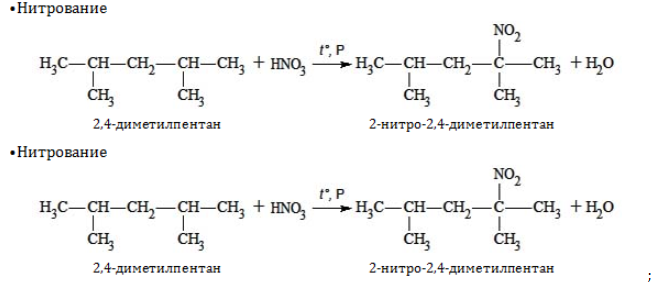
Химические свойства гептана:
Химические свойства гептана аналогичны свойствам других представителей ряда алканов. Поэтому для него характерны аналогичные химические реакции.
Применение и использование гептана:
Н-гептан применяют при определении детонационной стойкости карбюраторных топлив. Его октановое число по определению равно 0.
Примечание: © Фото //www.pexels.com, //pixabay.com

Мировая экономика
Справочники
Востребованные технологии
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Изомеры гептана, строение и свойства
Гептан – седьмой член гомологического ряда алканов. Вследствие различий в порядке соединения и пространственного расположения атомов в молекуле гептан образует несколько изомеров, проявляющих разные свойства. Источником получения гептана служат нефть и нефтепродукты, попутный и природный газ.
Химическое строение и формула гептана
Предельные углеводороды, к числу которых относится гептан, характеризуются полным насыщением всех валентностей углерода. Располагая каждый четырьмя свободными валентностями, sp3-гибридизованные углеродные атомы в молекулах алканов образуют насыщенные водородом цепочки состава 
Каждая общая электронная пара, возникающая при взаимодействии атомов, соответствует одинарной (простой) ковалентной 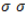
Скелетная формула представляет строение гептана в компактном виде как зигзагообразную линию. Атомы, формирующие углеродный скелет, находятся в вершинах и на концах линии; при записи их обозначения обычно опускают:
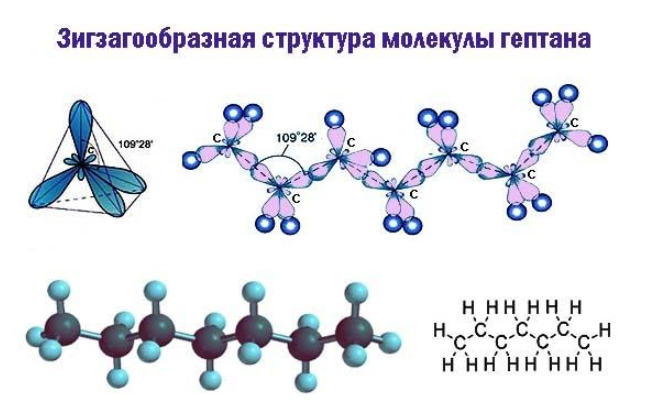
В двумерной форме зигзаг более точно показывает строение молекулы, так как ориентация связей C-C соответствует углу 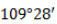
Изомеры гептана
Благодаря возможности ветвления углеродного скелета и пространственным различиям в положении одинаковых алкильных радикалов соединениям состава свойственна изомерия. Всего у гептана насчитывается 11 изомерных вариантов.
Структурная изомерия
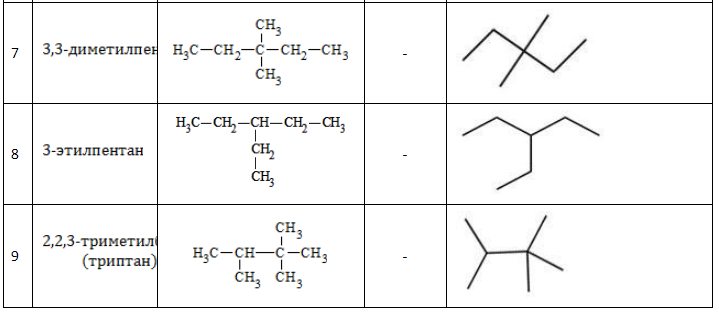
Существует девять изомеров с химической формулой C7H16, различающихся строением молекулы. По длине главной углеродной цепочки, по типу и числу радикалов они подразделяются следующим образом:
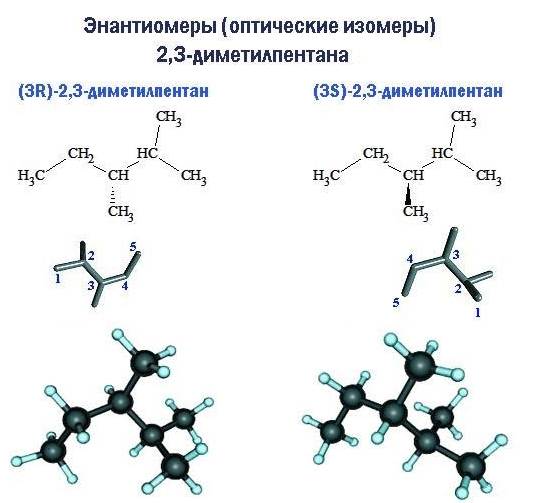
Оптическая изомерия
Если при одинаковой структуре молекулы расположение радикалов таково, что молекула не имеет зеркальной симметрии, возникает пространственная изомерия оптического типа.
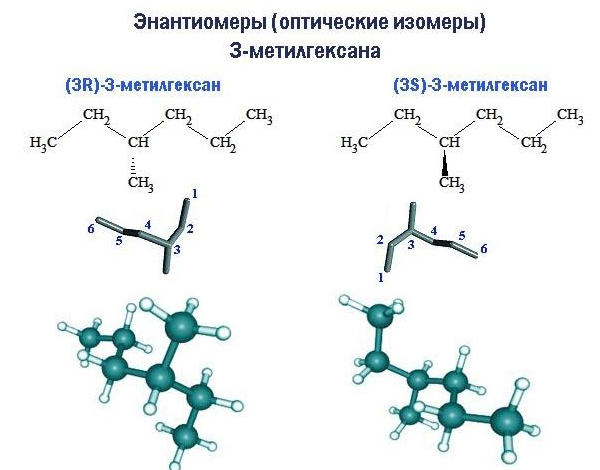
Молекулы оптических изомеров (иначе называемых энантиомерами) обладают свойством хиральности: зеркально отображая друг друга, они при вращении не становятся идентичными. Примером хиральности является отличие правой ладони от левой. Центром хиральности молекулы является тот атом углерода, к которому у энантиомеров присоединены радикалы, по-разному ориентированные в пространстве.
Хиральность свойственна двум из девяти структурных изомеров гептана. Каждое из этих соединений – 3-метилгексан и 2,3-диметилпентан – существует в форме двух энантиомеров, обозначаемых как правый (R) и левый (S) изомеры. При этом указывается номер центра хиральности в углеродной цепи.
В среде с оптической активностью или в химической реакции с другим хиральным соединением энантиомеры ведут себя различно. В других случаях их свойства одинаковы.
Список изомеров
Все изомеры гептана с названиями и формулами, с учетом наличия энантиомеров, перечислены в таблице:

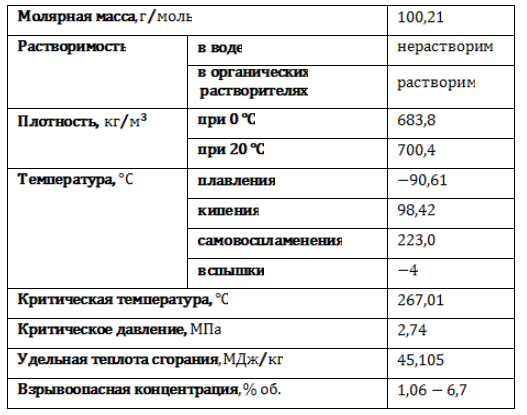
Физические свойства
Гептан в обычных условиях представляет собой легкую подвижную жидкость с резким специфическим запахом, без цвета. Пары гептана тяжелее воздуха и образуют с ним взрывоопасную смесь. Основные физические свойства н-гептана приведены в таблице:
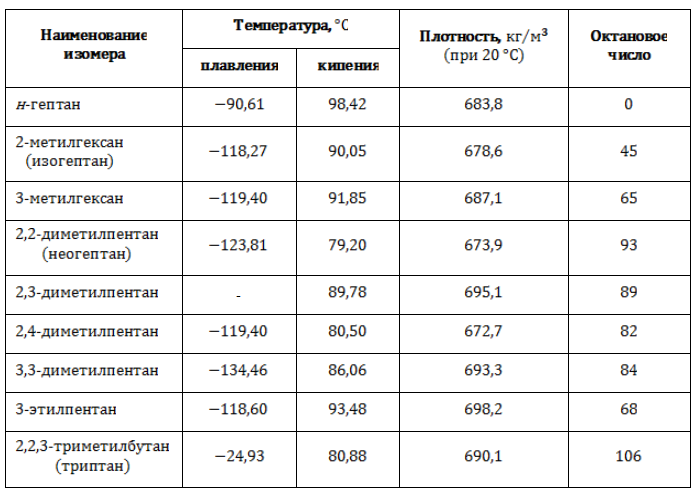
Свойства изомеров гептана
Различия в строении молекулы являются причиной неодинаковости плотностных и термических характеристик изомеров, в том числе и такой важной, как детонационные свойства.
Устойчивость горючего к взрыву при сжатии выражают через октановое число, сравнивая топливо с эталоном. В состав эталонной смеси входят н-гептан, который крайне склонен к детонации, и чрезвычайно устойчивый к ней изооктан. Процентное содержание изооктана в эталонной смеси называется октановым числом.
Существует зависимость между степенью разветвленности молекулы и стойкостью углеводорода к детонации. Чем больше алкильных радикалов и, соответственно, третичных и четвертичных углеродных атомов содержит молекула, тем выше антидетонационная характеристика и качество топлива.
Химические свойства
Гептан и его изомеры – предельные углеводороды и проявляют все химические свойства, присущие данному классу органических соединений. Вследствие насыщенного характера всех связей они вступают только в реакции, протекающие с разрывом ковалентной связи. При этом, как правило, необходимо подвергнуть реагенты нагреванию и использовать катализаторы.
При недостатке кислорода продуктами неполного сгорания гептана являются угарный газ и сажа:
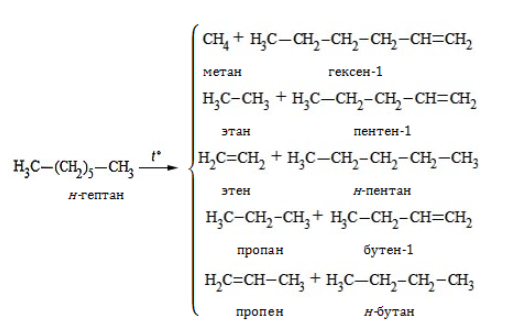
3. Разложение на низшие алканы и алкены при нагревании без доступа кислорода (крекинг):
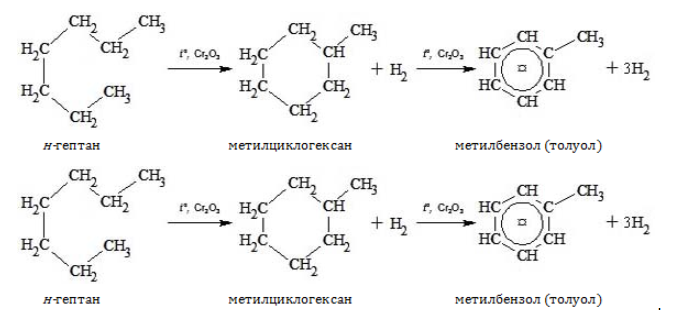
4. Дегидрирование с образованием циклического углеводорода (дегидроциклизация):
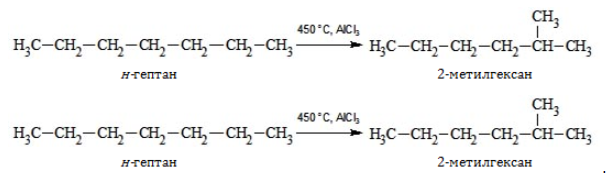
5. Изомеризация с ветвлением углеродного скелета:
Получение гептана и его изомеров
Промышленное получение соединений с химическим составом С7H16 проводится при добыче и переработке природного газа и нефти либо методом синтеза Фишера–Тропша наряду с прочими углеводородами:
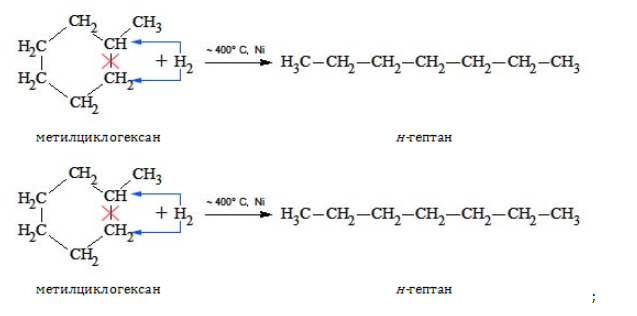
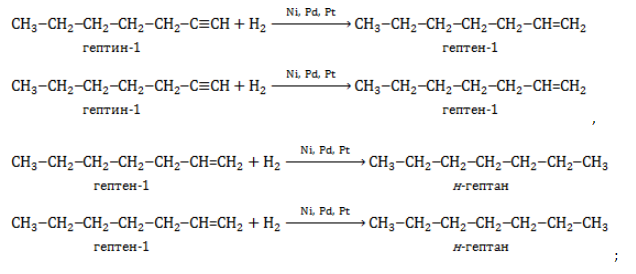
В лабораторной практике гептан и изомеры синтезируются следующими способами:
Применение гептана и его изомеров
Углеводороды состава C7H16 используются в различных отраслях в зависимости от свойств.
1. В топливной промышленности находят применение:
2. В нефтепереработке и химической промышленности:
3. В качестве растворителя (чистый н-гептан либо в смеси с изомерами):
Заключение
В отношении пожаро- и взрывоопасности гептан входит в число опасных грузов III класса (легковоспламеняющиеся жидкости). Гептан оказывает раздражающее воздействие на центральную нервную систему и по шкале токсикологической опасности относится к веществам IV класса. При длительной работе с ним необходимо защищать кожные покровы и органы дыхания.
При использовании защитных средств, соблюдении герметичности тары и оборудования, вентиляции помещений работа с гептаном не представляет угрозы. Большим преимуществом гептана, как и прочих жидких углеводородов, является удобство хранения и транспортировки по сравнению с газообразными низшими алканами.
Гептан: способы получения и химические свойства
Гексан C6H14 – это предельный углеводород, содержащий шесть атомов углерода в углеродной цепи. Бесцветная жидкость с характерным запахом, нерастворим в воде и не смешивается с ней.
Гомологический ряд гексана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Строение гексана
В молекулах алканов встречаются химические связи C–H и С–С.
Связь C–H ковалентная слабополярная, связь С–С – ковалентная неполярная. Это одинарные σ-связи. Атомы углерода в алканах образуют по четыре σ-связи. Следовательно, гибридизация атомов углерода в молекулах алканов – sp 3 :



Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:

Это соответствует тетраэдрическому строению.
| Например, в молекуле гексана C6H14 атомы водорода располагаются в пространстве в вершинах тетраэдров, центрами которых являются атомы углерода. При этом углеродный скелет имеет зигзагообразное строение. |
Изомерия гексана
Структурная изомерия
Дл я гексана характерна структурная изомерия – изомерия углеродного скелета.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета отличаются строением углеродного скелета.
Например.
Для гексана не характерна пространственная изомерия. Химические свойства гексанаГексан – предельный углеводород, поэтому он не может вступать в реакции присоединения. Для гексана характерны реакции: Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов. Поэтому для гексана характерны радикальные реакции. Гексан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой. 1. Реакции замещенияВ молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С. 1.1. ГалогенированиеГексан реагирует с хлором и бромом на свету или при нагревании. При хлорировании гексана образуется смесь хлорпроизводных. Бромирование протекает более медленно и избирательно.
|