Гибридизация ДНК
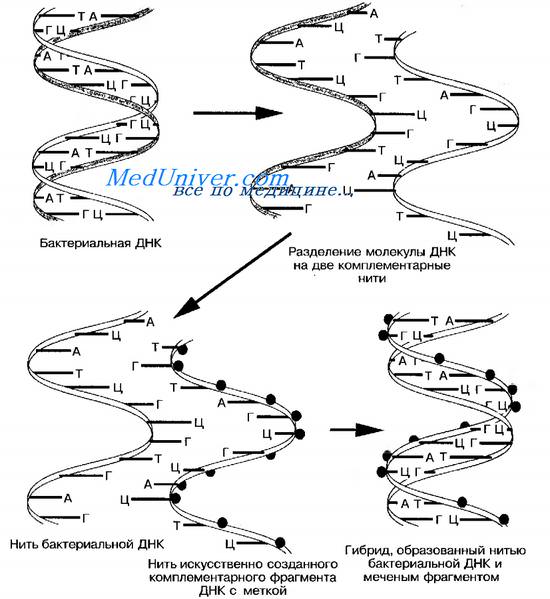
Гибридизация ДНК, гибридизация нуклеиновых кислот — соединение in vitro комплементарных одноцепочечных нуклеиновых кислот в одну молекулу. При полной комплементарности объединение происходит легко и быстро, а в случае частичной некомплементарности слияние цепочек замедляется, что позволяет оценить степень комплементарности. Возможна гибридизация ДНК-ДНК и ДНК-РНК.
Содержание
Протокол эксперимента
Анализ скорости отжига одноцепочечных ДНК позволяет оценивать сходства и различия в последовательностях ДНК между видами или особями одного вида.
Вычисление температуры плавления ДНК
Вторичная структура ДНК играет важную роль в биологии, генетической диагностики и других методов молекулярной биологии и нанотехнологии. Поэтому, точное определение температуры плавления ДНК или РНК молекул играет самую главную роль во всех молекулярно-биологических методах, например, как подбор проб или олигонуклеотидов для микрочипов или для подбора ПЦР праймеров. Существует несколько простых формул вычисления температуры плавления для коротких олигонуклеотидов. Грубое вычисление температуры плавления (Tm) короткого олигонуклеотида ( [1]
Усредненная формула подсчета Tm для короткого олигонуклеотида (и для длинных ДНК фрагментов), с учетом концентрации ионов K + и DMSO:

Однако, эти уравнения не учитывают инициацию связывания при гибридизации олигинуклеотида, не учитывают особенности самой последовательности и концевого эффекта, характерный для олигонуклеотидных дуплексов. Поэтому, данная формула пригодна в большей степени, где последовательность ДНК усредненная и длина дуплексов свыше 40 нуклеотидов.
ДНК термодинамика
Наиболее распространенный метод используемый сегодня для расчета температуры плавления двухцепочечной или одноцепочечной ДНК, основан на двух ступенчатой термодинамической модели. Две комплементарные ДНК молекулы А и В, либо они связаны друг с другом либо свободны в растворе («random coil state»). Обычно считается, что обе молекулы А и В полностью комплементарны, поэтому очевидна их гибридизация, а также разрешены одна или несколько ошибок комплементарности в дуплекс, в том числе допустимы и некомплементарные G-G, G-T и G-A пары (wobble pairs). В случае же только одной молекулу, предполагается упаковка ее в петлевую структуру. Процесс гибридизации в дуплекс описывается формулой:
Подставляем компоненты в формулы для вычисления k :
После перестановки получаем:
где 
где T температура в кельвинах, dH° (cal/mol) и dS° (cal/mol K).
Существует полезное соотношение, связывающее изменение свободной энергии Гиббса в ходе химической реакции с её константой равновесия:
где R – универсальная газовая постоянная (1.987cal/mol K).
Комбинируя обе формулы получаем:
Температура плавления (Tm) определяется при равновесии, когда половину цепей связаны друг с другом и другая половина находится в свободном состоянии, то есть k=1:
Температуру плавления для простой петли рассчитывают как 
Предполагается, что концентрация обоих цепей одинаковая [A] = [B] = C/2. В таком случае,
где f = 4. Для самокомплементарного олигонуклеотида [A0] = C и тогда и f = 1. Данная температура плавления определяется только в случае, когда половина молекул связаны друг с другом.
Для самокомплементарного олигонуклеотида, k = 1/[At] поэтому:
Для не комплементарного дуплекса, когда [At] ≥ [Bt], k =1/([At] – [Bt]/2), Tm вычисляют так:
где [At] молярная концентрация преобладающей цепи (как правило ПЦР праймер), а [Вt] молярная концентрация цепи с низкой концентрацией (геномная ДНК).
Вычисление температуры плавления
Термодинамические параметры dG, dH и dS рассчитываются на основе модели ближайших соседей (nearest neighbour). Для точного прогнозирования вторичной структуры ДНК при гибридизации с использованием динамических алгоритмов программирования требуется база данных по всем возможным термодинамическим параметрам для каждой комплементарной пары оснований, а также для для всех вариантов при не совпадающих нуклеотидов, для свободных концов, шпилек и петель. Термодинамическая формула вычисления короткого олигонуклеотида основывается на термодинамических параметрах — энтропии dS и энтальпии dH, для каждой из 10 вариантов сочетаний четырех нуклеотидов (Таблица 1). В Таблице 1 представлены термодинамические параметры для ближайших соседей (NN) для пар нуклеотидов при концентрации 1М NaCl.
Для подсчета Tm (°С) осуществляется суммирование всех значений свободной энергии Гиббса для каждой пары с шагом один нуклеотид:
| 5’-CGTTGA-3’ | = dGначальное + dGсиметрия + | CG + GT + TT + TG + GA + ATконец |
| 3’-GCAACT-5’ | GC CA AA AC CT |
Многие ДНК дуплексы имеют конкурирующие однонитевые структуры, и это сдвигает равновесии системы и как результат снижение значения Tm от предсказуемой формулой значения.
Общая формула для вычисления Tm с коррекцией на соль в растворе:
Одиночная ошибка внутри дуплекса
Модель ближайших соседей для комплементарных нуклеотидных пар может расширен для пары, включающие некомплементарные нуклеотиды. Было показано, что существует тенденция уменьшающая стабильность не комплементарных пар оснований в порядке убывания:
G-C > A-T > G·G > G·T ≥ G·A > T·T ≥ A·A > T·C ≥ A·C ≥ C·C
Что такое гибридизация нуклеиновых кислот
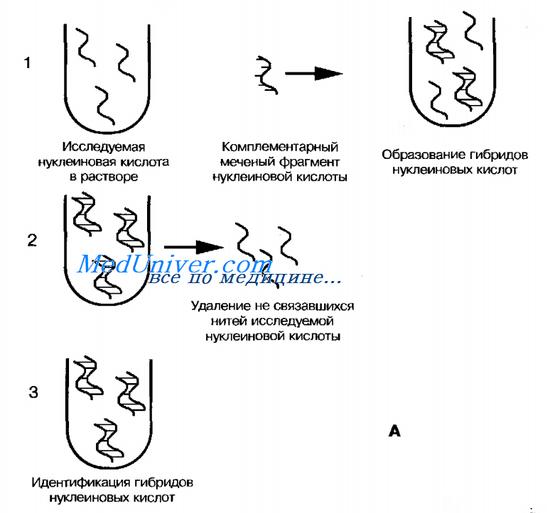
Метод гибридизации нуклеиновых кислот в растворах даёт наиболее быстрые результаты (рис. 11-18, А). Широкому внедрению метода препятствует проблема удаления несвязавшихся нитей нуклеиновых кислот.
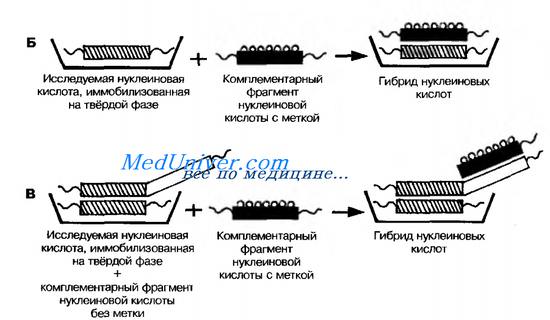
Метод гибридизации нуклеиновых кислот на твёрдой основе (рис. 11-18, Б) и его сэндвич-модификация (рис. 11-18, В) распространён больше. В качестве твёрдой основы служат мембраны из нитроцеллюлозы или нейлона. Несвязавшиеся реагенты удаляют многократным отмыванием.
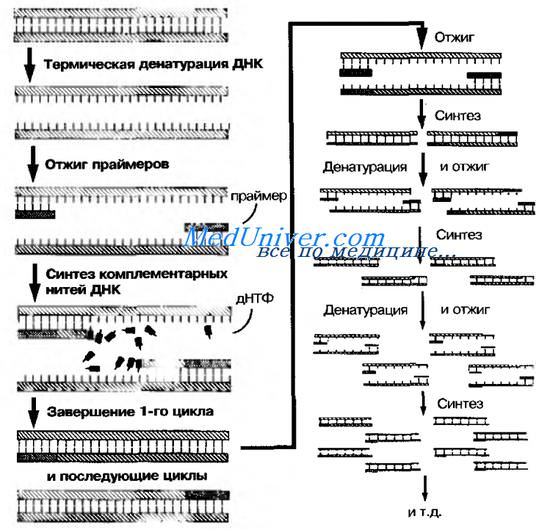
Полимеразная цепная реакция ( ПЦР )
Основу метода ы составляет катализируемое ДНК-полимеразой многократное образование копий определённого участка ДНК. Первоначально проводят отжиг — термическое разделение двухнитевой молекулы ДНК на отдельные цепочки. Затем среду охлаждают и вносят праймеры (затравки), комплементарные нуклеотидным последовательностям обеих цепочек. Для запуска реакции применяют синтетические праймеры — олигонуклеотиды, состоящие из 10-20 нуклеоти-дов (например, дезоксинуклеотидтрифосфат), взаимодействующие с окончаниями последовательностей и образующие последовательности в 50-1000 оснований. Затем в среду вносят термостабильную tag-полимеразу (по названию бактерии Thermits aquaticus), что запускает образование вторичных копий цепей ДНК, после чего образующиеся двухнитевые молекулы ДНК снова подогревают. Образующиеся отдельные цепочки остужают, вносят праимеры и снова повторяют процедуру подогрева и охлаждения; поскольку tag-полимераза термостабильна, то необходимость в её повторном внесении отсутствует (рис. 11-19). ПЦР позволяет получить большие количества изучаемого фрагмента ДНК даже в том случае, если в распоряжении исследователя имеется всего лишь одна исходная молекула геномной ДНК. Идентификацию копий ДНК проводят методом электрофореза. Метод полимеразной цепной реакции ( ПЦР ) лежит также в основе ДНК-идентификации личности, установления родства людей, выявления генов наследственных болезней и пр.
Серологические методы диагностики бактерий
Классические серологические реакции применяют для выявления бактериальных AT, а также для выявления Аг, особенно для идентификации бактериальных Аг. Среди современных методов наибольшее распространение нашли методы твердофазного ИФА и латекс-агглютинации.
Аллергологические методы диагностики бактерий
Сенсибилизирующей активностью обладает ограниченное количество бактериальных Аг. Поэтому метод кожных проб применяют лишь при диагностике туберкулёза, сапа, мелиоидоза, бруцеллёза и туляремии.
— Вернуться в оглавление раздела «Микробиология.»
Гибридизация нуклеиновых кислот. Нуклеиновые кислоты
Специфические характеристики любого организма зависят от определенной последовательности нуклеиновых кислот, содержащихся в его геноме.
Сами нуклеиновые кислоты состоят из цепей блоков, каждый из которых состоит из сахара (дезоксирибоза или рибоза, в зависимости от того, является ли нуклеиновая кислота ДНК или РНК), фосфоросодержащей группы и одного из четырех органических пуриновых или пиримидиновых оснований. ДНК состоит из двух таких цепочек, расположенных в виде двойной спирали и соединенных между собой связями между органическими основаниями. Основания избирательно связывают аденин с тимином и гуанин с цитозином. Именно последовательность оснований делает организмы уникальными.
Разработка зондов (проб) на основе нуклеиновых кислот
Зонды на основе нуклеиновых кислот — это небольшие сегменты однонитевой нуклеиновой кислоты, которая может быть использована для определения специфических генетических последовательностей в пробах. Зонды (пробы) могут разработаны для последовательностей ДНК или РНК. Привлекательность использования генных зондов в определении микроорганизмов заключается в том, что зонд, состоящий из последовательности лишь 20 нуклеотидов, уникален и может быть использован для точного определения микроорганизма [52].
Чтобы обнаружить связывание зонда с ДНК или РНК определяемого микроорганизма, он должен быть присоединен к какой-либо метке, которую легко выявить. Сначала работа выполнялась с радиоизотопными метками (например, на основе радиоактивного фосфора Р32), который мог быть определен авторадиографией или подсчетом сцинцилляций. Использование и утилизация радиоактивных изотопов, однако, неизбежно сопряжены с проблемами безопасности, что делает их непригодными для стандартных испытаний в лабораториях пищевых производств. Поэтому для широкого применения зондов на основе нуклеиновых кислот требовались иные метки.
Значительный объем исследований был посвящен мечению зондов с использованием связи «авидин-биотин». В основе этого приема лежит высокая специфичность связи между авидином и биотином. Зондовая последовательность нуклеиновой кислоты метится биотином и взаимодействует с определяемой ДНК. Затем добавляется авидин, связанный с подходящим индикатором, например, авидин-щелочной фосфатазой, и связывание затем обнаруживается по образованию окрашенного продукта в бесцветном субстрате. Применение таких новых систем мечения показало, что зонды с нерадиоактивными метками могут быть использованы для определения микроорганизмов, но они гораздо менее чувствительны, чем системы с радиоизотопным мечением, и требуемое для определения увеличение количества клеток (по сравнению с радиоизотопной системой) доходит до 100-кратного.
Для создания неизотопных зондов с чувствительностью, приближающейся к чувствительности изотопных меток, было необходимо изучить в клетках альтернативные мишени для зондов. Зонды, ориентированные на клетки ДНК, прикрепляются только к нескольким участкам на хромосоме клетки определямого микроорганизма. Изучая области клеточной нуклеиновой кислоты, которые присутствуют в относительно большом количестве копий в каждой клетке, и ориентируя зонды на эти участки, можно значительно увеличить чувствительность неизотопных зондов. Работа по увеличению чувствительности зондов сосредоточилась на использовании в качестве мишени РНК. РНК — это однонитевая нуклеиновая кислота, которая присутствует в клетках в разных формах. В одной из форм она обнаруживается в рибосомах, которые являются частью системы синтеза белка в клетке. Такая РНК (известная как рибосомная РНК — рРНК) присутствует в клетках в большом количестве копий. Ориентируя зонды из нуклеиновых кислот на рибосомную РНК, можно существенно увеличить чувствительность аналитической системы.
Пробы на микроорганизмы в пищевых продуктах
Процедуры гибридизации нуклеиновых кислот для определения патогенных бактерий в пищевых продуктах описаны для разновидностей Salmonella [35,47], Listeria [73,74], Yersinia enterocolitica [56,66], Listeria monocytogenes [38], вырабатывающей энтеротоксины Escherichia coli [55, 57], Vibrio vulnificus [87], вырабатывающей энтеротоксины Staphylococcus aureus [91], Clostridiumperfringens и Clostridium botulinum [134].
Первая промышленно выпускаемая аналитическая система для пищевых продуктов на основе зондов из нуклеиновых кислот была представлена компанией Gene Trak Systems (г. Фрэмингхэм, штат Массачусетс, США) в 1985 году [47]. В ней использовались зонды, избирательные для ДНК сальмонеллы и для определения сальмонеллы в обогащенных пищевых пробах, ориентированные на хромосомную ДНК. Процедура анализа включала гибридизацию определяемой ДНК, связанной с мембранным фильтром, и зондов, меченных фосфором-32. Общее время анализа складывалось из 40-44 ч обогащения пробы в неселективной и селективной средах и последующей процедуры гибридизации, длившейся 4-5 ч. Таким образом, полное время анализа составляло около 2 сут. Проверка теста на Salmonella в США показала, что он, по меньшей мере, эквивалентен стандартным методам, использующим культуры [49]. Компания Gene Trak создала на основе подобного подхода систему гибридизационного анализа для разновидностей Listeria [73].
Комплекты зондов компании Gene Trak были аттестованы в США, и ряд лабораторий начал их использовать. В Европе, однако, в лабораториях пищевых производств наблюдалось нежелание использовать радиоизотопы. Кроме того, фосфор-32 имеет малый период полураспада, что вызывало сложности при транспортировке комплектов в отдаленные районы. В 1988 г. компания Gene Trak начала поставлять зонды с неизотопным мечением для Salmonella, Listeria и Escherichia coli и колориметрической системой обнаружения. Для преодоления снижения чувствительности, вызванной использованием неизотопных меток, целевой нуклеиновой кислотой в клетке была рибосомная РНК. Количество копий этой нуклеиновой кислоты на одну клетку оценивается в 500-20 ООО.
Колориметрический гибридизационный анализ основан на реакции гибридизации в жидкости между определяемой рРНК и двумя отдельными олигонуклеотидами с помощью ДНК-зондов (иммобилизованного зонда и зонда-сигнализатора), специфическими для определяемого микроорганизма. Молекулы иммобилизованного зонда с помощью ферментов дополнены полимером, состоящим примерно из 100 остатков дезоксиаденозина монофосфата. Молекулы зонда-сигнализатора химически помечают гаптен флуоресцеином.
После соответствующего обогащения исследуемого продукта проба переносится в пробирку, и микроорганизмы разлагаются, выделяя определяемую рРНК. Затем добавляют иммобилизованные, и зонды-сигнализаторы проводят гибридизацию. Если определяемая рРНК присутствует в пробе, то происходит гибридизация между зондами и определяемой рРНК. Раствор, содержащий комплекс «зонд-определяемый микроорганизм», затем приводят в контакт с датчиком, содержащим связанный гомополимер дезокситимидин (в условиях, при которых возможна гибридизация между полимером полидезоксиаденозином иммобилизованного зонда и полидезокситимидином на датчике). Негибридизованные нуклеиновые кислоты и остатки клеток затем смывают, оставляя иммобилизованный комплекс ДНК-РНК прикрепленным к поверхности датчика. Связанный зонд-сигнализатор с флюоресцеином определяется путем добавления антифлюоресцеинового антитела, конъюгированного с ферментом пероксидазы. Последующее добавление хромогенного субстрата для фермента приводит к появлению окраски, которая может измеряться спектрофотометром.
Результаты колориметрических анализов [88] показали хорошее совпадение между зондовыми методами и традиционными, основанными на культурах для Salmonella и Listeria. Оказалось, что чувствительность комплектов лежит между 105 и 106 определяемых микроорганизмов на 1 мл, в связи с чем важным этапом является процедура обогащения. После внедрения трех указанных комплектов компания Gene Trak начала выпуск систем для Staphylococcus aureus, разновидностей Campylobacter и Yersinia enterocolitica.
Серийно выпускаемые зонды на основе нуклеиновых кислот для подтверждения наличия Campylobacter, Staphylococcus aureus и Listeria поставляются компанией Gen- probe (Gen Probe Inc., г. Сан-Диего, США). Эти комплекты основаны на зонде из однонитевой ДНК, комплементарной рибосомной РНК определяемого микроорганизма. После того как рибосомная РНК выделена из микроорганизма, меченый зонд ДНК соединяется с ней и образует стабильный гибрид комплементарных ДНК и РНК. Гибридизированный зонд может быть обнаружен благодаря люминесценции.
Для анализа также используется метод гибридизационной защиты, основанный на использовании хемилюминесцентного сложного эфира акридина. Этот эфир реагирует с пероксидом водорода в щелочных условиях, испуская свет, который можно измерить в люминометре. Сложные эфиры акридина ковалентно связаны с синтетическими ДНК- зондами через алкиламиновую цепь. Анализ основан на дифференциальном химическом гидролизе эфирной связи. Гидролиз этой связи делает акридин постоянно нехемилюминесцентным. Когда ДНК-зонд, к которому прикреплен эфир, гибридизируется с РНК-мишенью, акридин защищен от гидролиза и может поэтому стать люминесцентным. В комплектах для анализа на Campylobacters Listeria используются лиофилизированный реагент-зонд. Зонд Campylobacter реагирует с С. jejuni, С. coli и С. pylori; зонд Listeria реагирует с L. monocytogenes. В обоих случаях перед использованием зонда для подтверждающих испытаний необходимо значительное обогащение культур.
Оценка комплекта зондов для L. monocytogenes [21] показала, что он абсолютно специфичен к организму-мишени. Для получения положительного результата требовалось присутствие около 106 L. monocytogenes. Данный комплект представляется быстрым и надежным тестом для подтверждения присутствия культуры и может использоваться непосредственно с бульоном для обогащения, тем самым дополнительно снижая продолжительность теста.
Будущее зондов
Разработка и использование зондов в пищевой промышленности в последние годы продвинулись недостаточно. Выпускаемые комплекты демонстрируют свой большой потенциал, но используются не так широко, как иммунологические тесты. Микробиологи всегда должны учитывать полезность анализа клеточной генетической информации. Возможно, однако, что достижения молекулярной биологии означают, что лучший способ получения подобной информации — это использование методов амплификации нуклеиновых кислот (например, цепной реакция полимеразы — ЦРП).
Методы амплификации нуклеиновых кислот
В последние годы разработаны и усовершенствованы несколько генетических амплификационных методов (методов усиления). Эти методы обычно опираются на биохимическую амплификацию клеточной нуклеиновой кислоты и могут привести к увеличению числа копий за 2-3 ч в 10 7 раз. Очень быстрое увеличение количества мишеней, достигаемое с помощью методов амплификации нуклеиновых кислот, делает их идеальными для разработки систем ускоренного обнаружения микроорганизмов. В настоящее время разработан ряд методов амплификации, примененных для определения микроорганизмов:
Из этих амплификационных методов только ЦРП была внедрена в промышленность в виде методики, основанной на комплекте для определения пищевых микроорганизмов. С помощью NASBA проведены различные исследования, имеется ряд работ, описывающих применение этого метода для определения пищевых патогенов, но до сих пор на рынке отсутствуют серийно выпускаемые комплекты для анализа.
Цепная реакция полимеразы (ЦРП)
ЦРП — это метод, применяемый для повторяемого in vitro ферментного синтеза специфических последовательностей ДНК с использованием двух коротких олигонуклеотидных праймеров Эти праймеры гибридизируются с противоположными нитями молекулы ДНК и примыкают к представляющей интерес области ДНК-мишени. ЦРП протекает через серию вторичных циклов, включающих денатурацию ДНК, отжиг праймеров и увеличение праймеров под действием полимеразы ДНК. Эти три стадии каждого цикла регулируют, изменяя температуру реакции, так как каждая стадия происходит только при определенных температурах. Эти изменения температуры осуществляются с помощью специального прибора для термоциклирования. Продукты увеличения праймеров после одного цикла служат матрицами для следующего цикла, и, таким образом, количество копий ДНК-мишени удваивается в каждом цикле.
Цепная реакция «обратная транскриптаза-полимераза» (ЦРОТ-П)
Эта реакция включает использование для ЦРП РНК-мишени. ЦРП должна работать на молекуле ДНК, и поэтому первоначально обратная транскриптаза используется для получения копии ДНК, после чего эта копия используется в традиционной ЦРП. Цепная реакция «обратная транскриптаза-полимераза» (ЦРОТ-П) особенно хорошо подходит для определенных микробиологических тестов. Некоторые пищевые вирусы содержат в качестве генетического материала РНК. Поэтому, если необходимы амплификация и, соответственно, определение вирусов, необходимо использовать именно ЦРОТ-П. Второе применение ЦРОТ-П — это определение жизнеспособных микроорганизмов. Одна из проблем, связанных с ЦРП — ее высокая чувствительность и способность увеличивать очень низкие концентрации определяемой нуклеиновой кислоты. Таким образом, при использовании ЦРП для определения наличия или отсутствия определенного микроорганизма в пищевом продукте эта реакция может определить микроорганизм даже в том случае, если он предварительно был сделан неактивным вследствие соответствующего технологического процесса. Это может привести к ошибочному положительному результату определения. Для преодоления этой проблемы можно использовать ЦРОТ-П, направленную на информационную РНК клетки, которая производится только активными клетками и после образования имеет короткое время полураспада. Таким образом, определение специфической информационной РНК (инфРНК) с помощью ЦРОТ-П указывает на наличие жизнеспособных микроорганизмов.
NASBA
NASBA — это многоферментная многократная процедура амплификации, требующая большего числа ферментов и реагентов, чем стандартная ЦРП. Ее преимущество в том, что это изотермическая процедура, и, следовательно, все стадии реакции происходят при одной температуре, что делает ненужным устройство для термоциклирования. Опубликован ряд работ по применению NASBA для определения пищевых патогенов (см., например, [128]), но эта процедура еще не нашла широкого применения.
Промышленные комплекты на основе ЦРП
В настоящее время комплекты на основе ЦРП для определения микроорганизмов в пищевых продуктах выпускаются тремя фирмами. В комплекте ВАХ (фирма Qualicon, США) используются таблетированные реагенты, традиционное устройство для термоциклирования и метод, основанный на электрофорезе в геле. Пробы с положительной реакцией видны как полосы на геле для электрофореза. Выпускаются комплекты ВАХ для Salmonella [9], Listeria рода Listeria monocytogenes, и для E. coli 0157:Я7. Анализы на Salmonella и E.coli 0157:#7 прошли испытания в Ассоциации научно-исследовательского института химиков-аналитиков (AOACRI) и были им аттестованы.
Вторая серийно выпускаемая группа комплектов для ЦРП — это комплект Probelia (фирма Sanofi, Франция), где используется традиционная ЦРП с последующим иммунологическим анализом и системой колориметрического определения Salmonella и Listeria.
Последняя выпускаемая система для ЦРП — это система TaqMan (фирма Perkin- Elmer, США). В ней используется новая зондовая система, включающая метку TaqMan Label Она не флюоресцирует в исходном виде, но после того, как зонд связан между праймерами ЦРП, на него может действовать фермент полимераза ДНК, используемый в ЦРП для формирования флюоресцирующего конечного продукта. Эта флюоресценция определяется с помощью специальной системы обнаружения. Выпускаются комплекты TaqMan для Salmonella, разрабатываются комплекты для Listeria и E. coli 0157. Одна из наиболее интересных перспектив применения TaqMan — это количественное определение. В настоящее время все системы на основе ЦРП служат для определения наличия или отсутствия микроорганизмов, а методики и приборы TaqMan могут дать информацию о фактической численности микроорганизмов, то есть ЦРП здесь применяется для их быстрого подсчета.
Выделение микроорганизмов из пищевых продуктов и их концентрирование
Один из способов решения этой проблемы связан с отделением и концентрированием микроорганизмов из пищевых продуктов, чтобы можно было определять микроорганизмы в более высокой концентрации. Дополнительное преимущество заключается в том, что клетки микроорганизмов могут быть отделены от пищевой матрицы, которая в некоторых случаях может содержать материалы, мешающие определению. Простой пример использования концентрирования — это анализ чистых жидкостей (воды, прозрачных безалкогольных напитков, вин, пива и т. п.), в которых уровни загрязнения обычно очень низки. Поэтому для концентрирования микроорганизмов в небольшой зоне большие их объемы подвергают мембранному фильтрованию. Задержанные микроорганизмы могут затем быть проанализированы. Подробный анализ методов концентрирования приведен в работе [11]. Можно выделить пять категорий таких методов: фильтрация, центрифугирование, фазовое разделение, электрофорез и иммунные методы.
Из этих категорий стадии промышленного производства для применения в анализе твердых пищевых продуктах достигли лишь иммунные методы. Иммуномагнитное отделение основано на покрытии маленьких магнитных частиц специфическими антителами для определенной клетки. Покрытые частицы могут быть добавлены в пищевую суспензию или питательную среду, и в случае присутствия определяемых клеток они прикрепляются к антителам на этих частицах.
Применение магнитного поля удерживает частицы с прикрепленными к ним клетками, позволяя слить избыток жидкости и пиЩевые остатки, и, тем самым, отделить клетки от пищевой матрицы и сконцентрировать их. Такая система выпускается компаниями Dynal (Норвегия), LabM (Великобритания) и Denka (Япония), а автоматизированную систему на основе такой процедуры производит Foss Electric (EIAFOSS). Комплекты для Salmonella, Listeria, Е. coli 0157, других производящих вероцитотоксин Е. coli и Campylobacter производят разные фирмы. Системы, реализующие методы иммуномагнитного разделения для определения присутствия Е. coli 0157, нашли широкое применение, и во многих странах эти методы стали стандартными.
Распознавание и определение характеристик микроорганизмов
После выделения микроорганизмов из пищевого продукта иногда необходимо установить, какой именно это микроорганизм. Это особенно важно, если предполагается, что это патоген. Традиционно в методах идентификации использовались биохимические или иммунологические анализы, а также очищенные микроорганизмы. Прогресс молекулярной биологии сделал возможным идентификацию микроорганизмов по структуре их ДНК. Чувствительность методов, основанных на ДНК, фактически делает возможной идентификацию до уровня ниже, чем вид (обычно эту процедуру называют характеризацией или субтипированием). Субтипирование — это новый мощный инструмент, используемый микробиологами не только для обозначения микроорганизма, но и для установления его происхождения. Поэтому в некоторых случаях можно выделить микроорганизм в готовом продукте, а затем с помощью структурированной серии тестов найти, было ли его источником определенное сырье, среда в производственной зоне или плохо вымытые части оборудования.
Разработан ряд основанных на ДНК методов анализа, которые делают возможным субтипирование (многие из них рассмотрены в [17]), однако лишь один метод был полностью автоматизирован и стал доступен для микробиологов лабораторий пищевых предприятий. Это риботипирование с помощью прибора Qualicon RiboPrinter (фирмы Qualicon, США). В этот полностью автоматизированный прибор подают выделенные очищенные колонии бактерий и получают образцы диапазонов ДНК (RiboPrint-структуры), которые автоматически сравнивают с базами данных для идентификации и характеризации. Метод успешно применен в пищевой промышленности для определения загрязнений, выявления источников и путей загрязнения, а также проверки аутентичности культур [12].
Будущее микробиологических методов
Традиционные микробиологические методы в последние несколько десятилетий не очень существенно изменились. Для подсчета, обнаружения и идентификации микроорганизмов в пробах микробиологи в основном продолжают использовать длительное обогащение и методы, основанные на росте микроорганизмов на агаре. По мере развития технологии пищевых производств постоянно растет потребность во все более быстром получении микробиологических данных.
Ускоренное развитие рынка охлажденных продуктов и производство продуктов с относительно короткими сроками хранения привели к созданию ускоренных автоматических методов и систем для их реализации. Их применение делает возможным: а) тестирование сырья перед использованием; б) контроль санитарно-гигиенического состояния технологических линий в реальном времени и в) тестирование готовых продуктов за более короткое время. Все это должно привести к созданию продуктов более высокого качества с увеличенными сроками хранения.
Все рассмотренные в этой главе методы в настоящее время используются в лабораториях пищевых производств. Некоторые методы (например, электрические) разработаны, внедрены и используются уже достаточно давно, тогда как другие (например, ЦРП) разработаны гораздо позже. Все эти методы имеют хорошие перспективы, приняты в качестве стандартных и не являются совершенно новыми. Некоторые производители пищевых продуктов уже начинают понимать преимущества комбинирования различных экспресс-методов для получения еще более быстрых результатов. Примером может служить использование ферментного иммунологического анализа для обнаружения присутствия подвидов Listeria с последующим использованием зондов из нуклеиновых кислот (специфичных для разновидностей микроорганизмов) для подтверждения присутствия или отсутствия L. monocytogenes.
Одной из проблем некоторых экспресс-методов является их недостаточная чувствительность. Во многих случаях это означает, что перед их использованием требуется длительное обогащение. Исследования методов отделения и концентрирования микроорганизмов из пищевых проб позволили бы отделить микроорганизмы от пищевых остатков и сконцентрировать их, исключая необходимость в длительных процедурах инкубации. Разработки в области ДНК-методов для обнаружения и идентификации/характеризации ведут к созданию новых средств для микробиологов пищевых производств. Несомненно, что в будущем они дадут такие возможности для анализа, которые сегодня трудно себе представить.
Литература для всего раздела » Традиционные и ускоренные методы микробиологического анализа.»




















