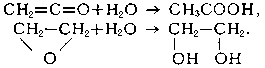Гидратация
Полезное
Смотреть что такое «Гидратация» в других словарях:
Гидратация — иона натрия Гидратация (от др. греч. ὕδωρ вода) присоединение молекул воды к молекулам или … Википедия
Гидратация — 1. Процесс связывания частиц растворимого в воде вещества с молекулами воды. Г. является частным случаем сольватации присоединения к веществам какого либо растворителя. Г. электролитов в растворах является главной причиной их диссоциации на ионы … Геологическая энциклопедия
ГИДРАТАЦИЯ — Общее название, прилагаемое обыкновенно ко всем химическим реакциям, при котор. происходит присоединение воды. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. гидратация ((гр. hydor вода) присоединение воды к… … Словарь иностранных слов русского языка
ГИДРАТАЦИЯ — ГИДРАТАЦИЯ, хим. термин, обозначающий процесс присоединения воды к какому либо веществу. Сюда относятся: I. Выделение из водного раствора какого либо вещества кристаллов, содержащих на одну молекулу вещества разное колич. молекул воды.… … Большая медицинская энциклопедия
ГИДРАТАЦИЯ — присоединение воды к веществу. Может протекать с разрушением молекул воды, напр., при синтезе этанола гидратация этилена, или без их разрушения, напр., при образовании кристаллогидратов. Обусловливает растворимость веществ в воде,… … Большой Энциклопедический словарь
гидратация — сольватация Словарь русских синонимов. гидратация сущ., кол во синонимов: 5 • гипергидратация (1) • … Словарь синонимов
Гидратация — [гр. hydro – вода] – межмолекулярное взаимодействие веществ, обладающих избыточной свободной энергией, с водой, при котором молекулы воды не разрушаются, с образованием новых соединений – гидратов постоянного или переменного… … Энциклопедия терминов, определений и пояснений строительных материалов
ГИДРАТАЦИЯ — ГИДРАТАЦИЯ, присоединение воды ионом или веществом. Гидрат комплексное соединение, как, например, сульфат меди (II), которое содержит связанную воду, чьи молекулы слабо привязаны к каждому кристаллу (CuSO435H2O). ЭТАН может быть гидратирован для… … Научно-технический энциклопедический словарь
гидратация — Химическое присоединение воды к различным веществам [Терминологический словарь по строительству на 12 языках (ВНИИИС Госстроя СССР)] EN hydration DE Hydration FR hydratation … Справочник технического переводчика
гидратация — Вид механического выветривания горных пород, когда при наличии воды внутри минералов она расширяет поры и приводит к разрушению породы … Словарь по географии
ГИДРАТАЦИЯ — присоединение молекул воды к различным веществам; является частным случаем (см.). Г. широко применяют для получения кислот, спиртов, альдегидов, гашёной извести и др … Большая политехническая энциклопедия
ГИДРАТАЦИЯ. ГИДРАТЫ. ГИДРОЛИЗ
ГИДРАТАЦИЯ. ГИДРАТЫ. ГИДРОЛИЗ. Гидратация (греч. «хюдор» – вода) – присоединение воды к ионам, атомам или молекулам. Продукты такого процесса называются гидратами. Гидролиз (греч. «лисис» – разложение, растворение) – химическая реакция разложения вещества водой.
В течение многих лет химики считали растворение веществ в воде чисто физическим процессом. И сейчас в школьных учебниках к таковым относят, например, растворение в воде сахара. Действительно, при испарении воды из раствора сахара при пониженном давлении легко получить исходное вещество в неизменном виде.
В то же время накапливались данные о том, что процесс растворения нельзя считать чисто механическим смешением компонентов, как, например, гексана и гептана. Так, растворы хлорида натрия и многих других соединений обладают электропроводностью, а сам процесс растворения нередко сопровождается значительными тепловыми эффектами (см. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ). Более того, некоторые соединения при растворении изменяют даже цвет. Например, сульфат меди бесцветный, а его разбавленный раствор – голубой, хлорид кобальта(II) голубой, а его водные растворы розовые. Все эти факты показывают, что растворение в воде – физико-химический процесс, вызванный гидратацией, то есть взаимодействием вещества с водой.
В ходе гидратации в ряде случаев происходит обратимое присоединение воды к ионам, атомам или молекулам растворяемого вещества с образованием гидратов. Так, при растворении в воде кристаллических ионных соединений (солей, щелочей, а также некоторых кислот, например, лимонной и щавелевой), молекулярных соединений (хлороводорода, серной кислоты, спирта, глюкозы и др.) происходит гидратация катионов и анионов, из которых состоит растворяемое вещество, либо гидратация ионов, образующихся в процессе растворения. При этом молекулы воды сохраняются как целое.
| Ион | Энергия гидратации, кДж/моль | Ион | Энергия гидратации, кДж/моль |
| H + | 1076 | Sr 2+ | 1477 |
| H3O + | 460 | Ba 2+ | 1339 |
| Li + | 502 | Zn 2+ | 2130 |
| Na + | 410 | Al 3+ | 4548 |
| K + | 329 | F – | 473 |
| NH4 + | 330 | Cl – | 330 |
| Rb + | 314 | Br – | 296 |
| Cs + | 264 | I – | 264 |
| Mg 2+ | 1887 | OH – | 339 |
| Ca 2+ | 1569 | MnO4 – | 247 |
Алгебраическая сумма энергии кристаллической решетки (или энергии разрыва связей) растворяемого вещества и энергии гидратации ионов определяет суммарный тепловой эффект растворения. В случае ионных соединений процесс может быть существенно экзотермическим (растворение в воде серной кислоты, гидроксидов натрия и калия может вызвать даже вскипание раствора), существенно эндотермическим (стакан с водой, в котором быстро растворяют нитрат аммония, примерзает к влажной подставке) или термонейтральным (растворение бромида натрия практически не сопровождается изменением температуры).
При кристаллизации многих солей из их водных растворов молекулы воды входят в состав кристаллической решетки с образованием кристаллогидратов различного состава, например, LiCl·H2O, CuCl2·2H2O, Ba(ClO4)2·3H2O, CdBr2·4H2O, Na2S2O3·5H2O, AlCl3·6H2O, FeSO4·7H2O, MgI2·8H2O, Fe(NO3)3·9H2O, Na2SO4·10H2O, Na2HPO4·12H2O, Al2(SO4)3·18H2O и др. При нагревании, а также при хранении на воздухе (особенно при низкой влажности) многие кристаллогидраты выветриваются, теряя частично или полностью молекулы воды.
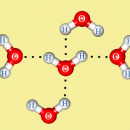
Гидратация молекулярных соединений происходит обычно за счет водородных связей и, как правило, не сопровождается существенным тепловым эффектом. Примером может служить растворение сахара. Молекулы воды легко образуют водородные связи с гидроксильными группами, поэтому даже вещества с большими молекулами хорошо растворяются в воде, если содержат много гидроксильных групп (сахароза, поливиниловый спирт). Соединения с небольшими полярными молекулами также легко гидратируются полярными молекулами воды, поэтому такие соединения обычно хорошо растворяются в воде. Примером может служить ацетонитрил СН3CN, который смешивается с водой в любых отношениях.
Необычные гидраты с некоторыми соединениями образует вода, находящаяся в твердом состоянии. В этих гидратах атомы, молекулы ряда веществ включаются в пустоты кристаллической решетки льда. Эти пустоты могут заполняться небольшими молекулами, такими как О2, N2, H2S, СН4, атомами благородных газов. Такие соединения «без химической связи» называют газовыми гидратами. Другие их название – клатраты (соединения включения). Отсутствие химических связей приводит к самым необычным соотношениям молекул воды и включенного вещества. Например, при низких температурах устойчивы соединения, содержащие на 46 молекул Н2О восемь атомов аргона, криптона, ксенона или радона. А вот маленькие атомы гелия и неона таких клатратов не образуют, так как они «ускользают» из слишком больших для них пустот. Клатрат состава Сl2·8H2O получил еще Дэви в 1811 из насыщенного при 0° С водного раствора хлора.
Клатраты, образованные водой и метаном, а также другими газами, часто называют газовыми гидратами. Внешне они похожи на снег или рыхлый лет, но под давлением могут существовать и при плюсовых температурах. Поэтому газовые гидраты могут закупорить газопровод и привести к аварии. Гидраты метана широко распространены в природе, в особенности на шельфе океанов; запасы природного газа в виде газовых гидратов значительно превышают его запасы в свободном состоянии.
Гидратация как химическое взаимодействие с водой может сопровождаться разрушением молекул воды, в этом случае происходит необратимая химическая реакция, которую обычно называют гидролизом – разложением водой. Реакции гидролиза известны как в неорганической, так и в органической химии. Примерами гидролиза неорганических соединений могут служить следующие процессы:
Гидролиз солей, образованных сильным основанием (щелочью) и слабой кислотой или слабым основанием и сильной кислотой сопровождается изменением кислотности среды: Na2S + H2O ® NaHS + NaOH, AlCl3 + H2O ® Al(OH)Cl2 + HCl. В случае таких солей как Al2S3 (их можно получить только сухим путем) гидролиз идет до конца с выделением гидроксида металла и слабой кислоты.
В органической химии реакции гидролиза сопровождаются либо разрушением органической молекулы (гидролиз сложных эфиров, белков): CH3COOC2H5 + H2O ® CH3COOH + C2H2OH, либо заменой в молекуле какой-либо группы на остаток молекулы воды, обычно гидроксил (гидролиз алкилгалогенидов): C2H5Br + H2O ® C2H5OH + HBr. В обоих случаях гидролизу способствует присутствие щелочи, которая связывает выделяющуюся кислоту. В случае белков и других биологически активных молекул реакцию гидролиза направляют в нужном направлении специальные ферменты – гидролазы. Например, фермент амилаза способствует гидролизу крахмала; фермент трипсин направленно гидролизует в белках пептидные связи, образованные аминокислотами аргинином и лизином.
Примерами реакции гидратации в органической химии может служить каталитическая гидратация алкенов с образованием спиртов:
Реакции гидратации широко используются в промышленном органическом синтезе. Например, каталитической гидратацией из этилена получают этиловый спирт, из пропилена – пропиловый спирт, из ацетилена – уксусный альдегид, из метилацетилена – ацетон. Реакция гидратации с образованием гидратов является ключевой при формовании изделий из гипса, при «схватывании» цемента. Образование газовых гидратов используют для разделения многокомпонентных газовых смесей. Наличие запасов гидратов метана в недрах Земли перспективно для будущей добычи природного газа. Реакции гидролиза широко используются в лабораторной практике и в промышленности. Гидролизом целлюлозы получают называемый гидролизный этиловый спирт, гидролизом сахарозы – глюкозу и фруктозу, гидролизом жиров – глицерин и соли карбоновых кислот – мыла. Ферментативный гидролиз органических соединений широко применяется в пищевой, текстильной и фармацевтической промышленности.
Что такое гидратация пример
В течение многих лет химики считали растворение веществ в воде чисто физическим процессом. И сейчас в школьных учебниках к таковым относят, например, растворение в воде сахара. Действительно, при испарении воды из раствора сахара при пониженном давлении легко получить исходное вещество в неизменном виде.
В то же время накапливались данные о том, что процесс растворения нельзя считать чисто механическим смешением компонентов, как, например, гексана и гептана. Так, растворы хлорида натрия и многих других соединений обладают электропроводностью, а сам процесс растворения нередко сопровождается значительными тепловыми эффектами ( см. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ). Более того, некоторые соединения при растворении изменяют даже цвет. Например, сульфат меди бесцветный, а его разбавленный раствор голубой, хлорид кобальта(II) голубой, а его водные растворы розовые. Все эти факты показывают, что растворение в воде физико-химический процесс, вызванный гидратацией, то есть взаимодействием вещества с водой.
В ходе гидратации в ряде случаев происходит обратимое присоединение воды к ионам, атомам или молекулам растворяемого вещества с образованием гидратов. Так, при растворении в воде кристаллических ионных соединений (солей, щелочей, а также некоторых кислот, например, лимонной и щавелевой), молекулярных соединений (хлороводорода, серной кислоты, спирта, глюкозы и др.) происходит гидратация катионов и анионов, из которых состоит растворяемое вещество, либо гидратация ионов, образующихся в процессе растворения. При этом молекулы воды сохраняются как целое.
| Ион | Энергия гидратации, кДж/моль | Ион | Энергия гидратации, кДж/моль |
| H + | 1076 | Sr 2+ | 1477 |
| H 3 O + | 460 | Ba 2+ | 1339 |
| Li + | 502 | Zn 2+ | 2130 |
| Na + | 410 | Al 3+ | 4548 |
| K + | 329 | F – | 473 |
| NH 4 + | 330 | Cl – | 330 |
| Rb + | 314 | Br – | 296 |
| Cs + | 264 | I – | 264 |
| Mg 2+ | 1887 | OH – | 339 |
| Ca 2+ | 1569 | MnO 4 – | 247 |
Алгебраическая сумма энергии кристаллической решетки (или энергии разрыва связей) растворяемого вещества и энергии гидратации ионов определяет суммарный тепловой эффект растворения. В случае ионных соединений процесс может быть существенно экзотермическим (растворение в воде серной кислоты, гидроксидов натрия и калия может вызвать даже вскипание раствора), существенно эндотермическим (стакан с водой, в котором быстро растворяют нитрат аммония, примерзает к влажной подставке) или термонейтральным (растворение бромида натрия практически не сопровождается изменением температуры).
При кристаллизации многих солей из их водных растворов молекулы воды входят в состав кристаллической решетки с образованием кристаллогидратов различного состава, например, LiCl·H2O, CuCl2·2H2O, Ba(ClO4)2·3H2O, CdBr2·4H2O, Na 2S2O3·5H2O, AlCl3·6H2O, FeSO4·7H2O, MgI2·8H2O, Fe(NO3)3·9H2O, Na2SO4·10H2O, Na2HPO4·12H2O, Al2(SO4)3·18H2O и др. При нагревании, а также при хранении на воздухе (особенно при низкой влажности) многие кристаллогидраты выветриваются, теряя частично или полностью молекулы воды.
Гидратация молекулярных соединений происходит обычно за счет водородных связей и, как правило, не сопровождается существенным тепловым эффектом. Примером может служить растворение сахара. Молекулы воды легко образуют водородные связи с гидроксильными группами, поэтому даже вещества с большими молекулами хорошо растворяются в воде, если содержат много гидроксильных групп (сахароза, поливиниловый спирт). Соединения с небольшими полярными молекулами также легко гидратируются полярными молекулами воды, поэтому такие соединения обычно хорошо растворяются в воде. Примером может служить ацетонитрил СН3CN, который смешивается с водой в любых отношениях.
Необычные гидраты с некоторыми соединениями образует вода, находящаяся в твердом состоянии. В этих гидратах атомы, молекулы ряда веществ включаются в пустоты кристаллической решетки льда. Эти пустоты могут заполняться небольшими молекулами, такими как О2, N2, H2S, СН4, атомами благородных газов. Такие соединения «без химической связи» называют газовыми гидратами. Другие их название клатраты (соединения включения). Отсутствие химических связей приводит к самым необычным соотношениям молекул воды и включенного вещества. Например, при низких температурах устойчивы соединения, содержащие на 46 молекул Н2О восемь атомов аргона, криптона, ксенона или радона. А вот маленькие атомы гелия и неона таких клатратов не образуют, так как они «ускользают» из слишком больших для них пустот. Клатрат состава Сl2·8H2O получил еще Дэви в 1811 из насыщенного при 0° С водного раствора хлора.
Клатраты, образованные водой и метаном, а также другими газами, часто называют газовыми гидратами. Внешне они похожи на снег или рыхлый лет, но под давлением могут существовать и при плюсовых температурах. Поэтому газовые гидраты могут закупорить газопровод и привести к аварии. Гидраты метана широко распространены в природе, в особенности на шельфе океанов; запасы природного газа в виде газовых гидратов значительно превышают его запасы в свободном состоянии.
Гидратация как химическое взаимодействие с водой может сопровождаться разрушением молекул воды, в этом случае происходит необратимая химическая реакция, которую обычно называют гидролизом разложением водой. Реакции гидролиза известны как в неорганической, так и в органической химии. Примерами гидролиза неорганических соединений могут служить следующие процессы:
Гидролиз солей, образованных сильным основанием (щелочью) и слабой кислотой или слабым основанием и сильной кислотой сопровождается изменением кислотности среды: Na2S + H2O ® NaHS + NaOH, AlCl3 + H2O ® Al(OH)Cl2 + HCl. В случае таких солей как Al2S3 (их можно получить только сухим путем) гидролиз идет до конца с выделением гидроксида металла и слабой кислоты.
В органической химии реакции гидролиза сопровождаются либо разрушением органической молекулы (гидролиз сложных эфиров, белков): CH3COOC2H5 + H2O ® CH3COOH + C2H2OH, либо заменой в молекуле какой-либо группы на остаток молекулы воды, обычно гидроксил (гидролиз алкилгалогенидов): C2H5Br + H2O ® C2H5OH + HBr. В обоих случаях гидролизу способствует присутствие щелочи, которая связывает выделяющуюся кислоту. В случае белков и других биологически активных молекул реакцию гидролиза направляют в нужном направлении специальные ферменты гидролазы. Например, фермент амилаза способствует гидролизу крахмала; фермент трипсин направленно гидролизует в белках пептидные связи, образованные аминокислотами аргинином и лизином.
Примерами реакции гидратации в органической химии может служить каталитическая гидратация алкенов с образованием спиртов:
Реакции гидратации широко используются в промышленном органическом синтезе. Например, каталитической гидратацией из этилена получают этиловый спирт, из пропилена пропиловый спирт, из ацетилена уксусный альдегид, из метилацетилена ацетон. Реакция гидратации с образованием гидратов является ключевой при формовании изделий из гипса, при «схватывании» цемента. Образование газовых гидратов используют для разделения многокомпонентных газовых смесей. Наличие запасов гидратов метана в недрах Земли перспективно для будущей добычи природного газа. Реакции гидролиза широко используются в лабораторной практике и в промышленности. Гидролизом целлюлозы получают называемый гидролизный этиловый спирт, гидролизом сахарозы глюкозу и фруктозу, гидролизом жиров глицерин и соли карбоновых кислот мыла. Ферментативный гидролиз органических соединений широко применяется в пищевой, текстильной и фармацевтической промышленности.
ГИДРАТАЦИЯ
(от греч. hydor-вода), присоединение воды к молекулам, атомам или ионам. Может осуществляться без разрушения или с разрушением молекул воды. Г. без разрушения молекул воды приводит к гидратам. Обусловлена электростатич. и ван-дер-ваальсовым взаимодействиями, координационными и иногда водородными связями. Г. в растворе-частный случай сольватации.
Г. молекул в р-рах изучена недостаточно. Энтальпии Г. молекул, отсчитанные, как и для ионов, от их стандартных состояний в вакууме, содержат вклад, обусловленный влиянием молекул растворенного в-ва на водородные связи между молекулами воды, и обычно не превышают неск. десятков кДж/моль.
Г.-важный фактор, обусловливающий р-римость в-в в воде, электролитич. диссоциацию, распределение в-в между фазами в многокомпонентных системах, содержащих воду, кинетику и равновесие р-ций в водных р-рах, образование кристаллогидратов (см. также Растворы неэлектролитов, Растворы электролитов, Гидраты):
Г.с разрушением молекул воды широко распространена в неорг. и орг. химии. Г. оксидов элементов приводит в зависимости от их природы к образованию щелочей, к-т или амфотерных гидроксидов. Эта р-ция-основа мн. пром. процессов, напр. получения серной и азотной к-т, твердения вяжущих материалов (при этом происходит также образование кристаллогидратов). С .И. Дракин.
Г. непредельных углеводородов-важнейшая стадия во мн. процессах переработки нефтяного сырья, попутных и прир. газов. Г. используется в пром-сти для получения, напр., этанола из этилена, изопропанола из пропилена, ацетальдегида и ацетона из ацетилена, этиленгликоля из этиленоксида, уксусной к-ты и ее ангидрида из кетена. Г.-одна из стадий синтеза карбоновых к-т из олефинов. См. также Дегидратация.
Лит.: Креетов Г. А., Термодинамика ионных процессов в растворах, 2 изд., Л., 1984.
Смотреть что такое ГИДРАТАЦИЯ в других словарях:
ГИДРАТАЦИЯ
общее название, прилагаемое обыкновенно ко всем тем хим. реакциям, при которых происходит присоединение воды. Реакции эти чрезвычайно многочисленны и р. смотреть
ГИДРАТАЦИЯ
(от греч. hydor — вода) процессы связывания воды химическими веществами. Различают несколько видов Г. Г. окислов приводит к гидроокисям. смотреть
ГИДРАТАЦИЯ
гидратация ж. Физико-химический процесс взаимодействия растворенных веществ с водой.
ГИДРАТАЦИЯ
ГИДРАТАЦИЯ
ГИДРАТАЦИЯ
Гидратация — общее название, прилагаемое обыкновенно ко всем тем химическим реакциям, при которых происходит присоединение воды. Реакции эти чрезвычайно многочисленны и разнообразны, совершаются повсюду в природе и беспрестанно применяются как в лабораторной практике, так и в различных производствах. При всем их разнообразии можно ясно различить три типа реакций Г.: 1) прямые реакции соединения с водой; 2) реакции соединения, совершающиеся при участии хим. деятелей, и 3) гидролиз или разложения (образование двух или более веществ из одного + вода), производимые водой через ее присоединение, большей частью также требующие воздействия третьего тела. Прямо соединяются с водой: кислотные и основные (щелочные и щелочноземельные) ангидриды, образуя соответствующие гидраты; безводные соли, а также многие из вышеупомянутых гидратов, образуя кристаллогидраты; простые эфиры многоатомных спиртов, образуя соответствующие спирты. Все эти реакции за немногими исключениями (напр. переход метафосфорной кислоты в ортофосфорную, Г. окиси этилена и некотор. др.) идут более или менее легко и быстро либо при простом соприкосновении с водой, либо при растворении в ней, и сопровождаются отделением тепла, часто весьма значительным [Некоторые случаи Г. ангидридов соединены с распадением сложной частицы на 2 простейшие, напр. уксусный анг., соединяясь с водой, распадается с образованием 2 частиц уксусной кислоты: Тем не менее, эта и др., подобные ей, реакции по всему своему характеру принадлежат к 1-ой группе реакций Г. точно так же, как образование хлористого водорода из хлора и водорода (Н 2 + Cl2 = 2НCl) есть реакция соединения. Реакции разложения водой хлорангидридов кислот, в сущности, представляют также реакции Г., сходные с Г. смешанных кислотных ангидридов.]. Вторая группа реакций Г. обнимает собой сравнительно немногие случаи присоединения воды к непредельным соединениям, как то: Г. этиленных углеводородов в одноатомные предельные спирты и непредельных одноатомных спиртов в гликоли при нагревании их с разведенными кислотами, присоединение воды к ацетилену, пропаргиловому спирту и т. п. в присутствии бромной ртути и Г. некоторых терпенов под влиянием кислот. Несравненно более разнообразны реакции гидролиза. Сюда относятся: омыление (см.) сложных эфиров водой и основаниями, при чем происходит распадение эфиров на спирт и кислоту C2H3 O.С 2H5 O (уксусноэтиловый эфир) + Н 2O = C2H4O2 (уксусн. эт. спирт) + C 2H6O; гидролиз при кипячении с разведенными кислотами или под влиянием неорганизованных ферментов (диастаза, растворимого фермента дрожжей и друг.), глюкозидов [напр.: С 13 Н 18 О 7 (салицин) + Н 2O = C6 Н 12O6 (глюкоза) + C7H8O2 (салигенин)] и углеводов (напр. превращение крахмала при действии диастаза солода в мальтозу: (C6H10O5)n + (Н 2O)n = nC6H12O6, и инверсия сахара (C12H22O11 (сахар) + H 2O = C6H12O6 (глюкоза) + C 6H12O6 (фруктоза); Г. нитрилов, илидов, амидов и аминовых кислот, распадающихся при действии водных минеральных кислот или оснований на кислоты и аммиак (напр. С 2O2(NH2)2 (оксамид) + 2Н 2O = C2H2O4 (щавел. к.) + 2NH 3 или CNOH (циановая кисл.) + Н 2 O = СО 2 (углек.) + NH 3; Г. с помощью кислот альдоксимов, кетоксимов и гидроксамовых кислот, гидразонов и озазонов, которые разлагаются при этом на альдегиды, кетоны, кислоты, глюкозы и оксиглюкозы, с одной стороны, и гидроксиламин и фенилгидразин, с другой, и, наконец, реакции Г. амидоксимов, изонитрилов, ортоэфиров, имидоэфиров, ангидримидокислот и амидинов и некотор. др. Более сложные относящиеся сюда случаи Г. представляют белковые вещества. Таковы процессы пептонизации белков (см. Пептоны) под влиянием, напр., неорганизованного фермента желудочного сока, пепсина, в присутствии слабой соляной кислоты и процессы гниения их [Здесь Г. соединена с окислением.] под влиянием жизнедеятельности особых бактерий, сопровождающиеся постепенным распадом белковых тел с образованием сперва пептонов, лейцина и тирозина и далее аммиака, сероводорода, угольной, серной и органических (жирных и ароматических) кислот, фенолов, индола, скатола и др. тел. Вода, щелочи и кислоты также способны при нагревании различным образом гидратировать белки, расщепляя их на тела отчасти такие же, отчасти подобные тем, которые происходят при гниении. Реакции Г. 2 и 3 группы протекают по большей части медленно, не обнаруживая значительных тепловых явлений. Что касается роли третьего вещества при них, то она может быть троякой. Гидратирующее вещество реагирует с одним из продуктов Г., вступая с ним в соединение, напр., щелочь с кислотой, образующейся при омылении эфиров, или минеральная кислота с аммиаком при распадении амидов. Гидратирующее вещество, само оставаясь в конце превращения неизмененным, тем не менее принимает непосредственное участие в реакции, как, напр., серная кислота при Г. этилена, выражающейся след. 2 уравнениями: CH2.CH2 + H(HSO4) = CH3.CH2(HSO4) и СН 3.СН 2 (НSО 4) + Н 2 O = СН 3.СН 2 (НО) + H(HSO 4). Наконец, оно может действовать контактом (см). Таково, по-видимому, действие диастаза и слабых кислот на глюкозиды и углеводы и пепсина на белки. П. П. Рубцов. Δ.
ГИДРАТАЦИЯ
— 1. Процесс связывания частиц растворимого в воде вещества с молекулами воды. Г. является частным случаем сольватации — присоединения к веществам какого-либо растворителя. Г. электролитов в растворах является главной причиной их диссоциации на ионы, обусловливает устойчивость ионов в растворах и препятствует обратному соединению ионов в молекулы. Реакции гидратации б. ч. обратимы; обратная реакция называется дегидратацией. Получаемые при этом соединения называются гидратами, а входящая в них вода — гидратной. Иногда гидратная вода так прочно связана с частицами растворенного вещества, что при выделении его из раствора входит в состав образующихся к-лов, называемых кристаллогидратами, а содержащаяся в них вода называется кристаллизационной. Особенно легко образуются кристаллогидраты разл. солей, причем на единицу разл. солей приходится от 1 до 12 молекул воды. В формулах ее пишут отдельно, напр., гипс — СаSО4·2Н2О, мирабилит — Na2SO4·10H2О и др. 2. Гидратация окислов заключается в разложении воды и окислов и построении новых соединений — гидроокисей. Н и О, входившие в состав воды, занимают в структуре новых соединений разл. самостоятельные позиции. Напр., брусит — Mg(OH)2, гидраргиллит — Аl(ОН)3 и др. Такая вода называется конституционной.3. Г. называют также поглощение воды коллоидами — адсорбция поверхностью частиц и поглощение цеолитной воды — в каналах кристаллической решетки (см. Вода в минералах). Г. характерна для процессов выветривания и регрессивного метаморфизма.