Гиперчувствительный пневмонит: от этиологии и патогенеза к диагностике и лечению
Иркутская государственная медицинская академия последипломного образования, кафедра клинической аллергологии и пульмонологии, Иркутск, Россия
В обзоре представлена характеристика внешнесредовых аллергенов, способных инициировать развитие гиперчувствительного пневмонита (ГП). Патогенез ГП рассматривается с позиции иммунокомплексной и Т-клеточной гиперчувствительности, в результате которых развиваются интерстициальная лимфоцитарная пневмония с гранулемами и сосуществующим бронхио-литом. По течению заболевание классифицируется как острое и хроническое, в рамках которого выделяется фибротический фенотип. Этиологические, патогенетические и клинические особенности заболевания лежат в основе диагностического алгоритма: оценки экспозиционного воздействия, характерных признаков компьютерной томографии легких, лимфоцитоза жидкости бронхоальвеолярного лаважа и при необходимости – легочной биопсии. Лечение направлено на основные патогенетические звенья ГП и включает элиминацию аллергена, противовоспалительную, иммуносупрессивную и при фибротическом варианте антифибротическую терапию.
Введение
Гиперчувствительный пневмонит (синонимы: экзогенный аллергический альвеолит, гиперсенситивный пневмонит) – интерстициальное заболевание легких, развивающееся в результате иммунологически опосредованного воспаления в ответ на повторно вдыхаемые вещества антигенной природы восприимчивыми лицами. Гораздо реже возможен неингаляционный вариант гиперчувствительного пневмонита (ГП) в качестве одной из форм лекарственно-индуцированных заболеваний легких.
Первое научное описание клинической картины ГП, возникшего у пяти фермеров после работы с влажным сеном, выполнено в 1932 г. J. Campbell, назвавшим заболевание «легкое фермера» [1]. Только через 30 лет установлены его этиологический фактор (Thermophilic actinomycetes) и иммунные механизмы патогенеза [2]. К тому времени стали определяться и другие клинические варианты ГП, в частности «легкое любителей птиц» среди лиц, занимавшихся разведением голубей [3]. В 1967 г. J. Pepys предложил обобщающее название «экзогенный аллергический альвеолит», под которым понималось заболевание, инициируемое различными внешнесредовыми антигенными факторами [4]. В современной медицинской литературе преобладает обозначение болезни как ГП, что наиболее полно отражает характер патологического процесса, т.к. кроме альвеол в него вовлекаются и другие легочные структуры: интерстиций, бронхиолы, сосуды, плевра, лимфоидная ткань.
Эпидемиология
Данные о заболеваемости и распространенности ГП на популяционном уровне ограниченны, что связано с его невысокой частотой и отсутствием стандартизованных методов диагностики. В то же время эти показатели при ГП значительно варьируются в различных когортах населения в зависимости от климатогеографических, экологических, бытовых и профессиональных факторов, особенностей хобби, а также этиологии болезни. Наиболее часто ГП регистрируется среди работников сельского хозяйства и птицеводов, рабочих пищевой и химической промышленности, деревообработчиков, варьируясь в исследованных группах в диапазоне от 1,3 до 16,1% [5–8]. Среди любителей голубей и других декоративных птиц заболевание выявляется от 6 до 30% случаев, показан 14-кратный риск ГП для лиц, длительно контактирующих с ними [9, 10].
Гораздо меньше исследований ГП на популяционном уровне. Заболеваемость ГП в Великобритании (база данных первичной медицинской помощи за 1991–2003 гг.) составила 0,9 случая на 100 тыс. в год [11], в Дании (Национальный регистр пациентов за 1998–2010 гг.) – 1,16 случая на 100 тыс. в год [12]. По данным эпидемиологического исследования в США (база данных медицинского страхования более 150 млн человек за 2004–2013 гг.), ежегодные показатели заболеваемости и распространенности ГП колебались в пределах 1,28–1,94 и 1,67– 2,71 на 100 тыс. человек соответственно [13].
Для оценки распространенности ГП также анализируется его удельный вес среди интерстициальных заболеваний легких (ИЗЛ). В большинстве европейских стран и США доля ГП среди других ИЗЛ находится в пределах 7–20%, по частоте уступая только идиопатическому легочному фиброзу (ИЛФ) и ИЗЛ в рамках ревматических заболеваний [14, 15]. В диапазон европейских показателей укладываются и данные по удельному весу ГП среди ИЗЛ в РФ: 10,0–12,5% [16–18].
Этиология
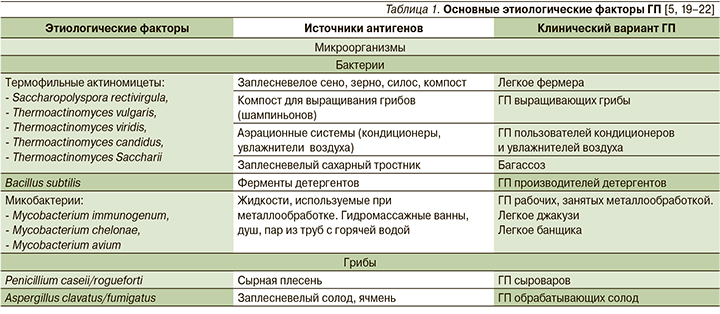
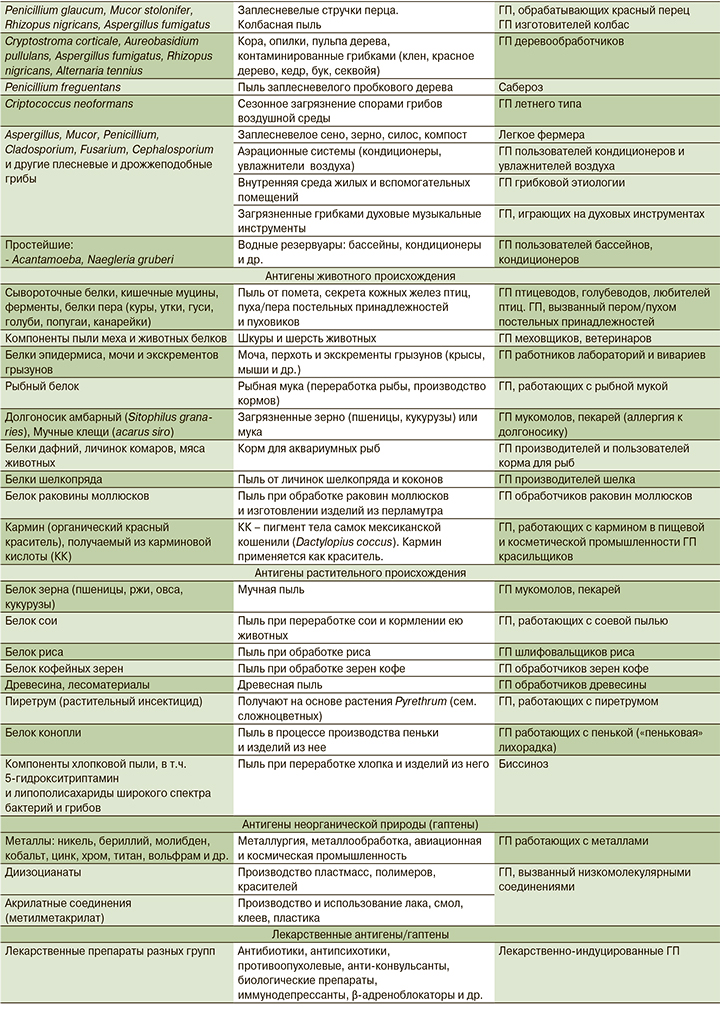
К настоящему времени известно более 200 внешнесредовых аллергенов, способных индуцировать развитие ГП. С учетом иммунобиологических и химических особенностей их обычно подразделяют на несколько групп (табл. 1): антигены микроорганизмов, животного и растительного происхождения, антигены неорганической природы (гаптены), лекарственные антигены/гаптены [19–22].
С экспозицией различных аллергенов человек сталкивается на работе, в домашних условиях, в процессе занятий, связанных с хобби. К наиболее частым причинам ГП относятся антигены микроорганизмов и животного происхождения. Среди людей, работающих в условиях сельского хозяйства, на приусадебных, дачных участках, контактирующих с гниющим и заплесневелым органическим материалом, пользующихся кондиционерами или увлажнителями воздуха, возможными причинами ГП могут быть бактериальные (термофильные актиномицеты) или грибковые аллергены. Термофильные актиномицеты широко распространены в почве, компосте, водной и влажной среде. Кроме высокой влажности необходимым условием для их жизнедеятельности является температура в пределах 40–60°С, развивающаяся при гниении органического субстрата или возникающая в бытовых приборах при их работе, где может накапливаться водный конденсат.
Кроме термофильных актиномицетов и Bacillus subtilis, используемых в производстве детергентов, большое значение придается другой разновидности бактерий – нетуберкулезным микобактериям (НТМ), распространенным в водных средах и способных контаминировать смазочноохлаждающие жидкос.
ПНЕВМОНИТ ГИПЕРЧУВСТВИТЕЛЬНЫЙ
Этиология
Патогенез
Длительный контакт с компонентами пыли приводит к образованию преципитирующих AT и формированию иммунных комплексов (ИК), а также активации альвеолярных макрофагов и Т-лим-фоцитов — эффекторов гиперчувствительности замедленного типа. Формирование ИК на уровне альвеолярно-капиллярной мембраны, а также высвобождение ферментов альвеолярными макрофагами и лим-фокинов Т-клетками сопровождается инфильтрацией интерстиция лимфоцитами и плазматическими клетками с образованием гранулёмы и нарушением процессов диффузии. В зависимости от интенсивности и продолжительности контакта с Аг, а также реактивности организма процесс может протекать в виде острого, подострого и хронического пневмонита, приводя в случае несвоевременного выявления и терапии к развитию фиброза лёгкого с прогрессирующей дыхательной недостаточностью и формированию лёгочного сердца.
Факторы риска
• Длительный контакт с пылью
• Размер частиц менее 5 мкм в диаметре (более крупные частицы до альвеол не проникают).
Клиническая картина
Специальные исследования
• Наличие преципитирующих AT в сыворотке. Следует учитывать, что у 40-50% лиц без признаков заболевания, но имевших длительный контакт с патогенными факторами окружающей среды, этот тест ложноположителен.
• Бронхоальвеолярный лаваж (редко). Характерные изменения:
• Острая форма: нейтрофилы и лимфоциты
• Хроническая форма: высокое содержание лимфоцитов (60%), в основном Т-клетки типа CD8 (в отличие от саркоидоза, при котором большинство Т-клеток типа CD4).
• Биопсия лёгкого (редко). Характерные изменения:
• Острый ГП
• Инфильтрация стенок альвеол нейтрофилами, плазматическими клетками, лимфоцитами, макрофагами
• Отёк межальвеолярных перегородок, в полости альвеол — экссудат
• Альвеолярные капилляры с фибриновыми и тромбоцитарными тромбами, но без признаков васкулита
• Хронический ГП
• Альвеолит и интерстициальное воспаление (присутствуют плазматические клетки и гистиоциты), формирование гранулём
• Локальное гранулематозное воспаление бронхиол
• Интерстициальный фиброз, в тяжёлых случаях образование сотового лёгкого.
• Провокационный ингаляционный тест с предполагаемыми аллергенами проводят прежде всего в исследовательских целях в специализированных отделениях.
Дифференциальный диагноз
Лечение:
• Прекращение воздействия аллергена
• Острая форма (тяжёлое течение)
• Глюкокортикоиды — преднизо-лон 60 мг/сут или его аналоги в эквивалентных дозах в течение 1-2 нед с последующим постепенным снижением дозы в течение 2 нед до 20 мг/сут, а затем — на 2,5 мг/нед вплоть до отмены
• Оксигенотерапия, бронхолитические, жаропонижающие, противокашлевые средства — при необходимости
• Антибиотики — только при присоединении инфекции
• Хроническая форма — лечение глюкокортикоидами продолжают в случае положительной клинической и рентгенологической динамики.
Осложнения
• Прогрессирующий интерстициальный фиброз
• Хроническое лёгочное сердце.
Прогноз хороший при остром ГП и своевременной элиминации и эффективном лечении начальных стадий заболевания.
Профилактика
• Борьба с запылённостью на рабочем месте
• Использование защитных масок
• Очистка систем вентиляции, кондиционеров и рабочих помещений.
Синонимы
• Экзогенный аллергический альвеолит
• Аллергический интерстициальный пневмонит
См. также Лёгкое фермера. Болезнь лёгких диффузная интерстициальная, Недостаточность дыхательная, Сердце лёгочное хроническое
Сокращения
• ГП — гиперчувствительный пневмонит
• ИК — иммунные комплексы
J67 Гиперчувствительный пневмонит, вызванный органической пылью
Примечания
• Остаточный объём (00) — объём воздуха, остающийся в лёгких после максимально усиленного выдоха
• Средняя объёмная скорость (СОС25-75% ) — скорость потока форсированного выдоха в его середине (т.е. между 25 и 75% ФЖЕЛ). СОС25_г5% прежде всего отражает состояние мелких дыхательных путей, что более информативно, чем ОФВ| при выявлении ранних обструктивных нарушений, и не зависит от усилия
• Объём форсированного выдоха за первую секунду (ОФВ1) — объём воздуха, изгоняемый с максимальным усилием из лёгких в течение первой секунды выдоха после глубокого вдоха. Прежде всего ОФВ, отражает состояние крупных дыхательных путей и часто выражается в процентах от ЖЕЛ (нормальное значение ОФВ, = 75% ЖЕЛ)
• ОФВ1/ФЖЕЛ — отношение ОФВ1 к ФЖЕЛ (индекс Тиффно), выраженное в процентах (в норме больше или равно 70%). Значение ОФВ1/ФЖЕЛ, прямо пропорциональное силе выдоха, важно для выявления обструктивных нарушений, но также помогает в диагностике рестриктивных расстройств. Снижение только ОФВ1 (ОФВ1/ФЖЕЛ <70%) свидетельствует об обструкции; снижение обоих показателей указывает на рестриктивную патологию
• Растяжимость лёгких (С) определяют по наклону кривой давление-объём (P-V) над уровнем дыхательного объёма: С = V/P (в норме 200 мл/см вод. ст.).
Полезное
Смотреть что такое «ПНЕВМОНИТ ГИПЕРЧУВСТВИТЕЛЬНЫЙ» в других словарях:
АСТМА БРОНХИАЛЬНАЯ — мед. Бронхиальная астма (БА) хроническое воспалительное заболевание дыхательных путей, сопровождающееся гиперреактивностью бронхов. Основное клиническое проявление периодически возникающие приступы затруднённого дыхания или удушья, вызываемые… … Справочник по болезням
БОЛЕЗНЬ ЛЁГКИХ ДИФФУЗНАЯ ИНТЕРСТИЦИАЛЬНАЯ — мед. Диффузная интерстициальная болезнь лёгких (ДИБЛ) общий термин для группы заболеваний, характеризующихся диф фузнрй воспалительной инфильтрацией и фиброзом мелких бронхов и альвеол. Этяодогня • факторы риска • Ингаляция различных веществ •… … Справочник по болезням
Экзогенный аллергический альвеолит — Экзогенный аллергический альвеолит … Википедия
Альвеоли́ты — (alveolitis; единственное число; лат. alveolus лунка, ячейка + itis) группа диффузных воспалительных процессов в респираторном отделе легкого с тенденцией к формированию фиброза интерстициальной ткани. А. может быть самостоятельным заболеванием… … Медицинская энциклопедия
АСПЕРГИЛЛЁЗ — мед. Аспергиллёз оппортунистический микоз, характеризующийся первичным поражением лёгких; у больных с иммунодефи цитами нередко заканчивается фатально (особенно при нейт ропениях или у лиц с трансплантатами костного мозга). Клинические проявления … Справочник по болезням
НЕДОСТАТОЧНОСТЬ ДЫХАТЕЛЬНАЯ — мед. Дыхательная недостаточность нарушение газообмена между окружающим воздухом и циркулирующей кровью с развитием гипоксемии, складывающегося из 2 этапов. • Вентиляция газообмен между окружающей средой и лёгкими. • Оксигенация внутрилёгочный… … Справочник по болезням
ПНЕВМОНИЯ БАКТЕРИАЛЬНАЯ — мед. Бактериальная пневмония острый или хронический воспалительный процесс нижних отделов дыхательных путей бактериальной этиологии. Инфекция может быть внебольничной или госпитальной (у больных, находившихся в стационаре по крайней мере в… … Справочник по болезням
Экзогенный аллергический альвеолит

Более 300 антигенов способны вызывать гиперчувствительный пневмонит, а на восемь из них приходится примерно 75 % случаевальвеолита. Чаще всего развитие заболевания связано с профессиональными факторами. Наиболее распространенными из антигенов являются термофильные актиномицеты и антигены птиц.
Причины развития экзогенного аллергического альвеолита
Thermophilic Actinomycetes: Mycropolyspora faeni, Thermoactinomyces vulgaris; Aspergillus spp.
Mycropolyspora faeni, Thermoactinomyces sacchari
Легкое лиц, выращивающих грибы
Thermoactinomyces vulgaris, Mycropolyspora faeni
Легкое лиц, использующих кондиционеры
Кондиционеры, увлажнители, обогреватели
Thermoactinomyces vulgaris, Thermoactinomyces viridis, Аmeba, Fungi
Кора пробкового дерева
Легкое варщиков солода
Частицы сыра, плесень
Древесная пыль секвойи
Ggaphium spp., Pupullaria spp., Alternaria spp.
Легкое производящих детергенты
Легкое любителей птиц
Экскременты, перхоть птиц
Сывороточные белки птиц
Легкое лабораторных работников
Моча и перхоть грызунов
Протеины мочи грызунов
Легкое нюхающих порошок гипофиза
Свиные и бычьи протеины
Легкое занятых в производстве пластмасс
Toluene diisocianate, diphenylmethane diisocianate
Пыль влажных жилых помещений (Япония)
Среди грибковых антигенов наибольшее значение имеет Aspergillus spp. Различные виды Aspergillus связаны с развитием таких заболеваний, как «легкое варщиков солода», «легкое сыроваров», субероз (болезнь, развивающаяся у работающих с корой пробкового дерева), а также «легкое фермера», «легкое лиц, пользующихся кондиционерами». Aspergillus fumigatus может стать причиной развития альвеолита у городских жителей, так как является частым обитателем сырых непроветриваемых теплых помещений.
Необходимым условием развития является ингаляция антигена в достаточной для развития болезни дозе.Экзогенный аллергический альвеолит считается иммунопатологическим заболеванием, в развитии которого ведущая роль принадлежит аллергическим реакциям.
Выделяют три типа течения заболевания: острое, подострое и хроническое.
Гиперчувствительный пневмонит
Полный текст:
Аннотация
Гиперчувствительный пневмонит (ГП) является воспалительным заболеванием легких и дыхательных путей, которое развивается в ответ на повторные ингаляции аэрозольных антигенов широкого спектра. Клиническая картина и течение очень вариабельны и зависят от таких факторов, как природа «виновного» антигена, интенсивность и длительность экспозиции с антигеном, а также от особенностей иммунного ответа пациента. Заболеваемость ГП составляет 1,28—1,94 случая на 100 тыс. населения в год. В настоящее время диагноз ГП обычно основан на наличии характерной клинической картины, данных компьютерной томографии высокого разрешения (КТВР), бронхоскопии, биопсии легких и данных о возможном «виновном» антигене. КТВР играет центральную роль в диагностике ГП. Наиболее частой находкой по данным КТВР при ГП является признак «матового стекла», который может сочетаться с центролобулярными узелками и воздушными ловушками. В некоторых случаях картина при фибротическом ГП очень сильно схожа с таковой при идиопатическом легочном фиброзе — изменения преобладают в нижних отделах и субплеврально. Терапия ГП обычно включает в себя исключение контакта с «виновным» антигеном, рассмотрение назначения глюкокортикостероидов и / или иммуносупрессантов, направленного на подавление активного воспалительного / иммунного ответа и лечение сопутствующих заболеваний. Терапия нинтеданибом у пациентов с прогрессирующими фиброзными интерстициальными заболеваниями легких приводит к замедлению скорости снижения легочной функции по сравнению с плацебо.
Ключевые слова
Об авторе
Автор декларирует отсутствие конфликта интересов.
Список литературы
1. Costabel U., Bonella F., Guzman J. Chronic hypersensitivity pneumonitis. Clin. Chest Med. 2012; 33 (1): 151-163. DOI: 10.1016/j.ccm.2011.12.004.
2. Selman M., Pardo A., King T.E. Jr. Hypersensitivity pneumonitis: insights in diagnosis and pathobiology. Am. J. Respir. Crit. Care Med. 2012; 186 (4): 314—324. DOI: 10.1164/rccm.201203-0513CI.
3. Spagnolo P., Rossi G., Cavazza A. et al. Hypersensitivity pneumonitis: a comprehensive review. J. Investig. Allergol. Clin. Immunol. 2015; 25 (4): 237—250.
4. Thomeer M.J., Costabe U., Rizzato G. et al. Comparison of registries of interstitial lung diseases in three European countries. Eur. Respir. J. Suppl. 2001; 32: 114s—118s.
5. Coultas D.B., Zumwalt R.E., Black W.C., Sobonya R.E. The epidemiology of interstitial lung diseases. Am. J. Respir. Crit. Care Med. 1994; 150 (4): 967—972. DOI: 10.1164/ajrc-cm.150.4.7921471.
6. Bang K.M., Weissman D.N., Pinheiro G.A. et al. Twenty-three years of hypersensitivity pneumonitis mortality surveillance in the United States. Am. J. Ind. Med. 2006; 49 (12): 997—1004. DOI: 10.1002/ajim.20405.
7. Rittig A.H., Hilberg O., Ibsen R., L0kke A. Incidence, comorbidity and survival rate of hypersensitivity pneumonitis: a national population-based study. ERJ Open. Res. 2019; 5 (4): 00259—2018. DOI: 10.1183/23120541.00259-2018.
8. Fernandez P6rez E.R., Kong A.M., Raimundo K. et al. Epidemiology of hypersensitivity pneumonitis among an insured population in the United States: a claims-based cohort analysis. Ann. Am. Thorac. Soc. 2018; 15 (4): 460—469. DOI: 10.1513/AnnalsATS.201704-288OC.
9. Depierre A., Dalphin J.C., Pernet D. et al. Epidemiological study of farmer’s lung in five districts of the French Doubs province. Thorax. 1988; 43 (6): 429—435. DOI: 10.1136/thx.43.6.429.
10. Rodrfguez de Castro F., Carrillo T., Castillo R. et al. Relationships between characteristics of exposure to pigeon antigens: clinical manifestations and humoral immune response. Chest. 1993; 103 (4): 1059—1063. DOI: 10.1378/chest.103.4.1059.
11. Lacasse Y., Selman M., Costabel U. et al. Clinical diagnosis of hypersensitivity pneumonitis. Am. J. Respir. Crit. Care Med. 2003; 168 (8): 952—958. DOI: 10.1164/rccm.200301-137OC.
12. Cormier Y., Letourneau L., Racine G. Significance of precipitins and asymptomatic lymphocytic alveolitis: a 20-yr follow-up. Eur. Respir. J. 2004; 23 (4): 523—525. DOI: 10.1183/09031936.04.00021104.
13. Mohr L.C. Hypersensitivity pneumonitis. Curr. Opin. Pulm. Med. 2004; 10 (5): 401—411. DOI: 10.1097/01.mcp.0000135675.95674.29.
14. Cooper C.J., Teleb M., Elhanafi S. et al. Bird fanciers’ lung induced by exposure to duck and goose feathers. Am. J. Case Rep. 2014; 15: 155—158. DOI: 10.12659/AJCR.890184.
15. Chan A.L., Juarez M.M., Leslie K.O. et al. Bird fancier’s lung: a state-of-the-art review. Clin. Rev. Allergy Immunol. 2012; 43 (1—2): 69—83. DOI: 10.1007/s12016-011-8282-y.
16. Morell F., Villar A., Ojanguren I. et al. Hypersensitivity pneumonitis and (idiopathic) pulmonary fibrosis due to feather duvets and pillows. Arch. Bronconeumol. [Preprint. Posted: Feb. 11, 2020]. DOI: 10.1016/j.arbres.2019.12.003.
17. Morell F., Villar A., Montero M.A. et al. Chronic hypersensitivity pneumonitis in patients diagnosed with idiopathic pulmonary fibrosis: a prospective case-cohort study. Lancet Respir. Med. 2013; 1 (9): 685—694. DOI: 10.1016/S2213-2600(13)70191-7.
18. Pereira C.A., Gimenez A., Kuranishi L., Storrer K. Chronic hypersensitivity pneumonitis. J. Asthma Allergy. 2016; 9: 171—181. DOI: 10.2147/JAA.S81540.
19. Hankwitz P.E., Cervia J.S., Thomas C.F. et al. Non-tuberculous mycobacterial hypersensitivity pneumonitis related to a home shower: treatment and secondary prevention. BMJ Case Rep.2011; 2011: bcr0620114360. DOI: 10.1136/bcr.06.2011.4360.
20. Dhar S., Daroowalla F. Hypersensitivity pneumonitis. Clin. Pulm. Med. 2011; 18 (4): 169—174. DOI: 10.1097/CPM.0b013e3182217bbd.
21. Metersky M.L., Bean S.B., Meyer J.D. et al. Trombone player’s lung: a probable new cause of hypersensitivity pneumonitis. Chest. 2010; 138 (3): 754—756. DOI: 10.1378/chest.10-0374.
22. Gerfaud-Valentin M., Reboux G., Traclet J. et al. Occupational hypersensitivity peumonitis in a baker: a new cause. Chest. 2014; 145 (4): 856—858. DOI: 10.1378/chest.13-1734.
23. Morell F., Cruz M.J., Gdmez F.P. et al. Chacinero’s lung — hypersensitivity pneumonitis due to dry sausage dust. Scand. J. Work Environ. Health. 2011; 37 (4): 349—356. DOI: 10.5271/sjweh.3151.
24. Vasakova M., Selman M., Morell F. et al. Hypersensitivity pneumonitis: current concepts of pathogenesis and potential targets for treatment. Am. J. Respir. Crit. Care Med. 2019; 200 (3): 301—308. DOI: 10.1164/rccm.201903-0541PP.
25. Vasakova M., Morell F., Walsh S. et al. Hypersensitivity pneumonitis: perspectives in diagnosis and management. Am. J. Respir. Crit. Care Med. 2017; 196 (6): 680—689. DOI: 10.1164/rccm.201611-2201PP.
26. Okamoto T., Miyazaki Y., Tomita M. et al. A familial history of pulmonary fibrosis in patients with chronic hypersensitivity pneumonitis. Respiration. 2013; 85 (5): 384—390. DOI: 10.1159/000338123.
27. Rijavec M., Volarevic S., Osolnik K. et al. Natural killer T-cells in pulmonary disorders. Respir. Med. 2011; 105 (Suppl. 1): S20—25. DOI: 10.1016/S0954-6111(11)70006-3.
28. Jinta T., Miyazaki Y., Kishi M. et al. The pathogenesis of chronic hypersensitivity pneumonitis in common with idiopathic pulmonary fibrosis: expression of apoptotic markers. Am. J. Clin. Pathol.2010; 134 (4): 613—620. DOI: 10.1309/AJCPK8RPQX7TQRQC.
29. Hasan S.A., Eksteen B., Reid D. et al. Role of IL-17A and neutrophils in fibrosis in experimental hypersensitivity pneumonitis. J. Allergy Clin. Immunol. 2013; 131 (6): 1663—1673.
30. Newton C.A., Batra K., Torrealba J. et al. Telomere-related lung fibrosis is diagnostically heterogeneous but uniformly progressive. Eur. Respir. J. 2016; 48 (6): 1710—1720. DOI: 10.1183/13993003.00308-2016.
31. Travis W.D., Costabel U., Hansell D.M. et al. An official American Thoracic Society/European Respiratory Society statement: Update of the international multidisciplinary classification of the idiopathic interstitial pneumonias. Am. J. Respir. Crit. Care Med. 2013; 188 (6): 733—748. DOI: 10.1164/rccm.201308-1483ST.
32. Walsh S.L.F., Wells A.U., Desai S.R. et al. Multicentre evaluation of multidisciplinary team meeting agreement on diagnosis in diffuse parenchymal lung disease: a case cohort study. Lancet Respir. Med. 2016; 4 (7): 557—565. DOI: 10.1016/S2213-2600(16)30033-9.
33. Salisbury M.L., Myers J.L., Belloli E.A. et al. Diagnosis and treatment of fibrotic hypersensitivity pneumonia. Where we stand and where we need to go. Am. J. Respir. Crit. Care Med. 2017; 196 (6): 690—699. DOI: 10.1164/rccm.201608-1675PP.
34. Morisset J., Johannson K.A., Jones K.D. et al. Identification of diagnostic criteria for chronic hypersensitivity pneumonitis: An international modified Delphi survey. Am. J. Respir. Crit. Care Med. 2018; 197 (8): 1036—1044. DOI: 10.1164/rccm.201710-1986OC.
35. Lacasse Y., Selman M., Costabel U. et al. Classification of hypersensitivity pneumonitis: a hypothesis. Int. Arch. Allergy Immunol. 2009; 149 (2): 161-166. DOI: 10.1159/000189200.
36. Churg A., Sin D.D., Everett D. et al. Pathologic patterns and survival in chronic hypersensitivity pneumonitis. Am. J. Surg. Pathol. 2009; 33 (12): 1765-1770. DOI: 10.1097/PAS.0b013e3181bb2538.
37. Mooney J.J., Elicker B.M., Urbania T.H. et al. Radiographic fibrosis score predicts survival in hypersensitivity pneumonitis. Chest. 2013; 144 (2): 586-592. DOI: 10.1378/chest.12-2623.
38. Blanchet M.R., Israёl-Assayag E., Cormier Y. Inhibitory effect of nicotine on experimental hypersensitivity pneumonitis in vivo and in vitro. Am. J. Respir. Crit. Care Med. 2004; 169 (8): 903-909. DOI: 10.1164/rccm.200210-1154OC.
39. Ohtsuka Y., Munakata M., Tanimura K. et al. Smoking promotes insidious and chronic farmer’s lung disease, and deteriorates the clinical outcome. Intern. Med. 1995; 34 (10): 966-971. DOI: 10.2169/internalmedicine.34.966.
40. Lynch D.A., Newell J.D., Logan P.M. et al. Can CT distinguish hypersensitivity pneumonitis from idiopathic pulmonary fibrosis? AJR Am. J. Roentgenol. 1995; 165 (4): 807-811. DOI: 10.2214/ajr.165.4.7676971.
41. Tateishi T., Ohtani Y., Takemura T. et al. Serial high-resolution computed tomography findings of acute and chronic hypersensitivity pneumonitis induced by avian antigen. J. Comput. Assist. Tomogr. 2011; 35 (2): 272-279. DOI: 10.1097/RCT.0b013e318209c5a6.
42. Silva C.I., Churg A., Muller N.L. Hypersensitivity pneumonitis: spectrum of high-resolution CT and pathologic findings. AJR Am. J. Roentgenol. 2007; 188 (2): 334-344. Doi: 10.2214/AJR.05.1826.
43. Dias O.M., Baldi B.G., Pennati F. et al. Computed tomography in hypersensitivity pneumonitis: main findings, differential diagnosis and pitfalls. Expert Rev. Respir. Med. 2018; 12 (1): 5-13. DOI: 10.1080/17476348.2018.1395282.
44. Chong B.J., Kanne J.P., Chung J.H. Headcheese sign. J. Thorac. Imaging. 2014; 29 (1): W13. DOI: 10.1097/RTI.0000000000000067.
45. Walsh S.L., Sverzellati N., Devaraj A. et al. Chronic hypersensitivity pneumonitis: high resolution computed tomography patterns and pulmonary function indices as prognostic determinants. Eur. Radiol. 2012; 22 (8): 1672-1679. DOI: 10.1007/s00330-012-2427-0.
46. Tateishi T., Johkoh T., Sakai F. et al. High-resolution CT features distinguishing usual interstitial pneumonia pattern in chronic hypersensitivity pneumonitis from those with idiopathic pulmonary fibrosis. Jpn. J. Radiol. 2020; 38: 524-532. DOI: 10.1007/s11604-020-00932-6.
47. Adler B.D., Padley S.P., Muller N.L. et al. Chronic hypersensitivity pneumonitis: high-resolution CT and radiographic features in 16 patients. Radiology. 1992; 185 (1): 91-95. DOI: 10.1148/radiology.185.1.1523340.
49. Meyer K.C., Raghu G., Baughman R.P. et al. An official American Thoracic Society clinical practice guideline: the clinical utility of bronchoalveolar lavage cellular analysis in interstitial lung disease. Am. J. Respir. Crit.l Care Med.2012; 185 (9): 1004-1014. DOI: 10.1164/rccm.201202-0320ST.
50. The BAL Cooperative Group Steering Committee. Bronchoalveolar lavage constituents in healthy individuals, idiopathic pulmonary fibrosis, and selected comparison groups. Am. Rev. Respir. Dis. 1990; 141 (5, Pt 2): S169-202. DOI: 10.1164/ajrccm/141.5_Pt_2.S169.
51. Mooney J.J., Koth L.L. Surgical lung biopsy over bronchoalveolar lavage in chronic hypersensitivity pneumonitis. Am. J. Respir. Crit. Care Med. 2014; 189 (3): 371-372. DOI: 10.1164/rccm.201309-1736LE.
52. Morell F., Roger A., Reyes L. et al. Bird fancier’s lung: a series of 86 patients. Medicine (Baltimore) 2008; 87 (2): 110-130. DOI: 10.1097/MD.0b013e31816d1dda.