Химическое равновесие в гомогенной среде
Примером гомогенной среды может быть газовая смесь или различные жидкие растворы. Выражением условий химического равновесия для гомогенных систем является закон действующих масс или константы равновесия, согласно которому:
при постоянной температуре скорость реакции прямо пропорциональна произведению концентраций реагирующих веществ, причём каждое из них влияет на скорость в степени, равной стехиометрическому коэффициенту в уравнении реакции.
Пусть в гомогенной системе протекает реакция
где а, b, с, d – стехиометрические коэффициенты или количество молей веществ А, В, С, D соответственно.
Стрелки в уравнении указывают на возможность протекания реакции в обоих направлениях с определенной скоростью.
Если в начальный период скорость протекания реакции в прямом υ1и обратном υ2 направлении неодинаковы, то по мере приближения к состоянию равновесия они становятся близкими друг к другу. При равновесии υ1= υ2.
Согласно закону действующих масс
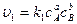
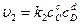
где сА, сB, сC, сD – концентрации веществ, выраженные в молях на литр; k1, k2 – константы скоростей реакции.
При равновесии 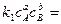
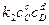
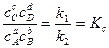
Если в реакции учувствуют газообразные вещества, то константа равновесия реакции может быть выражена через парциальные давления соответствующих веществ:
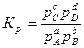
Кс и Кр связаны между собой зависимостью
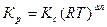
где Δn = (c+d-a-b) – изменение числа молей веществ, участвующих в реакции; R – универсальная газовая постоянная.
Закон действующих масс применим только для идеальных газов и разбавленных растворов, для которых произведение равновесных концентраций является функцией только температуры К=f(T).
Для реальных газов и растворов закон действующих масс применим, если вместо давления и концентрации используются соответственно фугитивности или активности, которые зависят не только от температуры, но и от давления и состава газовой смеси или раствора.
Дата добавления: 2014-12-05 ; просмотров: 1882 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
ХИМИЧЕСКОЕ РАВНОВЕСИЕ В ГОМОГЕННЫХ СИСТЕМАХ
Создание учения о химическом равновесии стало одним из главных достижений физической химии XIX века. Именно исследование химического равновесия положило начало изучению зависимости хода и результата химического процесса от таких факторов, как температура, давление, концентрации реагентов, природа растворителя и прочих внешних условий. В химической промышленности определение положения химического равновесия при различных давлениях и температурах и учет скоростей реакции позволяют выбирать оптимальные условия процесса, в частности, условия, при которых наблюдается максимальный выход химических продуктов. Примеры использования обратимых реакций в технологии: производства аммиака, окисление оксида серы (+2) в производстве серной кислоты и т.д.
Цель работы: рассмотреть кинетические и термодинамические представления о химическом равновесии; изучить факторы, влияющие на смещение равновесия в системе.
В соответствии с целью работы были поставлены следующие задачи:
— рассмотреть понятие «химическое равновесие»;
— изучить кинетические представления о химическом равновесии;
— изучить термодинамические представления о химическом равновесии;
— изучить факторы, влияющие на смещение равновесия в системе;
— экспериментально определить константу равновесия в системе: хлорное железо-иодид калия.
Теоретическая часть
Фазой называется часть системы, отличающаяся по своим физическим и химическим свойствам от других частей системы и отделенная от них поверхностью раздела, при переходе через которую свойства системы резко меняются.
Системы, состоящие из одной фазы, называются гомогенными, из нескольких фаз – гетерогенными. Соответственно реакции, в которых взаимодействующие вещества находятся в одной фазе, называются гомогенными, а реакции, в которых вещества соединяются в различных фазах – гетерогенными.
Химически необратимые реакции при данных условиях идут практически до конца, до полного расхода одного из реагирующих
Химически обратимые реакции протекают одновременно при данных условиях как в прямом, так и в обратном направлении. Необратимых реакций меньше, чем обратимых. Примером обратимой реакции служит взаимодействие водорода с йодом:
Через некоторое время скорость образования HI станет равной скорости его разложения:
Иными словами, наступит химическое равновесие:
Рис. 1. Изменение скорости прямой (1) и обратной (2) реакций с течением времени.
Равновесным считается состояние системы, которое остается неизменным, причем это состояние не обусловлено действием каких-либо внешних сил. Согласно химической кинетике, состояние системы реагирующих веществ, при котором скорость прямой реакции становится равной скорости обратной реакции, называется химическим равновесием. Такое равновесие называется еще подвижным или динамическим равновесием.
Признаки химического равновесия
1. Состояние системы остается неизменным во времени при сохранении внешних условий.
2. Равновесие является динамическим, то есть обусловлено протеканием прямой и обратной реакции с одинаковыми скоростями.
3. Любое внешнее воздействие вызывает изменение в равновесии системы; если внешнее воздействие снимается, то система снова возвращается в исходное состояние.
4. К состоянию равновесия можно подойти с двух сторон – как со стороны исходных веществ, так и со стороны продуктов реакции.
5. В состоянии равновесия энергия Гиббса достигает своего минимального значения.
На основании равенства скоростей прямой и обратной реакций при равновесии можно записать :
Из этого уравнения видно, что при установившемся равновесии произведение концентраций продуктов реакции, деленное на произведение концентраций исходных веществ, в степенях, равных соответствующим стехиометрическим коэффициентам, для данной реакции при данной температуре представляет собой постоянную величину, называемую константой равновесия.
В общем виде константа равновесия выглядит так :
КС— константа равновесия, индекс С показывает, что в выражение
для КС входят равновесные концентрации веществ; a, b, g, r- стехиометрические коэффициенты участвующих в реакции веществ
Поскольку для реакций с участием газов вместо молярных концентраций часто используют парциальные давления реагентов и продуктов, константу равновесия можно выразить и через равновесные парциальные давления
Константы равновесия КС и Кр связаны между собой выражением
Так же эти уравнения раскрывают смысл закона действующих масс, который формулируется так: В состоянии химического равновесия при постоянной температуре отношение произведений молярных концентраций продуктов реакции, взятых в степенях, равных их стехиометрическим коэффициентам, к произведению молярных концентраций оставшихся неизрасходованными исходных веществ, также взятых в степенях, равных их стехиометрическим коэффициентам, является величиной постоянной независимо от начальных концентраций веществ
Термодинамические представления о химическом равновесии
Каждая термодинамическая система характеризуется определенным набором параметров: давлением Р, объемом V, температурой Т, концентрациями веществ С, (i= A, В. G, R). Если температуру и объем системы поддерживают постоянными, то реакция протекает в изохорно-изотермических условиях. Если постоянны Р и Т, химический процесс протекает в изобарно-изотермических условиях.
В результате протекания обратимой реакции при V, Т = const или Р, Т = const в системе устанавливается состояние химического равновесия. Концентрации исходных веществ и продуктов реакции, изменявшиеся в ходе реакции, после достижения этого состояния далее уже не изменяются. Неизменность состава системы во времени при V, Т = const или Р, Т = const является необходимым, но еще не достаточным признаком установившегося химического равновесия. Реакция может протекать с очень малой (практически нерегистрируемой) скоростью.
Скорость реакции в заданных условиях (например, при низкой температуре и в отсутствие катализатора) может даже оказаться равной нулю. В последнем случае говорят, что система находится в метастабильном неустойчивом равновесии.
Кратко рассмотрим основные термодинамические функции для более полного понимания химического равновесия с точки зрения термодинамики.
Энергия Гиббса G – функция состояния термодинамической системы, равная разности между энтальпией и произведением температуры на энтропию:
Для идеального газа :
Энергия Гельмгольца F – функция состояния термодинамической системы, равная разности между внутренней энергией и произведением температуры на энтропию
Для идеального газа :
С точки зрения термодинамики состояние равновесия – это предел
убыли энергии Гиббса. В состоянии истинного химического равновесия: ∆G=0.
Изотерма химической реакции.
Для любого химического превращения связь между энергией Гиббса при стандартных условиях(∆G 0 ) и энергией Гиббса при любых других условиях (∆G) определяется уравнением
Где П-это отношение произведения концентрации продуктов реакции к произведению концентраций исходных веществ в неравновесных условиях, так называемая кажущаяся константа равновесия.
В состоянии равновесия ∆G=0 и кажущаяся константа равновесия становится равной истинной константе равновесия (К). Преобразованное уравнение имеет следующий вид:
∆G 0 =−RTlnK – стандартная изотерма Вант-Гоффа.
Если продифференцировать уравнение стандартной изотермы Вант- Гоффа по температуре при постоянном давлении, получим уравнение изобары Вант-Гоффа:
а если продифференцировать уравнение стандартной изотермы Вант- Гоффа по температуре при постоянном объёме, с учетом связей выражений для функций состояния получим уравнение изохоры Вант-Гоффа:
Эти уравнения применяются для расчетов Крвн при различных температурах при условии, что известны ∆H и ∆U (последнее особенно часто применяется к растворам).
Анализ уравнения изотермы показывает, что для эндотермических реакций (∆H>0) K 0 P с ростом температуры увеличивается, а для экзотермических ( ∆H
Лекция 2. Равновесие в гомогенных и гетерогенных системах
Лекция 2. Равновесие в гомогенных и гетерогенных системах
Равновесие в гомогенных системах (растворах электролитов).
Признаками гомогенной системы являются:
- отсутствие поверхности раздела; физические и химические свойства раствора в любой точке постоянны.
Все электролиты подразделяются на:
Степень диссоциации α – это отношение числа молекул, распавшихся на ионы к общему числу молекул в растворе или отношение концентрации продиссоциировавших молекул (моль/л) к начальной концентрации раствора.
Электролитическая диссоциация сильных электролитов протекает необратимо, т. е. практически полностью.
Для слабых электролитов этот процесс – обратимый.
К D = [ ] –равновесные концентрации, моль/л
· от природы растворителя (различные диэлектрические проницаемости);
Для слабых электролитов α _____ _____
Т. е. степень диссоциации слабого электролита пропорциональна корню квадратному из разбавления раствора. Уравнение пригодно для бинарных электролитов. Например, если раствор разбавить в 4 раза, то степень диссоциации возрастет в 2 раза.
Из уравнения следует:
· чем более разбавлен раствор, тем больше степень электролитической диссоциации;
· вычислить степень гидролиза солей α гидр
· вычислить степень электролитической диссоциации
К D = [Н+] = √ К D [СН3СООН]
Так как СН3СООН – слабый электролит, то равновесную концентрацию кислоты можно считать примерно равной общей концентрации [СН3СООН] = с СН3СООН
и [Н+] = √ К D сСН3СООН. Зная [Н+], легко вычислить и α.
Многоосновные кислоты диссоциируют ступенчато:
Пример: К D HNO 2 = 5,1·10-4. рК HNO 2 = 3,29
Диссоциация оснований также протекает ступенчато.
Кроме разбавления на степень диссоциации влияют:
- добавление одноименного иона, которое смещает равновесие в сторону исходных веществ; добавление разноименных ионов усиливает диссоциацию электролита, а значит и степень диссоциации.
Сильные электролиты закону действия масс не подчиняются: К D их, вычисленные по уравнению : α с2
не являются постоянными величинами при различных концентрациях. Пример: диссоциация хлорида калия при 18 ° С.
Концентрация с, моль/л
Константа диссоциации, К D
Согласно теории сильных электролитов (1923 г Дебай, Хюккель), сильные электролиты в водных растворах нацело диссоциируют на ионы. Между противоположно заряженными ионами действуют электростатические силы притяжения ( у незаряженных частиц – межмолекулярные силы). В результате этого каждый ион окружает «ионная атмосфера», состоящая из ионов противоположного заряда. Это уменьшает подвижность ионов. Межионные силы снижают активность ионов, и последние проявляют себя в реакциях так, как будто их концентрация меньше действительной, определяемой аналитически. Для учета этого влияния введен термин «активность».
Если f f = 1, т. е. а = с, то движения ионов не стеснено. Это имеет место в растворах слабых электролитов и очень сильно разбавленных растворах сильных электролитов (0,0001М).
Таким образом, для диссоциации сильного электролита КА « К+ + А-
закон действующих масс можно выразить следующим образом:
В таком виде закон действующих масс применим и к сильным электролитам.
Коэффициент активности f определяется ионной силой раствора.
Ионная сила раствора обозначается J или µ и вычисляется по формуле:
Т. е., ионная сила равна полусумме произведений молярных концентраций всех присутствующих ионов на квадраты их зарядов.
Пример. Для раствора, содержащего в 1 л 0,01моль ВаС l 2 и 0,1моль NaNO 3 ионная сила равна 0,13.
Ионная сила показывает интенсивность электрического поля ионов в растворе.
1.Вычислить степень диссоциации NH 4 OH в его деци-, санти-, и миллимолярных растворах. Построить график зависимости α от концентрации раствора.
Ответ: 0,0134, 0,0423, 0,1338
2..Что называется разведением раствора? Сделайте необходимые расчеты и постройте кривую зависимости степени диссоциации HNO 2 от разведения. К D HNO 2 = 4,0·10-4
3. Степень диссоциации 0,1 N раствора НС N 0,007%. Рассчитать рН р-ра. Определите характер среды.
Ответ: 5,15, среда слабо кислая.
Ответ: 0,05, 0,0425 моль/л
7.РассчитайтерН 0,05М водного раствора Н N О3.
8. Рассчитайте рН 0,005М водного раствора КОН.
10.Вычислить [Н+] и рН буферного раствора, представляющего смесь 20 мл 0,2М р-ра СН3 COONa и 80 мл 0,1М р-ра СН3 COO Н. К СН3 COO Н = 1,85·10-5 Ответ: 4,78
Равновесие в гетерогенных системах
В соответствии со структурой различают осадки: кристаллические и аморфные.
- имеют кристаллическую решетку, легко обнаруживаются микрокристаллоскопически; быстро осаждаются; легко фильтруются.
- не имеют кристаллической решетки. Поэтому их трудно обнаружить микрокристаллоскопически; студенистые; медленно осаждаются; трудно отделяются.
При получении осадков практически всегда происходит соосаждение с образованием химического соединения примесь-основное вещество, смешанных кристаллов, а также протеканием адсорбционных процессов во время роста кристаллов.
Для очистки осадков используют переосаждение. Для этого необходимо:
- получить осадок; растворить его; повторно осадить.
По аналогии ведут себя смеси Na 2 SO 4 + BaSO 4.
Для характеристики растворимости малорастворимых осадков используют постоянную величину, называемую произведением растворимости.
Пример: ПР Ca 3( PO 4)2 = [ Ca +2]3 [ PO 4-3]2
Произведение активностей при данной температуре для насыщенных водных растворов малорастворимых электролитов есть величина постоянная.
ПР характеризует растворимость вещества: чем > ПР, тем более растворимо вещество.
Связь между молярной концентрацией СМ и ПР выражается следующим уравнением:
СМ = √ ПР А mBn / mm · nn моль/л
Таким образом, растворение малорастворимого осадка происходит в тех случаях, когда связывается один из ионов, посылаемых осадком в раствор. При этом может образоваться: комплексное соединения, менее растворимое или малодиссоциирующее соединение.
Точное выражение ПР через активности может объяснить «солевой эффект», т. е. увеличение растворимости малорастворимого электролита в присутствии других солей, не имеющих с ним общих ионов, например, растворимость AgCl в присутствии KNO 3.
Пример 1: В какой последовательности выпадут осадки при приливании к раствору, содержащему ионы Ba +2, Sr +2, Ca +2, Mg +2 раствора серной кислоты.
ПР CaSO 4 = 6,26· 10-5
ПР MgSO 4 отсутствует, соль хорошо растворима в воде.
Первым выпадет осадок сульфата бария, вторым – сульфата стронция. третьим – сульфата кальция.
Пример 2: Если сравнить осадки Ag 2 C 2 O 4 и BaSO 4, то по ПР получается, что BaSO 4 более растворим, чем Ag 2 C 2 O 4. ПР BaSO 4 = 9,9 ·10-11, ПР Ag 2 C 2 O 4 = 5·10-12.
На самом деле BaSO 4 менее растворим, чем Ag 2 C 2 O 4.
Применение реакций осаждения в химическом анализе:
Растворимость сульфата свинца равна 4,1 10-3 г/100г воды. Найти молярную концентрацию.
ПР сульфида мышьяка ( III ) равно 4,1 10-29. Найти его растворимость.
Ответ: 2,03 10-5 г/100г воды
Растворимость сульфата кальция равна 1,08 10-1 г/100г воды. Найти ПР.
ПР карбоната кальция равно 4,93 10-9. Вычислить [Са2+] и ·[ CO 32-].
Исходя из ПР, определить, у какого вещества больше растворимость: Cr ( OH )3 или Zn ( OH )2. Во сколько раз?
Выпадет ли осадок, если к 3 объемам 0,01 N раствора Ca ( NO 3)2 прибавить 2 объема 0,1 N раствора ( NH 4)2 CO 3? Выпадет ли осадок, если к 100 мл 0,001М раствора PbCl 2 прибавить 1 мл 0,001М раствора серной кислоты? К 100 мл 0,01 N раствора Ва Cl 2 прибавили 5 мл 0,1 N раствора сульфата натрия. Выпал ли осадок? Смешали одинаковые объемы 0,02 N растворы хлорида стронция и хромата калия. Выпал ли осадок?
Лекция на тему «Гомогенные равновесия»
Тема : Гомогенные равновесия.
Цель: Актуализировать знания о гомогенном равновесии и условиях при котором оно смещается.
1. Скорость химической реакции.
2. Гомогенный катализ.
1.Скорость химической реакции определяется скоростью образования активированного комплекса, которая, в свою очередь, зависит от величины энергии активации. Во многих химических реакциях в структуру активированного комплекса могут входить вещества, стехиометрически не являющиеся реагентами; очевидно, что в этом случае изменяется и величина энергии активации процесса. В случае наличия нескольких переходных состояний реакция будет идти в основном по пути с наименьшим активационным барьером.
Катализ – явление изменения скорости химической реакции в присутствии веществ, состояние и количество которых после реакции остаются неизменными.
Различают положительный и отрицательный катализ (соответственно увеличение и уменьшение скорости реакции), хотя часто под термином «катализ» подразумевают только положительный катализ; отрицательный катализ называют ингибированием.
Вещество, входящее в структуру активированного комплекса, но стехиометрически не являющееся реагентом, называется катализатором. Для всех катализаторов характерны такие общие свойства, как специфичность и селективность действия.
Специфичность катализатора заключается в его способности ускорять только одну реакцию или группу однотипных реакций и не влиять на скорость других реакций. Так, например, многие переходные металлы (платина, медь, никель, железо и т.д.) являются катализаторами для процессов гидрирования; оксид алюминия катализирует реакции гидратации и т.д.
Селективность катализатора – способность ускорять одну из возможных при данных условиях параллельных реакций. Благодаря этому можно, применяя различные катализаторы, из одних и тех же исходных веществ получать различные продукты.
Причиной увеличения скорости реакции при положительном катализе является уменьшение энергии активации при протекании реакции через активированный комплекс с участием катализатора.
Если ΔEA = –50 кДж/моль, то отношение констант скоростей составит 2,7·10 6 раз (действительно, на практике такое уменьшение EA увеличивает скорость реакции приблизительно в 10 5 раз).
Необходимо отметить, что наличие катализатора не влияет на величину изменения термодинамического потенциала в результате процесса и, следовательно, никакой катализатор не может сделать возможным самопроизвольное протекание термодинамически невозможного процесса (процесса, ΔG (ΔF) которого больше нуля). Катализатор не изменяет величину константы равновесия для обратимых реакций; влияние катализатора в этом случае заключается только в ускорении достижения равновесного состояния.
В зависимости от фазового состояния реагентов и катализатора различают гомогенный и гетерогенный катализ.
Рис.1 Энергетическая диаграмма химической реакции без катализатора (1)
и в присутствии катализатора (2).
2.Гомогенный катализ – каталитические реакции, в которых реагенты и катализатор находятся в одной фазе. В случае гомогенно-каталитических процессов катализатор образует с реагентами промежуточные реакционноспособные продукты. Рассмотрим некоторую реакцию
В присутствии катализатора осуществляются две быстро протекающие стадии, в результате которых образуются частицы промежуточного соединения АК и затем (через активированный комплекс АВК # ) конечный продукт реакции с регенерацией катализатора:
Примером такого процесса может служить реакция разложения ацетальдегида, энергия активации которой EA = 190 кДж/моль:
В присутствии паров йода этот процесс протекает в две стадии:
Автокатализ – процесс каталитического ускорения химической реакции одним из её продуктов. В качестве примера можно привести катализируемую ионами водорода реакцию гидролиза сложных эфиров. Образующаяся при гидролизе кислота диссоциирует с образованием протонов, которые ускоряют реакцию гидролиза. Особенность автокаталитической реакции состоит в том, что данная реакция протекает с постоянным возрастанием концентрации катализатора. Поэтому в начальный период реакции скорость её возрастает, а на последующих стадиях в результате убыли концентрации реагентов скорость начинает уменьшаться; кинетическая кривая продукта автокаталитической реакции имеет характерный S-образный вид.
1. Какое явление можно назвать катализом?
2. Какие общие свойства характерны для катализаторов?
3. К реакциям какого катализа относится реакция разложения ацетальдегида?
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.














