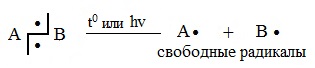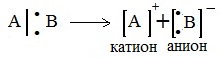Механизмы реакций в органической химии
Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии.
Механизмы разрыва химических связей в органических реакциях
| Гомолитический разрыв связи – это такой разрыв химической связи, когда каждый атом получает при разрыве связи по одному электрону из общей электронной пары. |
Образующиеся при этом частицы — это свободные радикалы.
| Свободные радикалы – это частицы, каждая из которых содержит один неспаренный электрон. A:B → A∙ + ∙B Гомолитический разрыв связи характерен для слабо полярных или неполярных связей. Условия протекания радикальных реакций: То есть реакция протекает как цепь последовательных превращений с участием свободных радикалов. Свободные радикалы R∙ – это атомы или группы связанных между собой атомов, которые содержат один или несколько неспаренных электронов. Свободные радикалы – очень активные частицы, которые стремятся образовать связь с каким-либо другим атомом. Этапы радикально-цепного процесса: Стадия 1. Инициирование цепи. Под действием кванта света или при нагревании молекула галогена распадается на радикалы: Cl:Cl → Cl⋅ + ⋅Cl Стадия 2. Развитие цепи. Радикалы взаимодействуют с молекулами с образованием новых молекул и радикалов. Радикал галогена взаимодействует с молекулой алкана и отрывает от него водород. При этом образуется промежуточная частица – алкильный радикал, который в свою очередь взаимодействует с молекулой хлора: CH4 + ⋅Cl → CH3⋅ + HCl Стадия 3. Обрыв цепи. При протекании цепного процесса рано или поздно радикалы сталкиваются с радикалами. При этом образуются молекулы, т.е. радикальный процесс обрывается. Могут столкнуться разные радикалы, в том числе два метильных радикала:
При гетеролитическом разрыве связи образуются ионы – положительно заряженный катион и отрицательно заряженный анион. A:B → A: – + B +
Гетеролитический (ионный) механизм характерен для полярных и легко поляризуемых связей. Условия протекания ионных реакций: Присоединение галогеноводородов (гидрогалогенирование). Например, этилен взаимодействует с бромоводородом: Реакция протекают по механизму электрофильного присоединения в несколько стадий. II стадия. Карбокатион взаимодействует с анионом Br – : При присоединении галогеноводородов и других полярных молекул к симметричным алкенам образуется одно вещество. При присоединении полярных молекул к несимметричным алкенам образуется смесь изомеров. При этом выполняется правило Марковникова.
В некоторых случаях присоединение к двойным связям происходит против правила Марковникова. Исключения из правила Марковникова: 1) Если в молекуле присутствует заместитель, который оттягивает на себя электронную плотность двойной связи. 2) Если в реакционной системе присутствуют свободные радикалы или источники свободных радикалов, то реакция присоединения полярных молекул вида НХ к двойной связи протекает по радикальному механизму против правила Марковникова. Что такое гомолитический и гетеролитический разрыв ковалентной связи для каких механизмовСпособы разрыва связей в молекулах органических веществ и механизмы органических реакций Разрыв ковалентной связи может происходить двумя способами. 1. Разрыв связи, при котором каждый атом получает по одному электрону из общей пары, называется гомолитическим: В результате гомолитического разрыва образуются сходные по электронному строению частицы, каждая из которых имеет неспаренный электрон. Такие частицы называются свободными радикалами. Радикал – свободный атом или частица с неспаренными электронами, неустойчив и способный быстро вступать в химическую реакцию. Гомолитический разрыв сопровождает процессы, осуществляемые при высоких температурах; на свету; при радиоактивном облучении в отсутствие растворителя (в газовой фазе) или неполярных растворителях. Гомолитическому разрыву подвергаются малополярные или неполярные связи C — C , C — H , Cl — Cl и др. 2. Если при разрыве связи общая электронная пара остается у одного атома, то такой разрыв называется гетеролитическим: Устойчивы более разветвлённые катионы! Ионный тип разрыва связи характерен для П- связей и полярных σ – связей; при наличии полярного растворителя или катализатора. Классификация органических реакций I . Классификация по механизму реакции В зависимости от способа разрыва ковалентной связи в реагирующей молекуле органические реакции подразделяются на радикальные и ионные реакции. 1. Гомолитические (радикальные) реакции Например, галогенирование алканов (реакция цепная) Внимание! В реакциях замещения алканов легче всего замещаются атомы водорода у третичных атомов углерода, затем у вторичных и, в последнюю очередь, у первичных. 1; 4 – первичные; 3 – вторичный; 2 – третичный. 2. Гетеролитические (ионные) Гетеролитический распад ковалентной полярной связи приводит к образованию нуклеофилов (анионов) и электрофилов (катионов): Образовавшиеся ионы вступают в дальнейшие превращения, например: Ионные реакции делятся по характеру реагента, действующего на молекулу, на электрофильные и нуклеофильные. Электрофил E (любящий электроны) – это частица, которая атакует атом углерода органического соединения, отнимая у него электронную пару (является акцептором электронов). Примеры частиц – электрофилов: H 3 O + , H + , HCl , HNO 3 , NO 2 + , AlCl 3 и др Нуклеофил N (любящий ядро) – это частица, которая атакует атом углерода, предоставляя ему электронную пару (является донором электронов). Такие частицы, как правило, обладают основными свойствами. К ним относятся: OH — , Cl — , S 2- , NH 3 , H 2 O , R — OH , CH 3 O — и др Нуклеофильные реакции – это реакции органических веществ с нуклеофилами, т.е. анионами или молекулами, которые предоставляют электронную пару на образование новой связи: С H 3 Br (субстрат) + NaOH (реагент-нуклеофил) → CH 3 OH + NaBr Электрофильные реакции – реакции органических соединений с электрофильными реагентами, т.е. катионами или молекулами, которые имеют свободную орбиталь, готовые принять электронную пару для образования новой связи II . Классификация по направлению и конечному результату химического превращения Это реакции замещения, присоединения, отщепления (элиминирования), перегруппировки, окисления и восстановления 1. Галогенирование (замещение атомов водорода на атомы галогенов) 2. Нитрование (замещение атомов водорода на нитрогруппу – NO 2 ) 3. Алкилирование (замещение атомов водорода на углеводородный радикал – R ) CH≡CH + H2O → CH3-C=O (kat – соли ртути : Hg 2+ ) *- использование правила Марковникова. 5. Реакции полимеризации (получение полимера без образования побочного продукта) 1. Дегидрирование (отщепление водорода): 2*. Дегидратация (отщепление воды) *- использование правила Зайцева 4. Дегидроциклизация (отщеплении Н2 с одновременным замыканием углеродной цепи в цикл) Подробнее о типах реакций по направлению и конечному результату химического превращения см. приложениях Урок 6. Классификация реакций |
 |  |
Классификация реакций по характеру изменения связей
(по механизмам)
Механизм реакции предполагает детальное постадийное описание химических реакций. При этом устанавливают, какие именно ковалентные связи разрываются, в каком порядке и каким путем. Столь же тщательно описывают образование новых связей в процессе реакции.
Рассматривая механизм реакции, прежде всего обращают внимание на способ разрыва ковалентной связи в реагирующей молекуле. Таких способов два – гомолитический и гетеролитический.
Схема гомолитического и гетеролитического
разрывов ковалентной связи
Радикальные реакции протекают путем гомолитического (радикального) разрыва ковалентной связи:
Радикальному разрыву подвергаются неполярные или малополярные ковалентные связи
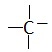
(С–С, N–N, С–Н) при высокой температуре или под действием света. Углерод в радикале СН3• имеет 7 внешних электронов (вместо устойчивой октетной оболочки в СН4). Радикалы неустойчивы, они стремятся захватить недостающий электрон (до пары или до октета). Один из способов образования устойчивых продуктов – димеризация (соединение двух радикалов):
СН3 • + • СН3 
Н • + • Н 
Радикальные реакции – это, например, реакции хлорирования, бромирования и нитрования алканов:
Ионные реакции протекают с гетеролитическим разрывом связи. При этом промежуточно образуются короткоживущие органические ионы – карбкатионы и карбанионы – с зарядом на атоме углерода. В ионных реакциях связывающая электронная пара не разъединяется, а целиком переходит к одному из атомов, превращая его в анион:
К гетеролитическому разрыву склонны сильно полярные (Н–O, С–О) и легко поляризуемые (С–Вr, С–I) связи.
Различают нуклеофильные реакции (нуклеофил – ищущий ядро, место с недостатком электронов) и электрофильные реакции (электрофил – ищущий электроны). Утверждение, что та или иная реакция является нуклеофильной или электрофильной, условно всегда относится к реагенту.
Реагент – участвующее в реакции вещество с более простой структурой.
Субстрат – исходное вещество с более сложной структурой.
Уходящая группа – это замещаемый ион, который был связан с углеродом.
Продукт реакции – новое углеродсодержащее вещество (записывается в правой части уравнения реакции).
К нуклеофильным реагентам (нуклеофилам) относят отрицательно заряженные ионы, соединения с неподеленными парами электронов, соединения с двойными углерод-углеродными связями.
К электрофильным реагентам (электрофилам) относят положительно заряженные ионы, соединения с незаполненными электронными оболочками (АlCl3, ВF3, FeCl3), cоединения с карбонильными группами, галогены. Электрофилы – любые атом, молекула или ион, способные присоединить пару электронов в процессе образования новой связи.
Движущая сила ионных реакций – взаимодействие противоположно заряженных ионов или фрагментов разных молекул с частичным зарядом (

Примеры ионных реакций разных типов.
Нуклеофильное замещение:
Электрофильное замещение:
Элиминирование при действии нуклеофилов (оснований):
Элиминирование при действии электрофилов (кислот):
Упражнения.
1. Для следующих ниже реакций укажите, какие связи разрываются и какие новые связи образуются:
2. Какой состав смеси монобромидов, образовавшихся при бромировании изобутана
(СН3)2СНСН3, если известно, что отношение реакционных способностей С–Н-связей в этой реакции у первичного, вторичного и третичного атомов углерода равно 1:82:1600?
3. Какие радикалы теоретически могут образоваться при гомолитическом разрыве связей в соединениях:
4. Из предложенных ниже реакций определите реакции замещения, реакции присоединения, реакции элиминирования:
5. В приведенных ниже соединениях у элементов, разность электроотрицательностей которых равна 0,5 или более, обозначьте частичные заряды 

6. Сколько 

7. Выберите из приведенных ниже частиц карбкатионы и карбанионы:
8. Какие из приведенных частиц и молекул являются нуклеофилами (обозначьте Nu) и какие электрофилами (Е):
9. Для приведенных ниже реакций укажите: а) субстрат; б) реагент; в) продукт реакции;
г) уходящую группу. Определите реакции: нуклеофильного замещения (NuS), электрофильного присоединения (ЕАd), элиминирования под действием оснований (ЕlNu) и элиминирования под действием кислот (ЕlE).
10. Укажите, какие реакции протекают по радикальному механизму, а какие по ионному:
Ответы на упражнения к теме 1
Урок 6
| № реакции | Разрываются связи | Образуются связи |
|---|---|---|
| 1 | С–Н и Cl–Cl | C–Cl и Н–Сl |
| 2 |  | C–H и C–Cl |
| 3 | C–Cl и K + OH – | C–OH и K + Cl – |
3. При гомолитическом разрыве связей в принципе могут образоваться радикалы:
Что такое гомолитический и гетеролитический разрыв ковалентной связи для каких механизмов
По способу разрыва ковалентных связей органические реакции подразделяются на радикальные и ионные реакции. Ионные реакции в свою очередь делятся по характеру реагента, действующего на молекулу, на электрофильные и нуклеофильные.
1. Свободнорадикальный (гомолитический) разрыв связей
Разрыв связи, при котором каждый атом получает по одному электрону из общей пары, называется гомолитическим:
Такому разрыву подвергаются неполярные и малополярные ковалентные связи под действием света или высокой температуры. Образующиеся частицы содержат неспаренные электроны и называются свободными радикалами. Эти частицы обладают большой энергией и очень активны.
2. Ионный (гетеролитический) разрыв связей
Если при разрыве связи общая электронная пара остается у одного атома, то такой разрыв называется гетеролитическим:
В результате образуются разноименно заряженные ионы – катион и анион. Если заряд иона сосредоточен на атоме углерода, то катион называют карбокатионом, а анион — карбанионом.
Устойчивы более разветвлённые катионы.
Такому разрыву подвергаются полярные ковалентные связи.
Образующиеся органические ионные частицы отличаются от неорганических тем, что они возникают в момент реакции.