Сода — общее название многих химических реактивов
С точки зрения химии содой называют целый класс соединений — натриевых 
— кальцинированную соду (карбонат натрия Na2CO3);
— кристаллогидраты карбоната натрия (Na2CO3•10H2O, Na2CO3•7H2O, Na2CO3•H2O);
— пищевую соду (натрий углекислый кислый NaHCO3, который также называют бикарбонатом или гидрокарбонатом натрия).
Все натриевые соли угольной кислоты представляют собой бесцветные кристаллы, которые, будучи размолотыми в мелкий порошок, становятся белыми; без запаха, хорошо растворяющиеся в воде.
Водный раствор имеет щелочную реакцию. При этом раствор NaHCO3 сохраняет стабильный рН в большом диапазоне концентраций, поэтому на его основе изготавливают стандарт-титр «Натрий углекислый кислый» 0,1 H.
При нагревании свыше 60 °С гидрокарбонат натрия разлагается с выделением углекислого газа. На этом свойстве основано применение пищевой соды в кулинарии в качестве разрыхлителя, а также в порошковых огнетушителях и противопожарных системах (выделяющийся СО2 не поддерживает горение и блокирует доступ кислорода к огню).
Производство
Соду добывают из минералов нахколита, натрита, термонатрита, троны. Также она содержится в золе некоторых растений. Само название химического реактива, «сода», возникло из-за того, что первоначально ее добывали из золы Salsola soda (Солянки содоносной).
Большую часть мирового объема соды производят искусственным путем.
Применение калицинированной соды и кристаллогидратов карбоната натрия:

— изготовление керамики; изделий из высококачественных марок стекла (хрустальных, из электровакуумного, оптического стекла); особых видов стекла (пеностекло, «жидкое стекло»);
— в процессах производства цветных и черных металлов — например, чугуна, алюминия, вольфрама; для обезжиривания металлов;
— для очистки нефтепродуктов;
— в изготовлении целлюлозы;
— в кожевенном производстве (дубление кож);
— для смягчения воды в промышленных установках;
— в мыловарении;
— для нейтрализации кислых сред;
— в газоочистке;
— в быту — для чистки и мытья посуды, обезжиривания, смягчения воды, нейтрализации кислоты.
Применение натрия углекислого кислого:
— в пищевой промышленности и домашней кулинарии как регулятор 
— в системах пожаротушения;
— при производстве красителей, органических продуктов, в т.ч. пенопластов, искусственной резины и кожи, фтористых хим. реактивов; для выделения H2S и СО2 из газовых смесей, товаров бытовой химии;
— в медицине, фармацевтике, быту для лечения изжоги, ожогов, укусов пчел и ос, в качестве антисептика;
— для обработки хлопковых и шелковых тканей; дубления кож;
— в качестве поглотителя запахов, чистящего средства, средства для удаления накипи.
Магазин химических реактивов и лабораторного оборудования Prime Chemicals Group предлагает купить кальцинированную соду и другие химреактивы по хорошим ценам, с самовывозом со склада в Мытищах или с доставкой по Москве и Московской области. Широкий выбор и отличный сервис делают сотрудничество с нами удобным.
Гидрокарбонат натрия
| Гидрокарбонат натрия | |
|---|---|
 | |
 | |
| Систематическое наименование | гидрокарбонат натрия |
| Традиционные названия | пищевая (питьевая) сода, сода двууглекислая, двууглекислый натрий, бикарбонат натрия, кислый углекислый натрий |
| Хим. формула | CHNaO₃ |
| Рац. формула | NaHCO3 |
| Состояние | твёрдое |
| Молярная масса | 84,0066 г/моль |
| Плотность | 2,159 г/см³ |
| Т. разл. | 60—200 °C |
| Растворимость в воде | 9,59 г/100 мл |
| ГОСТ | ГОСТ 2156-76 ГОСТ 4201-79 ГОСТ 32802-2014 |
| Рег. номер CAS | 144-55-8 |
| PubChem | 516892 |
| Рег. номер EINECS | 205-633-8 |
| SMILES | |
| Рег. номер EC | 205-633-8 |
| Кодекс Алиментариус | E500(ii) |
| RTECS | VZ0950000 |
| ChEBI | 32139 |
| ChemSpider | 8609 |
| ЛД50 | 4220 мг/кг |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Гидрокарбонат натрия (лат. Natrii hydrocarbonas ), другие названия: бикарбонат натрия, чайная сада, питьевая или пищевая сода, двууглекислый натрий — неорганическое соединение, натриевая кислая соль угольной кислоты с химической формулой NaHCO3.
В обычном виде — мелкокристаллический порошок белого цвета.
Используется в промышленности, пищевой промышленности, в кулинарии, в медицине как нейтрализатор химических ожогов кожи и слизистых оболочек концентрированными кислотами и для снижения кислотности желудочного сока. Также применяется в буферных растворах.
Содержание
Химические свойства
Гидрокарбонат натрия — кислая натриевая соль угольной кислоты. Проявляет все свойства соли сильного основания и слабой кислоты. В водных растворах имеет слабощелочную реакцию. В широком диапазоне концентраций в водном растворе pH раствора изменяется незначительно, на этом основано применение раствора вещества в качестве буферного раствора.
Реакция с кислотами
Гидрокарбонат натрия реагирует с кислотами с образованием соответствующей кислоте соли, например, хлорида натрия, сульфата натрия и угольной кислоты, которая в процессе реакции распадается на углекислый газ и воду, при этом углекислый газ выделяется из раствора в виде пузырьков:
В быту обычно применяется реакция «гашения соды» уксусной кислотой, с образованием ацетата натрия или гашение лимонной кислотой с образование цитрата натрия, реакция с уксусной кислотой:
Термическое разложение
При температуре выше 60 °C гидрокарбонат натрия начинает распадаться на карбонат натрия, углекислый газ и воду (процесс разложения наиболее эффективен при 200 °C, при более высоких температурах карбонат натрия начинает распадаться на оксид натрия и углекислый газ):
При этом процессе выделения воды в виде водяного пара и углекислого газa масса исходного продукта уменьшается примерно на 37 %.
Получение
В промышленности гидрокарбонат натрия получают аммиачно-хлоридным способом. В концентрированный раствор хлорида натрия, насыщенный аммиаком, под давлением пропускают углекислый газ. В процессе синтеза происходят две реакции:
В холодной воде гидрокарбонат натрия мало растворим, и его отделяют от охлаждённого раствора фильтрованием, а из полученного после фильтрования раствора хлорида аммония снова получают аммиак, возвращаемый в производство вновь:
Применение
Двууглекислый натрий (бикарбонат) применяется в химической, пищевой, лёгкой, медицинской, фармацевтической промышленности, цветной металлургии, в быту. Зарегистрирован в качестве пищевой добавки E500 (ii), входит в состав пищевой добавки E500.
В химической промышленности
Применяется для производства красителей, пенопластов и других органических продуктов, фторорганических соединений, продуктов бытовой химии, наполнителей в огнетушителях, Реагент для отделения диоксида углерода, сероводорода из газовых смесей, например, отходящих газов топливосжигающих установок. В этом процессе углекислый газ поглощается раствором гидрокарбоната натрия при повышенном давлении и пониженной температуре, далее поглощённый углекислый газ выделяется из раствора при подогреве и снижении давления;
В лёгкой промышленности — в производстве резины для подошв обуви и в производстве искусственных кож, кожевенном производстве при дублении и нейтрализации кожи после кислого дубления, текстильной промышленности при отделке шёлковых и хлопчатобумажных тканей;
В пищевой промышленности — в хлебопечении, производстве кондитерских изделий, приготовлении газированных напитков.
В кулинарии
Основное применение пищевой соды в пищевой промышленности и в быту — кулинария, где применяется, преимущественно, в качестве основного или дополнительного разрыхлителя в составе кислого и пресного теста. При добавлении питьевой соды в кислое тесто происходит реакция с молочной кислотой, продуцированной при заквашивании дрожжевыми микроорганизмами, при этой реакции выделяется углекислый газ, вспучивающий тесто.
При добавлении в пресное тесто углекислый газ выделяется при выпечке из-за термического разложения.
При применении соды в чистом виде важно соблюсти правильную дозировку, так как она оставляет в продукте карбонат натрия, дающий определённый привкус. Порядок замешивания для теста: соду — в муку, кислые компоненты (уксус, кефир и пр.) — в жидкость.
В медицине
Традиционно раствор питьевой соды используется для дезинфекции зубов и дёсен при зубных болях и полости рта и горла, при сильном кашле, ангине, фарингите, а также как общепринятое средство от изжоги и болей в желудке.
Применяется при заболеваниях, сопровождающиеся выраженным ацидозом (при диабете, инфекциях и др), для борьбы с ацидозом при хирургических вмешательствах (назначается 3-5 г. внутрь).
Применяется в качестве антиаритмического средства.
Как антацидное средство (как и все другие щелочи) применяется при язвенной болезни желудка, и двенадцатиперстной кишки, при повышенной кислотности желудочного сока.
Имеются так же данные о применении препарата (в виде капельных и внутривенных вливаний) при гипертонической болезни, симптоматической почечной гипертонии, и хронической почечной недостаточности. Эффект связан с увеличением выделения ионов натрия и хлора и возрастанием осмотического диуреза.
В виде свечей применяется против укачивания при морской и воздушной болезнях
Применяется в качестве отхаркивающего средства, т.к. повышая щелочные резервы крови, сдвигает в щелочную сторону реакцию бронхиальной слизи, делая мокроту менее вязкой.
Применяется внутривенно с целью быстрого устранения метаболического ацидоза во время реанимационных мероприятий, заболеваниях почек.
Нужно иметь ввиду, что в результате применения может возникнуть т.н. кислотный рикошет (при реакции содой с соляной кислотой происходит выделение CO2, который оказывает раздражающее действие на стенку желудка, усиливая выделение гастрина).
В альтернативной медицине питьевая сода иногда заявляется как «лекарство» от рака, однако, никакой экспериментально подтверждённой эффективности применения такого «лечения» не существует.
Противопоказания к применению в медицинских целях
Является источником натрия, тем самым увеличивая объём циркулирующей крови, усугубляя отёки и повышая артериальное давление. Применение при сниженной скорости клубочковой фильтрации может привести к метаболическому алкалозу.
Пожаротушение
Гидрокарбонат натрия вместе с карбонатом аммония используется в качестве наполнителя в огнетушителях с сухим наполнением и в стационарных системах сухого пожаротушения. Это применение обусловлено тем, что от воздействия высокой температуры в очаге горения вещество выделяет углекислый газ, атмосфера которого затрудняет доступ кислорода воздуха в очаг горения.
В быту
Применяется как безопасное для здоровья средство для чистки поверхностей столовой и кухонной посуды, поверхностей кухонных столов, иных поверхностей, соприкасающихся с пищей, путем протирки их с помощью влажной тряпки с сухим порошком питьевой соды.
В транспорте
Применяется для нейтрализации следов электролита — серной кислоты на поверхности пластмассовых корпусов свинцовых аккумуляторов насыщенным водным раствором питьевой соды.
Производство
В Российской Федерации двууглекислый натрий выпускается в соответствии с требованиями и техническими условиями, выпускается на предприятиях АО «Башкирская содовая компания» в г. Стерлитамак, Республика Башкортостан, а также на Крымском содовом заводе в г. Красноперекопск, Крымский полуостров.
Хранение
Гидрокарбонат натрия хранят в закрытых упаковках, в сухом месте вдали от источников огня. Гарантийный срок хранения натрия двууглекислого — 12 месяцев со дня изготовления. Срок годности не ограничен.
Безопасность
Вещество нетоксично, пожаро- и взрывобезопасно.
Натрий двууглекислый
Гидрокарбонат натрия NaHCO3 (другие названия: питьевая сода, пищевая сода, бикарбонат натрия, натрий двууглекислый) — кристаллическая соль, однако чаще всего она встречается в виде порошка тонкого помола белого цвета.
Содержание
Безопасность
Двууглекилый натрий не токсичен, пожаро- и взрывобезопасен.
Представляет собой мелкокристаллический порошок, который при попадании на слизистые оболочки вызывает раздражение. При постоянной работе в атмосфере, загрязненной пылью двууглекислого натрия, может возникнуть раздражение дыхательных путей. [1]
Химические свойства
Гидрокарбонат натрия — кислая натриевая соль угольной кислоты.
Молекулярная масса (по международным атомным массам 1971 г.) — 84,00. [1]
Реакция с кислотами
Гидрокарбонат натрия реагирует с кислотами, с образованием соли и угольной кислоты, которая тут же распадается на углекислый газ и воду:
в кулинарии чаще встречается такая реакция с уксусной кислотой, с образованием ацетата натрия:
Термическое разложение
При температуре 60 °C гидрокарбонат натрия распадается на карбонат натрия, углекислый газ и воду (процесс разложения наиболее эффективен при 200 °C):
При дальнейшем нагревании до 1000 °C (например при тушении пожара порошковыми системами) полученный карбонат натрия распадается на углекислый газ и оксид натрия:
Применение
Двууглекислый натрий (бикарбонат), применяется в химической, пищевой, легкой, медицинской, фармацевтической промышленности, цветной металлургии, поставляется в розничную торговлю.
Кулинария
Основное применение питьевой соды — кулинария, где она применяется, преимущественно, в качестве основного или дополнительного разрыхлителя при выпечке (так как при нагревании выделяет углекислый газ), самостоятельно или в составе комплексных разрыхлителей (например, пекарского порошка, в смести с карбонатом аммония), например, в бисквитном и песочном тесте.
Медицина
Раствор питьевой соды используется в качестве слабого антисептика для полосканий, а также как традиционное кислотонейтрализующее средство от изжоги и болей в желудке (современная медицина не рекомендует применять из-за побочных эффектов, в том числе, из-за «кислотного рикошета») или для устранения ацидоза и т. п.
Пожаротушение
Гидрокарбонат натрия входит в состав порошка, применяемого в порошковых системах пожаротушения, утилизируя тепло и оттесняя кислород от очага горения выделяемым углекислым газом.
Производство
В РФ производят соду по ГОСТ 2156-76 «Натрий двууглекислый. Технические условия».[2]
Хранение
Хранить в закрытых упаковках, не допуская попадания влаги.
Гарантийный срок хранения натрия двууглекислого — 12 месяцев со дня изготовления.
Срок годности не ограничен.
См. также
Примечания
Ссылки
Полезное
Смотреть что такое «Натрий двууглекислый» в других словарях:
НАТРИЙ — НАТРИЙ. Natrium, химич. элемент, симв. Na, серебристобелый, блестящий, при обыкновенной t° восковой плотности одноатомный металл, делающийся хрупким на холоду и при ярко краснокалильном жаре перегоняющийся; открыт Де.ви (1807) электролизом… … Большая медицинская энциклопедия
двууглекислый натрий — бикарбонат натрия (NaHCO3) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность Синонимы бикарбонат натрия EN bicarb … Справочник технического переводчика
Натрий* — (хим.; нем. Natrium, франц. и англ. Sodium). Сведения о соединениях этого металла ведут свое начало от очень старых времен. Еврейское слово neter (греч. νίτρον, лат. nitrum) встречается в Библии как название вещества, которое, по Соломону,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Натрий — (хим.; нем. Natrium, франц. и англ. Sodium). Сведения о соединениях этого металла ведут свое начало от очень старых времен. Еврейское слово neter (греч. νίτρον, лат. nitrum) встречается в Библии как название вещества, которое, по Соломону,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Гидрокарбонат натрия — Гидрокарбонат натрия … Википедия
Бикарбонат натрия — Гидрокарбонат натрия NaHCO3 (другие названия: питьевая сода, пищевая сода, бикарбонат натрия, натрий двууглекислый) кристаллическая соль, однако чаще всего она встречается в виде порошка тонкого помола белого цвета. Химическая формула Содержание… … Википедия
Натрия гидрокарбонат — Гидрокарбонат натрия NaHCO3 (другие названия: питьевая сода, пищевая сода, бикарбонат натрия, натрий двууглекислый) кристаллическая соль, однако чаще всего она встречается в виде порошка тонкого помола белого цвета. Химическая формула Содержание… … Википедия
Питьевая сода — Гидрокарбонат натрия NaHCO3 (другие названия: питьевая сода, пищевая сода, бикарбонат натрия, натрий двууглекислый) кристаллическая соль, однако чаще всего она встречается в виде порошка тонкого помола белого цвета. Химическая формула Содержание… … Википедия
Пищевая сода — Гидрокарбонат натрия NaHCO3 (другие названия: питьевая сода, пищевая сода, бикарбонат натрия, натрий двууглекислый) кристаллическая соль, однако чаще всего она встречается в виде порошка тонкого помола белого цвета. Химическая формула Содержание… … Википедия
2156 — ГОСТ 2156 < 76>Натрий двууглекислый. Технические условия. ОКС: 71.060.50 КГС: Л14 Соли Взамен: ГОСТ 2156 68 Действие: С 01.01.77 Изменен: ИУС 1/79, 7/86, 11/89, 8/92 Примечание: переиздание 1992 Текст документа: ГОСТ 2156 «Натрий двууглекислый.… … Справочник ГОСТов
Что такое натрий углекислый кислый
НАТРИЙ УГЛЕКИСЛЫЙ КИСЛЫЙ
Reagents. Sodium bicarbonate. Specifications
ОКП 26 2112 1070 01
Дата введения 1980-01-01
1. РАЗРАБОТАН И ВНЕСЕН Министерством химической промышленности СССР
2. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета СССР по стандартам от 26.01.79 N 246
4. В стандарт введен международный стандарт ИСО 6353-3-87
5. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
Обозначение НТД, на который дана ссылка
Номера пункта, подпункта
6. Ограничение срока действия снято по протоколу N 4-93 Межгосударственного Совета по стандартизации, метрологии и сертификации (ИУС 4-94)
7. ИЗДАНИЕ (октябрь 2001 г.) с Изменением N 1, утвержденным в июне 1989 г. (ИУС 9-89)
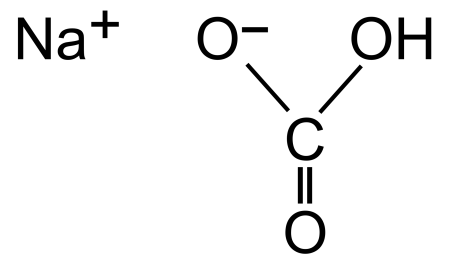
Настоящий стандарт распространяется на кислый углекислый натрий (натрий двууглекислый), который представляет собой белый кристаллический порошок, растворимый в воде, слаборастворимый в этиловом спирте, не токсичен, не взрывоопасен, нe пожароопасен.
Формула 
(Измененная редакция, Изм. N 1).
1. ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ
1.1. Кислый углекислый натрий должен быть изготовлен в соответствии с требованиями настоящего стандарта по технологическому регламенту, утвержденному в установленном порядке.
1.2. По физико-химическим показателям кислый углекислый натрий должен соответствовать нормам, указанным в таблице.
Химически чистый (х.ч.) ОКП 26 2112 1073 09
Чистый для анализа (ч.д.а.) ОКП 26 2112 1072 10
Чистый (ч.) ОКП 26 2112 1071 00
1. Массовая доля кислого углекислого натрия 
2. Массовая доля нерастворимых в воде веществ, %, не более
3. Массовая доля общего азота, %, не более
4. Массовая доля кремнекислоты 
5. Массовая доля сульфатов 
6. Массовая доля фосфатов 
8. (Исключен, Изм. N 1)
(Измененная редакция, Изм. N 1).
2. ПРАВИЛА ПРИЕМКИ
2.2. Определение массовой доли кремнекислоты, фосфатов, суммы кальция и магния в пересчете на магний и тяжелых металлов изготовитель проводит в каждой 20-й партии.
(Введен дополнительно, Изм. N 1).
3. МЕТОДЫ АНАЛИЗА
При взвешивании применяют лабораторные весы 2-го класса точности с наибольшим пределом взвешивания 200 г и ценой деления 0,1 мг и 3-го класса точности с наибольшим пределом взвешивания 500 г или 1 кг и ценой деления 10 мг или 4-го класса точности с наибольшим пределом взвешивания 200 г и ценой деления 1 мг.
Допускается применение импортной лабораторной посуды и аппаратуры по классу точности и реактивов по качеству не ниже отечественных.
(Введен дополнительно, Изм. N 1).
3.1. Пробы отбирают по ГОСТ 3885. Масса средней пробы должна быть не менее 200 г.
(Измененная редакция, Изм. N 1).
3.2. Определение массовой доли кислого углекислого натрия в препарате, высушенном над серной кислотой
3.2.1. Аппаратура, реактивы и растворы
Бюретка 1(2)-2-50-0,1 по нормативно-технической документации.
Колба Кн-2-250-34 ТХС по ГОСТ 25336.
Вода дистиллированная по ГОСТ 6709.
Кислота серная по ГОСТ 4204, концентрированная и раствор концентрации 
Кислота соляная по ГОСТ 3118, раствор концентрации 
Метиловый оранжевый (индикатор), раствор с массовой долей 0,1%; готовят по ГОСТ 4919.1.
3.2.2. Проведение анализа
Около 2,0000 г препарата, предварительно высушенного над концентрированной серной кислотой до постоянной массы, помещают в колбу и растворяют в 50 см воды. Полученный раствор титруют раствором соляной или серной кислоты в присутствии метилового оранжевого до перехода желтой окраски раствора в оранжевую, затем раствор нагревают и кипятят 2-3 мин (для удаления углекислоты).
Если после охлаждения вновь появится желтая окраска, титрование раствора продолжают до перехода желтой окраски в оранжевую, не исчезающую при кипячении.
3.2.3. Обработка результатов
Массовую долю кислого углекислого натрия ( ) в процентах вычисляют по формуле










