Нейробластома
Нейробластома – эмбриональная опухоль, возникающая в процессе внутриутробного или раннего постнатального периода жизни из стволовых нервных клеток – нейробластов.
Впервые описание этой опухоли, названной впоследствии «детской глиомой», дал Рудольф Людвиг Карл Вирхов в 1864 году. Позднее в 1891 году немецким ученым патоморфологом Феликсом Маршандом был определен источник опухоли – клетки симпатической нервной системы и надпочечники. Симпатическая нервная система – это часть автономной (вегетативной) нервной системы. Она контролирует непроизвольную работу внутренних органов человека, например, работу сердца, кишечника, мочевого пузыря, процесс кровообращения.
Эпидемиология
Нейробластома составляет около 7-8% от всех злокачественных новообразований в детском и подростковом возрасте. Это наиболее часто возникающий вид детских новообразований после опухолей кроветворной и центральной нервной системы. Примерно 40% случаев заболевания встречается на первом году жизни, с возрастом количество случаев уменьшается. Средний возраст на момент диагностирования составляет 19 месяцев.
Причины и риски
Причины появления опухоли до конца не изучены. Нейробластома возникает в том случае, когда нормальные нейробласты не созревают в нервные клетки. Вместо этого они продолжают бесконтрольно расти и делиться. Предполагают, что эти несозревшие (эмбриональные) нервные клетки начинают мутировать еще до рождения ребенка, когда начинают меняться хромосомы и/или происходит сбой в регулировании работы генов. Как подтверждают актуальные исследования, у большинства детей болезнь не является наследственной̆. Только около 1% случаев нейробластомы имеют наследственную основу, чаще всего, вследствие мутаций в гене, который̆ называется ALK (или ген киназы анапластической лимфомы), либо в гене PHOX2B. На сегодняшний̆ день нет клинических исследований, доказывающих, что внешние факторы (окружающая среда, вредные условия работы родителей ребенка, прием каких-либо медикаментов, курение и употребление алкоголя во время беременности) могут стать причиной болезни.
Клиническая картина при нейробластоме
Нейробластома может возникать в любой анатомической области, где располагается симпатическая нервная система: надпочечники, шейный, грудной и брюшной симпатический отделы, параганглии.
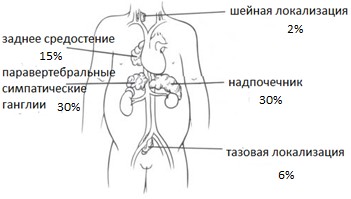
Самой частой локализацией нейробластомы является забрюшинное пространство (одинаково часто опухоль диагностируется в надпочечниках и паравертебральных забрюшинных ганглиях). У 15% детей нейробластома локализуется в заднем средостении. Реже опухоль возникает в области таза (6%) и шеи (2%) (рис. 1).
Рис. 1. Локализация нейробластомы
При ранних стадиях заболевания у многих детей может не быть никаких симптомов. Опухоль у них находят случайно, например, при плановом УЗИ обследовании младенцев при диспансеризации. Как правило, жалобы у детей появляются тогда, когда опухоль уже успела сильно вырасти и давит на соседние органы, нарушая их работу, или когда опухоль дала метастазы.
Среди общих симптомов заболевания можно выделить следующие: потеря веса, слабость, костные и суставные боли, некупируемая диарея.
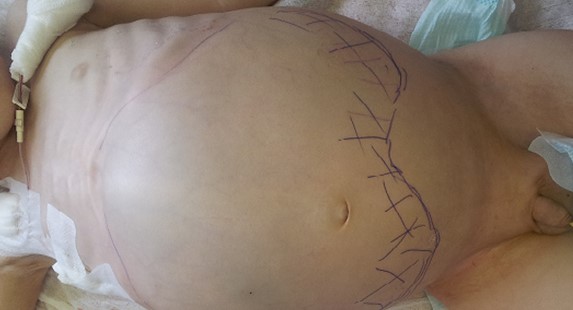
Большинство проявлений болезни и их выраженность зависят от расположения опухоли и ее взаимосвязи с соседними органами и тканями. Так, для пациентов в возрасте до 2-х лет при забрюшинной локализации характерно увеличение размеров живота, лихорадка и потеря веса. Нейробластома забрюшинного пространства пальпируется через переднюю брюшную стенку в виде бугристого, несмещаемого опухолевого узла (рис. 2). У детей старшего возраста заболевание может манифестировать болевым синдромом, обусловленным метастатическим поражением костей, респираторными нарушениями, увеличением размеров живота, появлением запоров. У пациентов с большими забрюшинными опухолями можно обнаружить развитую сеть подкожных вен, развернутые края грудной клетки.
Рис. 2. Нейробластома забрюшинного пространства
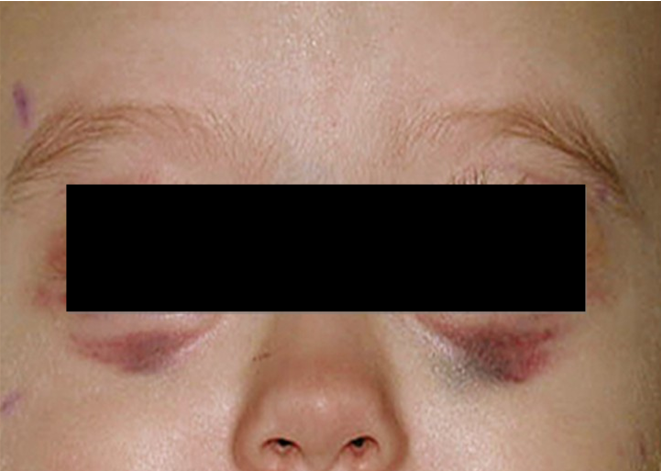
Локализация опухоли в шейно-грудном отделе симпатического отдела позвоночника вызывает синдром Горнера (сужение зрачка, разные размеры зрачков, покраснение и/или опущение верхнего века и небольшое поднятие нижнего). Другими изменениями в области глаз могут быть кровоизлияния в кожу или слизистую оболочку, «синяки» на веках и под глазами. На поздней стадии болезни иногда появляются черные круги вокруг глаз (гематома в виде очков) (рис. 3).
Рис. 3.1. Симптом «очков»
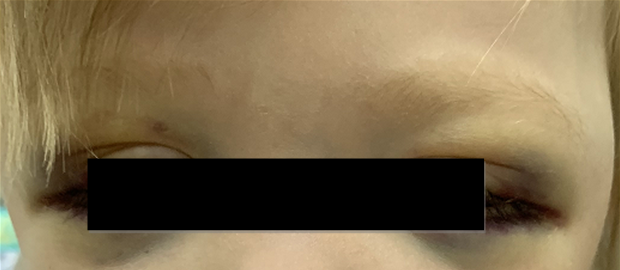
Рис. 3.2. Симптом «очков» при метастазах в орбиту
Поражение заднего средостения может стать причиной сухого кашля, дыхательных расстройств, деформации грудной клетки, частого срыгивания. При локализации опухоли в полости таза отмечают нарушение функции тазовых органов (периодическое недержание мочи, нарушение акта дефекации), отёки нижних конечностей.
При распространении опухоли в позвоночный канал и сдавлении ею спинного мозга могут развиваться слабость в ногах, неустойивость походки, параличи нижних конечностей, а также дисфункции органов малого таза (задержка мочеиспускания или непроизвольное мочеиспускание, запоры).
Редко, примерно в 2-4% всех случаев, у детей встречается ассоциированный с нейробластомой церебеллярный синдром («опсоклонус-миоклонус» или энцефалопатия Кинсбурна), характеризующийся некоординированными, нерегулярными движениями туловища и конечностей, миоклонусом и хаотичными движениями глазных яблок.
Нейробластома ‒ гормонопродуцирующая опухоль, способная к секреции физиологически активных веществ – катехоламинов ‒ адреналина, норадреналина и дофамина. В моче, как правило, повышено выведение их метаболитов ‒ ванилилминдальной и гомованилиновой кислот. В 95% случаев гормональная активность нейробластомы тем больше, чем выше степень её злокачественности. Эффекты секретируемых гормонов вызывают специфические клинические симптомы нейробластомы ‒ резкое повышение артериального давления, диарею (вызывается секрецией вазоактивного интестинального полипептида), потливость, эмоциональную лабильность, периодическое повышение температуры.
Нейробластома метастазирует чаще всего в костный мозг, кости, в отдаленные лимфатические узлы, печень или кожу, редко — в головной мозг или легкие. Признаки отдалённых метастазов можно обнаружить в виде экзофтальма, кровоизлияний в орбиты, опухолевых узлов на голове.
Среди особенностей течения нейробластомы можно выделить следующие:
Гистологическая классификация
Существующая гистологическая классификация нейробластомы INPC-Shimada основана на степени зрелости (дифференцировки) опухолевой ткани и выделяет 4 категории (от недифференцированных до зрелых форм):
1) нейробластома, бедная шванновской стромой: недифференцированная, низкодифференцированная, дифференцированная;
2) нодулярная ганглионейробластома;
Стадии заболевания
Существует несколько систем стадирования нейробластомы. Наиболее точной является модифицированная система, разработанная Международным противораковым союзом (INSS) (табл. 1).
Диагностика нейробластомы
Лабораторные методы
В клиническом анализе крови при поражении костного мозга может наблюдаться снижение показателей крови: анемия, лейконейтропения, тромбоцитопения.
В сыворотке крови также можно определить специфические для нейробластомы маркеры: нейрон-специфическую енолазу (НСЕ), уровень метаболитов катехоламинов, лактатдегидрогеназу (ЛДГ) и ферритин.
Простым в выполнении специализированным тестом при диагностировании нейробластомы является определение уровня ванилилминдальной и гомованилиновой кислот в анализе мочи. Их также называют «тестом на оценку метаболитов катехоламинов в моче». Данный анализ может проводиться при сборе мочи ребенка в течение суток или в однократной порции мочи.
Перед началом специфической терапии всегда проводится верификация диагноза; диагноз нейробластомы ставится при гистологическом исследовании биоптата первичной опухоли или метастазов, или при сочетании наличия опухолевых клеток в костном мозге и повышенного уровня суточной экскреции катехоламинов.
Молекулярно-генетическое исследование
Инструментальные методы
Ультразвуковое исследование
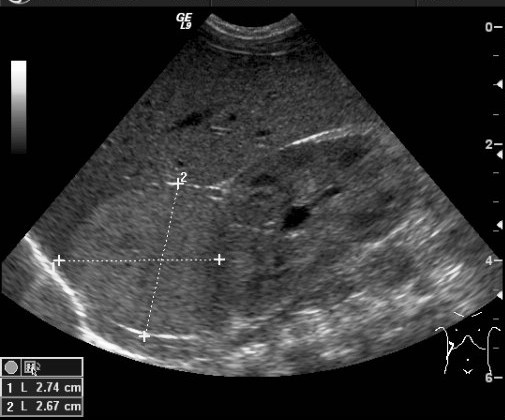
Ультразвуковой метод исследования позволяет выявить наличие опухоли и ее расположение по отношению к внутренним органам. УЗИ позволяет оценить степень местного и отдаленного распространения злокачественного процесса и выявляет метастатическое поражение печени и лимфатических узлов (рис. 4).
Рис. 4. УЗИ образования правого надпочечника
Компьютерная томография брюшной полости и забрюшинного пространства
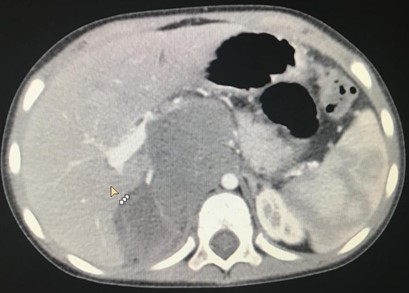
Компьютерная томография более детально дает информацию об анатомическом отношении опухоли к окружающим тканям и органам, позволяет оценить структуру опухоли (рис. 5).
Рис. 5. КТ нейрогенного образования забрюшинного пространства справа
Магнитно-резонансная томография органов брюшной полости, забрюшинного пространства и позвоночника
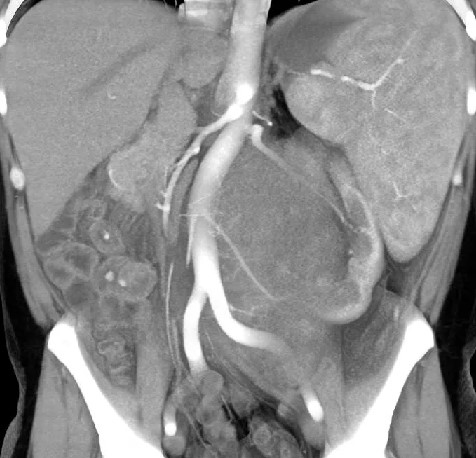
МРТ органов брюшной полости и забрюшинного пространства ‒ это безопасный и высокоинформативный метод исследования, который позволяет не только уточнить локализацию опухоли, точные размеры новообразования и соотношение его с окружающими тканями, но и выявить метастатические очаги в печени и брюшной полости. Также МРТ дает возможность оценить состояние костных структур и мягких тканей позвоночного столба и позвоночного канала (рис. 6).
Рис. 6. МРТ нейрогенного образования забрюшинного пространства слева
Радиоизотопные исследования
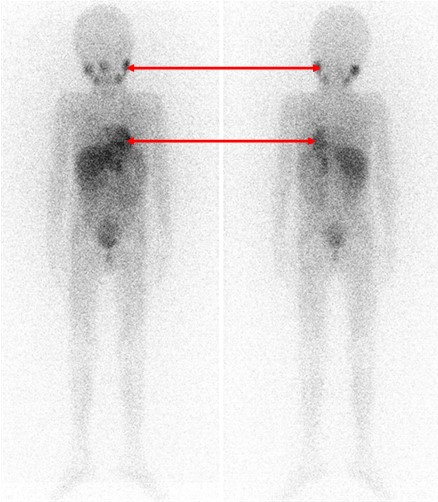
Одним из наиболее информативных специфических методов топической диагностики нейробластом является сцинтиграфия с метайодбензилгуанидином (МЙБГ), меченным 123I. МЙБГ по своей химической структуре сходен с катехоламинами в организме. Это вещество концентрируется в тех опухолях, которые вырабатывают катехоламины. МЙБГ метят радиоактивным изотопом йода (например, 123I) в безопасной для жизни дозе, и готовый препарат внутривенно вводят в кровоток. Накапливаясь в клетках опухоли, он дает излучение. Эти сигналы регистрирует специальная камера и переводит их в изображение. Таким образом, метод позволяет выявить не только первичную опухоль, но и наличие регионарных и отдаленных метастазов (рис. 7).
Рис. 7. Сцинтиграфия с метайодбензилгуанидином (визуализируется первичная паравертебральная опухоль с метастазами в кости черепа)
Остеосцинтиграфия – метод сканирования костей скелета с помощью внутривенного введения радиофармпрепарата. Радиофармпрепарат накапливается участками, пораженными опухолевыми клетками в костях, что видно на снимках, выполняемых гамма-камерой. Таким образом, данный метод исследования позволяет выявить возможные метастазы костей скелета.
Исследование костного мозга (миелограмма и трепанобиопсия) используется для уточнения наличия поражения опухолевыми клетками костного мозга.
Лечение нейробластомы
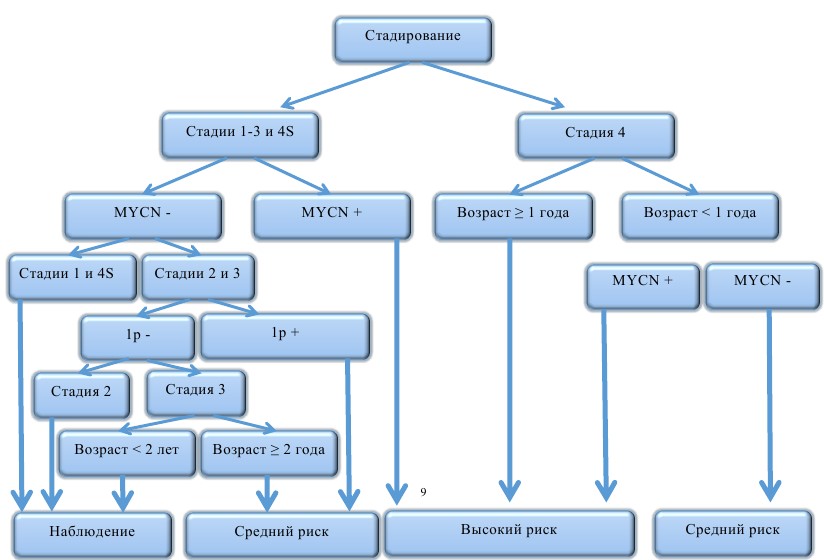
Учитывая разнообразные сценарии развития исхода заболевания (от спонтанной регрессии до летального исхода от прогрессирования), в терапии нейробластомы предлагаются риск-адаптированные принципы. Стратификация пациентов проводится согласно факторам риска до начала лечения (как правило, это клинические и молекулярно-генетические данные) и на основании ответа опухоли во время лечения (response-adapted). При выделении групп риска перед началом лечения используются следующие прогностические критерии: стадия заболевания, возраст на момент диагностики, результаты молекулярно-генетических данных — амплификация MYCN и делеция короткого плеча 1р (рис. 8).
Рис. 8. Стратификация пациентов на группы риска согласно наличию факторов неблагоприятного прогноза
Неоадъювантная (предоперационая) полихимиотерапия
Особенности хирургического лечения
Адъювантная (постоперационная) полихимиотерапия
Лекарственное лечение необходимо начать через 5-7 дней после оперативного вмешательства. При отсутствии показаний для проведения 2-й линии полихимиотерапии в схемах лечения используются те же базовые препараты, как и при неоадъювантной терапии.
Лучевая терапия
В случае наличия неблагоприятных прогностических факторов, в частности выявления в опухоли мутации MYCN онкогена, рекомендовано проведение высокодозной полихимиотерапии с аутологичной трансплантацией гемопоэтических стволовых клеток.
Для больных с высоким риском развития рецидива (распространенные стадии заболевания с наличием неблагоприятных молекулярно-генетических маркеров) рекомендовано проведение «поддерживающей» дифференцирующей терапии 13-цис-ретиноевой кислотой и пассивной иммунотерапией антиGD2 моноклональными антителами.
Иммунотерапия
Иммунотерапия – новый метод лечения нейробластомы, который используется для уничтожения раковых клеток. Дисиалоганглиозид GD2 – молекула- антиген, экспрессируемая клетками нейробластомы, это делает ее идеальной мишенью для иммунотерапии антителами: антитело действует против этой молекулы. Клетки иммунной системы могут способствовать гибели клеток нейробластомы.
В НМИЦ онкологии им. Н.Н. Петрова проводятся все этапы лечения, включая минимально-инвазивные операции (лапаро- и торакоскопические), тандемную трансплантацию и пассивную иммунотерапию.
Интенсифицируя терапию у детей с нейробластомой группы высокого риска (с включением тандемной высокодозной полихимиотерапии в консолидацию и пассивной иммунотерапии в постконсолидацию) удалось повысить результаты выживаемости на 20%.
Рекомендации после лечения
СПИСОК ЛИТЕРАТУРЫ
Авторы:
Под научной редакцией:
Кулева С.А.
Заведующий детским онкологическим отделением, врач-детский онколог, ведущий научный сотрудник, профессор, доктор медицинских наук, главный внештатный детский специалист-онколог Комитета по здравоохранению Санкт-Петербурга
Нейробластома
В 1910 году Wright доказал, что развивается она из эмбриональных нейробластов симпатической нервной системы и дал ей настоящее название. Это наиболее частая экстракраниальная солидная бластома, встречающаяся у детей, и составляет 14% всех новообразований детского возраста.
Несмотря на определенные успехи в лечении детей с этим заболеванием, все еще имеется много проблем, особенно при наличии отдаленных метастазов у детей старше 1 года. Последние, уже при установлении первичного диагноза, встречаются в 70% случаев.
Число неустановленных зон первичного развития опухоли было в 17% случаев. Нейробластома имеет тенденцию к метастазированию в определенные зоны, такие как кости, костный мозг, лимфатические узлы. Редко отсевы опухоли встречаются в коже и печени; как исключение, поражается головной мозг. Нейробластомы раннего детского возраста обладают удивительной способностью, а именно, способностью к спонтанному созреванию в ганглионеврому. Интересно, что Нейробластома нередко случайно, при микроскопическом исследовании обнаруживается у маленьких детей, погибших от неопухолевых заболеваний. Это говорит о том, что ряд этих бластом протекает бессимптомно и спонтанно регрессирует.
Что провоцирует / Причины Нейробластомы:
Многие исследователи полагают, что нейробластома возникает в том случае, когда нормальные эмбриональные нейробласты не созревают в нервные клетки или клетки коры надпочечников. Вместо этого, они продолжают расти и делиться.
Нейробласты могут полностью не созреть к моменту рождения ребенка. В действительности, показано, что небольшие скопления нейробластов часто выявляются у младенцев до 3-месячного возраста. Большинство таких клеток в итоге созревают в нервные клетки и не образуют нейробластому. Иногда нейробласты, остающиеся у младенцев, продолжают расти и образуют опухоль, которая может даже метастазировать в различные органы. Однако многие такие опухоли, в конце концов, созревают или исчезают.
По мере роста ребенка вероятность созревания таких клеток уменьшается, а вероятность формирования нейробластомы увеличивается. При достижении нейробластомой больших размеров и появлении симптомов созревание клеток прекращается, они продолжают расти и распространяться, если не проводится лечение.
У некоторых онкологических больных имеются мутации (изменения) ДНК, которые они унаследовали от одного из родителей, что повышает риск развития опухоли. Некоторые полагают, что некоторые семейные случаи нейробластом возникли в результате наследуемых мутаций гена, угнетающего опухолевый рост.
Большинство нейробластом не являются следствием наследуемых мутаций ДНК. Они вызваны мутациями, приобретенными в ранний период жизни ребенка. Эти мутации присутствуют в опухолевых клетках родителя ребенка и не передаются детям. Причины, вызывающие изменения ДНК, приводящие к возникновению нейробластом, не известны.
Патогномоничными хромосомными нарушениями являются делеция короткого плеча хромосомы 1 с нарушением функции локуса 1 р 31-32. К нарушениям кариотипа относят гиперплоидию или диплоидию опухолевой ДНК. У 30% заболевших в клетках нейробластомы выявляют амплификацию и (или) экспрессию N-myc онкогена, что достоверно коррелирует с неблагоприятным прогнозом (резистентность к полихимиотерапии, склонность процесса к генерализации и т.д.).
Заслуживает внимания исследование клинико-генетических аспектов нейробластом. В литературе описаны случаи возникновения множественных нейробластом различной локализации у двух братьев. Была сделана попытка объяснить семейные случаи нейробластом, медуллобластом и глиом с точки зрения гипотезы о двух мутациях. Предполагается, что в некоторых случаях, одна мутация наследуется, а вторая появляется в соматической клетке; в других случаях обе мутации происходят в одной соматической клетке.
Исследователи, активно работающие в области эпидемиологии опухолей у детей, сообщают, что увеличенный риск заболевания раком коррелирует с врожденными уродствами и врожденной иммунологической недостаточностью.
Патогенез (что происходит?) во время Нейробластомы:
Неоплазмы развиваются из симпатических ганглиев. Различают три типа опухолей, отличающихся друг от друга степенью дифференциации.
Нейробластома является недифференцированной формой неоплазмы состоящей из мелких круглых клеток с темно-пятнистыми ядрами. Часто могут встречаться розетки и характерные нейрофибрилы. В опухоли обнаруживаются геморрагии и участки кальцификации.
Симптомы Нейробластомы:
Первоначальные симптомы нейробластомы не имеют специфичности и могут имитировать различные педиатрические заболевания. Это объясняется, во-первых, возможностью поражения опухолью и метастазами нескольких зон организма ребенка, а также метаболическими нарушениями, обусловленными ростом этих опухолевых очагов.
Клиническая картина зависит от места образования опухоли, локализации метастазов, количества продуцируемых опухолевой тканью вазоактивных веществ.
Растущая инфильтрирующая опухоль, располагающаяся на шее, в грудной клетке, брюшной и тазовых полостях, может, прорастая и сдавливая окружающие ее структуры, давать соответствующий симптомокомплекс.
При локализации в области головы и шеи первыми симптомами могут быть появление пальпируемых опухолевых узлов и развитие синдрома Горнера. Развиваясь в грудной клетке, она может стать причиной нарушения дыхания, дисфагии, сдавления вен.
Первым сигналом наличия опухоли в брюшной полости может быть наличие в ней пальпируемых опухолевых масс, в то время как новообразования таза могут проявляться нарушением акта дефекации и мочеиспускания.
Нейробластомы, прорастающие через межвертебральные отверстия со сдавлением спинного мозга (опухоли в виде «гантели»), вызывают характерные неврологические симптомы, к которым можно отнести такие, как вялый паралич конечностей и/или нарушение мочеиспускания с напряженным мочевым пузырем.
К основным клиническим проявлениям нейробластомы относятся:
• опухоль в брюшной полости
• отёк
• похудание,
• боли в костях, обусловленные метастазами
• анемия
• лихорадка.
Основные жалобы предъявляются на боль (30-35 % случаев), лихорадку (25-30 % случаев), потеря веса (20 % случаев). При росте опухоли в заднем средостении дети жалуются на постоянный кашель, дыхательные расстройства, дисфагию и постоянные срыгивания; наблюдается деформация грудной стенки. При поражении костного мозга вызывает анемию и геморрагический синдром. При росте опухоли в ретробульбарном пространстве возникает характерный «синдром очков» с экзофтальмом. Если нейробластома возникает в забрюшинном пространстве, то она быстро врастает в спинномозговой канал, пальпируясь как бугристая, несмещаемая опухоль каменной констистенции. При распространении опухоли из грудной полости в забрюшинное пространство через диафрагменные отверстия она принимает вид песочных часов или гантели. Метастазы нейробластомы в кожу имеют вид синюшно-багровых узлов с плотной консистенцией.
Клинические симптомы, обусловленные метастазами также весьма многообразны. У новорожденных первым признаком развития метастазов является быстрое увеличение печени, иногда сопровождающееся образованием на коже узлов голубоватого цвета и поражением костного мозга.
У детей более старшего возраста развитие метастазов может вызвать боли в костях и увеличение лимфатических узлов. Иногда заболевание имеет признаки, характерные для лейкемии, т. е. у детей развиваются анемия и кровоизлияния на слизистых оболочках и коже, что обуславливается панцитопенией, вызванной поражением костного мозга клетками нейробластомы.
Метаболические изменения, развивающиеся в результате роста опухоли, ведут к появлению ряда общих симптомов. Так, в результате повышения уровня катехоламинов и, иногда, вазоактивных интестинальных пептидов (VIP) у детей могут появляться приступы потливости и бледности кожных покровов, сопровождающиеся жидким стулом и гипертензией. Эти симптомы могут проявляться независимо от локализации бластомы, и их интенсивность снижается при успешном лечении больного.
Стадия нейробластомы
В литературе встречается довольно большое число систем стадирования нейробластомы. Из них до 1988 года наиболее популярными были классификация, предложенная в США группой по изучению рака у детей (CCSG, Evans et al., 1971); система TNM, разработанная Международным противораковым союзом (INSS, 1987).
В 1988 году была предложена модифицированная система стадирования нейробластомы, в которую были включены элементы обеих указанных классификаций (INSS, Brodeur et al., 1988).
Диагностика Нейробластомы:
Важным тестом в диагностике и дифференциальной диагностике нейробластом является определение суточной экскреции с мочой катехоламинов, их предшественников и метаболитов (ванилминдальной и гомованилиновой кислот). У детей с нейробластомой, в отличие от других опухолей, наблюдается резкое повышение экскреции указанных веществ почти в 85% случаев. Кроме того, в крови или моче больного определяются и другие опухолевые маркеры: нейроно-специфическая энолаза, ферритин и ганглиосайды.
Их определение является не только ценным диагностическим тестом, но и может помочь в объективизации данных и динамике опухолевого процесса после лечения.
Хорошее понимание синтеза и метаболизма катехоламинов имеет большое значение для клинических целей, как при установлении диагноза, так и в ходе лечения больного и последующего наблюдения за ним. В последние 20 лет определение уровня в моче ванилилминдальной и гомованилиновой кислот стало рутинным методом для указанных целей. Однако некоторые вопросы, касающиеся значимости этого теста еще продолжают обсуждаться.
Так, например, некоторые исследователи предлагают использование определения катехоламинов с целью «массового» скрининга.
В Японии обследовали более полумиллиона младенцев. В результате было выявлено 25 детей с бессимптомно текущей нейробластомой. 92% из них наблюдается длительные сроки без рецидива заболевания.
В США и Европе также наметилась тенденция к проведению аналогичной программы. Однако имеются и определенные недостатки этого метода, связанные с тем, что благодаря скринингу, определяются также дети с новообразованиями, которые могли бы спонтанно регрессировать.
Спорным остается вопрос о прогностическом значении уровней ванилилминдальной и гомованилиновой кислот у детей с нейробластомой. В ранних сообщениях указывалось, что высокий их Уровень обязательно ассоциируется с плохим прогнозом, в то время как в более поздних работах не было найдено значимой связи с прогнозом.
Поэтому, определение NSE при диагностике должно оцениваться с большой долей осторожности. Однако этот тест имеет определенное прогностическое значение. В частности, низкие уровни содержания NSE увязываются с хорошим прогнозом, а у детей с диссеминированной формой заболевания, т. е. прогностически неблагоприятной, отмечают высокие уровни содержания сывороточной NSE.
Необходимо подчеркнуть, что нейроно-специфическая энолаза является недостаточно специфичным маркером нейробластомы.
Ферритин. У детей с нейробластомой наблюдается повышение уровня ферритина, который снижается в процессе лечения и нормализуется в период ремиссии. Полагают, что повышение содержания ферритина в сыворотке крови происходит по следующим причинам: из-за повышения количества неиспользуемого железа, обусловленного анемией; из-за увеличения синтеза ферритина нейробластоматозными клетками с последующей секрецией в плазму.
Отмечается, что количество этого маркера почти не увеличивается у детей с нейробластомой I и II стадий, но оно заметно изменяется у больных с III и IV стадиями заболевания. Evans et al. (1987) выделили три группы больных, имевших различный прогноз течения заболевания:
— хороший, при нормальном содержании ферритина в сыворотке и возрасте менее 2-х лет; в этой группе прожило 93% детей;
— умеренный, при нормальном уровне ферритина и возрасте 2 года и старше; 2 года без признаков заболевания наблюдалось
58% больных;
— плохой, при повышенном содержании ферритина; двухлетняя продолжительность жизни у этих детей была 19%.
Кроме клинического и лабораторного обследования ребенка, обязательно выполнение костно-мозговой пункции или трепанобиопсии грудины и крыла подвздошной кости. Полученные аспираты или биоптаты изучаются цитологически, иммунологически или с помощью проточной цитометрии. Отмечено, что при этом они должны быть получены не менее, чем из 4-х зон. Лучевые методы исследования являются одними из решающих в клинической диагностике.
Ультразвуковое исследование должно всегда выполняться первым, при подозрении или наличии опухоли в брюшной или тазовой полостях. Повторная эхография, компьютерная томография проводятся перед решением вопроса о первичном или отсроченном оперативном вмешательстве. Данные, полученные при этом, помогают уточнить локализацию, распространенность опухоли и ее связь с интра- и экстраперитонеальными структурами тазовой и брюшной полостей, а также выявить наличие в ней мелких кальцинатов, которые не определяются обычной рентгенографией. Возможно также выполнение абдоминальной аортографии, нижней венокаваграфии, которые могут помочь в уточненной диагностике распространенности забрюшинных нейробластом.
Заключительным этапом клинической диагностики заболевания является аспирационная биопсия с цитологическим, иммунологическим исследованием пунктата. Кроме того, аспираты могут быть изучены с помощью проточной цитометрии.
При диагностике отдаленных метастазов нейробластомы необходимо, кроме костного мозга, тщательное обследование костей скелета, которые часто ими поражаются, особенно у детей в возрасте 2 года и старше. При стандартной рентгенографии, выполненной во время первичной диагностики, костные метастазы выявляются в 50-60% случаев. Проведение радиоизотопного исследования с использованием радиоактивного технеция (99 mTc ) повышает этот показатель до 80%. В последние годы для диагностики нейробластом предложено проведение радиоизотопного исследования с применением метайодобензилгванидина (131-J-mJBG), аналога гванетедина, меченного йодом-131. Скенирование, проведенное после введения этого препарата, позволяет выявить первичную остаточную и рецидивную опухоль, наличие метастатического поражения костного мозга, костей, лимфатических узлов и мягких тканей. В обзорном сообщении, содержащем данные о 550 больных нейробластомой было показано, что более чем 90% этих опухолей способны накапливать 131-J-MJBG.
При динамическом наблюдении за детьми после лечения необходимо уделять пристальное внимание поиску метастатического поражения костного мозга и костей, используя сцинтиграфию с метайодобензилгванидином, аспирационную и трепанобиопсию. Для этих целей используется также ЯМР-томография.
Следует отметить, что за последние 10 лет, в связи с развитием ультразвуковой, компьютерной и ЯМР-томографии и радиоизотопной сцинтиграфии, значительно повысилась точность диагностики заболевания, определения его стадии и возможности эффективного наблюдения за детьми после лечения.
Лечение Нейробластомы:
Несмотря на то, что нейробластома интенсивно изучается клиницистами и экспериментаторами уже более 100 лет, лечение этого заболевания остается важной проблемой детской онкологии. Выбор стратегии лечения, по крайней мере, зависит от двух факторов:
— прогностических признаков, выявленных у детей во время установления диагноза заболевания;
— реакции опухоли на лечение.
Химиотерапия
Ninane (1990) приводит следующие схемы противоопухолевого лекарственного лечения детей с нейробластомой.
До 1980 года ряд химиотерапевтических режимов состоял из винкристина и циклофосфамида с или без адриамицина. Результаты лечения с использованием этих схем оказались разочаровывающими для детей старше 1 года с местнораспространенной опухолью, так как 2 года переживало только 10% детей. Добавление цисплатины, вепезида и тенипозида привело к повышению начального противоопухолевого эффекта, но мало сказалось на отдаленных результатах.
В последние годы для повышения результатов химиотерапии были предложены высокодозные схемы лечения с пересадкой костного мозга).
Отметим следующее:
1. Использование высоких доз мелфалана в виде единственного Препарата позволяло получить результаты, по своему эффекту мало отличающиеся от результатов, которые наблюдались после интенсивной полихимиотерапии или комбинации ее с тотальным облучением.
2. Смертность из-за токсичности проводимого лечения была наименьшей в группе больных, которым проводилось только введение высоких доз мелфалана.
Необходимо отметить, что указанное лечение проводилось в виде консолидирующей терапии у детей с распространенными формами заболевания. Было показано, что больные с полной или значительной регрессией опухоли после начальной химиотерапии имели лучшие показатели 2 летней продолжительности жизни по сравнению с теми, у которых опухоль мало реагировала на начальное лечение.
Интересные данные о многолетнем наблюдении за больными с нейробластомой, подвергшимися интенсивной химиотерапии были представлены Philip et al. (1990) и Dini et al. (1990).
Оперативное лечение
Оперативное лечение широко используется для радикального удаления ограниченной первичной опухоли. Кроме того, в последние годы оперативному вмешательству подвергаются больные с местнораспространенными или метастатическими нейробластомами. После начальной химиотерапии нередко возникает возможность радикального удаления первичной опухоли и метастазов вследствие их значительной регрессии. В ряде случаев прибегают и к повторным оперативным вмешательствам, если первичная операция оказалась нерадикальной, но затем опухоль уменьшилась после проведения дополнительной химиотерапии.
Лучевая терапия
В настоящее время, в связи с прогрессивным развитием противоопухолевой лекарственной терапии, роль традиционного лучевого лечения больных нейробластомой уменьшилась. Это связано еще и с тем, что эта опухоль в основном поражает маленьких детей, облучение которых несет опасность отдаленных лучевых повреждений.
Все же в некоторых клинических ситуациях имеются показания к ее применению. Во-первых, лучевое лечение может быть проведено при нерадикальном оперативном удалении первичной опухоли и ма¬лой эффективности химиотерапии, во-вторых, при наличии местнораспространенной неоперабельной первичной или метастатической опухоли, не реагирующей на современные курсы химиотерапии.
Величина дозы излучения, прежде всего, зависит от возраста ребенка и величины остаточной опухоли. По мнению Tereb, Tent, при облучении ребенка до года адекватной дозой могут быть 10 Гр, подведенных в течение двух недель (по 1 Гр за фракцию). Jacobson (1984), поддерживая эту точку зрения, рекомендует дозу в 12 Гр за две недели.
Нередко после подведения указанных доз опухоль либо полностью регрессирует, либо значительно уменьшается в размерах. В последнем случае становится возможным оперативное удаление остатков нейробластомы. Симптоматический эффект может быть достигнут после однократного облучения в дозе 5 Гр, но в случаях относительно удовлетворительного состояния ребенка лучше использовать курс облучения с разовой дозой 3 Гр, подводимых за 5 фракций.
При лучевом лечении необходимо захватывать всю опухоль или ее ложе с 2 см прилежащих тканей.
Полагаем, что вопрос о применении лучевой терапии больных нейробластомой должен решаться в каждом случае индивидуально. При этом необходимо учитывать возможный непосредственный эффект на растущую опухоль. Например, даже при больших нерезектабельных опухолях бывает достаточно подвести дозу излучения в 10-15 Гр за 2-3 недели (1 Гр ежедневно), чтобы добиться эффекта за счет спонтанного их созревания.
При опухолях заднего средостения с использованием фотонов или электронов в зону облучения необходимо включать всю опухолевую массу и грудные позвонки на всю их ширину, для предупреждения деформации позвоночника. По достижении верхнего предела лучевой толерантности спинного мозга, необходима его защита. При этом необходимо помнить, что толерантность его меняется с возрастом. Также необходима тщательная защита плечевых суставов. При нейробластомах в настоящее время облучения всей брюшной полости используется редко, так как у больных с III стадией заболевания обычно применяют агрессивную полихимиотерапию.
При облучении тазовой области пристальное внимание уделяется защите тазобедренных суставов. У девочек необходимо, по возможности, выводить из зоны действия прямого пучка ионизирующего излучения яичники путем оперативного их перемещения. Последнее предохраняет ребенка от стерилизации и сохраняет его гормональную функцию.
Некоторые схемы лечения детей с нейробластомой в зависимости от стадии заболевания
Стадия I. Выполнение радикального оперативного удаления опухоли бывает достаточным для излечения больного. Тем не менее, эти дети нуждаются в динамическом наблюдении, так как возможны рецидивы заболевания или отдаленные метастазы.
Стадия IIА. При этой стадии нейробластомы излечения больного, так же как и при I стадии, можно достичь с помощью оперативного удаления опухоли.
Два исследования показали, что без признаков рецидива прошло 100% детей как получавших послеоперационное лечение, так и не получавших его (Ninane et al., 1982; Hayes et al., 1983). Исключение составила «гантелеподобная» форма паравертебральной нейробластомы, при которой необходимо проведение адекватного химиолучевого лечения.
Стадия IIВ. При этой стадии заболевания лечение должно начинаться с химиотерапии с последующим оперативным вмешательством. Трудно однозначно сказать, есть ли необходимость ее применения у детей до 6 месяцев, так как течение заболевания в этом возрасте достоверно благоприятно.
Стадия III (опухоль нерезектабельна) и стадия IV. Лечение детей с этими стадиями заболевания весьма трудная задача и решается, в основном, исходя из опыта конкретного специализированного отделения детской онкологии. Однако можно указать на два основных принципа к подходу терапии:
1. Необходима агрессивная тактика хирургического лечения при III стадии заболевания.
2. Дети с IV стадией в возрасте старше 1 года нуждаются в интенсивной высокодозной химиотерапии с пересадкой костного мозга.
Стадия IVa. В основном, при этой стадии заболевания проводится химиотерапия (несколько курсов циклофосфамида и винкристина), до и после оперативного вмешательства, выполняемого для удаления первичной опухоли.
Пример блоков полихимиотерапии, используемых в современных протоколах
CAV-Pt (протокол N 3891, CCG, США)
Цисплатин по 60 мг/м2 в 1-й день,
VP-16 по 100 мг/м2 в 3-й, 6-й день.
Циклофосфан по 900 мг/м2 в 4-й, 5-й день
Доксорубицин по 30 мг/м2 в 3-й день.
Интервал 3 нед
Прогностичекие факторы
Эти факторы получены в результате выявления достоверной связи между продолжительностью жизни больных после лечения с возрастом, стадией и биологическими параметрами опухоли. Используя многофакторный анализ, Evans et al. (1987) определили, что комбинация таких признаков, как возраст, стадия, уровень сывороточного ферритина и морфологического строения нейробластом, позволяет выделить три группы детей с различным прогнозом:
— благоприятную, в которой более 80% больных живут более 2-х лет;
— промежуточную;
— неблагоприятную, в которой только около 20% детей наблюдаются 2 года.
Возраст при установлении заболевания является единственным важным прогностическим фактором. Так, у детей до 1 года течение заболевания всегда благоприятно. Далее, значимыми признаками, влияющими на прогноз, являются стадия и первичная локализация нейробластомы.
При этом хотелось бы отметить, что 80% детей поступают в специализированную клинику на III-IV стадиях заболевания.
Профилактика Нейробластомы:
В настоящее время не существует рекомендаций по предотвращению развития нейробластомы, так как нет факторов риска, которые можно было бы избежать.
При наличии семейных случаев нейробластомы необходима консультация генетика для уточнения риска возникновения данной опухоли у ребенка.