Нейровирусная инфекция: как уберечь своё здоровье?
Мы знаем, что наша центральная нервная система выполняет одну из ключевых функций в работе всего организма. Нервные волокна полностью обволакивают человеческое тело с головы до ног, где беспрерывно работают нервные импульсы, которые отвечают за чувствительные факторы, двигательные и смешанные – работа импульсов из рецептора в центральную нервную систему и наоборот. Функционал центральной нервной системы может быть нарушен при возникновении в организме нейровирусной инфекции.
Инфекцию можно считать нейровирусной в случае соответствия следующим критериям. Если возникает нейроинвазивность – процесс проникновения конкретного вируса в нервную систему организма; если проявляется нейротропизм – когда происходит инфицирование вирусом клеток головного мозга, а конкретно его нейронов; и, наконец, если врач обнаруживает у пациента нейровирулентность – заболевание нервной системы, возникающее при вторжении в организм массовой группы вирусов.
Для того, чтобы своевременно предотвратить возможность развития нейровирусной инфекции, необходимо обратиться к ЛОР-специалисту, сделать полное обследование на отсутствие стоматологических патологий, полностью исключить контакт с уже инфицированными людьми, носить головной убор при низкой температуре воздуха и укреплять иммунитет, употреблять фрукты, овощи и полезные витамины. Казалось бы, ничего сложного в этом нет, и данные рекомендации легко соблюдать. Однако, некоторые люди пренебрегают своим здоровьем, за что потом им же и расплачиваются, когда появляются симптомы болезни, и вирус в организме дает о себе знать. Уже при возникновении стадии высокого развития нейроинфекции пациенты начинают обращаться к специалисту за эффективным и быстрым лечением. Только в данном случае на выздоровление заболеваний потребуется масса времени и усилий.
Электроэнцефалография (ЭЭГ) — диагностика головного мозга
В медицинских справочниках нейровирусное заболевание трактуется как инфекционное, вызванное грибками, вирусами или бактериями, которое поражает нервную систему, при этом имеет тяжелое течение с высоким процентом смертности. Нейроинфекция включает в себя достаточно большой список заболеваний, многие из которых губительны для головного мозга. Все они могут иметь острую форму течения или переходить в хроническую и протекать достаточно вяло. Как показывает медицинская практика, эти заболевания могут пройти в острой форме один раз и больше не беспокоить больного или иметь частые и яркие рецидивы до конца его дней. У взрослого человека после перенесенных заболеваний остается головная боль, постоянные болевые ощущения в спине, которые усиливаются при изменении погоды. Многие специалисты констатируют тот факт, что у таких больных после выздоровления ухудшается память, отмечаются проблемы с запоминанием, может нарушаться слух, зрение. Встречаются и такие единичные случаи, когда нейроинфекционное заболевание приводит к полной потере зрения и слуха. К счастью, это происходит крайне редко.
Методики проведения терапии во многом зависят от того, какая именно инфекция спровоцировала возникновение патологии, от места локализации, а также вида самой инфекции. К основным задачам проведения медикаментозной терапии относятся: нормализация деятельности нервной системы; восстановление иммунной системы организма; устранение путей распространения инфекции и его возбудителя.
Если же пациенту удалось вылечить сложную стадию нейровирусной инфекции, то всё равно степень осложнения на здоровье организма остается. Последствия перенесенной нейроинфекции зависят от вида заболевания и времени начала лечения. У пациентов может остаться головная или спинная боль, усиливающиеся при изменениях погоды. Стоит отметить, что на фоне нейровирусной инфекций могут активироваться и сопутствующие заболевания. Например, при миелите практически всегда наступает паралич. Самыми серьезными считаются последствия нейроинфекции головного мозга, перенесенной во внутриутробном периоде. Они влекут за собой аномалии развития ребенка, различные пороки внутренних органов и систем.
Запомните, что нейроинфекционные процессы, поражающие нервную систему, несут серьёзную угрозу для жизни человека, поэтому крайне важно своевременно обращаться к доктору при наличии симптомов болезни, а также проводить профилактику своего здоровья.
Инфекции нервной системы
Инфекции нервной системы являются одними из самых сложных инфекций с точки зрения заболеваемости и смертности среди пациентов и, следовательно, требуют срочной и точной диагностики. несмотря н ато, что вирусные менингиты встречаются чаще, именно бактериальные менингиты могут вызвать быстро ухудшающееся состояние больного, с которым должен быть знаком врач. Вирусный энцефалит часто сопровождает вирусный менингит и может вызвать очаговые поражения мозга и когнитивные нарушения, которые могут имитировать другие психоневрологические расстройства. Абсцессы мозга также могут имитировать другие неврологические расстройства, и вызывать более отчетливые очаговые нарушения. Наконец, стоит обратить внимание и на другие инфекционные заболевания центральной нервной системы, такие как прионовая болезнь.
Менингиты
Энцефалиты
Вирус бешенства является частью семейства вирусов Rhabdoviridae, которое включает линейный одноцепочечный РНК-вирус с отрицательным знаком, обнаруживаемый в оболочке в форме пули. Это зоонозная инфекция, распространяющаяся от животных к человеку главным образом в результате укуса, причем основными виновниками во всем мире являются собаки. С другой стороны, известно, что грызуны и зайцы не переносят этот вирус и не передают его людям. Инкубация вируса обычно происходит в течение 1-3 месяцев, а заражение ЦНС происходит в результате ретроградного распространения вируса от периферических нервов к центральным нервам и, наконец, в паренхиму головного мозга. Окончательный диагноз у людей может быть поставлен с помощью ПЦР с обратной транскриптазой, обнаруживающей вирус бешенства в тканях ЦНС. Лечение состоит из тщательной очистки ран, срочного введения иммуноглобулина человека как в месте заражения, так и в внутримышечно, после чего в течение первого месяца должны быть сделаны пять постконтактных прививок. Вакцинация проводится путем введения человеческой вакцины против бешенства на диплоидных клетках по 1,0 мл внутримышечно.
Абсцесс мозга
Абсцессы головного мозга часто могут сопровождаться новой головной болью, которая может развиваться в течение нескольких часов или нескольких недель, и сопровождается очаговым неврологическим дефицитом. Летаргия, затылочная ригидность, тошнота, рвота и новые приступы головной боли часто сопровождают развитие абсцессов. Двумя основными причинами абсцессов головного мозга являются гематогенное распространение патогенов через гематоэнцефалический барьер и через прямое смежное распространение из пазухи после синусной инфекции, причем на долю последних приходится более 70% всех абсцессов головного мозга. Дифференциальный диагноз абсцессов головного мозга всегда включает новообразования, хотя абсцессы, как правило, более остры в своем начале и часто сопровождаются другими системными симптомами, такими как лихорадка и лейкоцитоз, хотя они обычно присутствуют только у половины всех пораженных пациентов, а положительные культуры в крови обнаруживаются гораздо реже. КТ или МРТ показаны при подозрении на абсцесс, при этом МРТ более чувствительна и специфична для выявления различных аспектов абсцесса, в том числе массовых эффектов, окружающего отека и реакции на терапию.
Поражение нервной системы ретровирусами: патологическая реакция хозяина или нейровирулентность как результат действия вирусных генов
Кристофер Пауэр
Лаборатория нейровирологии, Неврологическая исследовательская группа, г. Калгари, провинция Альберта, Канада
TRENDS in Neurosciences, Vol. 24, No. 3, March 2001.
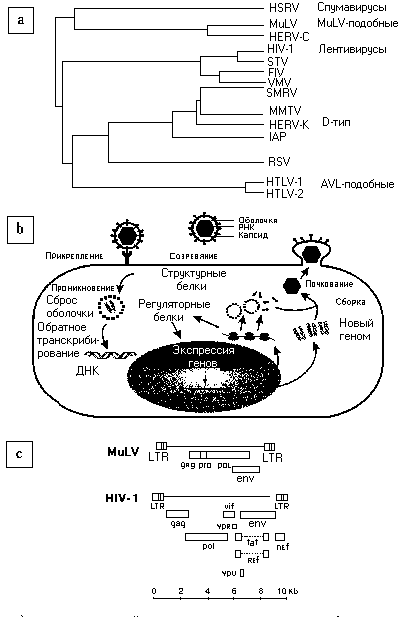
Ретровирусы представляют важную группу РНК-вирусов, которые вызывают ряд болезней нервной системы. Более того, потенциальную угрозу представляют вновь выявленные ретровирусные инфекции нервной системы и некоторые ритровирусные векторв или белки, используемые как переносчики генов. Данная статья описывает различные ретровирусы и их этиологическую роль в развитии болезней нервной системы, или, по другому, нейровирулентностъ. Специфические последовательности в пределах ретровирусных генов могут быть ответственны за нейровирулентностъ. Другой механизм заключается в активации иммунных реакций хозяина нейровирулентны-миретровирусами, что запускает нейропатогенетический каскад, медиаторами которого служат провоспалительные и нейротоксичные молекулы, а заканчивается все смертью нейрона. Таким образом, ретровирусные инфекции нервной системы иллюстрируют молекулярное взаимодействие между определенными вирусными возбудителями инфекций и патологическими реакциями хозяина; результатом такого взаимодействия является нейровирулентностъ.
Значение вирусных инфекций нервной системы все время возрастает, что видно по появлению за последние 5 лет нескольких глобальных нейрови-русных эпидемий [1]. Кроме того, повышается интерес в использовании вирусных векторов для генной экспрессии и для лечения заболеваний головного мозга [2]. Инфекцию считают нейровирусной, если она соответствует следующим критериям: нейроинвазивность, или проникновение вируса в нервную систему; нейротропизм (см. список терминов) или инфицирование вирусами клеток головного мозга, причем селективно инфицируются нейроны (это и называется нейротропизмом); и нейровирулентность или заболевание нервной системы, индуцированное вирусами. Хотя многие ретровирусы удовлетворяют этим критериям, но некоторые ретровирусные свойства усложняют их ней-робиологию, среди этих свойств: 1) предрасположенность к геномным мутациям; 2) способность вызывать как врожденный, так и адаптационный иммунный ответ в нервной системе; 3) способность вызывать патологические изменения за пределами нервной системы.
Иммунологические нарушения, вызываемые некоторыми ретровирусами, приводят ко вторичным инфекциям за пределами нервной системы и к злокачественным процессам в нервной системе. Однако, настоящая статья рассматривает только прямую нейровирулентность ретровирусов, с особым вниманием к механизмам нейровирулентности и ней-ротропизма, кроме того, всесторонне описываются ретровирусы типа С (также именуемые онкогенными), в том числе, вирус лейкемии грызунов (MuLV) и вирусы, тропные к человеческим Т-лимфоцитам (HTLV), а также лентивирусы, такие, как вирусы иммунодефицита человека. Нейротропные
штаммы этих вирусов изучались широко. Они способны вызвать серьезные нарушения здоровья у человека.
Таблица 1. Типичные нейротропные ретровирусы: штаммы, нейропатология и клеточный тропизм.
| Группа ретровирусов | Вирус | Патоструктурные измененияв нервной системе а) | Клетки нервной системы инфицированные in vivo |
| Тип С | CasBrE | губчатость, глиоз (СМ) | эндотелий, нейроны, глия |
| NE-8 | губчатость, глиоз (СМ, СтМ, Мзж) | эндотелий, астроциты, нейроны | |
| FrCas е) | губчатость, глиоз (СМ, СтМ, Мзж) | эндотелий, микроглия, нейроны, олигодендроциты | |
| Fr98D | губчатость, глиоз (Мзж, БВ, СВ) | микроглия, нейроны (?) | |
| MoMuLV-tsl | губчатость, глиоз (СМ, СтМ, Тал, СВ,БВ) | эндотелий, астроциты, макрофаги | |
| PCV-211 | губчатость (Пол, СМ, СтМ, Мзж, БВ) | эндотелий | |
| TR1.3 | кровоизлияние (Мзж) | эндотелий | |
| LP-BM5 | глиоз (Пол, Мзж, БВ) | астроциты, микроглия, сосудистое сплетение | |
| WB91-GV | глиоз | олигодендроциты, астроциты | |
| HTLV-I/II | демилиенизация, глиоз, лимфоцитарнаяинфильтрация (СМ) | лимфоциты, астроциты | |
| Лентивирусы | вирус иммуно- дефицита человека | глиоз, микроглиальные узелки, многоядерные гигантские клетки, диффузноепобледнение миелина(СМ, Пол, Мзж, БВ, СВ, ПН) | макрофаги, микроглия, астроциты |
| вирус visna-maedi | глиоз, периваскулярное воспаление, демиелинизация (БВ) | макрофаги, микроглия, астроциты | |
| вирус иммуно- дефицита кошек | периваскулярное воспаление, глиоз, микроглиальные узелки (БВ, СВ, Мзж, СМ, ПН) | макрофаги, микроглия | |
| вирус карпального артрита/энцефалита | глиоз, демиелинизация (БВ) | макрофаги и микроглия | |
| вирус инфекционной анемии лошадей | эпендимит, периваскулрное воспаление (Мзж) | клетки периваскулярных зон и мозговых оболочек | |
| вирус иммуноде- фицита коров | периваскулярное воспаление (БВ) | глиальные клетки | |
| вирус иммуноде- фицита обезьян | периваскулярное воспаление, глиоз, многоядерные гигантские клетки (БВ, Мзж, СВ, СМ) | макрофаги, микроглия, астроциты, эндотелий |
Нейропатологические механизмы развития MuLV-инфекции являются примером взаимодействия разных последовательностей в геноме ретровируса, обычно расположенных в генах env или gag, и параллельно действует патологическая реакция организма-хозяина, определяемая генотипом мыши. Например, у штамма Fr-98 MuLV два отдельных участка гена env регулируют реализацию нейровирулентности в особых мышиных линиях [7], при этом нейровирулентность проявляется в разных нейроповеденческих нарушениях, приводящих к смерти. В отличие от этого штамма, его штамм-предшественник, хотя и имеет похожий клеточный тропизм (микроглия), но авирулентен в отношении нервной системы. У некоторых разновидностей MuLV нейровирулентности способствуют изменения во внутриклеточном цикле и в экспрессии белков MuLV, кодируемых геном env, а также изменения уровня вирусной репликации в головном мозге [7]. Патологические реакции хозяина, инициируемые инфекцией MuLV, остаются плохо изученными, но обнаруживалась корреляция между нейро-вирулентностью и повышенным про-воспалитель-ным образованием цитокинов в гиальных клетках [9]. К другим патологическим реакциям хозяина, индуцируемым инфекцией MuLV, относятся изменение проницаемости гематоэнцефалического барьера и повышение внеклеточной концентрации глутамата, что ведет к смерти нейрона посредством механизма внешней цитотоксичности [10].
Проведено картирование некоторых участков генов хозяина, ответственных за резистентность к неврологическому заболеванию, индуцируемому MuLV. К этим участкам относятся FV-1, FV-4 и Akvr-1, кодирующие эндогенные ретровирусные гены env и gag, которые мешают проявлениям нейровирулентности, так как связываются с предполагаемым рецептором к вирусу, или, может быть, блокируют этап после входа [5]. Кроме того, нейровирулентность, вызванная несколькими разновидностями MuLV, зависит от возраста хозяина, причем новорожденные имеют повышенную подверженность, ввиду слабости иммунной защиты.
Что такое нейротропные вирусы
Нейроинвазия и нейротропизм являются общей чертой коронавирусов человека. Установлено, что вирус SARS-CoV-2 способен проникать в центральную нервную систему (ЦНС) посредством нейрональной диссеминации, при которой вирус сначала инфицирует периферические нейроны, а оттуда, используя механизм клетки-хозяина, инфицирует нейроны ЦНС. Данный факт подтверждает нарушение обоняния у пациентов с COVID-19. Кроме того, известен и гематогенный путь распространения коронавирусов в ЦНС.
Нейротропность и нейровирулентность SARS-CоV-2
Михаил Селицкий, доцент кафедры неврологии и нейрохирургии БелМАПО, кандидат мед. наук. В настоящее время все больше данных свидетельствует о том, что SARS-CоV-2 является как нейротропным, так и нейровирулентным. Вирус проникает в ЦНС вскоре после заражения и обнаруживается в спинномозговой жидкости и ткани головного мозга.
После преодоления гематоэнцефалического барьера вирус может размножаться в микроглии и нейронах с последующим повреждением гематоэнцефалического барьера, что приводит к воспалительному каскаду. Экспрессия рецептора ACE2 в нейронах и эндотелиальных клетках подчеркивает нейроинвазивный потенциал вируса. При этом дифференцированный иммунный ответ может определять последующие альтернативные иммуноопосредованные неврологические осложнения.
Представляют интерес данные исследований, проведенных с использованием вируса гепатита мыши (РНК-вирус с оболочкой, который принадлежит к семейству Coronaviridae).
Этот вирус вызывает иммунные нарушения, приводящие к хронизации инфекции ЦНС и прогрессирующей демиелинизации в мозге, что является отличительной чертой рассеянного склероза (РС). Поскольку SARS-CoV-2 принадлежит к тому же семейству, он также может быть ответственным за демиелинизацию в мозге и приводить к состояниям, подобным тем, которые отмечаются у пациентов с РС.
Важно помнить, что пациенты с РС лечатся кортикостероидами, что приводит к иммуносупрессии и обусловливает высокий риск протекания COVID-19 в тяжелой форме. Современные научные публикации подтверждают результаты предыдущих исследований о том, что пациенты с РС имеют более высокий риск нейроинвазии HCoV.
Кроме того, имеющиеся данные свидетельствуют о том, что у пациентов с болезнью Паркинсона (БП) также может ухудшаться состояние после перенесенных системных инфекционных заболеваний. Клинические проявления инфекционных осложнений при БП могут проявляться от легкого обострения заболевания до акинетического криза.
Механизмы, лежащие в основе ухудшения клинических симптомов БП, включают: изменение фармакодинамики дофаминергических лекарств, измененный метаболизм дофамина в мозге, периферические воспалительные процессы, циркулирующие токсины и цитокины. Таким образом, пациенты с БП должны тщательно наблюдаться на предмет ухудшения моторики в течение периода активной инфекции, вызванной SARS-CoV-2, и далее в период реконвалесценции.
Заслуживают внимания симптомы COVID-19 в виде нарушения обоняния и вкуса, т. к. это характерные продромальные немоторные проявления БП, которые могут появляться за несколько лет до возникновения двигательных симптомов заболевания. Появляются научные работы, авторы которых прогнозируют связь COVID-19 c последующим развитием симптомов паркинсонизма.
В последние годы была описана тесная связь между микробиотой кишечника, нейровоспалением и заболеваниями ЦНС. Известно, что SARS-CoV-2 инфицирует клетки слизистой оболочки кишечника, вызывая воспаление и дисбиоз кишечника. Это может привести к кратковременным и долгосрочным изменениям в микробиоте, которые могут способствовать нейровоспалению и нейродегенерации.
В поисках алгоритмов
Все чаще к нам обращаются пациенты с теми или иными неврологическими жалобами после COVID-19. Наблюдаемые клинические симптомы и данные инструментальных исследований (МРТ, ЭНМГ) свидетельствуют о том, что страдает не только ЦНС, но и периферическая нервная система.
Совместно с коллегами с кафедры инфекционных болезней БГМУ, из лаборатории иммунологии и клеточной биотехнологии РНПЦ эпидемиологии и микробиологии, биохимической группы НИЛ БелМАПО, РКМЦ Управления делами Президента мы изучаем механизмы возникновения неврологических осложнений, оцениваем особенности клинической картины и структурных изменений центральной и периферической нервной системы.
Данная работа выполняется в рамках финансируемой государством научно-исследовательской работы на тему «Разработать алгоритм прогнозирования течения неврологических заболеваний (рассеянный склероз, воспалительные полиневропатии, болезнь Паркинсона) у пациентов, перенесших коронавирусную инфекцию (COVID-19)».
Иммуно-опосредованный механизм поражения нервной системы
Далеко не всегда симптомы поражения нервной системы появляются на фоне или сразу же после перенесенного COVID-19.
Многие пациенты отмечают возникновение жалоб только через несколько недель после выздоровления, что наталкивает на мысль об иммуноопосредованном механизме развития этих нарушений. Иными словами, коронавирус запускает поломку иммунитета, в результате которой вырабатываются аутоантитела против нервной системы.
Болезнь Паркинсона
На сегодняшний день считается, что БП — это хроническое нейродегенеративное заболевание с неустановленной этиологией. Однако в последнее время появляется множество научных публикаций, которые подтверждают наличие нейровоспалительного компонента в патогенезе этого заболевания.
На практике мы видим, что многие пациенты с БП, которые перенесли COVID-19, стали чувствовать себя хуже. При обращениях в медицинские учреждения у них объективно подтверждается нарастание неврологических симптомов, что требует коррекции дозы противопаркинсонических препаратов. И не всегда есть взаимосвязь с тяжестью и длительностью перенесенной инфекции. Кроме того, мы стали выявлять пациентов, у которых симптомы БП после COVID-19 появились впервые.
Клинический случай
Пациентка (63 года) через 3 недели после COVID-19 стала отмечать появление неловкости и дрожания в левой руке. На амбулаторном приеме неврологом 5-й ГКБ Минска были выявлены характерные для БП симптомы: тремор покоя, повышение мышечного тонуса по экстрапирамидному типу, замедление движений. Все симптомы наблюдались на одной половине тела (гемипаркинсонизм), что наиболее типично именно для БП. Следует отметить, что пациентка перенесла COVID-19 в легкой форме. При назначении прамипексола симптомы заболевания значительно уменьшились.
Рассеянный склероз
Относится к группе аутоиммунных заболеваний нервной системы. Это хроническое прогрессирующее заболевание, причины которого до сих пор не известны. Еще до начала коронавирусной пандемии на кафедре неврологии и нейрохирургии БелМАПО длительное время наблюдались более 150 пациентов с РС. После того как некоторые из них переболели COVID-19, мы заметили, что у этих пациентов стали отмечаться обострения заболевания даже в стадии длительной ремиссии на фоне приема препаратов группы ПИТРС (препараты, изменяющие течение рассеянного склероза).
У пациентов с рецидивно-ремиттирующим типом течения РС обострения проявлялись преимущественно появлением новой очаговой неврологической симптоматики в виде ретробульбарных невритов, усилением или возникновением слабости в конечностях (парезов), а также сенсорными нарушениями. После патогенетического лечения (во всех случаях метилпреднизолон) средний балл EDSS восстановился, что свидетельствует о хорошем терапевтическом эффекте применения ГКС при обострениях РС, ассоциированных с COVID-19. У пациентов со вторично прогрессирующим типом течения РС ухудшение самочувствия выражалось преимущественно в виде нарушения функции ходьбы и нарастания пирамидной симптоматики. На фоне проведенного лечения (метилпреднизолон) восстановление неврологической симптоматики было частичным.
Полученные результаты свидетельствуют о возможном влиянии SARS-CoV-2 на течение РС в виде провоцирования обострений при рецидивно-ремиттирующем типе течения или прогрессирования заболевания при вторично прогрессирующем типе течения.
Рисунок 1. МРТ головного мозга с контрастированием гадолинием пациентки с РС (режим Т1; стрелками указаны очаги, накапливающие контраст). Клинический случай
Пациентка (26 лет) болеет РС в течение 5 лет. Последние два года отмечалась стойкая ремиссия. Тип течения РС — рецидивно-ремиттирующий. В мае 2020 года перенесла COVID-19 в легкой форме. Через 2 недели после выздоровления появилось онемение левой руки и грудной клетки.
При выполнении МРТ головного мозга (см. рис. 1) и шейного отдела позвоночника с контрастированием выявлены множественные очаги демиелинизации, накапливающие контраст, в количестве 15 штук. Из них 13 очагов располагались в головном мозге (как супратенториально, так и инфратенториально) и 2 очага — в спинном.
Назначен метилпреднизолон 1 000 мг № 5, после чего неврологическая симптоматика обострения регрессировала.