Нитроглицерин
| Нитроглицерин | |
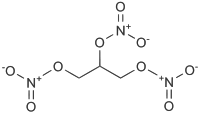 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Нитроглицерин |
| Химическая формула | CHONO2(CH2ONO2)2 |
| Физические свойства | |
| Молярная масса | 227.0865 г/моль |
| Плотность | 1.595 г/см³ |
| Термические свойства | |
| Температура плавления | 13 °C |
| Классификация | |
| SMILES | C(C(CO[N+](=O)O |
Нитроглицерин (глицеринтринитрат, тринитроглицерин, тринитрин, НГЦ) — сложный эфир глицерина и азотной кислоты. Исторически сложившееся название «нитроглицерин» с точки зрения современной номенклатуры является несколько некорректным, поскольку нитроглицерин является нитроэфиром, а не «классическим» нитросоединением. Широко известен благодаря своим взрывчатым (и в некоторой степени лекарственным) свойствам. Химическая формула O2NOCH2CH(ONO2)CH2ONO2. Впервые синтезирован итальянским химиком Асканьо Собреро в 1847 году, первоначально был назван «пироглицерин» (итал. pyroglycerina ).
Согласно номенклатуре IUPAC именуется 1,2,3-тринитроксипропан.
Содержание
Получение
В лаборатории получают этерификацией глицерина смесью концентрированной азотной и серной кислот. Кислоты и глицерин должны быть очищены от примесей. Для этерификации предварительно при постоянном перемешивании и охлаждении смешивают кислоты, изготавливая таким образом нитрующую смесь, и добавляют по каплям глицерин при постоянном охлаждении колбы льдом и контроле температуры.
Описание реакции: 2H2SO4 + HNO3 ↔ H2SO4 · H2O + NO2 HSO4 Реакция равновесна с сильным смещением равновесия влево.
Затем реакционную смесь кислот и глицерина выдерживают непродолжительное время, при охлаждении льдом. Жидкость расслаивается на два слоя. Нитроглицерин легче нитрующей смеси и всплывает в виде мутного слоя.
Физико-химические свойства
Сложный эфир глицерина и азотной кислоты. Прозрачная вязкая нелетучая жидкость (как масло), склонная к переохлаждению. Смешивается с органическими растворителями, почти нерастворим в воде [1] (0.13 % при 20 °C, 0,2 % при 50 °C, 0,35 % при 80 °C, по другим данным [источник не указан 1317 дней] 1,8 % при 20 °C и 2,5 % при 50 °C). При нагревании с водой до 80 °C гидролизуется. Быстро разлагается щёлочами.
Токсичен, всасывается через кожу, вызывает головную боль. Очень чувствителен к удару, трению, высоким температурам, резкому нагреву и т. п. Чувствительность к удару для груза 2 кг — 4 см (гремучая ртуть — 2 см, тротил — 100 см). Весьма опасен в обращении. При осторожном поджигании в малых количествах неустойчиво горит синим пламенем. Температура кристаллизации 13,5 °C (стабильная модификация, лабильная кристаллизуется при 2,8 °C). Кристаллизуется со значительным увеличением чувствительности к трению. При нагревании до 50 °C начинает медленно разлагаться и становится ещё более взрывоопасным. Температура вспышки около 200 °C. Теплота взрыва 6,535 МДж/кг. Температура взрыва 4110 °C. Несмотря на высокую чувствительность, восприимчивость к детонации довольно низка — для полного взрыва необходим капсюль-детонатор № 8. Скорость детонации 7650 м/с. 8000-8200 м/c — в стальной трубе диаметром 35 мм, инициирован с помощью детонатора № 8. В обычных условиях жидкий НГЦ часто детонирует в низкоскоростном режиме 1100—2000 м/с. Плотность 1,595 г/см³, в твёрдом виде — 1,735 г/см³. Твёрдый нитроглицерин менее чувствителен к удару, но более к трению, поэтому очень опасен. Объем продуктов взрыва 715 л/кг. Фугасность и бризантность сильно зависят от способа инициирования, при использовании слабого детонатора мощность сравнительно невелика. Фугасность в песке — 390 мл, в воде — 590 мл (кристаллического несколько выше), работоспособность (фугасность) в свинцовой бомбе 550 см³. Применяется как компонент некоторых жидких ВВ, динамитов и главным образом бездымных порохов (пластификатор — нитроцеллюлоза). Кроме того, в малых концентрациях применяется в медицине.
Применение
Я пью его в мельчайших дозах,
На сахар капаю раствор,
А он способен бросить в воздух
Любую из ближайших гор.
Он, растворенный в желатине
И превращенный в динамит,
В далекой золотой долине,
Взрывая скалы, загремит.
И содрогнулся шнур бикфордов,
Сработал капсюля запал,
И он разламывает твердый,
Несокрушимый минерал.
Сердечной боли он – причина,
И он один лекарство мне –
Так разъяснила медицина
В холодной горной стороне.
В фармакологии
Нитроглицерин относится к категории веществ, называемых вазодилататорами — средствам, понижающим кровяное давление, расслабляет гладкую мускулатуру кровеносных сосудов, бронхов, желчных и мочевых путей, желудочно-кишечного тракта. Основное применение имеет при стенокардии, главным образом для купирования острых приступов спазмов коронарных сосудов. Для предупреждения приступов он мало пригоден из-за кратковременности действия. Иногда применяется при эмболии центральной артерии сетчатки, а также функциональных холицистопатиях.
Применяется в виде таблеток по 0,5 мг для помещения под язык; а также в 1 % спиртовом растворе.
Во взрывотехнике
Нитроглицерин широко применялся во взрывотехнике. В чистом виде он очень неустойчив и опасен. После открытия Собреро нитроглицерина, в 1853 г. русский химик Зинин предложил использовать его в технических целях. Спустя 10 лет инженер Петрушевский первым начал производить его в больших количествах, под его руководством нитроглицерин был применён в горном деле в 1867 г. Альфред Нобель в 1863 г. изобрёл инжектор-смеситель для производства нитроглицерина и капсюль-детонатор, а в 1867 г. — динамит, получаемый смешением нитроглицерина с кизельгуром (диатомитом, инфузорной землёй).
В литературе и кино
Герои приключенческого романа «Таинственный остров» (1874) Жюль Верна использует нитроглицерин для подрыва гранитной скалы. Автор подробно описывает процесс получения нитроглицерина из природных веществ, обнаруженных на острове (хотя Жюль Верн намеренно опустил один из важных этапов синтеза). Писатель характеризует это вещество следующим образом [3] :
Основная часть сюжета фильма «Плата за страх» (1953) заключается в процессе перевозки нитроглицерина на грузовиках.
В романе Чака Паланика «Бойцовский клуб» (1996) и одноимённом фильме (1999) главный герой получает нитроглицерин путём плавления мыла и добавления глицерина в азотную кислоту.
Возьмите одну часть 98%-ной дымящей азотной кислоты, и смешайте с тремя частями концентрированной серной кислоты. Делать это надо на ледяной бане. Затем добавляйте глицерин по капле из глазной пипетки. Вы получили нитроглицерин.
В фильме «Вертикальный предел» (2000) есть эпизод с самопроизвольной детонацией жидкого нитроглицерина от прямого воздействия солнечных лучей.
В сериале Побег сезон 2 серия 9 в ботаническом саду находят ящик с ампулами нитроглицерина, который спрятал Майкл Скофилд.
В фильме «Легенда Зорро» (2005) главный злодей демонстрирует нитроглицерин заказчикам, также финальная сцена фильма происходит в поезде, перевозящем нитроглицерин.
Свойства и получение нитроглицерина
Зависимость давления насыщенного пара от температуры жидкости. Физико-химические свойства нитроглицерина. Уравнение его образования. Этерификация глицерина, проводимая серно-азотной кислотной смесью. Расчет объема газов при сгорании его одного килограмма.
| Рубрика | Химия |
| Вид | контрольная работа |
| Язык | русский |
| Дата добавления | 08.03.2014 |
| Размер файла | 99,4 K |
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru
1. Свойства жидкостей
2. Физико-химические свойства нитроглицерина
3 Технология производства
Одно и то же вещество в зависимости от соотношения между средней кинетической и средней потенциальной энергиями частиц может находиться в одном из трех агрегатных состояниях: твердом, жидком или газообразном.
Рассмотрим пример (рис. 1):
Рис. 1. Изотермы газа при температурах Т1 TКР не может быть превращен в жидкость ни при каком давлении. Значения PКР, VКР, TКР называются критическими параметрами газа.
Данное свойство жидкости используется, например, при тушении пожаров водой: резкое испарение воды охлаждает зону горения.
Кстати, наш организм при жаркой погоде выделяет пот. Какой его смысл? А смысл в том, что при испарении пота охлаждается кожа человека, и он не перегревается.
Испарение происходит при любой температуре и возрастает при ее повышении до появления кипения. При температуре кипения интенсивное испарение происходит не только с ее поверхности, но и во всем объеме жидкости с образованием пузырьков пара. При этом эффект охлаждения резко возрастает.
Если кипение происходит при постоянном давлении, то температура жидкости остается постоянной, т.к. все подводимое тепло тратиться полностью на парообразование (рис. 3).
С повышением давления в закрытом сосуде температура кипения возрастает. Например, ТКИП воды равно 1000С при P=101,3 кПа и ТКИП=1890С при P=1013 кПа (10 атм). Такая ситуация наблюдается, в частности, в паровых котлах, где существует вода в жидком виде при температуре выше 1000С (это так называемая перегретая вода), либо в кастрюле-скороварке (при РИЗБ=0,2 атм, ТКИП=1200С).
Если прекратить нагрев и расходовать пар, то кипение продолжается до снижения температуры до 1000С и атмосферного давления. Если же резко сбросить давление (например, при лопнувшей трубе котла), то перегретая вода мгновенно превращается в пар с резким скачком его давления и взрывом. Напротив, в условиях пониженного давления атмосферы температура кипения снижается. Это повышает взрывоопасность горючих жидкостей, из-за повышения интенсивности испарения и создания взрывоопасных концентраций паров.
Рис. 4. Диаграмма упругости насыщенного пара
Зависимость давления насыщенного пара Рн от температуры жидкости Тж рассчитывается по уравнению Антуана:
Это уравнение используется для оценки условий взрываемости паровоздушных смесей.
Физико-химические свойства нитроглицерина
Сложный эфир глицерина и азотной кислоты. Прозрачная вязкая нелетучая жидкость (как масло), склонная к переохлаждению. Смешивается с органическими растворителями, почти нерастворим в воде (0.13% при 20C, 0,2% при 50C, 0,35 % при 80 °C, по другим данным 1,8 % при 20 °C и 2,5 % при 50C). При нагревании с водой до 80 °C гидролизуется. Быстро разлагается щёлочами.
Получение нитроглицерина с последующей сепарацией его от отработанной кислоты является одним из самых опасных процессов химической технологии.
Уравнение образования нитроглицерина:
Все технологические стадии производства нитроглицерина, благодаря жидкому агрегатному состоянию реагентов и большой скорости их взаимодействия, легко осуществляется в аппаратах непрерывного действия, которые, в свою очередь, можно легко автоматизировать.
Периодические процессы. Более 60 лет нитроглицерин получали в малогабаритных аппаратах периодического действия, конструкция которых исключала возможность каких-либо ударов или трения. Перемешивание на стадии этерификации и промывки производили сжатым воздухом, перемещение нитроглицерина из одного аппарата в другой осуществлялось только самотеком.
Наиболее совершенный технологический процесс получения нитроглицерина был разработан Нобелем. По этому способу этерификацию проводили в цилиндрическом аппарате—нитраторе, снабженном змеевиком для подачи воды на охлаждение. Перемешивание нитромассы осуществлялось сжатым воздухом.
но и повышает скорость сепарации в результате образования пузырьков газа SiF4.
Несколько более совершенным с точки зрения техники безопасности был способ Натана, Томсона и Ринтула, принятый в производстве в 1904 г.. Основным преимуществом его была компактность установки, достигнутая благодаря совмещению функций нитратора и сепаратора в одном аппарате. Кроме того, на трубопроводах для передачи нитроглицерина вместо кранов были поставлены зажимы.
Этерификация в нитраторе проводится как обычно. В нижнюю часть его через трубу заливают нитросмесь, а сверху подают глицерин. По окончании процесса воздушное перемешивание прекращают и начинают сепарацию с помощью отработанной кислоты, подаваемой по той же трубе, через которую заливали нитросмесь. Нитроглицерин начинает постепенно выдавливаться отработанной кислотой в бак предварительной промывки. Контроль за ходом сепарации осуществляется через смотровое стекло. Такой способ сепарации лучше отвечает требованиям техники безопасности. Способ Натана, Томсона и Ринтула на некоторых заводах сохранился до сих пор.
Безопасность работы периодических установок получения нитроглицерина обеспечивалась рядом специальных правил ведения этого процесса. Основные из них: тщательный контроль за чистотой исходных материалов, точность соблюдения дозировок и температурного режима, а также хорошее перемешивание нитромассы, исключающее образование зон застоя (что вполне возможно из-за несовершенства воздушного перемешивания).
Наиболее опасным процессом была сепарация, вследствие низкой стойкости кислого нитроглицерина. Во всех случаях появления опасности разложения продукта реакционную массу спускали в аварийный чан, заполненный водой. Следует отметить, что спуск содержимого нитратора или сепаратора в аварийный чан не всегда спасает положение [50]. Из 100 случаев 20 кончается взрывом в чане, иногда остаток нитроглицерина взрывается в нитраторе. Для более безопасного и надежного спуска нитромассы аппараты (нитратор и сепаратор) снабжаются кранами, открывающимися автоматически с помощью сжатого воздуха. Пуск автомата в действие может быть произведен не только непосредственно с рабочего места, но также и из убежища. При включении автомата для спуска нитромассы в аварийный чан начинает работать сигнализация, предупреждающая об опасности всех лиц, находящихся в данном помещении.
Определить объем газов при сгорании одного килограмма нитроглицерина
2С3H5N3O9 +2,5O2 = 3CO2 +6NO2+5H2O
Определяем количество вещества нитроглицерина С3H5N3O9
n(С3H5N3O9) = 1к г/ 227к г/кмоль = 0,0044 кмоль
а) при сгорании 0,0044 кмоль С3H5N3O9 образуется х кмоль CO2
при сгорании 2 кмоль С3H5N3O9 образуется 3 кмоль CO2
нитроглицерин жидкость этерификация сгорание
Определяем объем CO2
V(CO2 = 0,066 кмоль *22,4м3/кмоль = 0,14м3
б) при сгорании 0,0044 кмоль С3H5N3O9 образуется х кмоль NO2
при сгорании 2 кмоль С3H5N3O9 образуется 6 кмоль NO2
Определяем объем NO2
V(NO2 = 0,0132 кмоль *22,4м3/кмоль = 0,29м3
в) при сгорании 0,0044 кмоль С3H5N3O9 образуется х кмоль H2O
при сгорании 2 кмоль С3H5N3O9 образуется 5 кмоль H2O
Определяем объем H2O
V(H2O = 0,011 кмоль *22,4м3/кмоль = 0,25м3
1. Артеменко А. И., Практикум по органической химии. Учебное пособие для ВУЗов, М.: Высшая школа, 2001, с.187
2. Ким А.М., Органическая химия, 2004
Размещено на Allbest.ru
Подобные документы
Зависимость температуры кипения водных растворов азотной кислоты от содержания HNO. Влияние состава жидкой фазы бинарной системы на температуру кипения при давлении. Влияние температуры на поверхностное натяжение водных растворов азотной кислоты.
реферат [3,9 M], добавлен 31.01.2011
Составы равновесных жидкости и пара. Определение состояние пара. Законы Коновалова. Дробная перегонка и ректификация. Зависимость состава паровой фазы от температуры. Давление насыщенного пара в системах с ограниченной взаимной растворимостью компонентов.
лекция [600,0 K], добавлен 28.02.2009
Аналитическая зависимость теплового эффекта реакции от температуры. Интервалы температур теплоты испарения, возгонки и плавления. Температурная зависимость давлений насыщенного пара для твердого и жидкого вещества. Равновесные парциальные давления.
лабораторная работа [263,4 K], добавлен 03.05.2009
Физические и физико-химические свойства азотной кислоты. Сырье для производства азотной кислоты. Характеристика целевого продукта. Процесс производства слабой (разбавленной) и концентрированной азотной кислоты. Действие на организм и ее применение.
презентация [1,6 M], добавлен 05.12.2013
Хлорид кальция: физико-химические свойства. применение и сырье. Получение плавленого хлорида кальция из дистиллерной жидкости содового производства. Получение хлорида кальция и гидроксилохлорида из маточного щелока. Безводный кальций из соляной кислоты.
реферат [84,4 K], добавлен 09.08.2008
Расчет основных характеристик газа на основании закона Дальтона, понятие парциального давления. Определение плотности смеси газов, значения молекулярной массы. Основные виды вязкости: кинематическая и динамическая. Пределы воспламенения горючего газа.
контрольная работа [65,7 K], добавлен 11.07.2017
Химическая формула молекулы воды и ее строение. Систематическое наименование – оксид водорода. Физические и химические свойства, агрегатные состояния. Требования к качеству воды, зависимость ее вкуса от минерального состава, температуры и наличия газов.
презентация [6,1 M], добавлен 26.10.2011
Нитроглицерин концентрат : инструкция по применению
Состав
действующее вещество: nitroglycerin;
вспомогательное вещество: этанол (96 %).
Фармакотерапевтическая группа
Периферические вазодилататоры, применяемые при лечении заболеваний сердца. Органические нитраты. Код АТС C01D А02.
Сильная и продолжительная боль ишемического генеза в области сердца, ассоциированная с инфарктом миокарда или нестабильной стенокардией.
Недостаточность насосной функции сердца и отек легких, ассоциированный с острым инфарктом миокарда.
Артериальная гипертензия, связанная с операцией на открытом сердце и другими хирургическими вмешательствами.
Обеспечение контролируемой гипотензии во время хирургических вмешательств.
Противопоказания
Повышенная чувствительность к нитроглицерину и к другим нитросоединениям. Гиповолемия, выраженная артериальная гипотензия (систолическое давление
Способ применения и дозы
Режим дозирования устанавливают индивидуально, в зависимости от клинического ответа и систолического артериального давления.
Обычно применяют инфузионный раствор, содержащий 100 мкг/мл нитроглицерина. Такой раствор готовят путем разведения 1 ампулы Нитроглицерина, концентрата для раствора для инфузий, 10 мг/мл (= 20 мг нитроглицерина) в 200 мл 0,9 % раствора натрия хлорида, 5 % раствора глюкозы или изотонического глюкозо-солевого раствора для получения концентрации раствора 100 мкг/мл. Можно применять большие концентрации, но не больше 400 мкг/мл.
Системы для инфузий должны быть изготовлены из полиэтилена (РЕ), полипропилена (РР), политетрафторэтилена (PTFE) или стекла. Нитроглицерин абсорбируется материалами, изготовленными из поливинилхлорида (PVC) и полиуретана (PU), что требует повышения его дозы.
| Дозировка Нитроглицерина, раствора, приготовленного из концентрата для раствора для инфузий. Рекомендуемая скорость внутривенной инфузии: 10-200 мкг/мин, которая при необходимости может быть увеличена до 400 мкг/мин.Внутривенную инфузию можно начинать со скоростью 10-20 мкг/мин. В дальнейшем скорость можно увеличивать на 10-20 мкг/мин каждые 5-10 минут, в зависимости от реакции пациента. Хороший терапевтический эффект наблюдается при скорости введения 50-100 мкг/мин. При длительном введении больших доз через 8-24 ч возможно развитие толерантности и может понадобиться увеличение дозы. Максимальная скорость составляет 400 мкг/мин.Титрование дозы проводят под регулярным наблюдением состояния пациента, мониторингом артериального давления, также могут быть использованы измерения давления заклинивания легочных капилляров и пропускной способности сердца. | |||
| мкг/мин | мг/ч | мл/ч, при концентрации раствора 100 мкг/мл | капель/мин, при концентрации раствора 100 мкг/мл |
| 10 | 0,6 | 6 | 2 |
| 20 | 1,2 | 12 | 4 |
| 30 | 1,8 | 18 | 6 |
| 40 | 2,4 | 24 | 8 |
| 50 | 3 | 30 | 10 |
| 60 | 3,6 | 36 | 12 |
| 70 | 4,2 | 42 | 14 |
| 80 | 4,8 | 48 | 16 |
| 90 | 5,4 | 54 | 18 |
| 100 | 6 | 60 | 20 |
| 150 | 9,0 | 90 | 30 |
| 200 | 12 | 120 | 40 |
| 300 | 18 | 180 | 60 |
| 400 | 24 | 240 | 80 |
Применение в хирургии: для контроля гипертонических эпизодов рекомендуемая начальная доза составляет 25 мкг/мин с пошаговым увеличением на 25 мкг/мин каждые 5 минут до достижения целевого снижения артериального давления. Хотя у большинства пациентов эффективны дозы 10-200 мкг/мин, при некоторых хирургических процедурах могут потребоваться дозы до 400 мкг/мин. При лечении периоперационной ишемии миокарда, рекомендуемая начальная доза составляет 15-20 мкг/мин с пошаговым увеличением на 10-15 мкг/мин до достижения целевого эффекта.
Резистентная сердечная недостаточность вследствие острого инфаркта миокарда: рекомендуемая начальная доза составляет 20-25 мкг/мин. Доза может быть уменьшена до 10 мкг/мин или пошагово увеличена на 20-25 мкг/мин с 15-30 минутными интервалами до достижения целевого эффекта.
Нестабильная стенокардия: рекомендуемая начальная доза составляет 10 мкг/мин с пошаговым увеличением 5-10 мкг/мин с примерно 30-минутными интервалами.
Дети и пациенты пожилого возраста: использование нитроглицерина у детей и пожилых пациентов не рекомендуется, т.е. безопасность и эффективность препарата у данных возрастных категорий пациентов не установлены.
Нежелательные реакции представлены в соответствии с классификацией систем органов и частотой возникновения: очень часто (≥ 1/10), часто (≥ 1/100 до
Передозировка
Симптомы: артериальная гипотензия, тахикардия, ощущение жара, гиперемия, головная боль, ускоренное сердцебиение, синкопе. Повышение внутричерепного давления, которое может привести к спутанности сознания и неврологическим расстройствам. Передозировка в течение нескольких часов может привести к интоксикации этанолом.
Лечение. Чрезмерную артериальную гипотензию можно устранить путем снижения скорости инфузии препарата или прекращения его введения. При тяжелой артериальной гипотензии больного следует положить в горизонтальное положение с опущенным головным краем кровати. В тяжелых случаях назначают плазмозаменители, допамин. Гипоксия, вызванная метгемоглобинемией, может повлечь цианоз, метаболический ацидоз, кому, судороги, сосудистый коллапс. При метгемоглобинемии внутривенно вводят раствор метиленового синего (1-2 мг/кг массы тела).
Применение в период беременности или кормления грудью
Информация о применении препарата в период беременности ограничена, поэтому его не рекомендуется применять беременным. Побочные реакции, наблюдающиеся у младенца, которого кормит принимающая препарат женщина, маловероятны и слабо выражены. В период лечения кормление грудью следует прекратить. В случае необходимости применения препарата по жизненным показаниям следует сопоставить соотношение польза/риск.
Опыт применения детям ограничен.
Необходимо с осторожностью, сопоставляя риск и пользу, применять препарат при анемии, дефиците глюкозо-6-фосфатдегидрогеназы, метгемоглобинредуктазы, аортальном или митральном стенозе, «легочном сердце», тяжелых нарушениях функции печени, почек, гипотиреозе, гипотермии, недостаточном питании.
Возможно развитие толерантности к нитроглицерину, а также перекрестной толерантности к другим нитратам.
Во время лечения не следует употреблять алкогольные напитки.
Способность влиять на скорость реакции при управлении автотранспортом или работе с другими механизмами
Препарат применяют в условиях стационара.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
При одновременном применении с другими вазодилататорами, гипотензивными средствами (ингибиторами АПФ, блокаторами «медленных» кальциевых каналов, диуретиками, β-адреноблокаторами), трициклическими антидепрессантами, ингибиторами МАО, этанолом, этанол-содержащими препаратами, прокаинамидом, хинидином, новокаинамидом усиливается гипотензивное действие нитроглицерина.
Совместное применение нитроглицерина с ингибиторами фосфодиэстеразы типа 5 (например, силденафил, тадалафил, варденафил), которые используются для лечения нарушений эрекции или легочной гипертензии, строго противопоказано из-за риска развития тяжелой гипотензии. Применение нитроглицерина возможно не ранее чем через 24 часа после приема препаратов, содержащих силденафил и варденафил, не ранее чем через 48 часов после приема препаратов, содержащих тадалафил.
Противопоказано совместное применение нитратов со стимулятором растворимой гуанилатциклазы риоцигуатом.
Атропин и другие препараты, оказывающие М-холинолитические действие (этазицин, этмозин), могут уменьшить эффект нитроглицерина в результате снижения его биодоступности.
Сочетание с дигидроэрготамином может привести к повышению биодоступности последнего, увеличивая риск коронарного спазма.
При совместном применении с нитроглицерином возможно снижение антикоагулянтного эффекта гепарина.
Фенобарбитал активирует метаболизм нитратов в печени.
Вероятность развития толерантности возрастает при использовании в сочетании с другими препаратами из группы нитратов.
Применение донаторов сульфгидрильних групп (каптоприл, ацетилцистеин, унитиол) способствует восстановлению сниженной чувствительности к нитроглицерину.
Антиангинальное действие нитроглицерина связано главным образом с уменьшением потребности миокарда в кислороде за счет уменьшения преднагрузки (расширение вен и уменьшение притока крови к правому предсердию) и постнагрузки (уменьшение общего периферического сопротивления сосудов). Способствует распределению коронарного кровотока в ишемизированных областях миокарда. Повышает толерантность к физической нагрузке у больных с ишемической болезнью сердца, стенокардией. При сердечной недостаточности способствует разгрузке миокарда, главным образом за счет уменьшения преднагрузки. Снижает давление в малом круге кровообращения.
Фармакокинетика. Эффект наблюдается через 1-2 минуты с начала инфузии глицерилтринитрата и длится 3-5 минут.
Метаболизм нитроглицерина осуществляется преимущественно в печени под влиянием глутатионзависимой редуктазы. Кроме того, в сыворотке крови проходит спонтанный гидролиз и неорганическое расщепление нитроглицерина. Метаболиты преимущественно водорастворимые, частично или полностью освобождены от азота, в дальнейшем метаболизируются до глюкуронидов и экскретируются с мочой или желчью. Энтерогепатическая рециркуляция не наблюдается.
Фармакокинетика нитроглицерина сложная и зависит от индивидуальных особенностей пациентов. Колебания обусловлены, например, первичным метаболизмом при прохождении через печень, большим объемом распределения, концентрацией в стенках сосудов, значительным различием концентраций в артериях и венах, гидролизом в сыворотке крови и непостоянной концентрацией в плазме крови. Плазматический клиренс нитроглицерина при продолжительной инфузии составляет 230 ± 9 мл/мин/кг.
Основные физико-химические свойства
Прозрачная бесцветная или светло-желтая жидкость.
Применяют только перечисленные в разделе «Способ применения и дозы» растворители. Не следует вводить в одной емкости с другими лекарственными средствами.




