Низкомолекулярные гепарины: возможности применения при беременности
Существует целый ряд заболеваний, результаты лечения которых трудно предсказуемы. Невынашивание беременности относится именно к таким заболеваниям, однако, непредсказуемость результатов лечения в случае этой патологии имеет особое драматическое значение.
Об эффективности применения низкомолекулярных гепаринов (НМГ) при невынашивании беременности мы беседуем с главным акушером-гинекологом ПФО, заведующей кафедрой акушерства и гинекологии № 1 ГБОУ ДПО КГМА Минздрава России, профессором Ларисой Ивановной Мальцевой.
— Что такое низкомолекулярные гепарины?
— Гепарин является основным препаратом прямого антикоагулянтного или антитромботического действия. Его эффекты опосредуются несколькими протеинами плазмы: антитромбином III, гепариновым кофактором II, TFPI (ингибитор внешнего пути свертывания). Обычный (нефракционированный) гепарин (НГ) является высокомолекулярным соединением, его молекулярная масса — 15-20 тысяч Да, при этом биодоступность составляет всего 30%. Это определено гетерогенностью структуры, способностью связываться с различными белками и клетками-макрофагами, клетками эндотелия и др. Кроме того, нефракционированнный гепарин подвержен влиянию антигепаринового фактора тромбоцитов, образуя с ним специфический комплекс, который может вызвать гепариновую иммунную тромбоцитопению и тромбоз. Большие дозы гепарина снижают уровень антитромбина III, что может вызвать гиперкоагуляцию и также стать причиной тромбоза. Таким образом, наряду с множеством плюсов обычный гепарин обладает рядом нежелательных эффектов, которых лишен низкомолекулярный гепарин (НМГ). НМГ имеет молекулярную массу в 3-4 раза меньшую, чем нефракционированный гепарин и 100% биодоступность, благодаря чему препараты этой группы дольше циркулируют в крови, обеспечивают продолжительный противотромботический эффект в значительно меньших суточных дозах. Изменение структуры молекулы гепарина, то есть уменьшение молекулярной массы почти в три раза, повлекло за собой изменения в фармакодинамике и фармакокинетике препарата. Одно из важнейших качественных отличий НМГ от НГ — способность существенно не удлинять такие показатели как АЧТВ и ТВ, что связано преимущественно с воздействием на фактор Ха (а не на антитромбин III) и ингибицией внешнего пути свертывания. Меньшая зависимость НМГ от активности антитромбина III позволяет применять препараты НМГ у больных с дефицитом этого фактора. НМГ не вызывают гипокоагуляции и практически не требуют лабораторного контроля при своем использовании. В последнее время активно изучается способность НМГ блокировать системный воспалительный ответ, который является основой таких состояний в акушерстве, как преэклампсия, сепсис, антифосфолипидный синдром, невынашивание беременности. При невынашивании беременности препараты НМГ используются очень широко.
— С чем это связано?
— Дело в том, что более чем в 50% случаев, по некоторым данным, причиной невынашивания беременности являются различные формы тромбофилий, среди которых доминирует антифосфолипидный синдром (АФС). Его роль в невынашивании и недонашивании беременности доказана, и этот очевидный факт уже широко известен в акушерском сообществе. Основным средством лечения являются препараты НМГ. Другие причины невынашивани: острые и хронические инфекционные заболевания, генетические факторы, эндокринная патология, аномалии развития половых органов — имеют меньший удельный вес (особенно при привычном невынашивании), чем тромбофилии.
— Есть ли противопоказания к применению низкомолекулярных гепаринов?
В России зарегистрированы несколько препаратов НМГ, применяемых в акушерстве: надропарин, эноксипарин, дельтапарин. Противопоказанием для их применения являются наследственные или приобретенные тромбоцитопении и/или тромбоцитопатии, дефекты плазменного звена гемостаза — болезнь Виллебранда, носительство гемофилии А или В, редкие геморрагические дефекты (дефицит фактора V, V и VIII, VII, X, XI, XIII, II). Заподозрить патологию гемостаза можно при анализе анамнеза женщины: кровотечения после родов/абортов меноррагии, носовые, десневые кровотечения, при операциях, в т.ч. минимальных (тонзилэктомия, экстракция зуба и др.). Противопоказаны НМГ при кровотечении любого происхождения, высоком артериальном давлении, патологии печени с коагулопатией. В акушерском и гинекологическом отделениях РКБ № 2 широко применяются препараты НМГ для лечения невынашивания беременности и другой патологии, связанной с риском тромботических осложнений.
— Какие исследования в этом направлении ведутся на кафедре?
— Сфера научных интересов кафедры связана с оптимизацией лечения привычного невынашивания беременности, преждевременных родов и плацентарной недостаточности. Нами было установлено, что АФС часто сочетается с хроническими воспалительными заболеваниями половых органов: хроническим эндометритом, цервицитом, кольпитом. Антифосфолипидные антитела поддерживают воспалительный процесс, усиливая аутоиммунный компонент воспаления и не всегда НМГ могут снизить уровень воспалительного ответа. Отсюда, по нашему мнению, неэффективность лечения невынашивания в ряде случаев при доказанном АФС. Включение в комплекс лечения натурального прогестерона и аспирина в небольших дозах, а также обоснованной терапии иммуноглобулинами для внутривенного введения достоверно снижает уровень провоспалительных цитокинов, продуктов деградации фибрина, повышая эффективность лечения. Кроме того, различные препараты обладают неодинаковой противовоспалительной активностью. Исследования продолжаются.
Таким образом, созданные в 1995 году НМГ оказались практически незаменимыми препаратами при определенной патологии в акушерстве и гинекологии. Альтернативные методы лечения АФС при невынашивании беременности в виде плазмафереза, больших доз имунноглобулина для внутривенного введения, аспирина значительно уступают НМГ как по эффективности, так и по безопасности. Вместе с тем врач должен четко представлять себе, что применение НМГ требует навыков и четких знаний.
Некоторые аспекты антитромботической терапии у беременных женщин
По материалам ESC Guidelines on the management of cardiovascular diseases during pregnancy 2011
Механические протезы клапанов сердца и антикоагулянтная терапия у беременных
Целью терапии является предотвращение тромбоза клапанов и их летальных последствий для матери и плода.
Пероральные антикоагулянты (ОАК) следует принимать до наступления беременности. НФГ или НМГ не рекомендованы к приему в течение всей беременности, поскольку такой режим терапии ассоциируется с высоким риском тромбоза протеза, а, кроме того, прием ОАК во втором и третьем триместрах беременности связан с низким риском для плода.
Поскольку ОАК значительно более эффективны в отношении профилактики тромбоза протеза клапана, в случае, если поддерживающая суточная доза варфарина Рекомендации по антитромботической терапии в случае имплантированного механического протеза клапана:
В целом, диагностические критерии ИМ сходны с таковыми у обычных пациентов, однако отрицательные зубцы Т могут появляться у беременных по другим причинам. Кроме того, повышение уровня тропонина I может иметь место как признак преэклампсии, а также в послеродовом периоде при серьезных геморрагических осложнениях с геморрагическим шоком.
В качестве медикаментозной терапии ИМ могут быть использованы бета-блокаторы и ацетилсалициловая кислота (АСК) в небольших дозах. ИАПФ, ингибиторы АРА 2 и антагонисты альдостерона противопоказаны. Четких данных в отношении тиенопиридинов нет. Клопидогрел может быть использован только в особых случаях (в частности, после стентирования) и настолько коротко, насколько это возможно. Учитывая отсутствие информации относительно ингибиторов GPIIb/IIIa, бивалирудина, прасугрела и тикагрелора, применение этих препаратов у беременных не рекомендуется.
Чрескожные коронарные вмешательства у женщин во время беременности
Если вмешательство абсолютно необходимо, оптимальным сроком его проведения является 4-й месяц беременности: к этому времени органогенез плода уже завершился, щитовидная железа плода еще не функционирует, а матка еще достаточно мала, чтобы обеспечивать максимальную дистанцию между ней и грудной клеткой.
Гепарин следует назначать в дозе 40-70 Ед/кг, целевой уровень активированного времени свертывания составляет 200 сек (не более 300 сек).
Рекомендации по ведению ОКС у беременных женщин
Кардиомиопатии и сердечная недостаточность.
Перипартальная кардиомиопатия (идиопатическая сердечная недостаточность (СН) со сниженной систолической функцией ЛЖ, развивающаяся в конце беременности или в первые месяцы по ее окончании. Это диагноз исключения.).
Пациентам показана стандартная терапия сердечной недостаточности (за исключением препаратов, влияющих на РААС, по причине их фетотоксичности).
Учитывая повышенную коагуляционную активность в течение беременности и сниженную ФВ, пациентам должна проводиться терапия ОАК или НМГ (в зависимости от периода беременности). Такая терапия показана при выявлении внутрисердечных тромбов, после эпизодов системной эмболии, а также у пациентов с МА и СН. В случае применения НМГ, должна контролироваться анти-Ха активность.
Антикоагулянтная терапия должна проводиться с осторожностью в непосредственный послеродовой период. Однако когда кровотечение остановлено у пациентов с очень низкой фракцией выброса (ФВ) левого желудочка, такая терапия обязательно должна проводиться по причине высокой частоты периферических эмболий у этих пациентов.
Лечение дилатационной кардиомиопатии проводится сходным образом.
Рекомендации по антикоагулянтной терапии при кардиомиопатиях и сердечной недостаточности у беременных женщин.
Трепетание и мерцание предсердий
Антикоагулянтная поддержка кардиоверсий проводится в соответствии со стандартной тактикой: если эпизод фибрилляции предсердий длится более 48 часов или длительность его неизвестна, варфарин (или НМГ/НФГ в I триместре) назначается по крайней мере на 3 недели до кардиоверсии и 4 недели после. В случае длительности пароксизма менее 48 часов во время кардиоверсии могут быть использованы НМГ или в/в НФГ.
Дальнейшая антикоагулянтная терапия после кардиоверсии назначается при наличии факторов риска тромбоэмболических осложнений (индексы CHADS2 или СНА2DS2VASC ≥2 баллов). В случае отсутствия структурной патологии сердца и других факторов риска тромбоэмболических осложнений (“lone atrial fibrillation”), антикоагулянтная терапия не показана, однако специально спланированных исследований у беременных на эту тему не было.
Выбор антикоагулянтного препарата зависит от срока беременности: ОАК назначаются со второго триместра беременности до одного месяца до предполагаемой даты родов, НМГ – в 1 триместре и за 1 месяц до родов. Новые антагонисты тромбина (такие как дабигатран) продемонстрировали фетотоксичность, поэтому их не следует использовать во время беременности. Монотерапия антитромбоцитарными препаратами или комбинированная терапия (клопидогрел + АСК) уступают варфарину в эффективности предотвращения тромбоэмболических осложнений.
Мерцательная аритмия, ассоциированная с клапанной патологией (нативные клапаны)
С данной патологией ассоциирован высокий риск тромбоэмболических осложнений (в частности, при тяжелом митральном стенозе). В случае выявления МА необходимо сразу назначить в/в нефракционированный гепарин (НФГ) с последующим переходом на низкомолекулярные гепарины в I и III триместрах беременности, во II триместре возможна терапия НМГ или пероральными антикоагулянтами. НМГ должны назначаться в дозе, подобранной на основании веса, с отменой за 36 часов до родов (индуцированных). В случае назначения пероральных антикоагулянтов, целевой диапазон МНО 2-2,5 (для безопасности плода).
Венозная тромбоэмболия во время беременности и послеродового периода.
Беременность и послеродовый период ассоциированы с повышенным риском венозной тромбоэмболии. ТЭЛА является одной из самых частых причин материнской смертности.
Факторы риска ВТЭ, связанной с беременностью
(Королевский Колледж Акушерства и Гинекологии):
Предсуществующие факторы риска
— повторные эпизоды ВТЭ в анамнезе
-эпизоды неспровоцированных или ассоциированных с приемом эстрогенов ВТЭ в анамнезе
-предшествующие спровоцированные эпизоды ВТЭ
-семейный анамнез ВТЭ
-известная тромбофилия (Лейденская мутация, полиморфизм гена протромбина G20210A, дефицит антитромбина III, протеинов С, S)
-сопутствующие заболевания, такие как заболевания сердца и легких, системная красная волчанка, рак, воспалительные заболевания, нефритический синдром, серповидноклеточная анемия, в/в введение препаратов)
-возраст старше 35 лет
-≥ 3 родов в анамнезе
-выраженная варикозная деформация вен
Акушерские факторы риска
-синдром гиперстимуляции яичников
-многоплодная беременность или использование репродуктивных технологий
-экстренное кесарево сечение
-плановое кесарево сечение
-наложение выходных или полостных акушерских щипцов
-длительные роды (более 24 часов)
-кровотечение в родах (кровопотеря более 1 л или гемотрансфузия)
Приходящие факторы риска
-сопутствующая системная нфекция
-хирургическое вмешательство во время беременности или в течение 6 недель после родов)
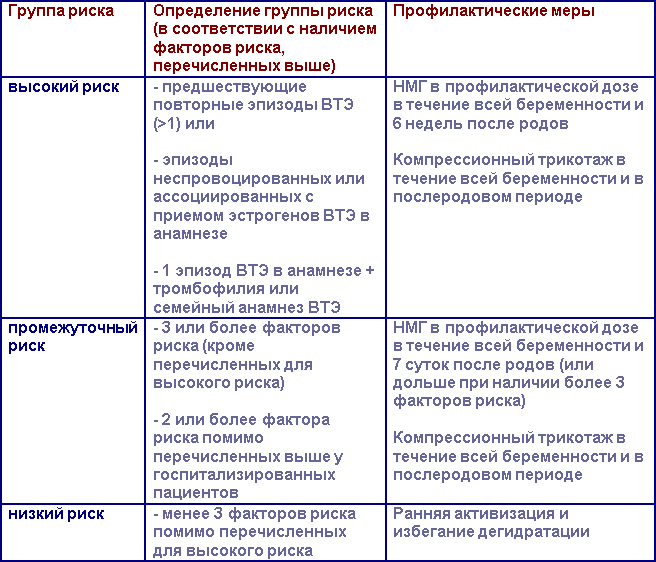
Наличие факторов риска ВТЭ должно быть оценено у всех женщин до беременности или на ранних сроках. В зависимости от типа и общего количества выявленных факторов риска выделяют 3 группы риска ВТЭ – высокий, промежуточный и низкий. Соответственно им проводят профилактические мероприятия.
Профилактика ВТЭ у беременных женщин
Препаратами выбора для профилактики и лечения ВТЭ у беременных женщин являются НМГ (они значительно реже, чем НФГ приводят к остеопорозу и, соответственно, реже вызывают переломы костей, а также реже развивается тромбоцитопения). Доза НМГ подбирается по массе тела. Нет четких рекомендаций относительно коррекции дозы у женщин с ожирением и в послеродовом периоде. Женщины с высоким риском ВТЭ (см. таблицу выше) должны получать эноксапарин 0,5 Ед/кг или дальтепарин 50 МЕ/кг дважды в день.
Лечение ВТЭ у беременных женщин
Стандартный диагностический алгоритм ВТЭ, отработанный на обычных пациентах, не вполне применим у беременных женщин, т.к. такие симптомы, как одышка и тахикардия свойственны беременным вообще, а уровень Д-димера повышается во время беременности пропорционально ее сроку.
НМГ являются препаратами выбора для лечения ВТЭ. Препарат должен назначаться и в случае предполагаемого диагноза ВТЭ до момента его исключения объективными методами.
Рекомендованная терапевтическая доза рассчитывается исходя из массы тела (эноксапарин 1 мг/кг дважды в день, дальтепарин 100 МЕ/кг дважды в день) с достижением максимальной анти-Ха активности через 4-6 часов после введения препарата 0,6-1,2 МЕ/мл.
В настоящее время неясно, необходимо ли регулярно мониторировать анти-Ха активность при лечении ВТЭ с помощью НМГ.
НФГ также не проникает через плаценту, но ассоциируется с большей частотой тромбоцитопении, остеопороза и необходимостью более частых инъекций при п/к введении. Его назначение оправдано у пациентов с почечной недостаточностью, при необходимости экстренной обратимой антикоагуляции с введением протамина, а также при лечении острой массивной ТЭЛА.
У пациентов с острой ТЭЛА с нестабильной гемодинамикой показано в/в назначение НФГ (нагрузочная доза 80 Ед/кг с последующей инфузией со скоростью 18 Ед/кг/час). АЧТВ должно контролироваться через 4-6 часов после начала терапии, изменения дозы НФГ, при стабильной скорости инфузии – по крайней мере, ежедневно. Целевой уровень АЧТВ – в 1,5-2,5 раза выше исходного (должно соответствовать уровню анти-Ха активности 0,3-0,7 МЕ/мл). После стабилизации состояния пациента и улучшения показателей гемодинамики НФГ может быть заменен на НМГ с последующей терапией в течение всей беременности. За 36 часов до индуцированных родов или кесарева сечения НМГ вновь заменяется на НФГ с его отменой за 4-6 часов до родов и возобновлением через 6 часов после родов при отсутствии геморрагических осложнений.
Ни НМГ, ни НФГ не обнаружены в грудном молоке и могут быть использованы во время грудного вскармливания.
Тромболитики относительно противопоказаны во время беременности и в послеродовом периоде за исключением пациентов высокого риска с гипотонией или шоком. Риск геморрагических осложнений (преимущественно гинекологических) составляет порядка 8%, гибели плода 6%, преждевременных родов 6%. В случае введения тромболитика нагрузочный болюс гепарина не вводится, проводится инфузия препарата со скоростью 18 Ед/кг/час. После стабилизации состояния пациента и улучшения показателей гемодинамики, НФГ может быть заменен на НМГ с последующей терапией в течение всей беременности.
Фондапаринокс. В одном из исследований применения фондапаринокса у беременных женщин было выявлено минорное проникновение этого препарата через плаценту, поэтому в настоящее время его применение во время беременности не рекомендуется.
Ривароксабан. Проникает через плацентарный барьер, поэтому не рекомендован к использованию у беременных.
Показания к имплантации кава-фильтров аналогичны таковым у обычных пациентов.
В послеродовом периоде после недавно перенесенной ТЭЛА терапия гепарином должна быть возобновлена через 6 часов после вагинальных родов и через 12 часов после кесарева сечения в случае отсутствия значимого кровотечения минимум на 5 суток с дальнейшим переходом на терапию ОАК. Антагонисты витамина К могут быть возобновлены со вторых суток после родов и продолжены в течение 3 месяцев или 6 месяцев в случае развития ТЭЛА на поздних сроках беременности. Целевой уровень МНО 2-3, контроль МНО предпочтительно осуществлять 1 раз в 1-2 недели. ОАК нее проникают в грудное молоко и безопасны для кормящих матерей.
Рекомендации по профилактике и лечению венозной тромбоэмболии во время беременности и в послеродовом периоде
1. Рутинный скрининг на наличие тромбофилий не рекомендован.
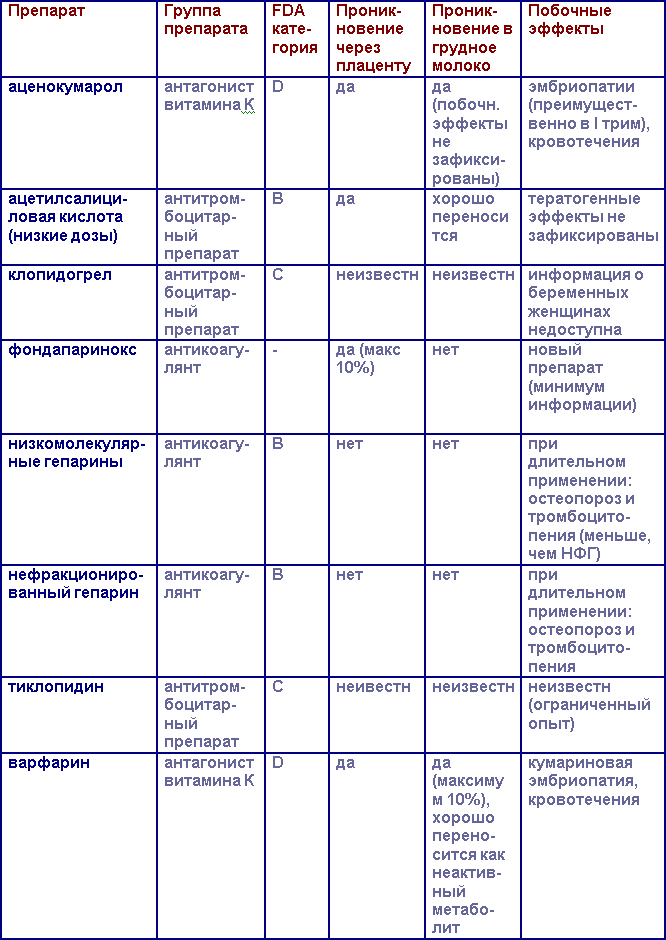
Антитромботические препараты в течение беременности
Все лекарственные препараты по степени безопасности разделены на 5 классов: от А (самые безопасные) до Х (высокая степень опасности, не использовать во время беременности и грудного вскармливания!).
Категория Б: исследования на животных не показали риска для плода, однако контролируемых исследований у беременных женщин не проводилось, либо исследования на животных моделях выявили побочные эффекты, которые не были подтверждены во время исследований у беременных женщин.
Категория С: во время исследований на животных были выявлены побочные эффекты, при этом исследований у беременных женщин не проводилось, либо недоступны исследования ни у животных, ни у людей. Лекарственный препарат должен назначаться только в том случае, если ожидаемая польза от лечения превышает потенциальный вред.
Категория D: есть данные о наличии риска для плода человека, но польза приема у беременной женщины приемлема несмотря на потенциальный риск (например, терапия жизнеугрожающих состояний).
Категория Х: есть данные о развитии фетопатий при исследованиях у животных и человека, риск использования этих лекарственных препаратов превышает потенциальную пользу. Эти препараты противопоказаны у беременных женщин и планирующих беременность.
По материалам: Task Force Members V. Regitz-Zagrosek, C Blomstrom Lundqvist, C Borghi. et al. ESC Guidelines on the management of cardiovascular diseases during pregnancy. European Heart Journal doi:10.1093/eurheartj/ehr218
| НАЦИОНАЛЬНОЕ ОБЩЕСТВО ПО АТЕРОТРОМБОЗУ WWW.NOAT.RU | |||
| 105082, Москва, а/я 8 | email: info@noat.ru | ||
| © 1997—2017 «НОАТ». Все права защищены. Создание сайта: Ай Ти Легион | |||
Уважаемый посетитель NOAT.RU!
Настоящий раздел предназначен исключительно для лиц, имеющих среднее и высшее медицинское образование, а также студентов медицинских ВУЗов.
Никакие из опубликованных материалов не могут служить заменой медицинскому осмотру и не должны быть использованы как руководство к лечению. Только врач, который имеет личный контакт с пациентом, знаком с его историей болезни и наблюдает за состоянием его здоровья, может рекомендовать тот или иной метод лечения. Информация на данном сайте или другие предоставляемые им услуги не могут служить основанием для диагностики или лечения без соответствующего участия врача.
Ни при каких обстоятельствах администрация, составители, консультанты и правообладатели сайта не могут быть ответственны за любой непрямой, случайный или косвенный вред, причиненный здоровью и жизни, а также материальный ущерб или утерю прибыли, наступившую в результате любого использования или доступа или невозможности использования или получения доступа к ресурсу NOAT.RU или его содержимому.
Администрация NOAT.RU не несет ответственности за содержание баннеров и информационных материалов третьих лиц.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом, фельдшером или студентом медицинского ВУЗа.
Обследование и ведение беременных пациенток с наследственной предрасположенностью к тромбофилическим осложнениям и тромбофилиями различного генеза
Тромбофилия не является заболеванием, ее стоит рассматривать скорее как патологическое состояние или синдром, возникающие под воздействием комбинации постоянных или временных факторов риска, вызывающих тромбозы [3].
Показанием к обследованию пациенток является возникновение идиопатических тромбозов, инсультов, инфарктов, наличие выкидышей, тяжелого гестоза, преждевременной отслойки нормально расположенной плаценты, преждевременных родов на сроках до 34 недель, синдрома задержки роста плода при предыдущих беременностях, тромбозов, возникших на фоне приема контрацептивных препаратов или заместительной гормональной терапии (ЗГТ) [2]. Показаниями к лабораторной диагностике тромбофилии у пациентки является наличие следующих общих признаков патологии:
первая манифестация тромбоза в возрасте 13–20–30 лет;
артериальные и венозные тромбозы (от тромбоза поверхностных вен до ТЭЛА);
тромбоз на фоне применения непрямых антикоа- гулянтов (варфарин – снижение витамина К);
у новорожденных: неонатальная коагулопатия, фульминантная пурпура как причина смерти. Сведения о патологических состояниях получают прежде всего из анамнеза.
КОМПЛЕКСНОЕ ОБСЛЕДОВАНИЕ
Таким образом, обследование беременной в I триместре при постановке на учет либо пациентки, планирующей беременность, начинают именно со сбора подробного анамнеза, который включает в себя семейный анамнез: семейный акушерский, семейный тромботический (в том числе сведения о заболеваниях матери и отца в трудоспособном возрасте, такие как гипертония (ГБ), ишемическая болезнь сердца (ИБС), острое нарушение мозгового кровообращения (ОНМК) и др. Также важны анамнез экстрагенитальных заболеваний пациентки, диагностированных до или во время беременности (ГБ, СД, СКВ и др.), и оценка репродуктивной функции пациентки.
При привычном невынашивании беременности рекомендуются дополнительные виды исследований, такие как Д-димер, растворимый фибрин-мономерный комплекс (РФМК), тромбоэластография, уровень ингибитора активатора плазминогена, исследование на антифосфолипидный синдром (АФС) с интервалом 6 недель:
IgM и IgG кардиолипину, фосфолипидам, гликопротеиду;
Высокоинформативным является анализ на полиморфизм генов тромбофилии. Причем приказом МЗ РФ № 572-Н предусмотрены исследования на определение уровня протромбина, протеинов С и S. Дополнительно к приказу рекомендуется назначить исследование на гомоцистеин.
Оценить вероятность предтромботического состояния и развития тромбоза, а также эффективность и безопасность терапии в тромбоцитарном звене позволит определение количества тромбоцитов (PLT). В норме PLT составляет 180 – 320 х 109 /л, при тромбоцитозе более 350 х 109 /л и тромбоцитопении менее 100 х 109 /л.
СРЕДНИЙ ОБЪЕМ ТРОМБОЦИТОВ (MPV) СОСТАВЛЯЕТ 3,6–9,4 МКМ. ОТ РАЗМЕРА ТРОМБОЦИТА ЗАВИСЯТ СОДЕРЖАНИЕ В НЕМ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ И ЕГО СКЛОННОСТЬ КЛЕТОК К АДГЕЗИИ. СЛЕДУЕТ ПОМНИТЬ, ЧТО ОБЪЕМ ТРОМБОЦИТОВ ИЗМЕНЯЕТСЯ ПЕРЕД АГРЕГАЦИЕЙ, И ЧЕМ БОЛЬШЕ ОБЪЕМ ТРОМБОЦИТОВ, ТЕМ ОНИ «МОЛОЖЕ» [1]. ПРЕОБЛАДАНИЕ В КРОВИ МОЛОДЫХ ФОРМ ТРОМБОЦИТОВ НАБЛЮДАЕТСЯ ПРИ КРОВОПОТЕРЕ И СВИДЕТЕЛЬСТВУЕТ ОБ УСИЛЕННОЙ РЕГЕНЕРАЦИИ. УВЕЛИЧЕНИЕ УРОВНЯ СТАРЫХ И УМЕНЬШЕНИЕ СОДЕРЖАНИЯ ЗРЕЛЫХ ТРОМБОЦИТОВ ХАРАКТЕРНЫ ДЛЯ РАЗЛИЧНЫХ ВОСПАЛИТЕЛЬНЫХ ПРОЦЕССОВ, ИНТОКСИКАЦИЙ, ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ.
ОЦЕНКА ФУНКЦИОНИРОВАНИЯ СИСТЕМЫ КОАГУЛЯЦИИ
Агрегация тромбоцитов. Для определения исходной функции тромбоцитов, эффективности антиагрегантной терапии назначается исследование спонтанной агрегации тромбоцитов или исследование с применением индукторов: аденозиндифосфатом (АДФ), адреналином, коллагеном ристоцетином.
ОПРЕДЕЛЕНИЕ ДЛИТЕЛЬНОСТИ КРОВОТЕЧЕНИЯ – ВАЖНЫЙ И ИНФОРМАТИВНЫЙ ТЕСТ, КОТОРЫЙ ПОЗВОЛЯЕТ ОДНОВРЕМЕННО КАЧЕСТВЕННО ОЦЕНИТЬ КОЛИЧЕСТВО ТРОМБОЦИТОВ В КРОВИ, ИХ АДГЕЗИВНЫЕ И АГРЕГАЦИОННЫЕ СВОЙСТВА, ФУНКЦИОНАЛЬНЫЕ ХАРАКТЕРИСТИКИ СТЕНКИ КРОВЕНОСНЫХ СОСУДОВ, А ТАКЖЕ ВЫРАЖЕННЫЙ ДЕФИЦИТ ПЛАЗМЕННЫХ ФАКТОРОВ СВЕРТЫВАНИЯ. В НОРМЕ ДЛИТЕЛЬНОСТЬ КРОВОТЕЧЕНИЯ СОСТАВЛЯЕТ 4–8 МИНУТ.
Агрегация тромбоцитов с АДФ показывает количество высвобождающихся собственных агонистов, содержащихся в гранулах тромбоцитов. Определение агрегации тромбоцитов с ристоцетином показано для диагностики болезни фон Виллебранда (увеличение времени кровотечения при нормальном количестве тромбоцитов и отсутствие явных причин для дисфункции тромбоцитов).
Удлинение времени кровотечения отражает на- рушение гемостаза вследствие тромбоцитопений, тромбоцитопатий врожденного и приобретенного генеза (нарушения функций тромбоцитов – адгезии и агрегации), нарушений сосудистой стенки или сочетания этих факторов. Время кровотечения мо- жет увеличиться при применении антиагрегантной терапии, синдроме диссеминированного внутрисосудистого свертывания (ДВС), синдроме «массивных» трансфузий. Увеличение длительности кровотечения при нормальном количестве тромбоцитов в крови позволяет предположить нарушение их функций.
Укорочение времени кровотечения характерно для гиперагрегации тромбоцитов.
Информативным для лечащего врача является также определение активированного частичного тромбопластинового времени (АЧТВ), которое при беременности в норме колеблется от 25 до 40 секунд. Удлинение АЧТВ свидетельствует о дефиците плазменных факторов коагуляции ниже 10–25 %, применении антикоагулянтов. Укорочение АЧТВ говорит о гиперкоагуляции, характерной для ДВС, а значит, необходимо решить вопрос о назначении антикоагулянтной терапии. При проведении терапии гепаринами осуществляется обязательный контроль АЧТВ: удлинение АЧТВ более чем в 2,5 раза от нормы перед очередным введением гепарина свидетельствует о высокой чувствительности к гепаринотерапии и требует снижения дозы.
ПРОТРОМБИНОВОЕ ВРЕМЯ (ПТВ) ПОЗВОЛЯЕТ ПРОИЗВЕСТИ ОЦЕНКУ ВНЕШНЕГО ПУТИ СВЕРТЫВАНИЯ КРОВИ 1 ФАЗЫ. В НОРМЕ ПТВ СОСТАВЛЯЕТ 12–16 СЕК. ЕГО УКОРОЧЕНИЕ ПОКАЗЫВАЕТ АКТИВАЦИЮ ВНЕШНЕГО ПУТИ КОАГУЛЯЦИОННОГО ГЕМОСТАЗА, А УДЛИНЕНИЕ – ДЕФИЦИТ, ЧТО ОЗНАЧАЕТ НЕОБХОДИМОСТЬ НАЗНАЧЕНИЯ ЛЕЧЕНИЯ ФАКТОРАМИ ПРОТРОМБИНОВОГО КОМПЛЕКСА (ПРОТРОМПЛЕКС, НОВОСЕВЕН И ДР).
Удлинение ПТВ наблюдается при заболеваниях печени и желчного пузыря, нарушениях эвакуации желчи, циркуляции ВА, дефиците или аномалии факторов протромбинового комплекса [5].
В процессе коагуляции важна концентрация фибриногена, которая в норме составляет 2–4 г/л. Ее повышение может наблюдаться в последние месяцы беременности, после родов и хирургических операций, в период воспалительных и неопластических заболеваний, при легких формах гепатитов, в I-й фазе ДВС.
СНИЖЕНИЕ КОНЦЕНТРАЦИИ ФИБРИНОГЕНА ХАРАКТЕРНО ДЛЯ ТЯЖЕЛЫХ ЗАБОЛЕВАНИЙ ПЕЧЕНИ, НАСЛЕДСТВЕННЫХ ГИПО-, АФИБРИНОГЕНЕМЙ, ПЕРВИЧНОГО ФИБРИНОЛИЗА, II И III СТАДИЙ ДВС, ПРИЧЕМ В ПОСЛЕДНЕМ СЛУЧАЕ ВАЖНЫ НЕ СТОЛЬКО ПОКАЗАТЕЛИ, СКОЛЬКО ДИНАМИКА, СКОРОСТЬ ИЗМЕНЕНИЯ КОНЦЕНТРАЦИИ.
При активации системы фибринолиза (взаимо- действие плазмина с фибриногеном и фибрином) образуются растворимые комплексы мономеров фибрина (РФМК), которые не должны превышать 10 мг/л. РФМК расценивается как ранний признак ДВС. О хроническом ДВС свидетельствует постоянная циркуляция мономерных комплексов в крови.
Исследование на Д-димеры используется для диагностики ДВС. При добавлении специфической сыворотки определяется количество Д-димеров, по которым судят о фибринолизе. Д-димер не повышается у пациентов с дефицитом тканевого активатора плазминогена или высокой активностью ингибитора активатора плазминогена часто даже при тромбозе глубоких вен (ТГВ) и тромбозе легочной артерии (ТЭЛА).
Информативно исследование на определение процента активности белка-антикоагулянта антитромбина III, нормальный показатель – 80–120 %. Любое изменение концентрации (как снижение, так и повышение) может указывать на наличие генетических мутаций в гене антитромбина III. Уменьшение характеризует заболевания печени, причем в этом случае снижение концентрации АТ III пропорционально тяжести заболевания. Кроме того, более низкие значения возможны при введении пациенту нефракционированного гепарина (НФГ), который при низкой концентрации АТ III не дает ожидаемого эффекта. Снижение концентрации также может наблюдаться при шоковых состояниях (например, при острой почечной недостаточности (ОПН) и активации ингибиторов АТ III в крови).
Следует помнить, что показатели содержания АТ III снижаются в середине менструального цикла, в послеоперационном периоде, при синдроме ДВС, приеме оральных контрацептивов, эстрогенов.
Повышение концентрации АТ III характерно для вирусного гепатита, холестаза, может наблюдаться при дефиците витамина К, приеме антикоагулянтов непрямого действия (например, варфарина) или во время менструации.
ЗАКЛЮЧЕНИЕ
Для получения точной информации о состоянии пациентки лабораторные методы исследований дополняются инструментальными: УЗИ, ЭКГ и УЗДГ сосудов нижних конечностей. В соответствии с приказом Министерства здравоохранения Российской федерации УЗИ рекомендуется проводить:
при постановке на учет;
на сроке 11–14 недель;
на сроке 18–21 неделя;
на сроке 30–34 недели;
планово с 33 недель КТГ;
Желательно получить информацию максимально рано, чтобы принять решение для назначения лечения: при пренатальном обследовании, обследовании в I триместре беременности, при возникновении осложнений во время настоящей беременности.
1. Агаркова Т. А., Трифонова Е. А., Габитова Н. А. Анализ генетических маркеров наследственной тромбофилии и эндотелиальной дисфункции при осложненном течении беременности. Всероссийский научный форум «Мать и дитя», 11-й. Материалы. М 2010; 6–7.
2.Баркаган З. С. Руководство по гематологии. М: Ньюдиамед, 2005; 3: 416.
4. Ройтберг Г. Е., Струтынский А. В. Лабораторная и инструментальная диагностика заболеваний внутренних органов – М.: ЗАО «Издательство БИНОМ», 1999 г. – 622 с.
6.Clark P., Brennand J., Conkie J. at al. Activated protein C sensitivity, protein C, protein S and coagulation in normal pregnancy // Thromb Haemost.. – 1998. – Вып. 79. – С. 1166–1170.