Для чего нужны оральные антикоагулянты?
Антикоагулянты — это лекарственные препараты, снижающие активность свертывающей системы крови и препятствующие чрезмерному образованию тромбов. Современные антикоагулянты оказывают влияние на различные звенья процесса коагуляции крови и применяются для профилактики и лечения артериальных или венозных тромбозов и тромбоэмболий.
Классификация антикоагулянтов
Все антикоагулянтные препараты разделяются на две большие группы:
Антикоагулянты непрямого действия
Витамин К — витамин естественного происхождения, содержащийся в основном в зеленых листовых овощах (шпинат, брокколи, латук) и попадающий в организм с пищей. Кроме того, витамин K синтезируется бактериями в кишечнике. Организм использует витамин К для образования в печени целого ряда белков, участвующих в свертывании крови. Суточная потребность витамина К: 0,03-1,5 мкг/кг/сут (до 105 мкг/сут).
Таблица 1. Содержание витамина К в продуктах (мкг/100 г продукта)
| Продукты | Содержание витамина К |
| Зеленый чай, листья | 964 |
| Салат-латук, зеленые листья | 850 |
| Мангольд, листья сырые | 830 |
| Капусты лист | 817 |
| Кочанная капуста, сырая | 487 |
| Брюссельская капуста | 434 |
| Шпинат, листья сырые | 383 |
| Шпинат, листья свежие/замороженные, сваренные | 360 |
| Черный чай, листья | 42 |
| Брюссельская капуста, свежая, замороженная | 289 |
| Цикорий сырой | 231 |
| Салат краснолистный | 210 |
| Брокколи сырая | 205 |
| Соевое масло | 193 |
| Брокколи свежая/замороженная, сваренная | 192 |
| Зеленый лук | 190 |
| Фасоль | 140 |
| Салат Айсберг | 123 |
Оральные антикоагулянты, вмешиваясь в этот процесс, существенно увеличивают время свертывания крови. Однако пероральные антикоагулянты не разжижают кровь и не растворяют уже образовавшиеся сгустки крови, хотя и позволяют прекратить рост имеющихся тромбов.
В норме естественные антикоагулянты крови способствуют тому, что ее свертывание происходит только при нарушении целостности кровеносных сосудов. Однако при определенных клинических состояниях, называемых тромбозными нарушениями, этот же механизм может приводить к нежелательному образованию опасных для жизни кровяных сгустков — тромбов. В таких ситуациях действие антикоагулянтов позволяет предотвратить избыточное тромбообразование.
Если у вас обнаружили тромб или существует опасность образования кровяных сгустков, в качестве одного из элементов лечения врач может назначить лечение антикоагулянтами (например, варфарином), которые предотвращают образование тромбов.
Классификация антикоагулянтов непрямого действия
Все антикоагулянты непрямого действия подразделяются на три основные группы:
Самым распространенным непрямым антикоагулянтом является варфарин, что связано с предсказуемостью его действия и стабильными показателями антикоагуляции.
Показания к назначению пероральных антикоагулянтов
Можно выделить следующие основные причины применения оральных антикоагулянтов:
Аспирин Кардио или варфарин?
Исходя из определенных критериев (возраста и дополнительных факторов риска), лечащий врач может назначить пациентам с мерцательной аритмией, один из двух вариантов антитромботических средств: антиагрегантные препараты, например, аспирин (препятствует склеиванию тромбоцитов) или антикоагулянтные препараты, например, варфарин (блокирует факторы свертывания крови):
Фармакологическое действие аспирина как антикоагулянта заключается в угнетении слипания тромбоцитов — основного компонента тромба, таким образом, ацетилсалициловая кислота, предупреждает развитие тромбоза кровеносных сосудов.
Показанием к применению аспирина для разжижения крови является наличие преходящего нарушения мозгового кровообращения в прошлом – т.е. такого нарушения, при котором неврологическая симптоматика проявлялась не более 24 часов.
Кроме того, в инструкции по применению Аспирин Кардио для разжижения крови отдельно указан значительный перечень противопоказаний. Так же в любой инструкции к аспирину упоминается о выраженных нежелательных эффектах, развивающихся при длительном применении аспирина для разжижения крови даже в низких дозировках. При длительном приёме ацетилсалициловой кислоты, входящей в состав Аспирин Кардио, возможно развитие эрозий и язв желудочно-кишечного тракта, тромбоцитопения (снижении числа тромбоцитов), повышение уровня печёночных ферментов.
У таблеток аспирина нет явных преимуществ и в отношении стоимости. Цена «аспирина для сердца» вполне сравнима со стоимостью лечения варфарином. Даже американский аспирин для разжижения крови – далеко не панацея.
В сравнении со случаями, когда никакое лечение не проводится, варфарин снижает опасность инсульта на 64 %, что почти в три раза больше, чем при приеме аспирина для разжижения крови (для получения дополнительной информации обратитесь к врачу, который сможет рекомендовать наиболее подходящий вам препарат).
Рисунок 1. Варфарин и риск инсульта
В некоторых случаях препараты непрямых антикоагулянтов нужно принимать несколько месяцев, иногда на протяжении всей жизни. Продолжительность курса определяет врач.
Прямые и непрямые антикоагулянты снижают свертываемость крови, следовательно, повышают риск кровотечения, поэтому соблюдение режима дозирования имеет жизненно важное значение. Ни в коем случае нельзя увеличивать дозировку или сокращать интервал приема антикоагулянтов.
Первостепенное значение также имеет контроль эффективности этих препаратов: анализ крови, который называется МНО (международное нормализованное отношение), помогает подобрать наиболее оптимальную дозировку оральных антикоагулянтов.
Антикоагулянты и их применение в медицине
Антикоагулянты – это противосвертывающие вещества, препятствующие образованию тромбов в кровотоке. Они поддерживают кровь в жидком состоянии и обеспечивают ее текучесть при целостности сосудов. Их разделяют на естественные антикоагулянты и синтетические. Первые вырабатываются в организме, вторые производятся искусственным путем и применяются в медицине в качестве лекарственных препаратов.
Естественные
Они могут быть физиологическими и патологическими. Физиологические антикоагулянты в норме присутствуют в плазме. Патологические появляются в крови при некоторых заболеваниях.
Физиологические антикоагулянты делятся на первичные и вторичные. Первичные синтезируются организмом самостоятельно и постоянно находятся в крови. Вторичные образуются при расщеплении факторов свертывания в ходе образования фибрина и его растворения.
Первичные естественные антикоагулянты
Их принято делить на группы:
При снижении в крови уровня первичных физиологических антикоагулянтов возникает риск развития тромбозов.
К этой группе веществ относятся:
Вторичные физиологические антикоагулянты
Как уже было сказано, они образуются в процессе свертывания крови и растворения фибриновых сгустков при расщеплении некоторых факторов свертывания, которые вследствие деградации утрачивают коагуляционные свойства и приобретают антикоагуляционные. К ним относятся:
Патологические антикоагулянты
При некоторых болезнях в крови могут образовываться и накапливаться специфические антитела, препятствующие свертыванию крови. Они могут вырабатываться против любых факторов свертывания, но чаще всего образуются ингибиторы VIII и IX факторов. При некоторых аутоиммунных заболеваниях в крови появляются патологические протеины, которые обладают антитромбиновым действием или подавляют факторы свертывания II, V, Xa.
Препараты антикоагулянты
Искусственные антикоагулянты, которых разработано большое количество, являются незаменимыми лекарственными средствами в современной медицине.
Показания к применению
Показаниями к приему пероральных антикоагулянтов являются:
Классификация антикоагулянтов
Медикаменты этой группы делятся на прямые и непрямые в зависимости от скорости и механизма действия, а также от продолжительности эффекта. Прямые непосредственно влияют на факторы свертывания крови и тормозят их активность. Непрямые действуют опосредованно: они замедляют синтез факторов в печени. Выпускаются в таблетках, в растворах для инъекций, в форме мази.
Прямые
Лекарства этой группы действуют на факторы свертывания напрямую, поэтому их называют препаратами быстрого действия. Они препятствуют образованию нитей фибрина, предотвращают формирование тромбов и прекращают рост уже имеющихся. Их делят на несколько групп:
Гепарин
Это самый известный и распространенный антикоагулянт прямого действия. Его вводят внутривенно, под кожу и внутримышечно, а также применяют в качестве местного средства в виде мази. К лекарствам гепаринового ряда относятся:
Гепарины местного действия отличаются незначительной проницаемостью в ткани и не слишком высокой эффективностью. Применяются для лечения варикоза ног, геморроя, синяков. Наиболее известны и часто применяются следующие средства с гепарином:
Гепарины для внутривенного и подкожного введения – большая группа медикаментов, которые подбираются индивидуально и в процессе лечения один другим не заменяются, поскольку равнозначными по действию не являются. Активность этих препаратов достигает своего максимума примерно через три часа, а действие продолжается в течение суток. Эти гепарины снижают активность тканевых и плазменных факторов, блокируют тромбин, препятствуют образованию фибриновых нитей, предотвращают слипание тромбоцитов.
Для лечения тромбоза глубоких вен, инфаркта, ТЭЛА, стенокардии обычно назначают Надропарин, Эноксапарин, Дельтапарин.
С целью профилактики тромбоэмболий и тромбозов назначают Гепарин и Ревипарин.
Гидроцитрат натрия
Этот антикоагулянт используется в лабораторной практике. Чтобы кровь не сворачивалась, его добавляют в пробирки. Его применяют при консервации крови и компонентов.
Непрямые
Они снижают выработку в печени некоторых факторов свертывания (VIII, IX, X, протромбина), замедляют образование белков S и C, блокируют выработку витамина К.
К непрямым антикоагулянтам относятся следующие препараты:
Варфарин нельзя пить при некоторых болезнях почек и печени, тромбоцитопении, при острых кровотечениях и склонности к кровотечениям, в период беременности, при лактазной недостаточности, врожденной нехватке протеинов C и S, ДВС-синдроме, если нарушена всасываемость галактозы и глюкозы.
Из побочных эффектов наблюдаются боли в животе, рвота, понос, тошнота, кровоточивость, мочекаменная болезнь, нефрит, аллопеция, аллергии. Может появиться сыпь на коже, зуд, экзема, васкулит.
Главный недостаток Варфарина – высокий риск развития кровотечений (желудочно-кишечных, носовых и других).
Пероральные антикоагулянты нового поколения (НОАК)
Современные антикоагулянты – незаменимые средства для лечения многих заболеваний, таких как инфаркты, тромбозы, аритмии, ишемия и многие другие. К сожалению, препараты, зарекомендовавшие себя как эффективные, имеют много побочных действий. Но разработки не прекращаются, и на фармацевтическом рынке периодически появляются новые оральные антикоагулянты. НОАК имеют как преимущества, так и недостатки. Ученые добиваются получения универсальных средств, которые можно принимать при разных заболеваниях. Ведутся разработки препаратов для детей, а также для пациентов, которым они на данный момент противопоказаны.
Новые антикоагулянты имеют следующие плюсы:
Есть у новых препаратов и недостатки:
Что касается непрямых антикоагулянтов, то кардинально отличающихся от Варфарина, Дикумарина, Синкумара пока не разработали.
Новые препараты Апиксабан, Ривароксабан, Дабигатран могут стать альтернативой при мерцательной аритмии. Их главное преимущество заключается в том, что во время их приема не требуется постоянно сдавать кровь, и они не взаимодействуют с другими лекарствами. В то же время эти препараты так же эффективны и могут предотвратить инсульт при аритмии. Что касается риска развития кровотечений, то он либо такой же, либо ниже.
Что нужно знать
Пациенты, которым назначены пероральные антикоагулянты, должны знать, что они имеют большое количество противопоказаний и побочных действий. При приеме этих лекарств нужно соблюдать режим питания и сдавать дополнительные анализы крови. Важно рассчитывать ежедневную дозу витамина К, поскольку антикоагулянты нарушают его метаболизм; регулярно контролировать такой лабораторный показатель, как МНО (или ПТИ). Больной должен знать первые симптомы внутреннего кровотечения, чтобы вовремя обратиться за помощью и поменять препарат.
Антиагреганты
Лекарства этой группы также способствуют разжижению крови и предотвращают образование тромбов, но механизм действия у них другой. Дезагреганты снижают свертываемость крови, благодаря способности тормозить слипание тромбоцитов. Их назначают для усиления действия антикоагулянтов. Кроме этого, они обладают спазмолитическим и сосудорасширяющим эффектом. Наиболее популярные антиагреганты:
К новому поколению лекарств относится препарат Брилинт с активным веществом тикагрелором. Он является обратимым антагонистом рецептора Р2У.
Природные средства для разжижения крови
Приверженцы лечения народными методами применяют для профилактики тромбозов травы с кроворазжижающим эффектом. Перечень таких растений достаточно длинный:
Прежде чем лечиться травами, желательно посоветоваться с врачом: не все растения могут быть полезны.
Заключение
Антикоагулянты – незаменимые препараты для лечения сердечно-сосудистых патологий. Самостоятельно принимать их нельзя. Они имеют много противопоказаний и побочных действий, а бесконтрольный прием этих лекарств может привести к кровотечениям, в том числе скрытым. Назначить их и определить дозировку должен врач, который способен учесть все особенности протекания болезни и возможные риски. Во время лечения нужен регулярный лабораторный контроль.
Важно не путать антикоагулянты и антиагреганты с тромболитическими средствами. Главное отличие в том, что первые не могут разрушить тромб, а лишь предотвращают или замедляют его развитие. Тромболитики – это препараты для внутрисосудистого введения, которые растворяют кровяные сгустки.
Антикоагулянты, действующие на процесс тромбообразования
Ч. 1 Тромбоэмболия легочной артерии и тромбоз глубоких вен — самые распространенные причины смертности и инвалидности при сердечно–сосудистых заболеваниях.
Преферанская Нина Германовна
Доцент кафедры фармакологии образовательного департамента Института фармации и трансляционной медицины Первого МГМУ им. И.М. Сеченова, к.фарм.н.
Единственным доказательным по эффективности методом профилактики тромбозов и тромбоэмболических осложнений является применение антикоагулянтов, изменяющих вязкость крови, способствующих разжижению и повышению текучести крови. Стандартная схема лечения рекомендует начинать использовать антикоагулянты сразу после диагностирования таких заболеваний. Применение антикоагулянтов с момента появления симптомов позволяет предотвратить формирование сгустка крови, его увеличение и закупоривание сосудов. Большинство антикоагулянтов оказывают влияние не на сам кровяной сгусток, а на активность свертывающей системы крови.
Низкомолекулярные гепарины для парентерального введения (селективные ингибиторы фактора Ха)
Низкомолекулярные гепарины состоят из фрагментов гепарина с молекулярной массой от 2000 до 10 000 (в среднем 4000–5000 Да), получают путем фракционирования, гидролиза или деполимеризации обычного нефракционированного гепарина. В отечественной практике используют следующие препараты низкомолекулярных (фракционированных) гепаринов:
Эти препараты неоднородны по своему составу, т.к. содержат разные фракции гепарина и отличаются друг от друга антикоагулянтной активностью, физико-химическими и фармакокинетическими свойствами, но обладают антикоагулянтным и антитромботическим действием. Антикоагулянтный эффект продолжительный и зависит от действующего вещества (от 6 до 18 час.). При выборе антикоагулянта не учитывается возраст больных, тяжесть сопутствующих заболеваний, уровень тромбоза и степень нарушения внутрисердечной гемодинамики.
Низкомолекулярные гепарины блокируют процесс свертывания крови, угнетая в большей степени преимущественно активность фактора Ха, некоторые из них незначительно оказывают влияние на снижение образования протромбиназы (активатора протромбина) и активность фактора IIа. Протромбиназа (prothrombinase complex) — сложный комплекс, состоящий из активированных факторов свертывания Ха и Vа и др. факторов, который формируется на поверхности мембран тромбоцитов в присутствии ионов кальция. В процессе свертывания крови образуется как тканевая, так и кровяная протромбиназа. При применении антикоагулянтов количество образовавшейся протромбиназы очень мало, оно недостаточно для перевода протромбина в тромбин.
Прямые антикоагулянты катализируют образование комплекса с антитромбином III, тромбином и др. активированными факторами. Образуется тройной комплекс с антитромбином III, они необратимо изменяют его конфигурацию и сокращают период его полужизни до 3–6 часов. Связывание с антитромбином III усиливает угнетающее действие на активность фактора Ха, тем самым снижается переход протромбина в тромбин. В результате нейтрализации происходит ингибирование тромбина и формирование тромбов. В отличие от гепарина низкомолекулярные гепарины не связываются с фактором фон Виллебранда, легко инактивируются на поверхности тромбоцитов, что снижает риск геморрагических осложнений, реже развивается тромбоцитопения и остеопороз.
Низкомолекулярные гепарины, так же, как и гепарин, действуют на факторы свертывания через антитромбин III, но отличаются от гепарина следующими свойствами:
Низкомолекулярные гепарины способны блокировать каскад коагуляции на более ранних его этапах, обладают быстрым, выраженным, стабильным и более предсказуемым антикоагулянтным эффектом. Они имеют меньшее сродство к фактору 4 тромбоцитов и поэтому реже, чем стандартный гепарин, вызывают побочные эффекты. Фактор 4 тромбоцитов — антигепариновый, обладает выраженной антигепариновой активностью, устраняет эффект гепарина, его влияние на образование протромбиназы и на увеличение проницаемости сосудов. Антигепариновой активностью обладают также разрушенные и интактные тромбоциты, что связано со способностью тромбоцитов адсорбировать гепарин и его фрагменты и выделять фактор 4 тромбоцитов в плазму крови.
Применяют низкомолекулярные гепарины в основном для профилактики и лечения тромбоза глубоких вен (после хирургического вмешательства), для предупреждения тромбоэмболии легочной артерии. Низкомолекулярные гепарины показаны при нестабильной стенокардии, остром ишемическом инсульте и инфаркте миокарда, для профилактики и терапии тромбозов в акушерско–гинекологической практике, колоректальной и ортопедической хирургии. Их используют для профилактики свертывания крови в системе экстракорпорального кровообращения при длительном проведении гемодиализа или гемофильтрации.
Важно! При применении низкомолекулярных гепаринов могут возникать кровотечения. В первые дни лечения возможна умеренная тромбоцитопения. Низкомолекулярные гепарины в ряде случаев повышают активность печеночных ферментов, могут вызвать аллергические реакции и при длительном применении возникает опасность развития остеопороза. При передозировке протамин сульфат полностью не устраняет эффекты низкомолекулярных гепаринов (≤ 60%). Противопоказанием к их применению является повышенная чувствительность к тому или иному препарату, тяжелая почечная дисфункция, внутричерепное кровоизлияние, беременность, кормление грудью и др.
Формы выпуска низкомолекулярных гепаринов – специальные шприцы-дозаторы разового использования (в блистере по 2 шприца одноразового применения, упак. — 10 шт.).
Доза действующего вещества выражается в международных единицах (МЕ) с активностью подавления фактора Ха в плазме крови и выпускается в виде раствора для инъекций в мл.
Выпускается в растворе для п/к и в/в введения 2,5 м/0,5 мл. 0,5 мл помещают в специальный шприц с иглой вместимостью 1 мл, снабженный автоматической системой безопасности. После подкожной инокуляции Фондапаринукс полностью всасывается из места инъекции, выводится почками в течение 3 суток.
Важно! Применяют с осторожностью при повышенном риске развития кровотечений и гиперчувствительности к препарату. Препарат не рекомендуется смешивать с другими медикаментами.
ПРЯМЫЕ НИЗКОМОЛЕКУЛЯРНЫЕ АНТИКОАГУЛЯНТЫ ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ
К пероральным антикоагулянтам, прямым ингибиторам фактора свертывания крови Ха (активированного фактора Стюарта–Прауэра) относят Апиксабан (Эликвис), Ривароксабан (Ксарелто).
Апиксабан (Эликвис, тб., покр. обол., 2,5 мг и 5 мг) является мощным прямым ингибитором фактора свертывания крови Xa. Он избирательно и обратимо блокирует активный центр фермента, угнетает активность протромбиназы. Для реализации его антитромботического действия не требуется наличия антитромбина III. В результате ингибирования фактора свертывания крови Xa изменяются значения показателей системы свертывания крови: удлиняется активированное тромбопластиновое время и протромбиновое время. Препарат опосредованно влияет на агрегацию тромбоцитов, оказывая антиагрегантный эффект. Апиксабан быстро всасывается из желудочно–кишечного тракта. Абсолютная биодоступность при приеме 10 мг достигает 50%, максимальная концентрация достигается в течение 3 час. после приема внутрь. Период полувыведения (Т½) составляет около 12 час. Прием пищи не оказывает влияния на фармакокинетические показатели. С белками плазмы крови связывается на 87%. Основным путем выведения является кишечник.
Важно! При временном перерыве в терапии Апиксабаном (преднамеренном или случайном) возрастает риск тромбоза. Пациентов следует проинструктировать о необходимости избегать таких перерывов. При временной остановке антикоагуляционного лечения по любым причинам оно должно быть возобновлено как можно скорее.
Не рекомендуется применять у пациентов с заболеванием печени и с повышенным риском кровотечений, во время беременности и в период грудного вскармливания.
Ривароксабан (Ксарелто, тб., покр. обол., 2,5 мг, 10 мг, 15 мг, 20 мг) — высокоселективный дозозависимый прямой ингибитор фактора Ха. Активация фактора X с образованием фактора Ха через внутренний и внешний пути свертывания играет центральную роль в коагуляционном каскаде. Высокая биодоступность (80–100%) наблюдается при приеме в дозе 10 мг, которая не зависит от приема пищи. При приеме натощак 20 мг препарата биодоступность составляла всего F=66%. Максимальная концентрация достигается через 2–4 час. после приема. Большая часть Ривароксабана (92–95%) связывается с белками плазмы крови.
Ривароксабан, 2,5 мг, применяют с целью профилактики смертности вследствие сердечно–сосудистых осложнений, инфаркта миокарда у пациентов после острого коронарного синдрома; 10 мг — в профилактике венозной тромбоэмболии у пациентов, которым проводят обширные ортопедические хирургические вмешательства на нижних конечностях, 15 и 20 мг – для лечения тромбоза глубоких вен и тромбоэмболии легочной артерии, а также с целью профилактики их рецидивов и для профилактики системной тромбоэмболии и инсульта у пациентов с фибрилляцией предсердий неклапанного происхождения.
Важно! Не рекомендуется применять препарат во время беременности, в период грудного вскармливания, детям и подросткам до 18 лет, при наличии болезней почек, при наличии злокачественных новообразований и гиперчувствительности у пациентов.
НОАК (новые оральные антикоагулянты)
До недавнего времени варфарин был практически безальтернативным вариантом для длительной противотромботической терапии пациентов с неклапанной фибрилляцией предсердий, системной эмболией и/или тромбоэмболией легочной артерии (ТЭЛА), а также другими заболеваниями, которые подразумевают постоянное применение антикоагулянтов. Основной задачей при лечении таких больных с использованием варфарина и/или прямых антикоагулянтов (НФГ, НМГ, синтетические пентасахариды) является поиск золотой середины между высокой эффективностью данных препаратов и их безопасностью. Ведущей проблемой при лечении варфарином является сложность и одновременно жесткая необходимость поддержания МНО в пределах «терапевтического окна» в течение не менее 65–70 % времени лечения. Данная проблема легко решается путем самоконтроля его уровня при помощи специальных «домашних» коагулометров типа CoaguChek, но, как мы все понимаем, это не всегда возможно по самым разным причинам. Помимо этого, варфарин имеет очень сложные взаимоотношения с разными группами лекарственных средств и пищевыми продуктами, а также отличается изменчивостью метаболизма и фармакогенетическими особенностями. Все это сподвигло фармацевтический мир к созданию альтернативы варфарину. Так и были созданы новые оральные антикоагулянты (НОАКи), которые составили конкуренцию стандартной терапии варфарином.
Основные преимущества НОАК перед варфарином:
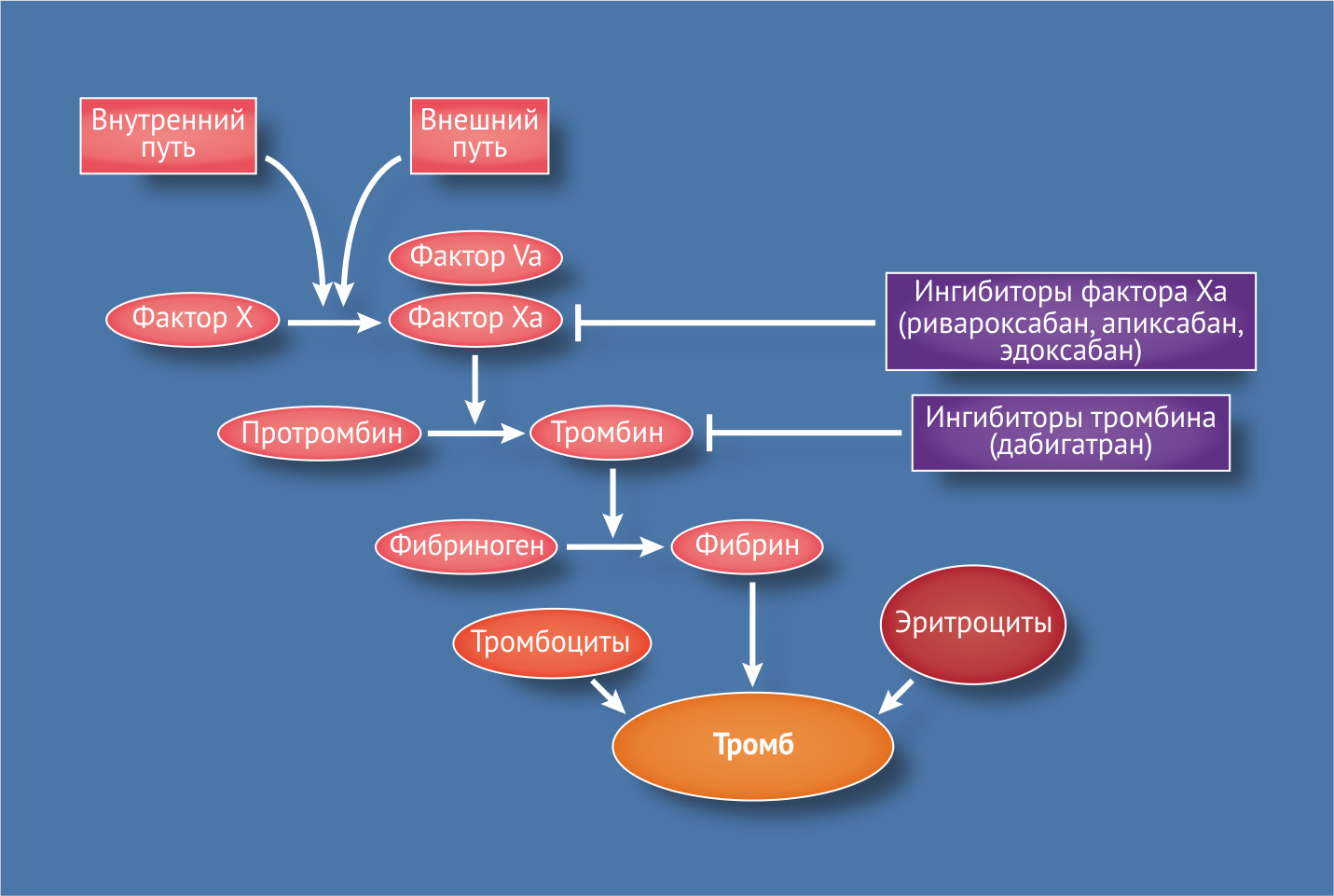
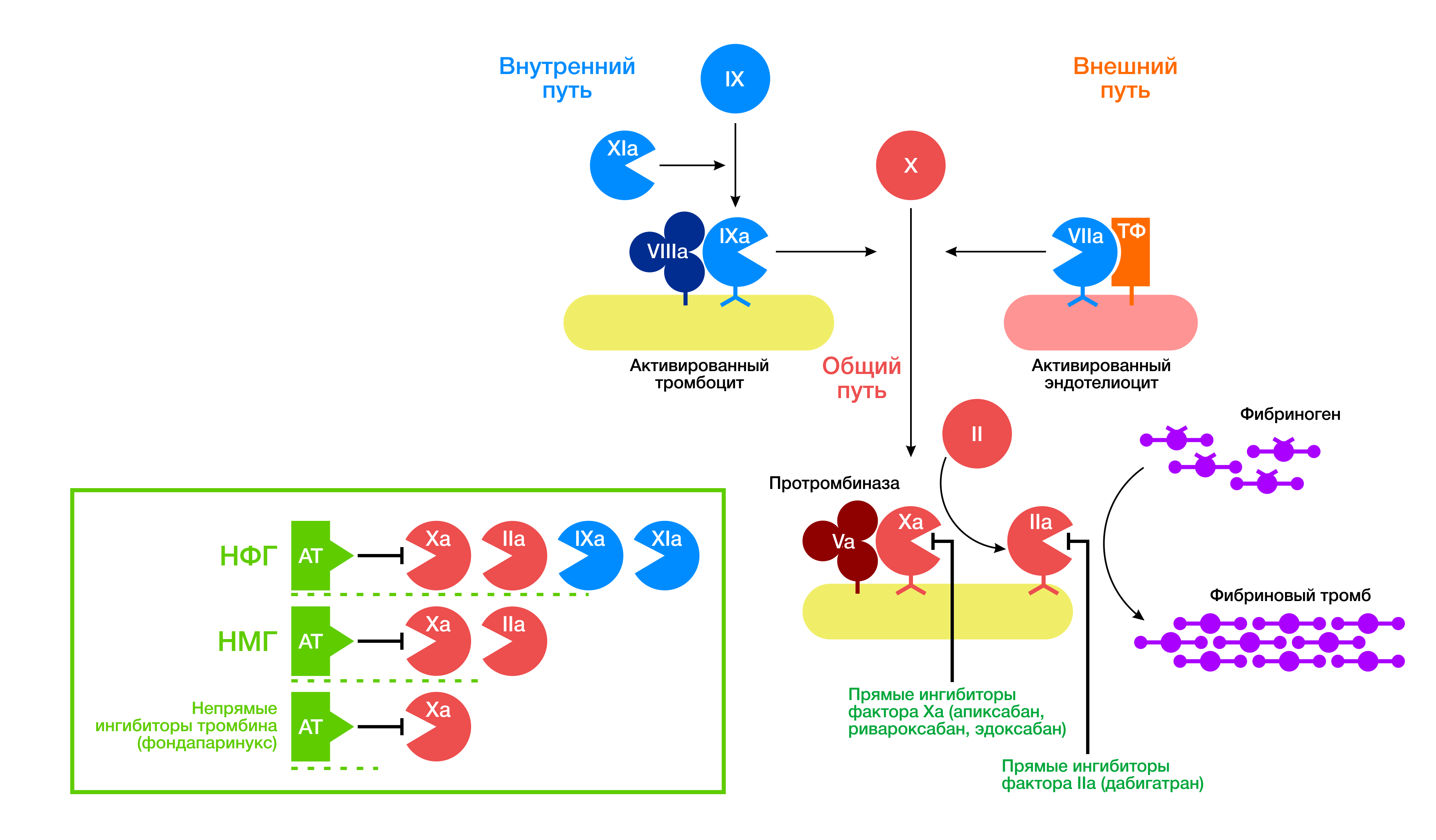
Все НОАК можно разделить на 2 группы: прямые ингибиторы тромбина (дабигатран) и прямые ингибиторы фактора Xa (ривароксабан, апиксабан, эдоксабан).
Дабигатран
Дабигатран (лекарственный препарат — дабигатрана этексилат, «Прадакса») — первый НОАК, который в 2010 году был одобрен FDA после 50-летнего затишья на рынке антикоагулянтов. Целью создания дабигатрана, как и всех НОАК, был поиск альтернативы традиционной антикоагулянтной терапии (НФГ/НМГ + варфарин) для профилактики инсульта и системных эмболий у больных неклапанной фибрилляцией предсердий, а также лечения и профилактики венозной тромбоэмболии (ВТЭ) у хирургических больных (FDA дало разрешение на это только в 2014 году).
Механизм действия
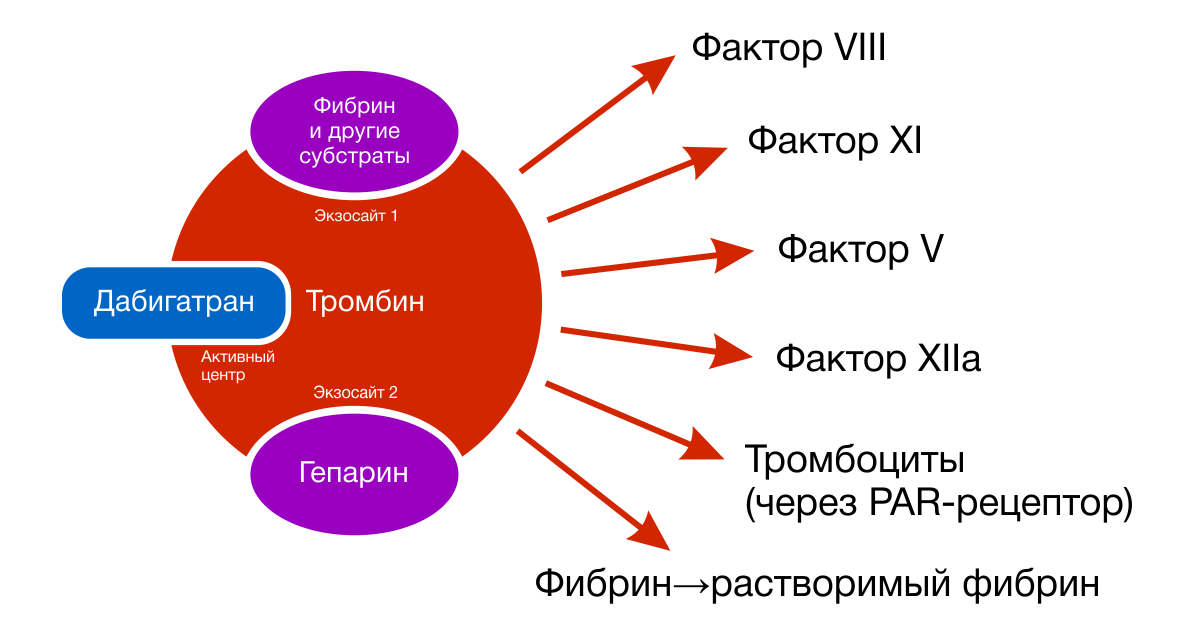
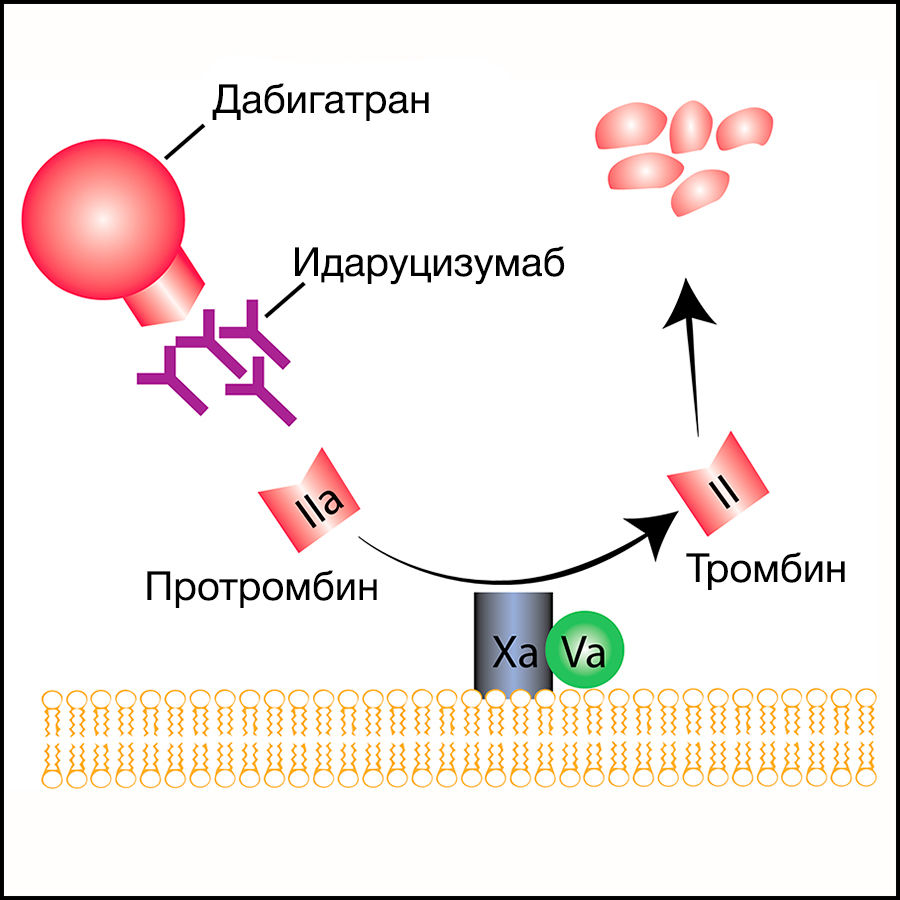
Дабигатран конкурентно связывается с активным центром тромбина, таким образом предотвращая превращение растворимого фибриногена в нерастворимый фибрин (рис. 1, 2). Препарат оказывает ингибирующее воздействие как на свободный тромбин, так и на тромбин, связанный с фибриновым сгустком, а также на вызванную тромбином агрегацию тромбоцитов.
Рисунок 1 | Точки приложения НОАК
Рисунок 2 | Дабигатран конкурентно связывается с активным центром тромбина, таким образом предотвращая превращение растворимого фибриногена в нерастворимый фибрин
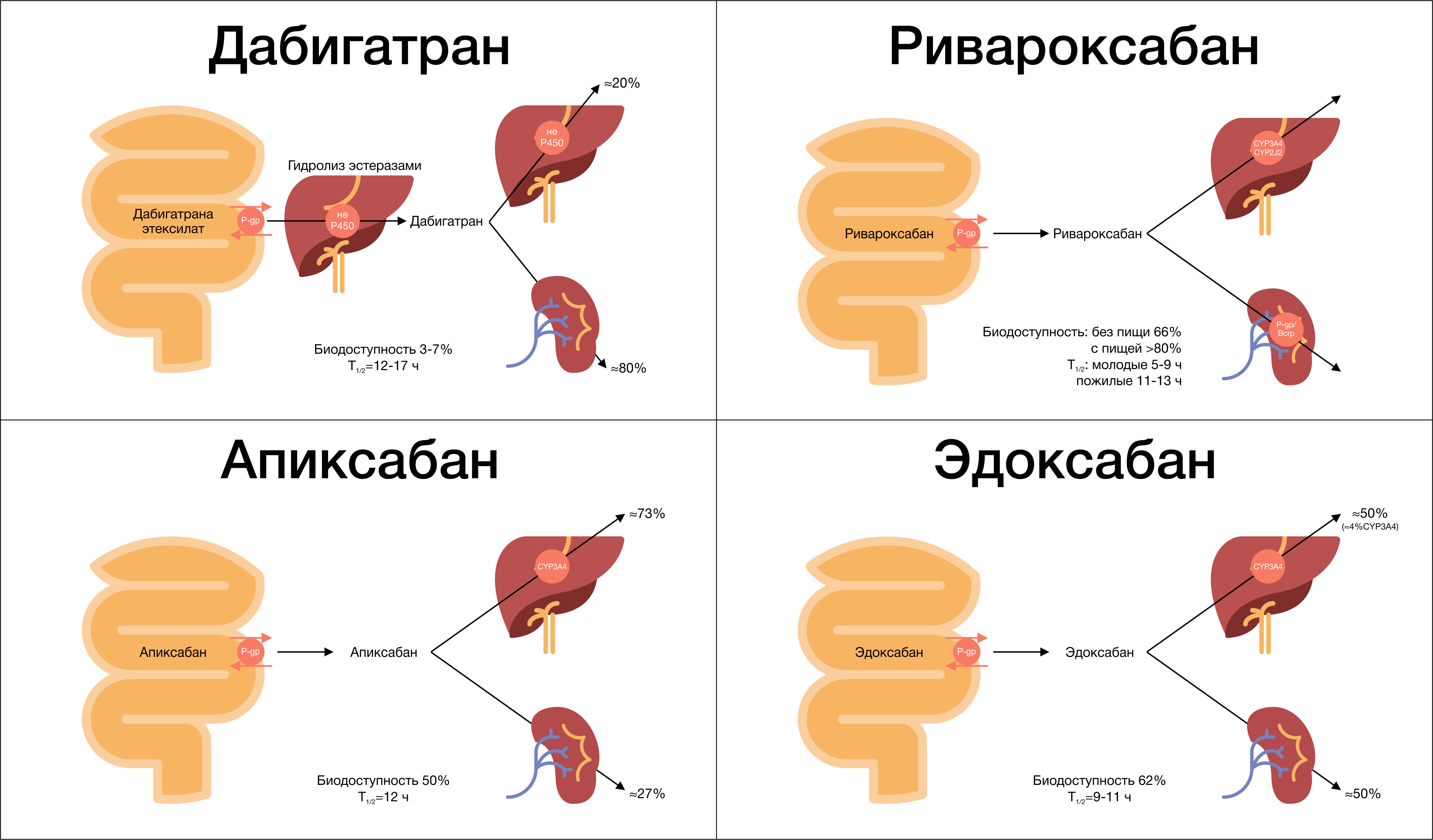
Фармакокинетика
Биодоступность дабигатрана после приема внутрь составляет всего 3–7 %. Отмечается быстрое дозозависимое повышение концентрации в плазме крови (максимальная концентрация наблюдается через 30–120 минут). Прием пищи не влияет на биодоступность дабигатрана, однако время достижения Cmax возрастает в среднем до 4 часов. Стоит упомянуть, что биодоступность может увеличиваться в 1,5–2 раза при нарушении целостности капсульной оболочки, что требует, в свою очередь, бережного хранения и использования препарата. Из всех НОАК только дабигатрана этексилат является пролекарством. После приема внутрь он быстро всасывается из ЖКТ и под влиянием эстераз печени гидролизуется в активную форму — дабигатран, при этом образуются 4 изомера активных ацилглюкуронидов, которые составляют не более 10 % от общего содержания дабигатрана в плазме крови.
По сравнению с варфарином, который взаимодействует с многочисленными классами лекарств, использование дабигатрана имеет значительно меньший риск лекарственного взаимодействия. Поскольку для его метаболизма не требуются ферменты системы цитохрома Р450, не ожидается никаких фармакокинетических взаимодействий с метаболизирующимися с их помощью лекарственными средствами. Одновременно с этим только дабигатрана этексилат (не дабигатран) является субстратом с умеренным сродством к P-гликопротеину, в связи с чем могут возникать нежелательные перекрестные реакции при его одновременном использовании с ингибиторами Р-гликопротеина (повышение плазменной концентрации дабигатрана).
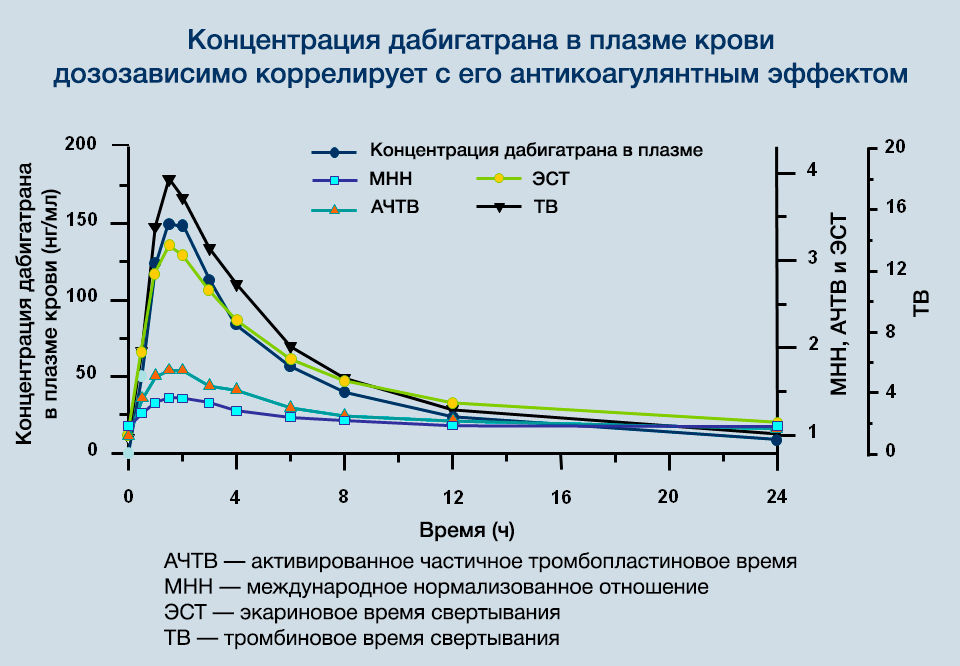
После достижения Cmax плазменные концентрации дабигатрана снижаются биэкспоненциально, что приводит к их уменьшению более чем на 70 % в течение 4–6 часов после приема внутрь (рис. 3). Период полувыведения в среднем составляет около 10 часов (может увеличиваться до 15–18 часов при нарушенной функции почек) и не зависит от дозы. Дабигатран обладает низкой способностью связывания с белками крови (34–35 %), и она не зависит от концентрации препарата. До 85 % выводится почками, и только 5 % препарата удаляется из организма через ЖКТ.
Рисунок 3 | Особенности фармакокинетики дабигатрана (после достижения Cmax плазменные концентрации дабигатрана снижаются биэкспоненциально, что приводит к их уменьшению более чем на 70 % в течение 4–6 часов после приема внутрь)
Показания и режим дозирования
Профилактика инсульта, системных тромбоэмболий и снижение сердечно-сосудистой смертности у пациентов с фибрилляцией предсердий
Данное показание к назначению было выявлено в крупном исследовании RE-LY (в сравнении с варфарином), которое было опубликовано еще в 2009 году. Так, по его результатам были одобрены 2 дозировки — 110 и 150 мг с кратностью приема 1 раз в 12 часов. Дозировка 150 мг была одобрена как FDA, так и EMA, в отличие от дозировки в 110 мг, которая не получила одобрение от FDA. Однако в 2011 году после введения дабигатрана в рутинную практику были получены данные о 900 случаев развития побочных эффектов, в связи с чем были внесены корректировки, направленные на увеличение безопасности применения данного препарата.
В итоге дабигатран в дозировке 150 мг оказался эффективнее варфарина в отношении профилактики инсульта и системных эмболий, но по развитию побочных эффектов находился на одном с варфарином уровне (сопоставимая частота развития жизнеугрожающих и экстракраниальных кровотечений). Дозировка в 110 мг оказалась более безопасной в отношении развития больших кровотечений, чем варфарин, и была рекомендована пациентам старше 80 лет и пациентам с высоким риском кровотечений (HAS-BLED > 3). При почечной недостаточности (но при СКФ не ниже 15–30 мл/мин) или при условии одновременного использования дабигатрана с ингибитором Р-гликопротеина требуется снижение дозировки дабигатрана до 75 мг 2 раза в сутки.
В плане побочных эффектов основные жалобы пациентов были связаны с ЖКТ (обычно беспокоили диспепсия и гастритоподобные симптомы). Также для дозировки в 150 мг была выявлена бо́льшая частота развития желудочно-кишечных кровотечений (ЖКК) в сравнении с варфарином. На данный момент производителем дабигатрана проводится исследование GLORIA-AF, целью которого является подтверждение роли дабигатрана, а также варфарина и ривароксабана в профилактике ТЭ у пациентов с фибрилляцией предсердий.
В августе 2017 года были опубликованы результаты исследования RE-DUAL PCI, в котором изучалась возможность использования дабигатрана в комбинации с одним из блокаторов P2Y12 — рецепторов в качестве средства профилактики тромбоза у больных с ФП, перенесших стентирование коронарных артерий. Сравнение проводилось со стандартной тройной антитромботической терапией: АСК + ингибитор P2Y12 + варфарин. В итоге было доказано, что в лечении пациентов, нуждающихся в одновременном назначении антикоагулянта и антиагрегантов, двойная терапия, включающая дабигатран и ингибитор P2Y12 — рецепторов, достоверно снижает риск кровотечений в сравнении с тройной антитромботической терапией (ТАТ). Эффективность применения дабигатрана в комбинации с ингибитором P2Y12 — рецепторов не уступала ТАТ в плане предотвращения ТЭ, летальных исходов или незапланированной реваскуляризации коронарных артерий. При этом наличие фиксированных дозировок (110 и 150 мг) дает возможность врачу проводить эффективную профилактику тромбоэмболических и атеротромботических событий у пациентов с ФП и высоким риском развития ишемического инсульта.
Профилактика ВТЭ у пациентов после протезирования тазобедренного и/или коленного сустава
Для определения эффективности применения дабигатрана с целью предотвращения венозных тромбозов после эндопротезирования коленного и тазобедренного сустава были проведены несколько исследований (RE-NOVATE и RE-NOVATE II, RE-MODEL, RE-MOBILIZE). Препаратом сравнения был выбран эноксапарин натрия в дозировке 40 мг 1 раз в сутки, начиная с вечера перед операцией. По итогам дабигатран и эноксапарин сопоставимы по эффективности и безопасности при использовании в целях профилактики ВТЭ у ортопедических пациентов. Побочные эффекты также в основном были связаны с ЖКТ (развитие диспепсии и ЖКК сопоставимо с эноксапарином). После достижения гемостаза при СКФ > 30 мл/мин рекомендуется однократное использование дабигатрана в дозе 110 мг в течение 1–4 часов после операции, затем рекомендованная доза составляет 220 мг однократно в сутки (2 капсулы по 110 мг) в течение 28–35 дней. Пациенты с умеренным нарушением функции почек имеют повышенный риск развития кровотечения, поэтому рекомендованная доза для этой группы составляет 150 мг однократно в сутки (2 капсулы по 75 мг).
Лечение острого и рецидивирующего тромбоза глубоких вен (ТГВ) и/или ТЭЛА и профилактика смертельных исходов, вызываемых этими заболеваниями
Данные об эффективности дабигатрана по этим показаниям были подтверждены результатами 4 клинических исследований — RE-COVER, RE-COVER II, RE-MEDY и RE-SONATE. В первых двух исследованиях сравнили эффективность и безопасность дабигатрана и варфарина у больных с острым эпизодом ТГВ, а в REMEDY и RE-SONATE оценили безопасность использования дабигатрана у больных с венозными тромбоэмболическими осложнениями (ВТЭО) в качестве средства профилактики рецидива ТГВ и/или ТЭЛА. При этом в RE-MEDY дабигатран сравнили с варфарином, а в RE-SONATE — с плацебо. По итогам RE-COVER, RE-COVER II и RE-MEDY эффективность дабигатрана (150 мг 2 раза в день) в отношении предупреждения рецидивирующих эпизодов ВТЭО была на уровне варфарина, а в отношении риска развития больших кровотечений дабигатран оказался более безопасным. В исследовании RE-SONATE по сравнению с плацебо дабигатран снижал риск рецидива ВТЭО больше чем на 90%, но увеличивал при этом риск больших или клинически значимых малых кровотечений почти в 3 раза.
Побочные эффекты
Главным побочным эффектом, связанным с использованием дабигатрана, считается желудочно-кишечное кровотечение. Если сравнивать риск развития массивных или клинически значимых малых кровотечений, то такой риск либо ниже, либо сравним с таковым у варфарина. Также частыми жалобами со стороны пациентов являются боль и чувство дискомфорта в эпигастрии или других областях живота (гастритоподобная симптоматика). Ну и конечно стоит упомянуть о реакциях гиперчувствительности, включая крапивницу, сыпь и зуд, а также анафилактический шок.
Контроль применения
Предсказуемый фармакокинетический профиль дабигатрана определяется наличием фиксированной дозы (110 или 150 мг), что обуславливает отсутствие необходимости рутинного контроля его антикоагулянтного эффекта. Однако в конкретных клинических ситуациях, таких как экстренное хирургическое вмешательство в связи с жизнеугрожающим состоянием, жизнеугрожающее кровотечение, почечная недостаточность или передозировка, реальный «антикоагулянтный статус» дабигатрана имеет важное значение и может быть оценен путем выявления специфических показателей коагулограммы, таких как экариновое время свертывания (ЭСТ), разбавленное тромбиновое время (dTT), или с помощью проведения эхитоксового теста (тест с ядом эфы).
Помимо этого, отмечается удлинение АЧТВ (до 65 сек) через 2–4 часа после приема дабигатрана. При необходимости проведения экстренной операции у больных на дабигатране показатель АЧТВ > 80 секунд свидетельствует о продолжающемся антикоагулянтном эффекте. dTT очень чувствителен к дабигатрану, и нормальное TT (14–19 секунд) исключает наличие высоких концентраций дабигатрана в крови, однако он не подходит для контроля или корректировки дозы. При увеличении концентрации в плазме крови более 500–600 нг/мл ни dTT, ни АЧТВ не являются чувствительными показателями в отношении передозировки дабигатраном.
Антидотная терапия
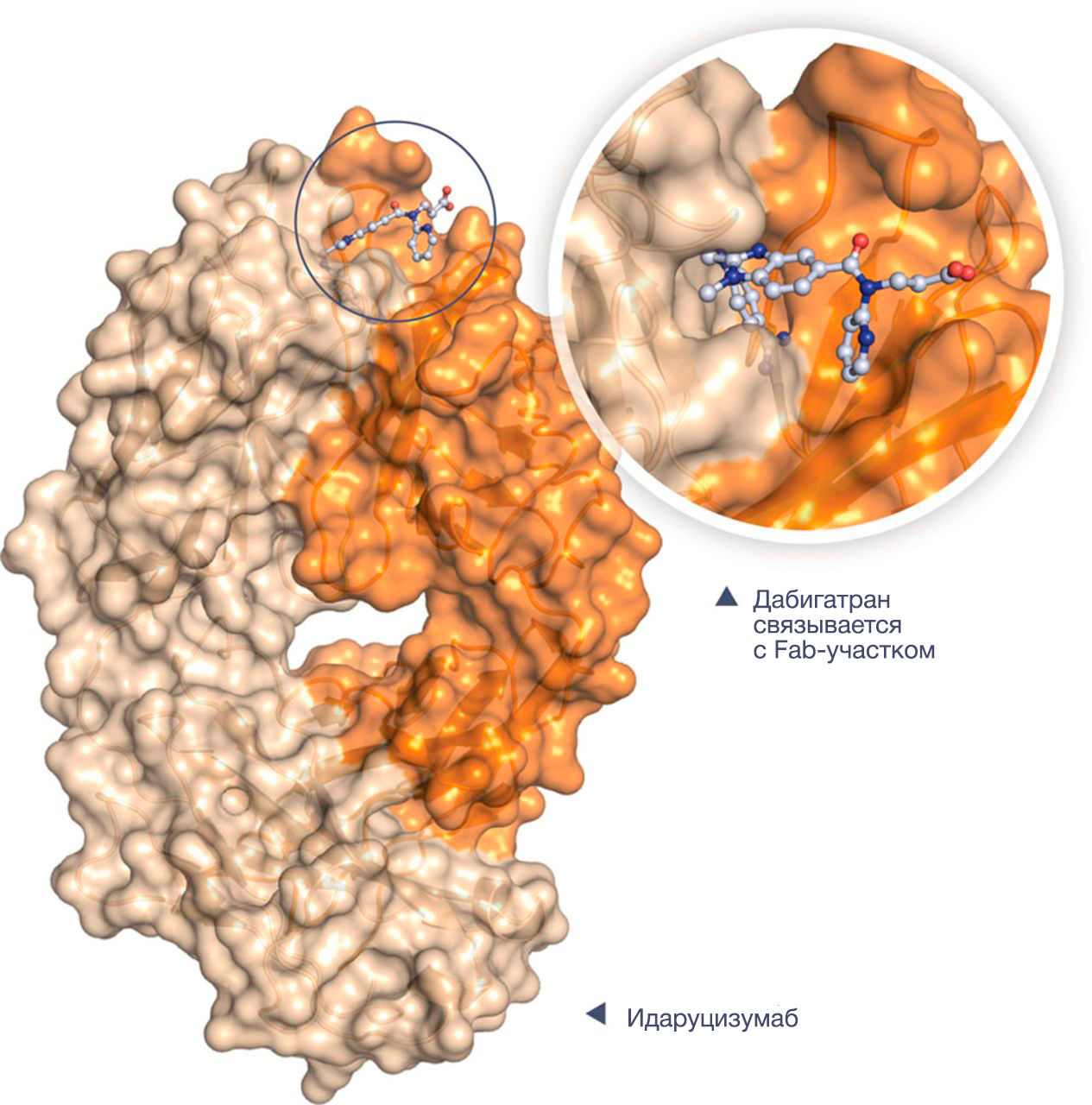
Безусловно, в процессе лечения любым антикоагулянтом может развиться кровотечение. Помимо этого, как говорилось выше, есть клинические ситуации, требующие резкой отмены НОАК. Однако в отличие от гепарина (антидот — протамина сульфат) или варфарина, в случае которого доступен витамин К, концентрат комплекса протромбина, на данный момент существует только 1 антидот против НОАК, допущенный до клинического применения — идаруцизумаб (2 других находятся на разных стадиях клинического исследования; о них будет сказано в конце). Идаруцизумаб представляет собой фрагмент моноклонального антитела, связывающий дабигатран в 350 раз сильнее, чем дабигатран связывается с тромбином (рис. 4, 5).
Рисунок 4 | Механизм действия идаруцизумаба. Идаруцизумаб взаимодействует и со свободным, и с тромбин-связанным дабигатраном; необратимо связывает активные метаболиты дабигатрана — ацилглюкурониды; не оказывает тромбиноподобного действия, как можно было бы ожидать исходя из его структуры (имеет в составе регион, очень близкий по структуре каталитическому активному центру тромбина)
Рисунок 5 | Идаруцизумаб представляет собой фрагмент моноклонального антитела (Fab), связывающего дабигатран в 350 раз сильнее, чем дабигатран связывается с тромбином
RE-VERSE AD ™ — это продолжающееся в настоящее время глобальное исследование III фазы, в которое включены пациенты, принимающие дабигатран, которым потребовалось проведение неотложных мероприятий в связи с развившимся у них массивным кровотечением. При применении идаруцизумаба в дозе 5 г в течение 4 часов степень связывания дабигатрана была измерена с помощью определения разведенного тромбинового времени (dTT) и экаринового времени свертывания крови (ECT) и оказалась равной 1:1.
Ривароксабан, апиксабан, эдоксабан
Фармакологию ривароксабана, апиксабана и эдоксабана можно рассмотреть единым блоком ввиду незначительных различий в их фармакокинетике и фармакодинамике.
Механизм действия
Механизм действия ривароксабана/апиксабана/эдоксбана связан с обратимым ингибированием свободного и связанного с тромбом фактора Ха (рис. 6). Для реализации своей прямой функции им не требуется наличие антитромбина III. Помимо этого, тот же апиксабан способен ингибировать активность протромбиназы, а также опосредованно ингибировать агрегацию тромбоцитов, индуцированную тромбином.
Рисунок 6 | Механизм действия ривароксабана/апиксабана/эдоксбана связан с обратимым ингибированием как свободного, так и связанного с тромбом активированного Х фактора
Фармакокинетика
Все 3 препарата быстро всасываются, Cmax достигается через 2–4 часа у риваро- и апиксабана, через 1–2 часа у эдоксабана (рис. 7). Здесь стоит отметить тот факт, что для первых двух представителей данной подгруппы НОАК характерна значительная фармакокинетическая вариабельность в отношении их плазменных концентраций (изменение Css в среднем до 40 %). Также для ривароксабана характерно уменьшение Cmax в зависимости от места высвобождения его в ЖКТ. Было показано, что максимальная его концентрация снижалась на 30 % при всасывании ривароксабана в дистальном отделе тонкой кишки.
Рисунок 7 | Фармакокинетика НОАК
Биотрансформация и элиминация
После приема внутрь 60 % от принятой дозы ривароксабана подвергается метаболизму в печени при помощи системы цитохрома р450 (в основном CYP3A4/5, CYP2J2), а также путем окисления морфолиновой группы и гидролиза амидных связей, неизмененная же часть препарата выводится через почки (до 30 %). Ривароксабан не образует активных метаболитов в крови, кроме своей неизмененной формы, через почки выводится до 66 % препарата: 30 % в неизменном виде, до 33 % после метаболизма в печени, 28 % препарата выводится с калом.
Ривароксабан является субстратом Р-гликопротеина (P-gp) и белка резистентности рака молочной железы (BCRP), при этом он не подавляет и не индуцирует изофермент CYP3A4 и другие важные изоформы цитохрома. Об этом следует помнить при комбинировании его с сильными индукторами Р-gp и CYP3A4, например, карбамазепином. Такая комбинация может приводить к снижению плазменных концентраций ривароксабана до 50 % со снижением его фармакодинамических эффектов. При этом совместное использование ингибиторов Р-gp и CYP3A4 (например, верапамила) с ривароксабаном у пациентов с нарушенной функцией почек может повышать время нахождения препарата в крови.
После приема внутрь 25 % апиксабана метаболизируется в печени в основном при помощи изофермента CYP3A4/5; в меньшей степени — с использованием CYP1A2, CYP2C8, CYP2C9, CYP2C19, CYP2J2. Апиксабан, так же как и ривароксабан, не образует активных метаболитов, а значит, его неизмененная форма является главным основным веществом в крови. Кроме того, апиксабан является субстратом P-gp, BCRP и изофермента CYP3A4/5, поэтому одновременное его использование с сильными двойными ингибиторами изоферментов системы цитохрома и Р-gp, например кетоконазолом, будет приводить к увеличению концентрации апиксабана в крови (требует снижения используемой дозировки на 50 %). Касаемо выведения апиксабана: в основном он выводится через кишечник, и только 27 % его метаболитов выводится через почки. О чем это может свидетельствовать? Апиксабан — единственный НОАК, который можно использовать при значении СКФ ниже 15 мл/мин, что роднит его со старичком варфарином. Но при этом стоит помнить о печени: не рекомендуется его использование у пациентов с печеночной недостаточностью тяжелой степени (класс С по Чайлд-Пью).
Рисунок 8 | Биотрансформация и элиминация НОАК
Эдоксабан на сегодняшний день — самый малоизученный НОАК. После приема внутрь минимально метаболизируется в печени с помощью изофермента CYP3A4/5, в основном метаболизм происходит при помощи механизмов, независимых от системы цитохромов — путем гидроксилирования и окисления. При этом в крови образуется активный метаболит М-4, который составляет не более 10 % от основного вещества и является субстратом Р-gp. Сильные ингибиторы Р-gp будут повышать плазменные концентрации эдоксабана, что требует снижения используемой дозировки 2 раза. Половина дозы эдоксабана выводится через почки в неизменном виде, другая половина элиминируется через желчь и кишечник. В исследовании ENGAGE-AF было показано, что снижение дозы эдоксабана (до 30 мг в сутки) при одновременном использовании ингибитора P-gp (верапамила, хинидина, дронедарона) приводило к повышению риска развития инсульта или системной эмболии в сравнении с варфарином. Поэтому эдоксабан в дозе 60 мг не рекомендуется использовать при СКФ выше 95 мл/мин (“терапевтическое окно” при СКФ от 50 до 95 мл/мин), а также надо помнить о том, что при СКФ в диапазоне от 15 до 50 мл/мин и одновременном использовании с ингибиторами Р-gp необходимо снижать дозировку до 30 мг.
Показания и режим дозирования
Ривароксабан
Общие показания для ривароксабана схожи с таковыми у дабигатрана. Основными из них являются:
Ривароксабан считается самым продаваемым НОАК с наибольшей доказательной базой (около 20 РКИ). Эффективность и безопасность использования ривароксабана в качестве средства профилактики инсульта и системных эмболий при неклапанной фибрилляции предсердий были выяснены в крупных исследованиях ROCKET-AF (в сравнении с варфарином) и XANTUS (первое в мире проспективное исследование IV фазы НОАК на предмет его безопасности). Благоприятный профиль эффективности и безопасности ривароксабана подтверждает то, что в РКИ у пациентов группы более высокого риска наблюдалась низкая частота больших кровотечений, инсультов/системных эмболий и инфарктов миокарда. Это в совокупности с однократным приемом в течении суток (20 мг, вечером, во время приема пищи) делает его практически «идеальным бойцом».
Эффективность применения ривароксабана с целью профилактики венозных тромбоэмболических осложнений (ВТЭО) после протезирования тазобедренного и коленного суставов была изучена в 4-х РКИ (RECORD 1, 2, 3, 4; в сравнении с эноксапарином). По итогам по профилю безопасности оба препарата показали приблизительно равные результаты, а по эффективности ривароксабан превзошел эноксапарин на 30–70 % в зависимости от исследования (10 мг однократно независимо от приема пищи в течение 35 дней при протезировании тазобедренного сустава и в течение 12 дней при протезировании коленного сустава).
Ривароксабан является единственным НОАК, для которого было доказано влияние на снижение риска развития ВТЭО у пациентов со стабильным течением ИБС или заболеванием периферических артерий (в комбинации с аспирином). По итогам исследования COMPASS, совместный прием ривароксабана в дозе 2,5 мг 2 раза/сут и аспирина в дозе 100 мг по сравнению со стандартной терапией аспирином 100 мг/сут достоверно снижал смертность от ССЗ и инсульта (в среднем на 25 %) и обладал большей суммарной клинической эффективностью в сравнении с монотерапией ривароксабаном.
Также было проведено спланированное проспективное исследование X-VeRT (в сравнении с варфарином), в котором ривароксабан в дозе 20 мг однократно был использован в качестве антикоагулянта при проведении кардиоверсии у пациентов с ФП. Была показана возможность проведения ранней кардиоверсии в срок от 4 часов до 5 суток после приема первой дозы препарата при отсутствии тромба в ушке левого предсердия, подтвержденного при помощи чреспищеводной ЭхоКГ (ЧПЭхоКГ). При проведении отсроченной кардиоверсии ривароксабан чаще позволял обеспечить готовность к кардиоверсии через 3 недели от начала приема препарата, не удлиняя этот период из-за подбора дозы в сравнении со стандартной схемой эноксапарин + варфарин. Безопасность была сравнима с данными проведенных исследований по ривароксабану.
Апиксабан
На данный момент показания для его применения полностью повторяют основные показания к назначению, характерные для всех НОАК, которые были описаны выше. В исследованиях ARISTOTLE и AVERROES было продемонстрировано, что апиксабан в дозе 5 мг 2 раза в сутки у пациентов с неклапанной ФП более эффективен в отношении снижения риска инсульта и системной эмболии (по сравнению с варфарином и АСК), общей смертности и больших кровотечений (в сравнении с варфарином) при сходном риске кровотечений с АСК в исследовании AVERROES (суточная дозировка в среднем составляла 165 мг) [12]. Коррекция дозировки апиксабана (снижение до 2,5 мг 2 раза в сутки) при использовании его по данному показанию требуется при наличии 2 из 3 следующих показателей: СКФ 80 лет, масса тела по эффективности он оказался на одном уровне со стандартной терапией (эноксапарин + варфарин), но был более безопасен в отношении развития геморрагических осложнений (снижение риска на 69 %); в качестве средства длительной терапии данные свидетельствовали о снижении риска рецидива ВТЭО на 80–82 % без повышения риска геморрагических осложнений. Таким образом, у апиксабана имеются изученные в клинических исследованиях дозы для каждого периода лечения и профилактики ВТЭО: 10 мг 2 раза/сут — для лечения острого периода в течение 7 дней; 5 мг 2 раза/сут — для дальнейшего лечения и профилактики рецидива, минимум 3 месяца; 2,5 мг 2 раза/сут — для длительной вторичной профилактики.
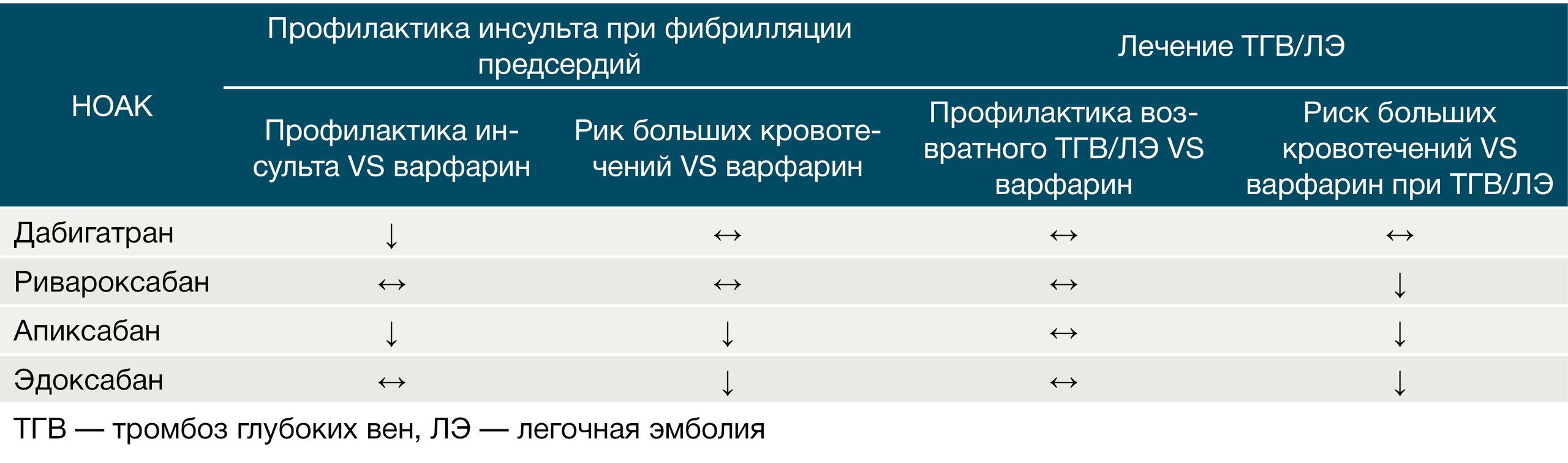
Были проведены сравнительные исследования между апиксабаном и ривароксабаном (EINSTEIN-DVT и EINSTEIN-РЕ). По их результатам при лечении острого эпизода ТЭЛА предпочтительным представляется назначение апиксабана, а при лечении острого эпизода изолированного ТГВ — ривароксабана. Эффективность ривароксабана и апиксабана в отношении вторичной профилактики ВТЭО оказалась одинаковой (снижение риска рецидива ВТЭО в EINSTEIN-Extension составило 82 %), но профиль безопасности ривароксабана был несколько хуже. Если сравнивать безопасность апиксабана с дабигатраном и ривароксабаном, то на данный момент он является наиболее безопасным из них с точки зрения развития риска массивных кровотечений при длительном приеме в течение, как минимум, 6 месяцев (рис. 9).
Рисунок 9 | Эффективность и безопасность НОАК в сравнении с варфарином.
При использовании апиксабана в качестве средства профилактики ВТЭО после протезирования тазобедренного или коленного суставов режим дозирования выглядит следующим образом: 2,5 мг 2 раза/сут в течение 35 дней после протезирования тазобедренного сустава и в течение 12 дней после протезирования коленного сустава (исследования ADVANCE-2 и ADVANCE-3).
Эдоксабан
Эдоксабан — последний из НОАК, был одобрен к использованию FDA и ЕМА в 2015 году; в нашей стране по состоянию на 2018 год он проходит регистрацию. Его можно использовать пока по двум показаниям:
В исследовании ENGAGE AF-TIMI 48 (сравнение с варфарином) была изучена эффективность и безопасность эдоксабана в качестве средства профилактики инсульта/системных эмболий у пациентов с ФП с использованием двух дозировок: 30 мг 2 раза/сут или 60 мг 1 раз/сут. По результатам эдоксабан не уступает варфарину в отношении профилактики инсульта и системной эмболии при условии хорошего контроля МНО на варфарине (70 % времени пребывания МНО в терапевтическом диапазоне) при значительно меньшем риске развития больших кровотечений. Однако Американская ассоциация сердца (American Heart Association, AHA) не рекомендует использовать эдоксабан в дозировке 60 мг 1 раз в сутки при СКФ выше 95 мл/мин в связи с повышенным риском развития ишемического инсульта в сравнении с тем же варфарином. Исследования на тему режима дозирования продолжаются и сейчас.
На данный момент было проведено спланированное проспективное исследование ENSURE-AF, в котором изучили возможность использования эдоксабана при проведении кардиоверсии у больных с ФП без предшествующего использования антикоагулянтов. Согласно его результатам эдоксабан — эффективная и безопасная альтернатива традиционной 3-недельной комбинации эноксапарин/варфарин для пациентов, подвергающихся плановой электрической кардиоверсии неклапанной ФП. Его однократный прием (60 мг 1 раз/сут) позволяет провести раннюю кардиоверсию (ФП при практически одинаковом профиле безопасности в сравнении с варфарином. Исследования по поиску точек приложения данного препарата продолжаются и сейчас. Также рано говорить и о конкретных побочных эффектах, связанных с приемом эдоксабана, поэтому стоит держать в уме общий для всех НОАК побочный эффект в виде повышенного риска развития массивного или клинически значимого малого кровотечения.
Побочные эффекты и противопоказания
Побочные эффекты, связанные с приемом риваро-/апиксабана, практически не отличаются от таковых при использовании других НОАК. Необходимо быть осторожным в следующих ситуациях:
Общим побочным эффектом для этих препаратов является повышенный риск развития скрытого или явного кровотечения, и, как следствие, развитие постгеморрагической анемии. Прием ривароксабана часто сопровождается зудом, кожной сыпью, развитием подкожных кровоизлияний. Также отмечаются головные боли и головокружения (остается открытым вопрос, являются ли они первичными или представляют собой признаки скрытого кровотечения). Прием апиксабана, так же, как и дабигатрана, может сопровождать «гастритоподобными» жалобами со стороны пациента. К «особенному» побочному эффекту апиксабана можно отнести меноррагию. Как говорилось выше, при использовании НОАК нельзя исключить риск развития большого или малого клинически значимого кровотечения. Рекомендации по ведению пациентов с кровотечениями на фоне применения апиксабана будут приложены к данному посту (рис. 10).
Рисунок 10 | Рекомендации по ведению пациентов с кровотечениями на фоне применения апиксабана
Антидотная терапия
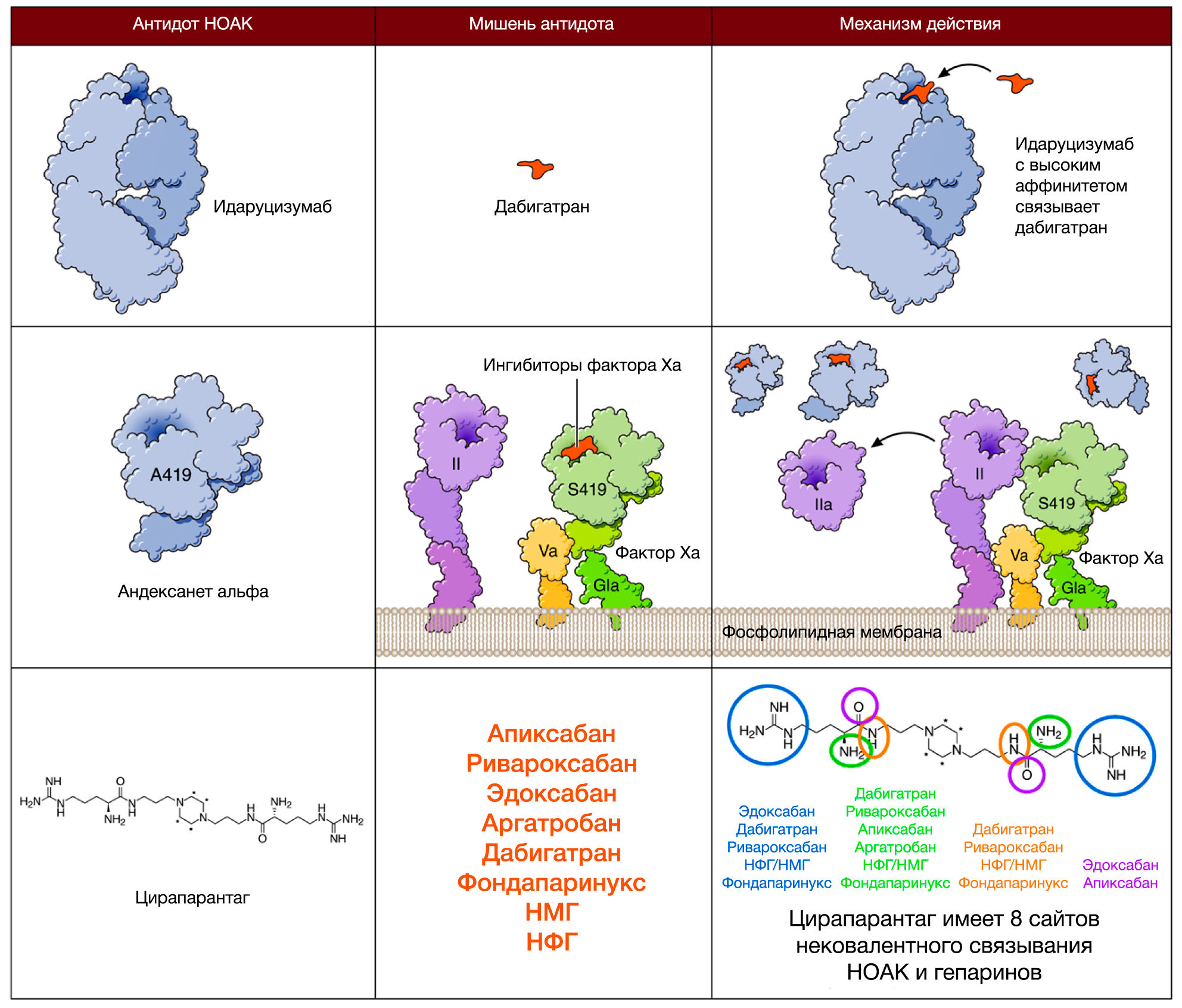
Как говорилось выше, на данный момент проводятся исследования еще 2 антидотов, способных устранить действие апиксабана — андексанета альфа и антидота «против всех» — цирапарантага/арипазина (PER977).
Андексанет альфа представляет собой рекомбинантный человеческий Ха фактор, который дозозависимо связывает прямые ингибиторы Ха фактора с той же аффинностью, что и нативный Ха фактор (рис. 11). Помимо этого, он также способен препятствовать связыванию НМГ и фондапаринукса с антитромбином III, тем самым «выключая» их из работы. Исследование ANNEXA-4 (III фазы), которое проводило оценку как профиля эффективности, так и безопасности андексанета у пациентов с большими кровотечениями на фоне терапии всеми известными на сегодняшний момент ингибиторами Xa фактора, должно было дать почву FDA для одобрения этого антидота еще в конце 2016 года. В связи с чем образовалась подобная задержка в регистрации препарата, остается загадкой.
Цирапарантаг представляет собой положительно заряженную молекулу, которая связывает НОАК при помощи водородных связей, однако такой механизм взаимодействия до конца не подтвержден. Цирапарантаг не связывается с белками плазмы и не имеет никаких лекарственных взаимодействией, что может быть его неоспоримым преимуществом. Но к настоящему времени опубликованы результаты лишь одного исследования I фазы (выборка составила около 80 человек), поэтому рано делать какие-либо выводы, остается надеяться и верить в конечный успех данного антидота.
Рисунок 11 | Механизм действия антидотов НОАК
Рисунок 12 | Показания к применению антидотов к НОАК
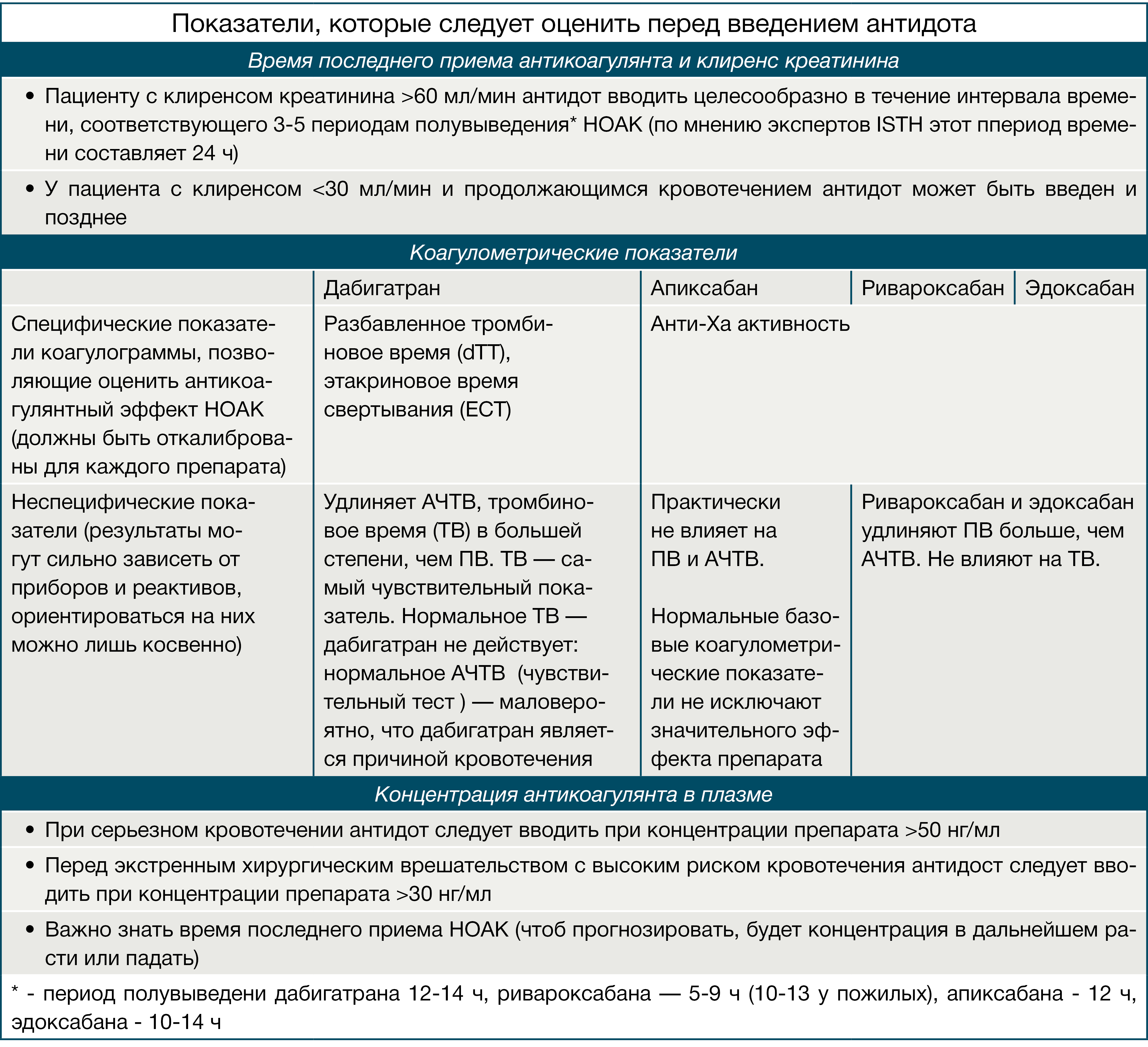
Рисунок 13 | Показатели, которые следует оценить перед введением антидота
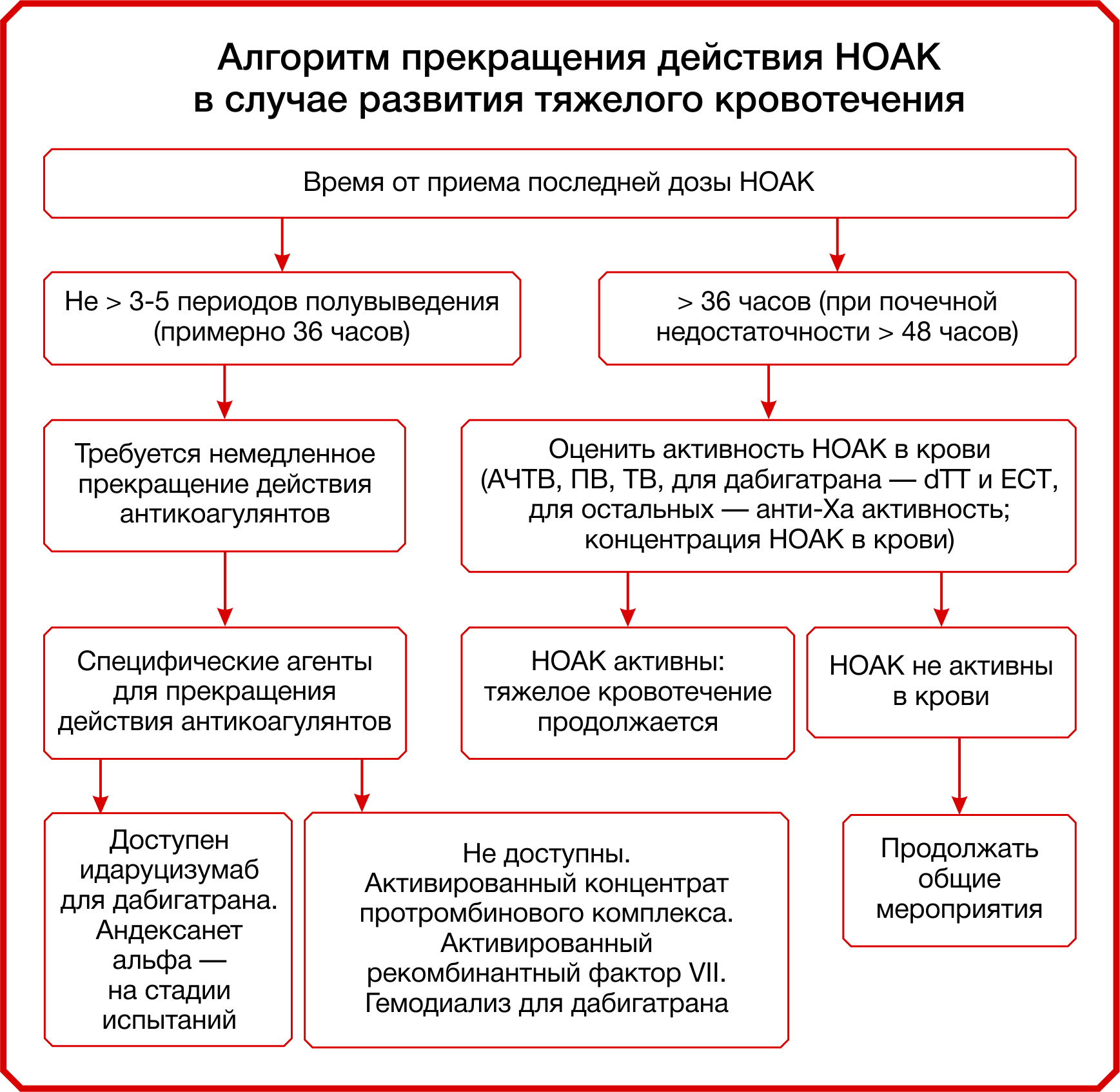
Рисунок 14 | Алгоритм прекращения действия НОАК в случае развития тяжелого кровотечения