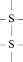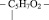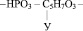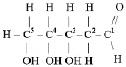Что такое нуклеиновые кислоты и их функции
Глава V. НУКЛЕИНОВЫЕ КИСЛОТЫ
§ 13. НУКЛЕИНОВЫЕ КИСЛОТЫ:
ФУНКЦИИ И СОСТАВ
Общие представления о нуклеиновых кислотах
Существует два различных типа нуклеиновых кислот – дезоксирибонуклеиновые кислоты (ДНК) и рибонуклеиновые кислоты (РНК). ДНК представляет собой генетический материал большинства организмов. В клетках прокариот, кроме основной хромосомной ДНК, часто встречаются внехромосомные ДНК – плазмиды. В эукариотических клетках основная масса ДНК расположена в клеточном ядре, где она связана с белками в хромосомах. Клетки эукариот содержат ДНК также в митохондриях и хлоропластах.
Что же касается РНК, то по выполняемым ими функциям различают:
В качестве генетического материала РНК входят в состав ряда вирусов. Например, вирусы, вызывающие такие опасные заболевания, как грипп и СПИД, являются РНК-содержащими.
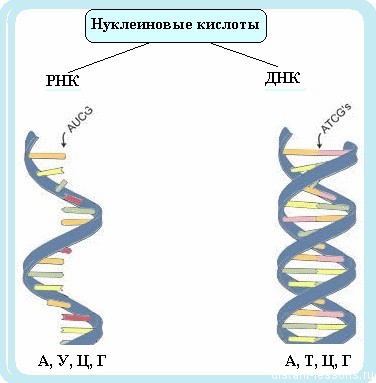
Нуклеиновые кислоты могут быть линейными и кольцевыми (ковалентно замкнутыми). Они могут состоять из одной или двух цепей. Ниже приведена схема, отражающая существование в природе различных типов нуклеиновых кислот:
Функции нуклеиновых кислот
Нуклеиновым кислотам присущи три важнейшие функции: хранение, передача и реализация генетической информации. Кроме этих, они выполняют и другие функции, например, участвуют в катализе некоторых химических реакций, осуществляют регуляцию реализации генетической информации, выполняют структурные функции и др. Роль хранителя генетической информации у большинства организмов (эукариот, прокариот, некоторых вирусов) выполняют двухцепочечные ДНК. Только у некоторых вирусов хранителем генетической информации являются одноцепочечные ДНК или одноцепочечные, а также двухцепочечные РНК. Генетическая информация записана в генах. Ген по своей природе является участком нуклеиновой кислоты. В них закодирована первичная структура белков. Гены могут также нести информацию о структуре некоторых типов РНК, например, тРНК и рРНК.
Генетическая информация передается от родителей к потомкам. Этот процесс связан с удвоением нуклеиновой кислоты (ДНК или РНК), выполняющей функцию хранителя генетической информации, и последующей передачи ее потомкам. Например, в результате деления дочерние клетки получают от материнской идентичные молекулы ДНК, а следовательно, и идентичную генетическую информацию (рис. 38). При размножении вирусы также передают дочерним вирусным частицам точные копии нуклеиновой кислоты. При половом размножении потомки получают генетическую информацию от обоих родителей. Вот почему дети наследуют признаки обоих родителей.
Рис. 38. Распределение ДНК при делении клетки
В результате реализации генетической информации происходит синтез белков, закодированных в ДНК в виде генов (или для некоторых вирусов – в РНК). В этом процессе информация о первичной структуре белка переписывается с молекулы ДНК на иРНК и затем расшифровывается на рибосомах при участии тРНК. В итоге образуется белок:
ДНК РНК
белок.
Состав нуклеиновых кислот
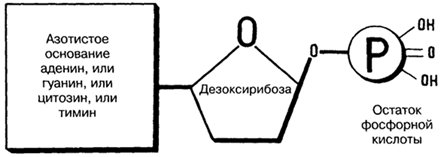
Нуклеиновые кислоты представляют собой полимеры, построенные из нуклеотидов, соединенных между собой фосфодиэфирными связями. Каждый нуклеотид состоит из остатков азотистого основания, пентозы и фосфорной кислоты.
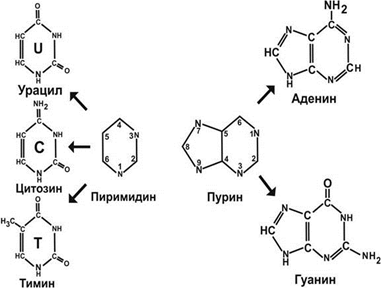
Различают пиримидиновые и пуриновые основания, называемые также соответственно пиримидины и пурины. Пиримидиновые основания являются производными пиримидина:
пуриновые основания – производными пурина:
К пиримидинам относятся урацил, тимин и цитозин, к пуринам – аденин и гуанин:
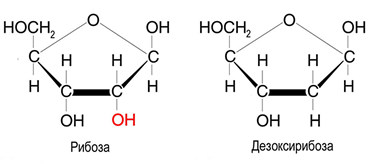
В состав ДНК входят тимин, цитозин, аденин и гуанин, в состав РНК – те же основания, только вместо тимина входит урацил. Кроме азотистых оснований, нуклеиновые кислоты содержат пентозы: ДНК – D-дезоксирибозу, а РНК – D-рибозу. Углеводы находятся в виде b-аномера фуранозной формы:
Азотистое основание связывается с углеводом за счет гликозидного гидроксила. Образуется нуклеозид. Схематически образование нуклеозида можно изобразить так:
В состав нуклеиновых кислот входят 8 нуклеозидов, 4 – в состав РНК и 4 – в состав ДНК (рис. 39).
Нуклеозиды, входящие в состав РНК:
Нуклеозиды, входящие в состав ДНК:
Нуклеозид, связанный с остатком фосфорной кислоты, называется нуклеотидом:
При этом остаток фосфорной кислоты может быть связан с 3’- или 5’- атомом углерода:
Сокращенно аденозин-5’-монофосфат обозначается как АМФ. Если нуклеотид образован дезоксорибозой, аденином и одним остатком фосфорной кислоты, то он будет носить название дезоксиаденозинмонофосфат, или сокращенно дАМФ. В таблице 5 представлена номенклатура нуклеотидов.
Номенклатура нуклеотидов, образующих ДНК и РНК
Научная электронная библиотека
§ 2.1.11. Аминокислоты. Белки. Нуклеиновые кислоты
Аминокислотами называются органические соединения, содержащие аминогруппу и карбоксильную группу. Например:
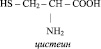
Аминокислоты относятся к веществам со смешанными функциями. Кроме того, они являются азотсодержащими и кислородсодержащими одновременно. Некоторые природные аминокислоты содержат также серу, как, например, цистеин:
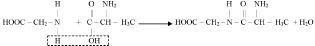
Наиболее характерным химическим свойством аминокислот является способность аминогруппы одной молекулы вступать в реакцию замещения с карбоксильной группой другой молекулы:
В результате образуется новая аминокислота, но уже с пептидной связью, способная взаимодействовать со следующей молекулой аминокислоты и образовать ещё одну пептидную связь. Последовательное увеличение количества пептидных связей в одной молекуле приводит к образованию полимеров, которые называются полипептидами, важнейшими представителями которых являются белки.
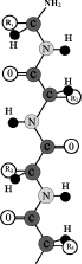
Белки – важнейшая составная часть клеток живых организмов – представляют собой полипептиды, составленные взаимодействием различных α-аминокислот. Таким образом, белки можно рассматривать как полимеры, мономером которых являются α-аминокислоты. Молекулярные массы природных белков колеблются от нескольких десятков тысяч до нескольких сот тысяч а.е.м. Аминокислотные остатки, являющиеся звеньями полипептида называют аминокислотными звеньями. Последовательность аминокислотных звеньев в линейной полипептидной цепи называется первичной структурой белковой молекулы (рис. 2.6).
Рис. 2.6. Первичная структура белков.
R1, R2, R3, R4 – радикалы остатков аминокислот
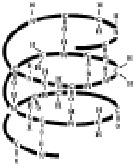
Благодаря многочисленным водородным связям между группами –СО– и –NH– первичная структура белков свёртывается в спираль, которая называется вторичной структурой белковой молекулы (рис. 2.7).
Рис. 2.7. Вторичная структура белков
В свою очередь, вторичная структура также способна свернуться, образовав третичную структуру (рис. 2.8).
Рис. 2.8. Третичная структура белков
Третичная структура поддерживается уже не только водородными связями, но также и ковалентными. В частности между атомами серы различных участков полипептида часто образуется дисульфидный мостик
Некоторые белковые макромолекулы могут соединяться друг с другом, образуя относительно крупные агрегаты. Подобные полимерные образования белков называются четвертичными структурами. Примером такого белка является гемоглобин, который представляет комплекс из четырёх макромолекул (рис. 2.9). Оказывается, что только при такой структуре гемоглобин способен присоединять и транспортировать кислород в организме.
Рис. 2.9. Четвертичная структура белков
Нуклеиновыми кислотами (полинуклеотидами) называют высокомолекулярные органические соединения, повторяющимся звеном которых являются нуклеотиды состоящие из
1. Остатка фосфорной кислоты – НРО3 –
2. Остатка рибозы 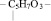
3. Радикалов азотистых оснований, а именно таких как: аденин, тимин, гуанин, цитозин, урацил.
Например, если радикал урацила обозначить У, то молекулярную формулу одного из нуклеотидов можно представить следующим образом:
К нуклеиновым кислотам относятся рибонуклеиновые кислоты (РНК) и дезоксирибонуклеиновые кислоты (ДНК). Рибонуклеиновые кислоты – это полинуклеотиды, включающие в себя остаток рибозы, радикалы аденина, гуанина, цитозина и урацила. Поскольку различные нуклеотиды РНК отличаются только радикалами азотистых оснований, то нередко каждый нуклеотид обозначают прописной первой буквой названия этого нуклеотида. Поэтому фрагмент какой либо РНК можно представить так
Первичная структура молекулы белка, синтезируемого на информационной (матричной) рибонуклеиновой кислоте (м-РНК) с помощью ферментов[31], определяется именно последовательностью нуклеотидов на этой РНК. Набору из трёх азотистых оснований, который называется триплет нуклеотидов или кодон, соответствует одна и только одна α-аминокислота. В настоящее время насчитывается 20 таких аминокислот (табл. х). Но одной аминокислоте может соответствовать несколько триплетов нуклеотида. Соответствие аминокислоты кодонам называется генетическим кодом. Реакции синтеза белка, у которого последовательность аминокислотных звеньев определяется последовательностью нуклеотидов м-РНК, называются реакциями матричного синтеза.
Последовательность нуклеотидов и-РНК в свою очередь определяется последовательностью азотистых оснований в дезоксирибонуклеиновой кислоте (ДНК), на которой и происходит синтез м-РНК
Дезоксирибонуклеиновые кислоты – это кислоты, состоящие из двух полинуклеотидных цепей, включающих в себя остаток дезоксирибозы, радикалы аденина, гуанина, цитозина, тимина и соединённых между собой по принципу комплементарности (совместимости) водородными связями. То есть, вместо радикала урацила, нуклеотиды ДНК содержат тимил, вместо остатка рибозы, остаток дезоксирибозы,
образующей замкнутый цикл соединением альдегидной группы с гидроксогруппой четвёртого атома углерода.
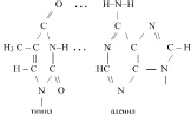
При этом А комплементарен Т, Г комплементарен Ц. То есть, фрагмент первичной структуры ДНК можно представить следующим образом:
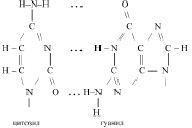
Действительно, аденил в ДНК образует водородную связь только с тимилом, а тимил, только с аденилом. Гуанил только с цитозилом, а цитозил только с гуанилом:
Молекулярную формулу одного из нуклеотидов ДНК можно представить так
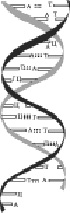
Вторичная структура ДНК представляет собой двойную спираль – две нити ДНК закручены одна вокруг другой (рис. 2.10).
Рис. 2.10. Вторичная структура ДНК
Ферментативный синтез м-РНК осуществляется на одной из цепей ДНК в соответствии с принципом комплементарности. При этом аденин ДНК комплементарен урацилу РНК, тимил ДНК коиплементарен аденину РНК, гуанил ДНК комплементарен цитозилу РНК, цитозил ДНК комплементарен гуанилу РНК. Затем с м-РНК осуществляется матричный синтез белка. К каждому кодону информационной РНК доставляется соответствующая аминокислота с помощью транспортной РНК (т-РНК).
Таким образом, основным хранителем информации о структуре всех белков, вырабатываемых организмом является ДНК.
Отрезок ДНК, содержащий информацию о первичной структуре одного определённого белка, называется геном.
Процесс переписывания информации, содержащейся в гене ДНК на м-РНК называется транскрипцией.
1. Приведите структурные формулы аминокислот, которые Вы знаете. Дайте им названия.
2. Дайте определения понятиям: полипептиды и белки.
3. Что представляют собой первичная, вторичная, третичная и четвертичная структуры белка?
4. В чём сходство и различия химического состава, строения ДНК и РНК? Что такое ген?
5. Каким образом в клетках живых организмов синтезируется м-РНК? Что такое транскрипция?
6. Что такое матричный синтез? Почему в качестве отдельной структурной единицы РНК рассматривают три соседних нуклеотида, а не два или, например, четыре?
Какие бывают типы нуклеиновых кислот? Что они собою являют?
Содержание:
Нуклеиновые кислоты – важнейшие органические соединения, осуществляющие хранение, передачу и реализацию наследственной информации. Это биополимеры – длинные молекулы, образованные мономерами – нуклеотидами. Нуклеиновые кислоты располагаются в ядре клетки.
Описание нуклеиновых кислот
Структура нуклеотидов
Нуклеотиды – это звено, состоящее из трех компонентов – азотистого основания, углеводной части (остатка моносахарида) и остатка фосфорной (ортофосфорной) кислоты.
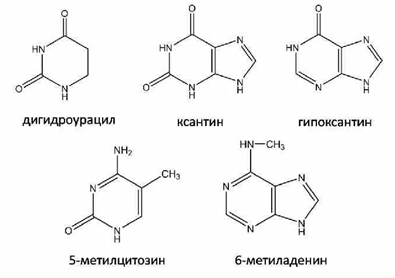
Азотистое основание – производное пурина и пиримидина. Они классифицируются на две группы – мажорные и минорные. Мажорные, или главные основания – соединения пуринового ряда (аденин А и гуанин) и пиримидинового ряда (цитозин Ц, тимин Т и урацил У).
Минорные основания – гипоксантин, 5-метилцитозин, 6-N-метиладенин, 1-N-метилгуанин и др.
Углеводная часть может состоять из рибозы или дезоксирибозы. Она представляет собой остаток моносахарида. В нуклеиновых кислотах они находятся в циклической форме.
Связь между углеводной частью и азотистым основанием называется гликозидной.
Остаток кислоты связывается с пятым углеродным атомом в сахаре и образует сложноэфирную связь.
Какие существуют типы нуклеиновых кислот
Дезоксирибонуклеиновая кислота ДНК
Рибонуклеиновая кислота РНК
Существует несколько типов РНК:
иРНК (информационная РНК) – РНК, считывающая информацию с ДНК;
тРНК (транспортная РНК) – РНК, которая считывает информацию с иРНК и образует антикодон;
рРНК (рибосомальная РНК) – РНК, с помощью которого происходит синтез белка.
Сходства и различия ДНК и РНК
Сходства ДНК и РНК:
структуры включают в себя остаток ортофосфорной кислоты;
Химия, Биология, подготовка к ГИА и ЕГЭ
Нуклеиновые кислоты содержатся абсолютно во всех клетках — как у живых организмов, так и у вирусов.
Это длинные полимерные цепочки, мономерами которых являются нуклеотиды.
Нуклеиновые кислоты бывают двух типов: ДНК и РНК
Были открыты в 1868 г. швейцарским ученым Ф. мишером, который обнаружил их в ядре.
В 1953 г. Биофизики Дж. Уотсон, М. Уилкинс и генетик Ф. Крик предложили трехмерную модель строения молекулы ДНК.
Строение ДНК и РНК
ДНК — дезоксирибонуклеиновая кислота
РНК — рибонуклеиновая кислота
Нуклеотиды — состоят из:
Азотистые основания ДНК: А — аденин, Т — тимин, Ц — цитозин, Г — гуанин
Азотистые основания ДНК: А — аденин, У — урацил, Ц — цитозин, Г — гуанин
РНК в отличие от ДНК не имеет тимина — вместо него стоит нуклеотид урацил — У
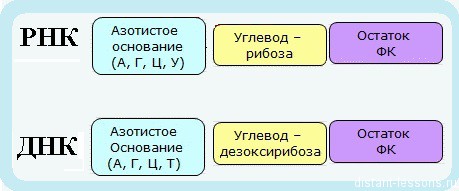
Это первичная структура молекул
Вторичная структура — это форма молекул нуклеиновых кислот.
РНК — «одинарная» длинная молекула.
Функции нуклеиновых кислот
участие в реализации наследственной информации ( синтез белка)
Дальше мы подробно разберем каждую молекулу в отдельности — ДНК и РНК.
3 интересных факта о ДНК:
По меньшей мере 8 процентов генома человека порождено вирусами, чей генетический код объединился с нашим в течении около 40 миллионов лет эволюции приматов.
Уже сегодня специалисты могут идентифицировать личность человека по остаткам «ДНК касания», которые остались в отпечатках пальцев на месте преступления.
Если размотать ДНК всех клеток вашего тела, то они растянутся на расстояние в 16 миллиардов километров — это примерно равно расстоянию от Земли до Плутона и обратно или более 30 раз от Земли до Солнца и обратно.
Биология. 10 класс
Конспект урока
Урок 3. «Органические вещества: белки и нуклеиновые кислоты и их значение. АТФ»
Перечень вопросов, рассматриваемых в теме;
Урок позволит выявить особенности строения макромолекул, определяющие многообразие белковых молекул, а также обеспечивающие возможность хранения и реализации генетической информации нуклеиновыми кислотами.
Глоссарий по теме (перечень терминов и понятий, введенных на данном уроке);
Белки; аминокислоты; пептидная связь; полипептид; незаменимые аминокислоты; структура белковой молекулы; глобулярные и фибриллярные белки; денатурация белка; ферменты; гормоны; антитела; рецепторы; нуклеиновые кислоты; нуклеотид; ДНК; РНК; АТФ; копмлементарность.
Белки – азотсодержащие высокомолекулярные органические соединения, нерегулярные полимеры, мономерами которых являются аминокислоты.
Аминокислоты – органические соединения, в молекуле которых одновременно содержатся карбоксильная группа (- СООН) и аминогруппа (- NН2).
Пептидная связь – это прочная ковалентная связь, возникающая при образовании белков (пептидов) в результате взаимодействия аминогруппы одной аминокислоты с карбоксильной группой другой аминокислоты.
Полипептид – соединение, состоящее из более 20 аминокислотных остатков.
Незаменимые аминокислоты – необходимые аминокислоты, которые не могут быть синтезированы в том или ином организме. Незаменимыми для взрослого здорового человека являются 8 аминокислот.
Структура белковой молекулы – сложная пространственная структура, обладающая первичным, вторичным, третичным и четвертичным уровнями организации. Особенности структурной организации белковой молекулы определяются первичным уровнем ее организации. Для того чтобы осуществлять свои биологические функции, белки сворачиваются в одну или несколько особых пространственных конфигураций, обусловленных рядом нековалентных взаимодействий, таких, как водородные связи, ионные связи, гидрофобные взаимодействия и др.
Глобулярные белки – белки, в молекулах которых полипептидные цепи плотно свёрнуты в глобулы (компактные шарообразные третичные структуры). Глобулярную структуру имеют ферменты, иммуноглобулины, некоторые гормоны.
Фибриллярные белки – белки, в молекулах которых расположенные параллельно друг другу вытянутые полипептидные цепи образуют длинные нити или слои (коллаген, кератин, фиброин).
Денатурация – это утрата белковой молекулой своей структурной организации. Она может быть вызвана изменением температуры, обезвоживанием, изменением кислотности раствора и другими воздействиями. В результате денатурации белок теряет способность выполнять свою функцию.
Ферменты – органические вещества белковой природы, которые синтезируются в клетках и во много раз ускоряют протекающие в них реакции, не подвергаясь при этом химическим превращениям.
Гормоны – биологически активные вещества органической природы, вырабатывающиеся в специализированных клетках желёз внутренней секреции, поступающие в кровь и оказывающие регулирующее влияние на обмен веществ и физиологические функции. Гормоны служат гуморальными (переносимыми с кровью) регуляторами определённых процессов в различных органах и системах. По химической природе могут быть белками, производными аминокислот, липидами.
Антитела (иммуноглобулины) – белковые соединения плазмы крови, образующиеся в ответ на введение в организм человека или теплокровных животных бактерий, вирусов, белковых токсинов и других антигенов. Связываясь активными участками (центрами) с бактериями или вирусами, антитела препятствуют их размножению или нейтрализуют выделяемые ими токсические вещества.
Клеточный рецептор – молекула (обычно белок или гликопротеид) на поверхности клетки, клеточных органелл или растворенная в цитоплазме. Специфично реагирует изменением своей пространственной конфигурации на присоединение к ней молекулы определённого химического вещества, передающего внешний регуляторный сигнал и, в свою очередь, передает этот сигнал внутрь клетки или клеточной органеллы.
Нуклеиновые кислоты – природные биополимеры, образованные остатками нуклеотидов, обеспечивающие хранение, передачу и реализацию наследственной (генетической) информации в живых организмах.
Нуклеотид – низкомолекулярные вещества, которые выполняют функции биорегуляторов (НАД, НАДФ, АТФ и др.) либо входят в состав полимерных молекул ДНК и РНК. В состав нуклеотида входит азотистое основание, углевод пентоза и остаток фосфорной кислоты.
Дезоксирибонуклеиновая кислота (ДНК) – макромолекула, обеспечивающая хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования живых организмов. Молекула ДНК хранит биологическую информацию в виде генетического кода, состоящего из последовательности нуклеотидов. ДНК содержит информацию о структуре различных видов РНК и белков.
Рибонуклеиновые кислоты (РНК) – макромолекулы, биологическая функция которых связана с реализацией наследственной информации в клетке.
Аденозинтрифосфорная кислота (аденозинтрифосфат, АТФ) – нуклеотид с тремя остатками фосфорной кислоты, имеющий большое значение в обмене энергии и веществ в организмах. АТФ — универсальный источник энергии для всех биохимических процессов, протекающих в живых системах.
Комплементарность – способность нуклеотидов к избирательному соединению друг с другом. Комплементарность обеспечивается взаимодополнением пространственных конфигураций молекул азотистых оснований, а также количеством водородных связей, возникающих между азотистыми основаниями.
Основная и дополнительная литература по теме урока (точные библиографические данные с указанием страниц);
1. Беляев Д.К., Дымшиц Г.М. Биология. 10 класс: учебник для общеобразовательных организаций: базовый уровень. – М.: Просвещение, 2014. – стр. 20-37;
2. Тейлор Д., Грин Н., Стаут У. Биология: в 3т. Том 1. – М.: Лаборатория знаний, 2016. – стр. 124-167
3. Кириленко А.А. Биология. ЕГЭ. Раздел «Молекулярная биология»: учебное пособие. – Ростов на Дону: Легион, 2017.
6. Открытые электронные ресурсы по теме урока (при наличии);
1. Молекулярная биология (белки, нуклеиновые кислоты) / Сайт Биология и медицина http://medbiol.ru/medbiol/biology_sk/000034fe.htm
2. Химия белков. Сайт Химик http://www.xumuk.ru/biologhim/001.html
Теоретический материал для самостоятельного изучения;
Белки — наиболее специфичны и важны для организма. Они относятся к непериодическим полимерам. В отличие от других полимеров их молекулы состоят из сходных, но нетождественных мономеров — 20 различных аминокислот.
Каждая аминокислота имеет свое название, особое строение и свойства. Их общую формулу можно представить в следующем виде
Молекула аминокислоты состоит из специфической части (радикала R) и части, одинаковой для всех аминокислот, включающей аминогруппу (— NH2) с основными свойствами, и карбоксильную группу (СООН) с кислотными свойствами. Наличие в одной молекуле кислотной и основной групп обусловливает их высокую реактивность. Через эти группы происходит соединение аминокислот при образовании полимера — белка. При этом из аминогруппы одной аминокислоты и карбоксила другой выделяется молекула воды, а освободившиеся электроны соединяются, образуя пептидную связь. Поэтому белки называют полипептидами.
Молекула белка представляет собой цепь из нескольких десятков или сотен аминокислот.
Молекулы белков имеют огромные размеры, поэтому их называют макромолекулами. Белки, как и аминокислоты, обладают высокой реактивностью и способны реагировать с кислотами и щелочами. Они различаются по составу, количеству и последовательности расположения аминокислот (число таких сочетаний из 20 аминокислот практически бесконечно). Этим объясняется многообразие белков.
В строении молекул белков различают четыре уровня организации (59)
Такая сложность структуры белковых молекул связана с разнообразием функций, свойственных этим биополимерам. Однако строение белковых молекул зависит от свойств окружающей среды.
Нарушение природной структуры белка называют денатурацией. Она может возникать под воздействием высокой температуры, химических веществ, лучистой энергии и других факторов. При слабом воздействии распадается только четвертичная структура, при более сильном — третичная, а затем — вторичная, и белок остается в виде первичной структуры — полипептидной цепи, Этот процесс частично обратим, и денатурированный белок способен восстанавливать свою структуру.
Роль белка в жизни клетки огромна.
Белки — это строительный материал организма. Они участвуют в построении оболочки, органоидов и мембран клетки и отдельных тканей (волос, сосудов и др.). Многие белки выполняют в клетке роль катализаторов — ферментов, ускоряющих клеточные реакции в десятки, сотни миллионов раз. Известно около тысячи ферментов. В их состав, кроме белка, входят металлы Mg, Fe, Мn, витамины и т. д.
Каждая реакция катализируется своим особым ферментом. При этом действует не весь фермент, а определенный участок — активный центр. Он подходит к субстрату, как ключ к замку. Действуют ферменты при определенной температуре и рН среды. Особые сократительные белки обеспечивают двигательные функции клеток (движение жгутиковых, инфузорий, сокращение мышц и т. д.). Отдельные белки (гемоглобин крови) выполняют транспортную функцию, доставляя кислород ко всем органам и тканям тела. Специфические белки — антитела — выполняют защитную функцию, обезвреживая чужеродные вещества. Некоторые белки выполняют энергетическую функцию. Распадаясь до аминокислот, а затем до еще более простых веществ, 1 г белка освобождает 17,6 кДж энергии.
Нуклеиновые кислоты (от лат. «нуклеус» — ядро) впервые обнаружены в ядре. Они бывают двух типов — дезоксирибонуклеиновые кислоты (ДНК) и рибонуклеиновые кислоты (РНК). Биологическая роль их велика, они определяют синтез белков и передачу наследственной информации от одного поколения к другому.
Фосфорная кислота и углевод одинаковы у всех нуклеотидов, а азотистые основания бывают четырех типов: аденин, гуанин, цитозин и тимин. Они и определяют название соответствующих нуклеотидов:
Каждая цепь ДНК представляет полинуклеотид, состоящий из нескольких десятков тысяч нуклеотидов. В ней соседние нуклеотиды соединены прочной ковалентной связью между фосфорной кислотой и дезоксирибозой.
При огромных размерах молекул ДНК сочетание в них из четырех нуклеотидов может быть бесконечно большим.
При образовании двойной спирали ДНК азотистые основания одной цепи располагаются в строго определенном порядке против азотистых оснований другой. При этом против А всегда оказывается Т, а против Г — только Ц. Это объясняется тем, что А и Т, а также Г и Ц строго соответствуют друг другу, как две половинки разбитого стекла, и являются дополнительными или комплементарными (от греч. «комплемент» — дополнение) друг другу. Если известна последовательность расположения нуклеотидов в одной цепи ДНК, то по принципу комплементарности можно установить нуклеотиды другой цепи (см. приложение, задача 1). Соединяются комплементарные нуклеотиды при помощи водородных связей.
Между А и Т возникают две связи, между Г и Ц — три.
Удвоение молекулы ДНК — ее уникальная особенность, обеспечивающая передачу наследственной информации от материнской клетки дочерним. Процесс удвоения ДНК называется редупликацией ДНК. Он осуществляется следующим образом. Незадолго перед делением клетки молекула ДНК раскручивается и ее двойная цепочка под действием фермента с одного конца расщепляется на две самостоятельные цепи. На каждой половине из свободных нуклеотидов клетки, по принципу комплементарности, выстраивается вторая цепь. В результате вместо одной молекулы ДНК возникают две совершенно одинаковые молекулы.
РНК — полимер, по структуре сходный с одной цепочкой ДНК, но значительно меньших размеров. Мономерами РНК являются нуклеотиды, состоящие из фосфорной кислоты, углевода (рибозы) и азотистого основания. Три азотистых основания РНК — аденин, гуанин и цитозин — соответствуют таковым ДНК, а четвертое — иное. Вместо тимина в РНК присутствует урацил. Образование полимера РНК происходит через ковалентные связи между рибозой и фосфорной кислотой соседних нуклеотидов. Известны три вида РНК: информационная РНК (и-РНК) передает информацию о структуре белка с молекулы ДНК; транспортная РНК (т-РНК) транспортирует аминокислоты к месту синтеза белка; рибосомная РНК (р-РНК) содержится в рибосомах, участвует в синтезе белка.
АТФ — аденозинтрифосфорная кислота — важное органическое соединение. По структуре это нуклеотид. В его состав входит азотистое основание аденин, углевод — рибоза и три молекулы фосфорной кислоты. АТФ — неустойчивая структура, под влиянием фермента разрывается связь между «Р» и «О», отщепляется молекула фосфорной кислоты и АТФ переходит в АДФ (аденозин-дифосфорную кислоту).
Эта реакция сопровождается выделением 40 кДж энергии, поэтому фосфорнокислородную связь называют макроэнергетической связью и обозначают знаком [бесконечность]. В АТФ имеются две такие связи. Если отщепляются две молекулы фосфорной кислоты, то АТФ переходит в АМФ (аденозинмонофосфорную кислоту).
АТФ играет центральную роль в превращении энергии в клетке.
Примеры и разбор решения заданий тренировочного модуля (не менее 2 заданий).
Все перечисленные ниже признаки, кроме двух, можно использовать для описания яичного белка альбумина. Определите два признака, «выпадающих» из общего списка.
1) состоит из аминокислот
2) пищеварительный фермент
3) денатурирует обратимо при варке яйца
4) мономеры связаны пептидными связями
5) молекула образует первичную, вторичную и третичную структуры
Тип вариантов ответов: (Текстовые, Графические, Комбинированные)
2) пищеварительный фермент
3) денатурирует обратимо при варке яйца
Подсказка: вспомните, какую роль выполняют ферменты.
Соберите из элементов изображение молекулы вещества, являющегося универсальным источником энергии для многих биохимических процессов, протекающих в живых системах.
Изображение необходимо разрезать на тайлы таким образом, чтобы была возможность выбора варианта соединения между разными компонентами молекулы.
Тип вариантов ответов: (Текстовые, Графические, Комбинированные)
Подсказка: универсальным источником энергии для многих биохимических процессов, протекающих в живых системах, является АТФ (аденозинтрифосфат). АТФ – адениловый нуклеотид, к которому присоединены ещё два остатка фосфорной кислоты.