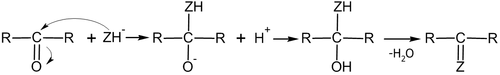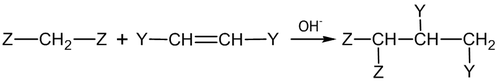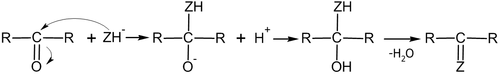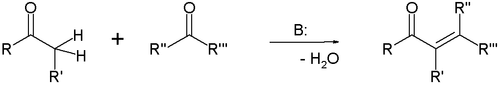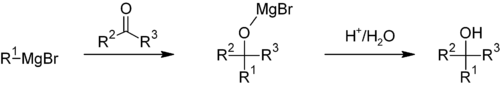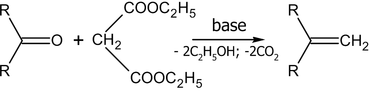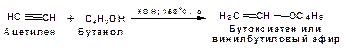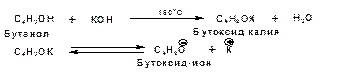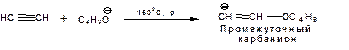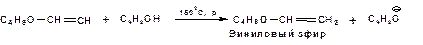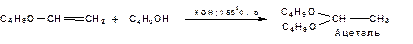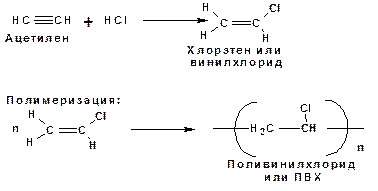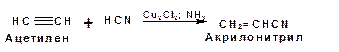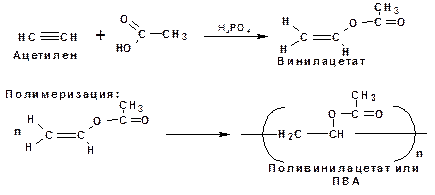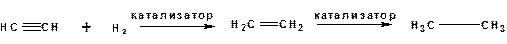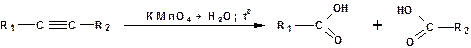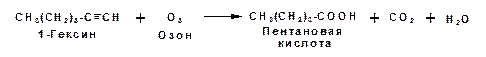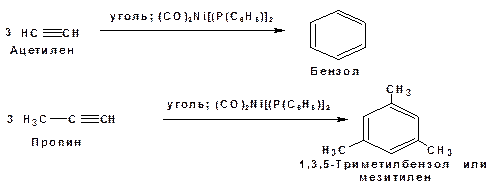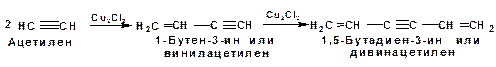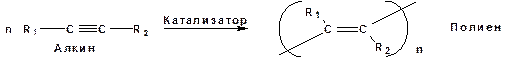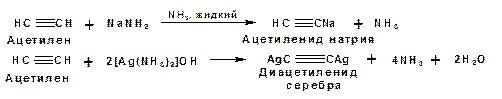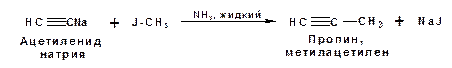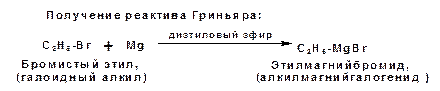Что такое нуклеофильное присоединение
Химия
3.6. Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров
Альдегиды и кетоны. Химические свойства. Реакции нуклеофильного присоединения
Химические свойства альдегидов и кетонов определяются наличием карбонильной группы.
Карбонильная группа содержит двойную углерод-кислородную связь. Поскольку подвижные p-электроны оттянуты к более электроотрицательному атому кислорода, он несёт частичный отрицательный заряд (δ—), а атом углерода – частичный положительный заряд (δ+). Таким образом двойная углерод-кислородная связь является полярной.
Положительно заряженный атом углерода карбонильной группы является местом нуклеофильной атаки, и большинство реакций присоединения являются нуклеофильными реакциями.
Реакции нуклеофильного присоединения
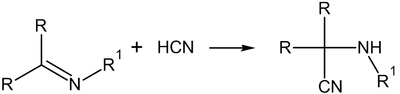
Присоединение HCN
Присоединение синильной кислоты к альдегидам и большинству кетонов приводит к образованию циангидринов.
Присоединение самой синильной кислоты протекает очень медленно, поскольку HCN является слабым нуклеофилом. Добавление цианида калия или другого основания, которое может генерировать цианид-анион (более сильный нуклеофил) из HCN, значительно повышает скорость реакции присоединения. Присоединение происходит с учетом распределения электронной плотности:
Циангидрины содержат нитрильную группу, и их главное использование основано на том, что они подвергаются гидролизу, в результате чего образуются a-гидроксикислоты, в нашем примере получается молочная кислота или a-гидроксипропановая кислота.
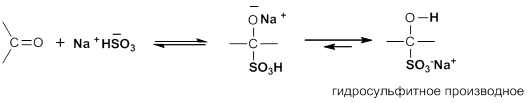
Присоединение гидросульфита натрия
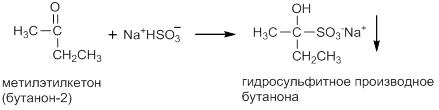
Гидросульфит натрия присоединяется к альдегидам и ко многим кетонам (особенно метилкетонам) с образованием продукта присоединения:
Кетоны, содержащие объемные заместители, в данную реакцию не вступают из-за пространственных затруднений.
Практическое применение данной реакции в том, что она позволяет отделить карбонильные соединения от некарбонильных. Выпавшее в осадок гидросульфитное производное отфильтровывают и подкисляют, при этом происходит регенерация карбонильного соединения.
Реакции нуклеофильного присоединения
Реакции нуклеофильного присоединения (англ. addition nucleophilic reaction ) — реакции присоединения, в которых атаку на начальной стадии осуществляет нуклеофил — частица, заряженная отрицательно или имеющая свободную электронную пару. На конечной стадии образующийся карбанион подвергается электрофильной атаке.
Несмотря на общность механизма различают реакции присоединения по связи углерод-углерод и углерод-гетероатом.
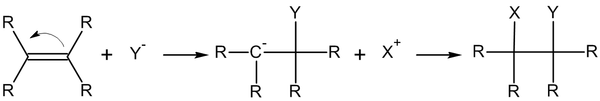
Общий вид реакций присоединения по двойной связи углерод-углерод:
Содержание
Реакции нуклеофильного присоединения по связи углерод-углерод
Механизм реакций нуклеофильного присоединения по связи углерод-углерод
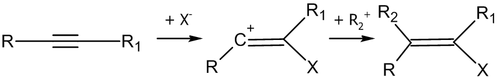
Нуклеофильное присоединение по кратной связи обычно двухстадийный процесс AdN2 — реакция бимолекулярного нуклеофильного присоединения (англ. addition nucleophilic bimolecular ) [2] :
Присоединение по тройной связи аналогично присоединению по связи С=C:
Реакции нуклеофильного присоединения по связи углерод-гетероатом
Механизм реакций нуклеофильного присоединения по связи углерод-гетероатом
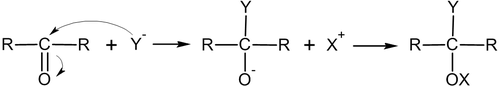
Нуклеофильное присоединение по кратной связи углерод-гетероатом имеет механизм AdN2:
Иногда продукты присоединения вступают в реакцию отщепления, тем самым совокупно давая реакцию замещения:
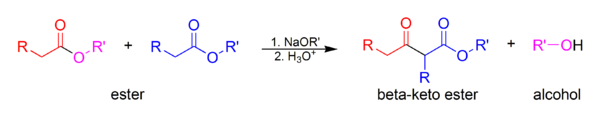
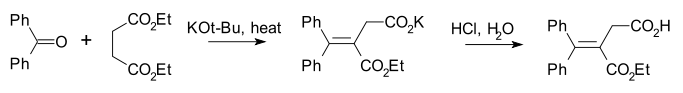
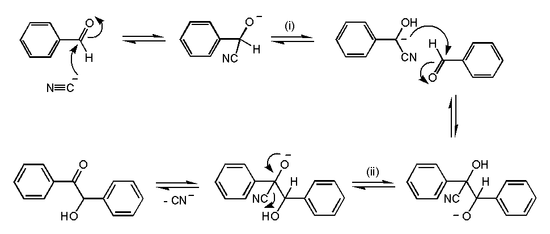
Типичные реакции нуклеофильного присоединения по связи C=O
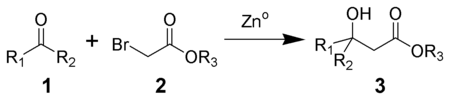
4. Реакция Реформатского.
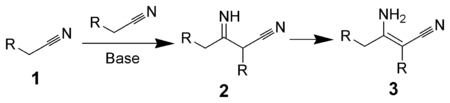
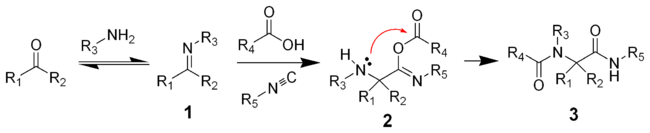
Типичные реакции нуклеофильного присоединения по связи C=N и С≡N
Примечания
 Химические реакции в органической химии Химические реакции в органической химии | |
|---|---|
| Реакции замещения | Реакции нуклеофильного замещения · Реакции электрофильного замещения · Реакции радикального замещения |
| Реакции присоединения | Реакции нуклеофильного присоединения · Реакции электрофильного присоединения · Реакции радикального присоединения · Реакции синхронного присоединения |
| Реакции элиминирования | Реакции гетеролитического элиминирования · Реакции перициклического элиминирования · Реакции радикального элиминирования |
| Реакции перегруппировки | Нуклеофильные перегруппировки · Электрофильные перегруппировки · Радикальные перегруппировки |
| Реакции окисления и восстановления | Реакции окисления · Реакции восстановления |
| Прочее | Именные реакции в органической химии |
Полезное
Смотреть что такое «Реакции нуклеофильного присоединения» в других словарях:
Реакции электрофильного присоединения — (англ. addition electrophilic reaction) реакции присоединения, в которых атаку на начальной стадии осуществляет электрофил частица, заряженная положительно или имеющая дефицит электронов. На конечной стадии образующийся… … Википедия
Реакции радикального присоединения — (англ. addition radical reaction) реакции присоединения, в которых атаку осуществляют свободные радикалы частицы, содержащие один или несколько неспаренных электронов. При этом радикалы могут атаковать как другие радикалы, так и… … Википедия
Реакции синхронного присоединения — реакции присоединения, в которых атака на оба атома кратной связи осуществляется одновременно. Другое название реакций этого типа реакции циклоприсоединения, так как конечным продуктом таких реакций являются циклические субстраты. Существует две… … Википедия
Реакции нуклеофильного замещения — (англ. nucleophilic substitution reaction) реакции замещения, в которых атаку осуществляет нуклеофил реагент, несущий неподеленную электронную пару.[1] Уходящая группа в реакциях нуклеофильного замещения называется нуклеофуг. Все … Википедия
Реакции присоединения — (англ. addition reaction) в органической химии так называются химические реакции, в которых одни химические соединения присоединяются к кратным (двойным или тройным) связям другого химического соединения. Присоединение может… … Википедия
Реакции замещения — (англ. substitution reaction) химические реакции, в которых одни функциональные группы, входящие в состав химического соединения, меняются на другие группы. Реакции замещения обозначают английской буквой «S». Общий вид реакций… … Википедия
Реакции электрофильного замещения — (англ. substitution electrophilic reaction) реакции замещения, в которых атаку осуществляет электрофил частица, заряженная положительно или имеющая дефицит электронов. При образовании новой связи уходящая частица электрофуг … Википедия
Реакции радикального замещения — (англ. substitution radical reaction) реакции замещения, в которых атаку осуществляют свободные радикалы частицы, содержащие один или несколько неспаренных электронов. Реакции радикального замещения обозначают SR. Содержание 1… … Википедия
Реакции элиминирования — Элиминирование (от лат. elimino изгоняю) это отщепление от молекулы органического соединения атомов или атомных групп без замены их другими. Реакция элиминирования может проходит в одну стадию (по механизму E2), либо в две стадии … Википедия
ПРИСОЕДИНЕНИЯ РЕАКЦИИ — ПРИСОЕДИНЕНИЯ РЕАКЦИИ, химические реакции, в ходе которых из двух или более веществ образуется новое сложное вещество (см. СЛОЖНОЕ ВЕЩЕСТВО): CaO + CO2 ® CaCO3. Различают гомолитическое (см. ГОМОЛИТИЧЕСКИЕ РЕАКЦИИ) и гетеролитическое (см.… … Энциклопедический словарь
Нуклеофильное присоединение.
В силу более высокой электроотрицательности атома углерода, в состоянии sp-гибридизации, по сравнеению с атомом углерода в состоянии sp 2 гибридизации, алкины, в отличии от алкенов могут вступать в реакции нуеклеофильного присоединения.
Реакциями нуклеофильного присоединения (реакции тип АdN) называют реакции присоединения, в скоростьлимитирующей стадии которых атакующей частицей является нуклеофил.
Примером нуклеофильного присоединения является присоединение спиртов к алкинам в присуствии щелочи (реакция Фаворского, 1887г.):
Механизм реакции нуклеофильного присоединения к тройной связи включает следующие стадии:
1. На первой стадии по кислотно-основной реакции образуется алкоголят-анион или алкоксид-ион, являющийся сильным основанием:
2. На второй стадии алкоксид-ион присоединяется к алкину. Эта стадия является скоростьлимитирующей. Причем, если алкин несиммеитричный, то присоединение протекает в соответствии с правилом Марковникова, а именно: анион, будучи нуклеофильной частицей, присоединяется к наименее гидрогенизированному атому углерода:
3. На третьей стадии образовавшийся карбанион отщепляет протон от другой молекулы спирта, что приводит к образованию эфира и регенерации алкоголят-аниона:
Образовавшийся виниловый эфир может присоединить еще одну молекулу спирта. При этом образуется соединение называемое ацеталем:
Винилирование.
Реакция образование виниловых эфиров из ацетилена и спиртов является примером так называемых реакций вининилирования. К числу этих реакций относятся:
1. Присоединение к ацетилену хлористого водорода:
2. Присоединение к ацетилену синильной кислоты в присутствии солей меди:
3. Присоединение к ацетилену уксусной кислоты в присутствии фосфорной кислоты:
Гидрирование
В условиях гетерогенного катализа алкины присоединяют водород аналогично алкенам:
Первая стадия гидрирования более экзотермична (протекает с большим выделением тепла), чем вторая, что обусловлено большим запасом энергии в ацетилене, чем в этилене:
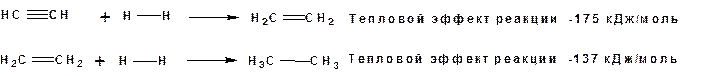
Окисление.
Алкины подобно алкенам окисляются по месту тройной связи. Окисление идет в жестких условиях с полным разрывом тройной связи и образованием карбоновых кислот. Аналогично исчерпывающему окислению олефинов. В качестве окислителей применяют перманганат калия при нагревании или озон:
Следует отметить, что при окислении терминальных алкенов и алкинов одним из продуктов окисления является углекислый газ. Его выделение можно наблюдать визуально и тем самым можно отличить терминальные от внутренних ненасыщенных соединений. При окислении последних выделение углекислого газа не будет наблюдаться.
Полимеризация.
Ацетиленовые углеводороды способны к полимеризации в нескольких направлениях:
1. Циклотримеризация ацетиленовых углеводородов, с использованием активированного угля (по Зелинскому) или комплексного катализатора из дикарбонила никеля и фосфорорганического соединения (по Реппе). В частности из ацетилена получается бензол:
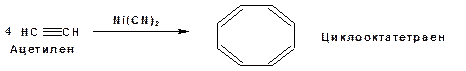
В присутствии цианида никеля ацетилен претерпевает циклотетрамеризацию:
В присутствии солей меди происходит линейная олигомеризация ацетилена с образованием винилацетилена и дивинилацетилена:
Кроме всего того, алкины способны к полимеризации с образованием сопряженных полиенов:
Реакции замещения.
Металлирование
При действии очень сильных оснований алкины, имеющие концевую тройную связь, полностью ионизируются и образуют соли, которые называются ацетиленидами. Ацетилен реагирует как более сильная кислота и вытесняет более слабую кислоту из ее соли:
Ацетилениды тяжелых металлов, в частности меди серебра, ртути, являются взрывчатыми веществами.
Алкинид-анионы (или ионы), входящие в состав ацетиленидов являются сильными нуклеофилами. Это свойство нашло применение в органическом синтезе для получения гомологов ацетилена с использованием галогенналкилов:
Кроме ацетилена подобное превращение можно провести для других алкинов, имеющих концевую тройную связь.
Гомологи ацетилена или терминальных алкинов можно получить другим путем. С использованием так называемого реактива Иоцича. Реактив Иоцича получают из реактива Гриньяра:
Далее проводят реакцию реактива Гриньяра с алкином, имеющим концевую двойную связь.
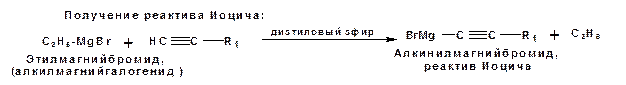
Реакции нуклеофильного присоединения к карбонильной группе альдегидов и кетонов
Вы будете перенаправлены на Автор24
Что обьясняется большим различием в электроотрицательности атомов кислорода и углерода. Следствием высокой полярности карбонильной группы является то, что альдегиды и кетоны обладают большими дипольными моментами. В табл. 1 приведены значения дипольных моментов для четырех самых распространенных карбонильных соединений.
Механизм реакций нуклеофильного присоединения
Готовые работы на аналогичную тему
Влияние заместителей на ход реакции нуклеофильного присоединения к карбонильной группе
Влияние строения соединений на ход реакции нуклеофильного присоединения к карбонильной группе
На реакционную способность оксосоединений влияют и стерические факторы: объемные радикалы затрудняют атаку нуклеофилом карбонильного атома углерода и, следовательно, снижают скорость реакции.
Подытоживая рассмотренные факторы, можно расположить отдельные типы карбонильных соединений в ряды по их активности в реакциях нуклеофильного присоединения.
По длине углеводородного радикала
По количеству электроноакцепторных заместителей
По расположению электроноакцепторных заместителей
По природе заместителя
По положению карбонильной группы
По стерическим и конформационным факторам
При наличии ароматичности
Получи деньги за свои студенческие работы
Курсовые, рефераты или другие работы
Автор этой статьи Дата последнего обновления статьи: 24 02 2021
Нуклеофильное присоединение
Реакции нуклеофильного присоединения (англ. nucleophilic addition reaction ) — реакции присоединения, в которых атаку на начальной стадии осуществляет нуклеофил — частица, заряженная отрицательно или имеющая свободную электронную пару. На конечной стадии образующийся карбанион подвергается электрофильной атаке.
Несмотря на общность механизма различают реакции присоединения по связи углерод-углерод и углерод-гетероатом.
Общий вид реакций присоединения по двойной связи углерод-углерод:
− C | = C | − + Y − → − C − | − C Y | − <\displaystyle <\mathsf <-<\stackrel <|>
− C − | − C Y | − + X + → − C X | − C Y | − <\displaystyle <\mathsf <-<\stackrel <|\ >
Содержание
Реакции нуклеофильного присоединения по связи углерод-углерод [ | ]
Механизм реакций нуклеофильного присоединения по связи углерод-углерод [ | ]
Нуклеофильное присоединение по кратной связи обычно двухстадийный процесс AdN2 — реакция бимолекулярного нуклеофильного присоединения (англ. addition nucleophilic bimolecular ) [2] :
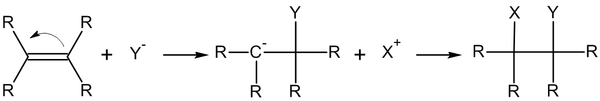
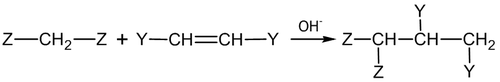
Присоединение по тройной связи аналогично присоединению по связи С=C:

Реакции нуклеофильного присоединения по связи углерод-гетероатом [ | ]
Механизм реакций нуклеофильного присоединения по связи углерод-гетероатом [ | ]
Нуклеофильное присоединение по кратной связи углерод-гетероатом имеет механизм AdN2:

Иногда продукты присоединения вступают в реакцию отщепления, тем самым совокупно давая реакцию замещения: