Определение уровня бактериальной обсемененности
Принято считать, что чем выше БО, тем ниже качество молока. Статистически это утверждение можно считать верным, так как вероятность наличия патогенных бактерий в насыщенной микробами среде намного выше, чем в сравнительно чистой от посторонних организмов. Но это не всегда так. Например, молочнокислые продукты обильно обсеменены разнообразной микрофлорой, но в то же время незначительная обсемененность продукта патогенными бактериями может привести к тяжелым последствиям.
Дело в том, что на характер БО влияет и множество других факторов, в том числе температура, кислотно-щелочной баланс среды и т.д. Ведь именно от этих характеристик зависит будут ли бактерии размножаться, сохранятся в состоянии покоя или погибнут. Таким образом, опасность этих организмов для здоровья людей и животных зависит не столько от степени обсеменения, а скорее от сроков прошедших после заражения.
Отсюда главное правило при измерении бактериальной обсемененности – замер должен производиться, учитывая динамичность и неравномерность распределения микроорганизмов. Для этого необходимо соблюдать ряд правил. Среди них: анализ нескольких повторов, большее количество проб, взятых на разных участках. В таких условиях полученные результаты будут давать показания измеряемого объекта в целом, а не отдельных его частей.
БО измеряют следующими методами:
• прямым подсчетом микроорганизмов
• титрационным посевом или чашечный метод
ПРЯМОЙ ПОДСЧЕТ МИКРООРГАНИЗМОВ
Первый метод довольно прост и доступен в использовании, но имеет ряд недостатков. Так при подсчете трудно различить микроорганизмы и прочие инородные частицы, среди которых могут быть и как механические загрязнения, так и соматические клетки. Эти загрязнения могут собираться в комочки. И в этом случае отличить живые микроорганизмы от мертвых не представляется никакой возможности.
ТИТРАЦИОННЫЙ ПОСЕВ (ЧАШЕЧНЫЙ МЕТОД)
Способ измерения БО методом определения микробного числа (титрационного посева) позволяет вести учет только живых организмов. Микробным числом называют количество бактериальных колоний, которые вырастают на мясопептонном агаре при посеве 1 мл пробы и культивировании при 37°С в течение 24-48 ч (или 72 ч при 22°С).
При определении микробного числа в первую очередь определяются колонии микробов, которые используют в качестве источников питания белок (из-за содержащегося в нем азота) и продуктов его распада. Эти микробы являются самыми активными потребителями органических веществ, соответственно развиваются быстрее остальных и также быстрее погибают при очищении среды. Выходит, что данные, получаемые при этом методе значительно меньше, чем при непосредственном подсчете, так как:
• мертвые клетки не могут приносить потомства, а соответственно их число в общей массе будет незначительным
• не будут расти живые клетки, которые утратили способность к размноджению
• не будут разрушаться конгломераты
• не вырастут анаэробы (т.к. испытания проводятся в аэробных условиях.
• не вырастут термофилы и психрофилы (из-за выращивания при 37°С, благоприятной для мезофиллов)
Таким образом, микробное число будет намного меньше и напрямую отразит только количество сапрофитных мезофильных аэробных микробов, именно которые и являются основными возбудителями порчи пищевых продуктов. И именно по микробному числу можно делать выводы о санитарному состоянии почвы, воды, воздуха и пищевых продуктов, которые принимает животное.
Основной недостаток титрационного посева – длительность его анализа. Питательная среда не должна ограничивать рост одних клеток и создавать условия для ускоренного развития других. В то же время необходимо чтобы размер колоний был видим и визуально замечен при подсчете, на что требуется время.
МЕТОД РЕДУКТАЗНОЙ ПРОБЫ
Согласно действующему ГОСТу (32901-2014 «Молоко и молочная продукция. Методы микробиологического анализа») молоко допустимо проверять на наличие БО экспресс-методом редуктазной пробы. Этот метод более быстрый, чем метод титрационного посева, так как для его проведения достаточно всего полтора часа. В то же время он намного эффективнее прямого подсчета, так как основывается на данные, получаемые от фермента редуктазы. А раз этот фермент выделяется только живыми организмами, то и полученные данные будут говорить о наличии только живых бактерий.
Редуктаза является продуктом жизнедеятельности бактерий. Так как в только что выдоенном молоке ее нет – необходимо создать благоприятные условия для ее появления. Для этого берут пробу молока и разогревают ее до температуры 36-38ºС. Затем это молоко смешивают с красителем резазурином и ставят в термостат на 1-1,5 часа.
Редуктаза имеет свойство обесцвечивать краситель. Так со временем любое окрашенное молоко должно побледнеть, а молоко с малым количеством бактерий будет дольше сохранять свой цвет. Таким образом высший и первый сорт молока даже через полтора часа нахождения в термостате останутся сиреневого цвета, а несортовое молоко уже через час вернет белый оттенок. Результаты сравниваются по таблице.
Сорт молока
Продолжительность
нахождения
в термостате, мин.
Санитарный контроль
в пищевой промышленности
Общая микробная обсемененность объекта
Принято считать, что чем выше общая микробная обсемененность объекта внешней среды, тем больше вероятность присутствия в них патогенных бактерий.
Логическая обоснованность этого положения не вызывает сомнений, если его рассматривать в статистическом плане, тогда как во многих конкретных случаях оно может не соответствовать действительности. Например, несмотря на то, что молочнокислые продукты обильно обсеменены специфической микрофлорой, они являются не только полезными, но и обладают диетическими свойствами. И, напротив, незначительная обсемененность продукта или корма патогенными микробами в результату их использования может привести к тяжелым последствиям.
Попавшие на объект (субстрат) патогенные бактерии вступают с его микрофлорой в определенные взаимоотношения, часто антагонистические. Кроме того, и другие внешние факторы, например температура, рН среды, оказывают неблагоприятное действие на болезнетворные бактерии. В результате чего только в редких случаях они размножаются на субстрате или сохраняются в состоянии покоя, а гораздо чаще погибают. Опасность таких объектов для здоровья людей и животных зависит не только от степени обсеменения их болезнетворными микроорганизмами, но и от сроков, прошедших после заражения.
При определении общей микробной обсемененности воды, воздуха, пищевых продуктов необходимо учитывать исключительную динамичность этих объектов, неравномерность распределения микробов в них, а также возможность взаимного обмена между микрофлорой указанных объектов. Поэтому при исследовании надо соблюдать следующие правила: анализировать в нескольких повторностях возможно большее количество проб, взятых из разных участков объекта; использовать различные методы количественного учета микроорганизмов. При выполнении вышеприведенных условий полученные величины микробной обсемененности будут характеризовать объект в целом. В санитарно-бактериологических лабораториях для количественного учета микроорганизмов применяют в основном прямой подсчет микроорганизмов и определение микробного числа. Реже используют титрационный посев (метод предельных разведений).
Сапрофитные микробы — основные возбудители порчи пищевых продуктов, поэтому при оценке качества мясных и молочных продуктов определяют микробное число.
Следовательно, по микробному числу можно судить 0 санитарном состоянии почвы, воды, воздуха, пищевых продуктов.
Для некоторых объектов внешней среды разработаны нормы допустимой микробной обсемененности (микробное число), например: для воды питьевой — не более 100 микробов в 1 мл; для консервов «Мясо тушеное» до стерилизации — не более 200 тыс. бактерий в 1 г; для молока пастеризованного категории «А» — до 75 тыс. микробов в 1 мл. При отсутствии официальных норм допустимой микробной обсемененности, введенных в государственные общесоюзные стандарты (ГОСТы), технические условия (ТУ), заключение о доброкачественности продукта, о реализации или браковке его дают на основе практического опыта работы. Так, вареные колбасы I и II сортов считают хорошего качества, если общая микробная обсемененность их не превышает 1000 в 1 г.
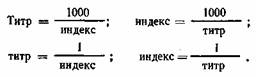
Микробную обсемененность объекта выражают в виде титра или индекса.
Титр —это наименьшее количество исследуемого субстрата, в котором обнаружен микроорганизм.
Индекс — количество клеток искомого микроорганизма, обнаруживаемого в определенном объеме исследуемого субстрата, например в 1000 мл воды, в 1 г почвы, в 1 г пищевых продуктов.
Пересчет титра в индекс и обратно производят следующим образом:
ГК «Униконс»
Продвижение и реализация комплексных пищевых добавок, антисептиков и др. продукции.
«Антисептики Септоцил»
Септоцил. Бытовая химия, антисептики.
«Петритест»
Микробиологические экспресс-тесты. Первые результаты уже через 4 часа.
«АльтерСтарт»
Закваски, стартовые культуры. Изготовление любых заквасок для любых целей.
Эндогенный путь обсеменения
Обсеменение органов и тканей микроорганизмами эндогенным путем может происходить при жизни животного или посмертно (после убоя).
Прижизненное обсеменение микроорганизмами наблюдается у животных, больных инфекционными заболеваниями, органы и ткани которых содержат возбудителя болезни. Распространение возбудителя по органам и тканям зависит от вида инфекции, ее течения и состояния организма больного животного. Так, при септических заболеваниях (сибирская язва, рожа свиней и др.) возбудитель сначала размножается в определенных тканях, а затем проникает в кровь и разносится по всем органам ив мышцы. При туберкулезе возбудитель чаще всего локализуется в одном или нескольких органах (легкие, вымя и др.), при лептоспирозе — преимущественно в почках и печени; при листериозе — главным образом в головном мозге и печени и т. д.
У здоровых животных эндогенное прижизненное микробное обсеменение органов и тканей происходит при ослаблении естественной сопротивляемости (резистентности) организма под влиянием различных неблагоприятных (стрессовых) факторов: утомления, голодания, переохлаждения или перегревания, травм и пр. При нормальном состоянии защитных сил животных стенка кишечника представляет собой почти непреодолимое препятствие для микроорганизмов. В результате снижения сопротивляемости организма создаются благоприятные условия для проникновения микроорганизмов из кишечника через лимфатические и кровеносные сосуды в органы и ткани, в том числе в мышцы. При этом могут проникать не только сапрофиты — постоянные обитатели кишечного тракта животных, но и некоторые патогенные бактерии, например сальмонеллы, носителями которых нередко являются сельскохозяйственные животные.
Наиболее часто эндогенное обсеменение тканей животных микроорганизмами происходит при утомлении, т. е. состоянии перенапряжения (стресса), возникающего при транспортировке или перегоне животных на мясокомбинаты. Внутренние органы и ткани животных, убитых сразу же после транспортировки по железной дороге, содержат в 3-4 раза больше микроорганизмов, чем у животных не утомленных, получивших предубойный отдых.
Степень эндогенного обсеменения микроорганизмами органов и тканей зависит от стадии утомления животных. У животных, убиваемых в состоянии резкого утомления, микроорганизмы содержатся почти во всех органах и тканях. Например, в продуктах убоя от сильно утомленного крупного рогатого скота почти всегда обнаруживают микроорганизмы в печени, селезенке, почках, легких, соматических и других лимфоузлах и довольно часто (до 30-40% случаев) в мышцах.
У крупного рогатого скота, имеющего незначительную степень утомления, микроорганизмы обычно выделяют только из печени и портального лимфоузла, мезентериальных лимфоузлов (в 30-50%) и легких (до 20% случаев). У свиней, убиваемых в степени незначительного утомления, микроорганизмы обнаруживают главным образом в печени (в 30%), паховых и подчелюстных лимфоузлах (в 20%), почках и селезенке (в 16-17% случаев).
Мышцы и соматические лимфоузлы животных, имеющих незначительную степень утомления, обычно не содержат микроорганизмов.
Степень утомления, а следовательно, и проникновения в ткани микроорганизмов из желудочно-кишечного тракта зависит от продолжительности и условий транспортировки животных.
При доставке животных автотранспортом на небольшие расстояния эндогенное обсеменение мышц и органов микроорганизмами незначительно.
После длительной транспортировки железнодорожным или водным транспортом в органах и тканях животных почти всегда содержится большое количество микроорганизмов, проникших из желудочно-кишечного тракта.
При транспортировке в жаркое время года, особенно в плохо вентилируемых, нагретых солнцем вагонах, у животных отмечается более высокая степень обсеменения микроорганизмами тканей, чем при транспортировке в прохладное время года (табл. 8).
Для приведения в нормальное физиологическое состояние здоровых, но утомленных в пути животных им предоставляется на мясокомбинатах предубойный отдых.
Восстановление естественных защитных сил и постепенное освобождение органов и тканей утомленных животных от проникших в них микробов из желудочно-кишечного тракта в значительной степени зависит от правильной организации предубойного отдыха (уход, условия содержания, кормления, поения).
У животных, находящихся перед убоем летом в незащищенных от солнца помещениях или зимой длительный срок на холоде (что приводит к переохлаждению организма), микроорганизмы, как правило, содержатся во всех внутренних органах, в лимфоузлах и мышцах. Если животных перед убоем содержат в крытых помещениях, в нормальных температурных условиях, то микроорганизмы обнаруживают главным образом в печени и портальном лимфоузле, иногда в других внутренних органах. Мышечная ткань и соматические лимфоузлы таких животных часто оказываются стерильными. У свиней, подвергавшихся перед убоем перегреву, бактерицидные свойства лимфы выражены слабо или совсем отсутствуют. Органолептические признаки порчи мяса, полученного от животных, перегретых или переохлажденных перед убоем, появляются на 1,5-2 сут раньше, чем мяса животных, содержавшихся перед убоем в нормальных условиях.
На степень микробного обсеменения внутренних органов и тканей животных во время предубойного отдыха влияют резкое ограничение поения, длительное голодание и сроки кормления перед убоем. Длительное голодание и недостаточный водопой способствуют проникновению микробов в ткани животных. Например, у крупного рогатого скота при голодании менее 1 сут наблюдается незначительное обсеменение органов и тканей микроорганизмами кишечного тракта. Начиная с 48 ч оно постепенно возрастает. После 7 дней голодания обсемененность мышц и внутренних органов Е. coli достигает 100%, а в отдельных случаях обнаруживают сальмонелл.
Кормление животных незадолго до убоя приводит к некоторому эндогенному обсеменению органов и тканей микробами из кишечного тракта. Так, при микробиологическом исследовании продуктов убоя животных, убитых через 4-6 ч после кормления, во всех случаях установлено наличие микроорганизмов в печени, почках, селезенке. Кроме того, у половины исследованных туш микроорганизмы обнаружены в крови, мышцах и костном мозге. Обсеменение микроорганизмами органов и тканей происходит также при травмах животных. В продуктах убоя животных с прижизненными механическими травмами степень обсеменения микроорганизмами лимфоузлов, внутренних органов и мышц значительно больше, чем животных, не имеющих травм.
В мышечной ткани, расположенной в нескольких сантиметрах от места травмы, содержится почти в 2 раза меньше гликогена, чем в мышечной ткани неповрежденной стороны туши. Вследствие нарушения процесса гликолиза в таких мышцах более интенсивно размножаются микроорганизмы.
При микробиологическом исследовании туш крупного рогатого скота, убитого с прижизненными механическими травмами, в поврежденных участках и в участках мышц, прилегающих к зоне повреждения на расстоянии до 10 см, выявляют бактерий группы кишечных палочек, стафилококков, вульгарного протея, диплококков и других микроорганизмов. Общая микробная обсемененность мышечной ткани с кровоизлияниями, гематомами, размозженными мышечными волокнами значительно больше, чем неповрежденных, симметрично расположенных мышц.
Посмертное эндогенное обсеменение органов и тканей начинается сразу после обескровливания, т. е. клинической смерти животных, так как в этом случае стенка кишечника становится легко проницаемой для микробов, содержащихся в кишечном тракте, и они проникают в окружающие ткани. Так, при удалении желудочно-кишечного тракта через 10-15 мин после обескровливания в 1 г мезентериальных лимфатических узлов здоровых свиней содержится в среднем 20 тыс. бактерий, а через 1 ч и более количество микроорганизмов составляет уже свыше 300 тыс. в 1 г.
Следовательно, для предотвращения обсеменения мяса и внутренних органов микроорганизмами необходимо как можно быстрее удалять кишечник из брюшной полости. При извлечении внутренних органов спустя 2 ч и более с момента обескровливания животных в ткани проникает большое количество микроорганизмов, в том числе патогенных и условно-патогенных бактерий. Поэтому в соответствии с действующими правилами ветеринарно-санитарной экспертизы мяса и мясопродуктов такие мясные туши подлежат обязательному микробиологическому исследованию.
Существует определенная зависимость между предубойным физиологическим состоянием организма животных, содержанием в их мышечной ткани гликогена и посмертным накоплением молочной кислоты (снижением рН) в процессе созревания мяса.
В мышечной ткани здоровых, упитанных животных содержится большое количество гликогена. В процессе созревания такого мяса происходит интенсивное накопление молочной кислоты и значительное снижение рН (табл. 9). Создаваемая в мясе таких животных кислая реакция среды тормозит или подавляет развитие гнилостных бактерий.
У животных больных, плохо упитанных, утомленных, т.е. убитых в состоянии резкого снижения резистентности организма, кроме прижизненного эндогенного микробного обсеменения органов и тканей наблюдается уменьшение количества гликогена в мышцах почти вдвое по сравнению с нормой. При созревании мяса таких животных посмертные окислительные процессы (т. е. накопление молочной кислоты) более замедленны по сравнению с процессами в мясе здоровых и отдохнувших животных. рН снижается незначительно (табл. 10).
Поскольку мясо, полученное от животных с пониженной сопротивляемостью организма, имеет после созревания более высокий рН, развитие гнилостных бактерий в нем подавляется слабо. В процессе хранения такое мясо быстрее портится.
ГК «Униконс»
Продвижение и реализация комплексных пищевых добавок, антисептиков и др. продукции.
«Антисептики Септоцил»
Септоцил. Бытовая химия, антисептики.
«Петритест»
Микробиологические экспресс-тесты. Первые результаты уже через 4 часа.
«АльтерСтарт»
Закваски, стартовые культуры. Изготовление любых заквасок для любых целей.
ЗАГРЯЗНЕНИЕ МИКРООРГАНИЗМАМИ И ИХ МЕТАБОЛИТАМИ
Загрязнение вызывает две формы заболеваний: пищевое отравление (пищевая интоксикация) и пищевую токсикоинфекцию.
ПИЩЕВАЯ ИНТОКСИКАЦИЯ:
ее вызывает токсин, продуцируемый микроорганизмом, который попадает и развивается в продуктах. Типичными примерами пищевой интоксикации являются стафилококковое отравление и ботулизм.
Пищевые интоксикации можно условно подразделить на бактериальные токсикозы и микотоксикозы.
Бактериальные токсикозы
В качестве примера можно привести стафилококковое пищевое отравление. Вызывается энтеротоксином, который продуцируется бактерией Staphylocосcus aureus (S. aureus) в период ее роста в пищевых продуктах. Идентифицировано шесть энтеротоксинов: A, B, C, D, E и F; выделены и получены две формы энтеротоксина С – С1 и С2.
Бактерия устойчива к нагреванию, сохраняет активность при 70 °С в течение 30 мин, при 80 °С – 10 мин. Еще более устойчивы к нагреванию энтеротоксины S. aureus, окончательная инактивация которых наступает только после 2,5-3 ч кипячения. S. aureus выдерживает высокие концентрации поваренной соли и сахара. Жизнедеятельность бактерии прекращается при концентрации хлорида натрия (поваренной соли) в воде более 12 %, сахара – 60 %, что необходимо учитывать при консервировании пищевых продуктов. При температуре 4-6 °С и ниже размножение S. aureus также прекращается. Оптимальная температура для размножения стафилококков – 22-37 °С.
Источником инфекции могут быть и человек, и сельскохозяйственные животные. Через последних заражается в основном молоко, мясо и продукты их переработки. У человека стафилококковая инфекция локализуется на кожных покровах, в носоглотке, кишечнике, других органах и тканях.
Попадая в продовольственное сырье, пищевые продукты и кулинарные изделия, стафилококки продуцируют токсины с различной интенсивностью, зависящей от уровня обсеменения, времени и температуры хранения, особенностей химического состава объекта загрязнения (содержание белков, жиров, углеводов, витаминов, pН среды и т. д.). Наиболее благоприятная среда для жизнедеятельности бактерий – молоко, мясо и продукты их переработки, поэтому именно эти пищевые продукты чаще вызывают стафилококковое отравление.
Молоко и молочные продукты
Загрязнение молока стафилококками может происходить от коров, больных маститом, при контакте с кожными покровами больных животных и человека, занятого переработкой молока. Отмечено, что стафилококки размножаются и продуцируют энтеротоксины в сыром молоке слабее, чем в пастеризованном, поскольку они являются плохим конкурентом в борьбе с другими микроорганизмами молока. Этим объясняется отсутствие энтеротоксинов и стафилококков в кисломолочных продуктах, для закваски которых используются активные молочные культуры. Кроме того, молочная кислота, образующаяся в процессе изготовления этих продуктов, тормозит размножение данных микроорганизмов.
Попадая в молоко, стафилококк начинает продуцировать энтеротоксины при комнатной температуре через 8 ч, при 35-37 °С – в течение 5 ч. При обсеменении стафилококками молодого сыра энтеротоксины выделяются на 5-й день его созревания в условиях комнатной температуры. По истечение 47-51 дня хранения сыра происходит гибель стафилококков, энтеротоксины же сохраняются еще в течение 10-18 дней.
В других молочных продуктах энтеротоксины можно обнаружить, если эти продукты были изготовлены из молока и молочных смесей, обсемененных стафилококками.
Мясо и мясные продукты
Загрязнение мяса стафилококками происходит во время убоя животных и переработки сырья. Как и в сыром молоке, конкурирующая микрофлора не дает возможности быстрого размножения этих бактерий в сыром мясе. В определенных технологических условиях, особенно при ликвидации конкурирующей микрофлоры, стафилококки могут активно размножаться в мясопродуктах и продуцировать энтеротоксины.
В мясном фарше, сыром и вареном мясе стафилококки продуцируют токсины при оптимальных условиях (22-37 °С) через 14-26 ч. Добавление в фарш белого хлеба увеличивает скорость образования токсических метаболитов в 2-3 раза. Концентрация соли, используемая для посола, не ингибирует S. aureus; уровень pН мяса и мясных продуктов, предотвращающий развитие бактерий, должен быть не выше 4,8. Копчение колбас при определенной температуре способствует росту стафилококков. В готовых котлетах, после их обсеменения, энтеротоксины образуются через 3 ч, в печеночном паштете – через 10-12 ч. Вакуумная упаковка мясопродуктов ингибирует рост стафилококков.
Для мяса птицы описанные выше данные аналогичны. Стафилококки не проникают и не растут в целых сырых яйцах. При тепловой обработке яиц их бактериостатические свойства уничтожаются, и они могут заражаться стафилококками в результате мойки и хранения.
Другие пищевые продукты
Благоприятной средой для размножения S. aureus являются мучные кондитерские изделия с заварным кремом. При обсеменении крема в условиях благоприятной для бактерий температуры (22–37 °С) образование токсинов наблюдается через 4 ч. Концентрация сахара в таких изделиях обычно составляет менее 50 %; содержание сахара в количестве 60 % и выше ингибирует образование энтеротоксинов.
Микотоксикозы
Наиболее распространенные и хорошо изученные микотоксикозы – афлатоксикоз (см. раздел 3.2.1), фузариотоксикоз и эрготизм.
Фузариотоксикозы
Согласно принятой в нашей стране классификации, к фузариотоксикозам относят следующие заболевания:
1. Алиментарно-токсическая алейкия – вызывается продуцентами микроскопических грибов Fusarium sporotrichiella var. Болезнь поражает как людей, так и сельскохозяйственных животных. Заболевание затрагивает кроветворные органы. У человека количество лейкоцитов снижается до 1000 и менее в 1 мм3, количество эритроцитов повышается до 1800 тыс., что служит наиболее ранними и объективными показателями алиментарно-токсической алейкии. Вспышки заболевания наблюдались у людей после употребления хлеба, изготовленного из пораженного зерна.
2. Отравление «пьяным хлебом». Болезнь обусловлена воздействием на организм токсического продуцента гриба Fusarium graminearum. Токсины гриба обладают нейротропным действием, сходным с действием алкоголя, отсюда и название болезни.
3. Уровская болезнь (болезнь Кашина – Бека). Впервые заболевание выявлено в 1860 г. Н. И. Кашиным у населения, проживающего в долине р. Уровы (Восточная Сибирь). В 1906 г. болезнь повторно зарегистрирована и изучена Е. В. Беком. Предполагают, что болезнь вызывается токсинами гриба Fusarium sporotrichiellavappoae, который поражает злаковые культуры. Болезнь проявляется в нарушении остеогенеза у детей, подростков и юношей, задержке роста отдельных костей, деформации скелета. Другая гипотеза связывает возникновение уровской болезни с высоким содержанием стронция в географической зоне проживания этих людей на фоне низкого содержания кальция.
Имеется ряд других данных по этиологии рассматриваемого заболевания, что свидетельствует о необходимости проведения специальных исследований и выявления истинных причин заболевания.
Эрготизм
Возникает при употреблении изделий из зерна, зараженного спорыньей. Последняя представляет собой склероции гриба Claviceps purpurea, содержит высокотоксичные алкалоиды (эрготоксин, эрготамин, эргометрин) и биогенные амины (гистамин, тирамин и др.). Эти соединения могут поражать нервную систему (судорожная форма) или нервно-сосудистый аппарат (гангренозная форма).
Ядовитые соединения спорыньи устойчивы при термической обработке и хранении хлебопродуктов. Гигиенические нормы допускают содержание спорыньи в муке не более 0,05 %.
Вопросам загрязнения пищевых продуктов микотоксинами и профилактики алиментарных микотоксикозов посвящен раздел 3.2.1.
ПИЩЕВАЯ ТОКСИКОИНФЕКЦИЯ: ее вызывают микроорганизмы – вирусы, сальмонеллы и др., – попавшие в продукт в большом количестве. Загрязнение пищевых продуктов происходит в основном бактериями, риккетсиями, вирусами, плесенями и паразитами.
Clostridium perfringens – спорообразующие анаэробные грамположительные бактерии, широко распространенные в природе вследствие своей стойкости к различным воздействиям. Вегетативные клетки бактерий имеют вид прямых толстых палочек размером 2–6 × 0,8–1,5 мкм. Изучено шесть штаммов Cl. perfringens: A, B, C, D, E и F, которые продуцируют многообразные по своим свойствам токсины. Пищевую токсикоинфекцию вызывают главным образом штаммы А и D. Токсикологическую картину при этом определяет А-токсин. Cl. perfringens развивается при температуре от 15 до 50 °С и рН 6,0–7,5. Оптимальные температура 45 °С и рН 6,5 обеспечивают продолжительность генерации около 10 мин. Энтеротоксины высвобождаются из вегетативных клеток в период образования из этих клеток зрелых спор. Это может происходить и в пищевых продуктах, и в кишечнике человека.
Источником заболевания служат в основном продукты животного происхождения – мясные и молочные, обсеменение которых происходит как при жизни животных (больных и бациллоносителей), так и после убоя (при нарушении санитарно-гигиенических норм переработки и хранения сырья). Источниками инфекции могут быть рыба и морепродукты, бобовые, картофельный салат, макароны с сыром.
После попадания инфекции в организм инкубационный период длится от 5 до 22 ч. Характерные признаки заболевания – понос, спазмы и боли в животе.
Профилактические мероприятия предусматривают соблюдение санитарно-гигиенических требований при переработке сырья, хранении готовой продукции.
Бактерии рода Salmonella. Изучено более 2000 серологических типов сальмонелл. Бактерии представляют собой грамположительные палочки, не образующие спор, длиной от 2 до 3 мкм и шириной около 0,6 мкм.
Существует три основных типа сальмонеллеза: брюшной тиф, гастроэнтерит и септицемия. Каждый штамм сальмонеллы способен вызвать любой из указанных выше клинических типов инфекции.
80-90 % сальмонеллезов вызывается четырьмя видами этих бактерий. Сальмонеллы характеризуются устойчивостью к воздействию различных физико-химических факторов. Растут при температуре от 5,5 до 45 °С, оптимальная – 37 °С. Сохраняют жизнеспособность при охлаждении до 0 °C в течение 142 дней, при температуре 10 °С – 115 дней. Нагревание до 60 °С приводит к гибели сальмонелл через 1 ч, при 70 °С – через 15 мин, при 75 °С – 5 мин, при кипячении наступает мгновенная гибель.
Заражение пищевых продуктов сальмонеллами может происходить как через животных, так и через человека.
Основные пищевые продукты, передающие сальмонеллезные токсикоинфекции, – мясо и мясопродукты, обсеменение которых осуществляется и при жизни животных, и после их убоя.
Животные, больные сальмонеллезами, выделяют сальмонеллы с молоком, следовательно, молоко и молочные продукты также способствуют распространению сальмонеллезных токсикоинфекций. Кроме того, переносчиками сальмонелл могут быть работники пищевых предприятий, болеющие скрытыми формами сальмонеллезов или являющиеся бактерионосителями.
Особую роль в этиологии сальмонеллеза играют прижизненно зараженные пищепродукты: яйца, мясо уток, гусей, кур, индеек.
1. Работа ветеринарно-санитарной службы непосредственно в хозяйствах по выявлению животных и птицы, больных сальмонеллезом.
2. Проведение санитарно-ветеринарной экспертизы во время первичной переработки сырья и изготовления продуктов питания.
Необходимо соблюдать санитарные требования по размораживанию мяса, хранить сырье и полуфабрикаты при температуре не выше 4–8 °С, использовать холод на всех этапах производственного процесса, включая транспортировку сырья, полуфабрикатов и готовой продукции, соблюдать сроки реализации, установленные для каждого продукта, а также режимы тепловой обработки. Последнее имеет принципиальное значение в предупреждении сальмонеллезных токсикоинфекций, учитывая губительное действие нагревания (не ниже 80 °С) на бактерии. Не разрешается реализация населению некипяченого и непастеризованного молока.
3. Осуществление систематической борьбы с грызунами как источником обсеменения сырья и продуктов на пищевых предприятиях.
4. Соблюдение соответствующих санитарных требований в отношении воды, льда, инвентаря, посуды и оборудования.
5. На предприятиях пищевой промышленности и общественного питания:
Пункты 3–5 имеют значение в профилактике заражения сальмонеллезом продуктов растительного происхождения, хотя такие случаи встречаются редко.
Бактерии рода Escherichia coli. Патогенные штаммы кишечной палочки способны размножаться в тонком кишечнике, вызывая токсикоинфекцию (основной симптом болезни – водянистый понос). Источником патогенных штаммов могут быть люди и животные. Обсеменяются продукты и животного, и растительного происхождения. Пути заражения те же, что и при сальмонеллезах.
1. Выявление и лечение работников пищевых предприятий – носителей патогенных серотипов кишечной палочки.
2. Осуществление ветеринарного надзора над животными. Мясо животных, больных колибацеллезом, считается условно годным и подлежит специальной тепловой обработке.
3. Выполнение санитарных норм и режимов технологии изготовления и хранения пищевых продуктов.
4. Соблюдение санитарного режима на предприятии (мытье и дезинфекция инвентаря и оборудования и т. д.).
Бактерии рода Proteus. Род Proteus включает пять видов. Возбудители пищевых токсикоинфекций – в основном Pr. mirasilis и Pr. vulgaris. Оптимальные условия для развития этих бактерий – температура 25–37 °С. Выдерживают нагревание до 65 °С в течение 30 мин, рН в пределах 3,5–12, отсутствие влаги – до 1 года, высокую концентрацию поваренной соли (13–17 %) – в течение 2 суток. Все это свидетельствует об устойчивости Proteus к воздействию внешних факторов среды.
Причинами возникновения протейных токсикоинфекций могут быть наличие больных сельскохозяйственных животных, антисанитарное состояние пищевых предприятий, нарушение принципов личной гигиены. Основные продукты, через которые передается это заболевание, – мясные и рыбные изделия, реже блюда из картофеля. Отмечены случаи заражения других пищевых продуктов.
Энтерококки. Потенциально патогенными штаммами среди энтерококков (Streptococcus faecalis) являются Str. faecalis var. Liguefaciens и Str. faecalis var. Zumogenes. Размножаются при температуре от 10 до 15 °С. Устойчивы к высыханию, воздействию низких температур, выдерживают 30 мин при 60 °С; погибают при 85 °С в течение 10 мин.
Источники инфекции – человек и животные. Пути обсеменения пищевых продуктов такие же, что и при других видах токсикоинфекций.
Ботулизм – представляет собой тяжелое пищевое отравление, вызывается токсинами, выделяемыми Clostridium botulinum. Изучено семь видов токсинов – А, В, С, D, Е, F и G. Наиболее токсичны ботулотоксины А и Е.
Бактерии Cl. botulinum широко распространены в окружающей среде. В виде спор попадают в почву при удобрении ее навозом, поэтому продукты растительного происхождения загрязняются спорами через почву.
Споры, по сравнению с вегетативной формой Cl. botulinum, устойчивы к воздействию физико-химических факторов окружающей среды. При 100 °С
они сохраняют жизнеспособность в течение 6 ч, при 120 °С – 10 мин. Споры прорастают при концентрации хлорида натрия до 6–8 %. Размножение бактерий прекращается при рН 4,4 и температуре 12–10 °С и ниже, при 80 °С они погибают в течение 15 мин. Оптимальной для жизнедеятельности Cl. botulinum является температура 20-37 °С.
Ботулотоксины характеризуются высокой устойчивостью к действию протеолитических ферментов, кислот и низких температур, однако инактивируются под влиянием щелочей и высокой температуры: при 80 °С – через 30 мин, при 100 °С – через 15 мин.
Описанные свойства вегетативных форм Cl. botulinum, спор и токсинов должны учитываться в технологии изготовления пищевых продуктов.
1. Предупреждение загрязнения туш сельскохозяйственных животных частицами земли, навоза, а также в процессе их разделки – содержимым кишечника; посол в условиях холода; соблюдение режимов термической обработки.
2. Использование свежего растительного сырья; предварительная мойка и тепловая обработка; стерилизация продукта с целью предупреждения прорастания cпор, размножения вегетативных форм и образования токсинов.
3.2.1. Микотоксины в пищевых продуктах, профилактика алиментарных микотоксикозов
Микотоксины (от греч. mỳkēs – гриб) (МТ) представляют собой вторичные метаболиты микроскопических плесневых грибов. Из кормов и продуктов питания выделено около 30 тыс. видов плесневых грибов, большинство из которых продуцируют высокотоксичные метаболиты, в частности более 120 микотоксинов. С биологических позиций, микотоксины выполняют в обмене микроскопических грибов функции, направленные на их выживание и конкурентоспособность в борьбе за место в различных экологических нишах. С гигиенических позиций – это особо опасные токсичные вещества, загрязняющие корма и пищевые продукты.
По данным ФАО, более 10 % пищевых продуктов и кормов ежегодно теряется вследствие поражения плесневыми грибами.
В продуктах питания и продовольственном сырье наиболее распространены следующие высокотоксичные МТ: афлатоксины, стеригматоцистин, охратоксины, патулин, исландитоксин, зеараленон, рубратоксины, цитреовиридин и др. В табл. 24 представлены сведения об изученных в настоящее время мико-
токсинах, их продуцентах и о характере токсического действия.
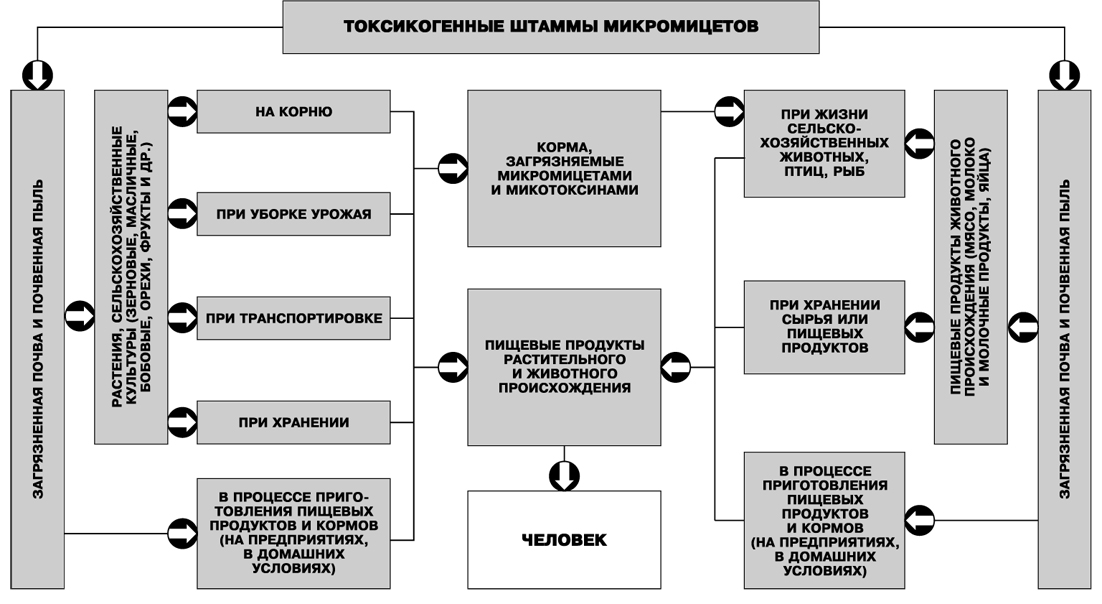
На рис. 9 показаны пути загрязнения пищевых продуктов токсигенными штаммами микромицетов и микотоксинами.
Рассмотрим наиболее типичных токсичных представителей микотоксинов, а также микотоксикозы, которые они вызывают.
Рис. 9. Основные пути загрязнения пищевых продуктов токсигенными штаммами микромицетов и микотоксинами
Основные сведения о микотоксинах
Афлатоксины (АТ). Наиболее опасны и лучше изучены. Продуцируются главным образом грибами Aspergillius flavus и A. parasiticus. К семейству АТ относится более 20 соединений, 4 из которых – основные: В1, В2, G1, G2. Остальные – их производные или метаболиты. Наиболее токсичные и широко распространенные АТ – В1.
Немаловажный интерес в плане загрязнения пищевых продуктов представляет АТ М1, который является метаболитом АТ В1 и выделяется с молоком у животных после употребления зараженного корма.
АТ характеризуются широким спектром токсического действия (см. табл. 24), ЛД50 (летальная доза – наименьшая доза, вызывающая смертность 50 % подопытных животных) АТ В1 для человека составляет около 2 мг на 1 кг массы тела.
Заболевание, вызываемое АТ, получило название афлатоксикоз. Основную роль в механизме токсического действия АТ играет нарушение проницаемости мембраны субклеточных структур и подавление синтеза ДНК и РНК. Последнее приводит к нарушению синтеза митохондральных белков и липидов, других обменных процессов, что проявляется в ряде серьезных клинических заболеваний.
Наряду с общетоксическим действием проявляется канцерогенная, мутагенная (генные и хромосомные мутации), тератогенная, гонадотоксическая и эмбриотоксическая активность АТ, что делает проблему профилактики алиментарных афлатоксинов особо актуальной.
Качественный и количественный состав рациона оказывает значительное влияние на токсический эффект АТ. Этот эффект усиливается при дефиците белков, незаменимых жирных кислот и ретинола. При избытке белков также наблюдается усиление канцерогенного действия, что объясняется снижением активности эпоксидгидролазы и глутатионтрансферазы – ферментов, ответственных за детоксикацию АТ и их метаболитов.
Согласно данным ВОЗ, человек при благоприятной гигиенической ситуации потребляет с суточным рационом не более 0,19 мкг АТ, что не оказывает отрицательного воздействия на организм. Однако чем выше суточная доза АТ (например, в Мозамбике – до 15,5 мкг), тем вероятнее заболеваемость первичным раком печени.
В России ПДК АТ В1 для всех пищевых продуктов, кроме молока, составляет 5 мкг/кг, для молока и молочных продуктов – 1 мкг/кг; АТ М1 – 0,5 мкг/кг.
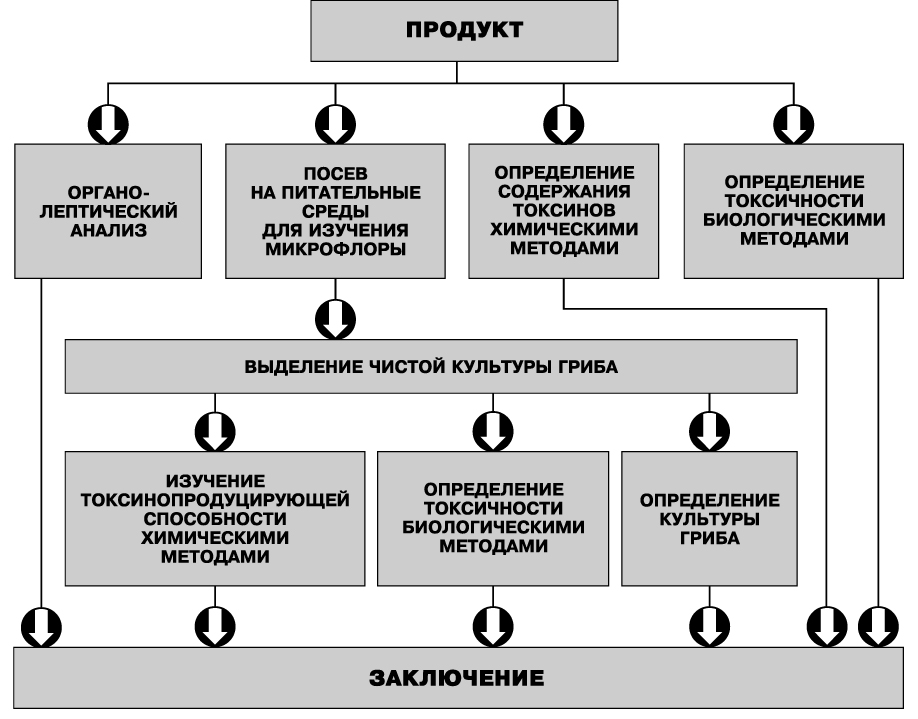
Рис. 10. Санитарно-микологический анализ пищевых продуктов
как часть системы мер профилактики микотоксикозов
Допустимая суточная доза этих веществ для взрослого человека массой 60 кг – в пределах 0,3–0,6 мкг (0,005–0,010 мкг/кг массы тела).
Патулин, продуцируемый пенициллами и аспергиллами, обнаруживается преимущественно в продуктах, полученных из заплесневелых фруктов и ягод. Во фруктовых и овощных соках, пюре для взрослых показатель ПДК патулина составляет 50 мкг/кг, для детского питания – 20 мкг/кг.
Система мер профилактики микотоксикозов включает в себя санитарно-микологический анализ пищевых продуктов (рис. 10). Кроме этого, много внимания уделяется изысканию способов деконтаминации и детоксикации сырья и пищевых продуктов, загрязненных АТ. С этой целью используют механические, физические и химические методы:
Механические и физические методы очистки нельзя считать высокоэффективными, кроме того, химические методы вызывают разрушение не только АТ, но и полезных нутриентов, а также приводят к нарушению их всасывания.
Допустимые уровни содержания микотоксинов в отдельных группах пищевых продуктов
При профилактике алиментарных микотоксикозов основное внимание уделяют зерновым культурам. В этой связи необходимо соблюдать следующие меры по предупреждению загрязнения зерновых культур и пищевых продуктов:
Важной задачей является выведение сортов, устойчивых к аспергиллам. Допустимые уровни содержания микотоксинов в отдельных группах пищевых продуктов представлены в табл. 25.
Установленные медико-биологическими требованиями и санитарными нормами качества продовольственного сырья и пищевых продуктов критерии безопасности включают определение следующих четырех групп микроорганизмов:
I группа – санитарно-показательные микроорганизмы. Определение мезофильных аэробных и факультативно-анаэробных микроорганизмов, что выражается количеством колониеобразующих единиц (КОЕ) в 1 г или 1 см 3 продукта. Показатель «Бактерии группы кишечных палочек» (БГКП) практически идентичен показателю «Колиформные бактерии». К этой группе относят грамотрицательные, не образующие спор палочки с учетом как цитратотрицательных, так и цитратположительных вариантов БГКП, включая роды: Escherichia, Klebsiella, Enterobacter, Citrobacter, Serratia.
II группа – потенциально патогенные микроорганизмы: коагулазоположительный стафилококк, Bacillus cereus, сульфитредуцирующие клостридии, бактерии рода Protea, парагемолитические галофильные вибрионы.
III группа – патогенные микроорганизмы, в том числе сальмонеллы.
Микробиологические исследования проводят в соответствии с ГОСТ, СанПиН, методическими указаниями, методическими инструкциями, другими нормативными документами, содержащимися в медико-биологических требованиях (МБТ).