Октетная теория
Правило октета (октетная теория) — предложено Г.Н. Льюисом для объяснения причин образования ковалентных химических связей. Согласно этому правилу при образовании молекул атомы удовлетворяют свою потребность в достижении 8 электронной валентной оболочки, подобной электронной конфигурации благородных газов за счет попарного обобществления своих валентных электронов. По своей важности это фундаментальное открытие Льюиса стоит в одном ряду с такими открытиями, как Периодический закон элементов и теория строения органических соединений. Широко распространенное мнение, что правило октета выполняется лишь в ограниченном числе случаев также ошибочно, как и утверждение того, что Периодический закон элементов не имеет всеобщего характера. Все примеры «невыполнения» правила октетов можно подразделить на следующие три группы:
2. Молекула образуется за счет трехцентровых связей, например KI3. В этой молекуле анион иода связан с молекулой иода трехцентровой четырехэлектронной связью. Молекула B2H6 построена за счет образования трехцентровых двухэлектронных связей Н-В-Н.
3. В образовании химических связей принимают участие d-орбитали. В этом случае правило октетов (в пределе, т.е. в случае участия всех пяти d-орбиталей) преобразуется в правило 18-электронов. Поскольку в целом ряде случаев участие d-орбиталей в образовании химических связей у некоторых элементов остается спорным вопросом, возникает иллюзия невыполнения правила октетов. Классическими примерами выполнения правила 18-электронов являются молекулы Fe(CO)5, Ni(CO)4, Co2(C)8, Fe(C5H5)2 (ферроцен).
История
В конце XIX века стало известно, что координационные структуры формируются атомами или молекулами таким образом, чтобы максимально удовлетворить валентность задействованных атомов. В 1893 Альфред Вернер показал, что число атомов или их групп, ассоциированных с центральным, часто равно 4 или 6, реже 8. В 1904 году Ричард Абегг сформулировал правило (известное как правило Абегга), утверждавшее, что максимальная разница между положительной и отрицательной валентностью элемента часто равна 8. Используя его Гилберт Ньютон Льюис в 1916 году записал правило октета для своей теории кубического атома.
Обзор
Валентная оболочка элемента полна и наиболее устойчива, если содержит 8 электронов (что является причиной низкой химической активности благородных газов).
Правило октетов
Правило октета (октетная теория) — предложено Г.Н. Льюисом для объяснения причин образования ковалентных химических связей. Согласно этому правилу при образовании молекул атомы удовлетворяют свою потребность в достижении 8 электронной валентной оболочки, подобной электронной конфигурации благородных газов за счет попарного обобществления своих валентных электронов. По своей важности это фундаментальное открытие Льюиса стоит в одном ряду с такими открытиями, как Периодический закон элементов и теория строения органических соединений. Широко распространенное мнение, что правило октета выполняется лишь в ограниченном числе случаев также ошибочно, как и утверждение того, что Периодический закон элементов не имеет всеобщего характера. Все примеры «невыполнения» правила октетов можно подразделить на следующие три группы:
2. Молекула образуется за счет трехцентровых связей, например KI3. В этой молекуле анион иода связан с молекулой иода трехцентровой четырехэлектронной связью. Молекула B2H6 построена за счет образования трехцентровых двухэлектронных связей Н-В-Н.
3. В образовании химических связей принимают участие d-орбитали. В этом случае правило октетов (в пределе, т.е. в случае участия всех пяти d-орбиталей) преобразуется в правило 18-электронов. Поскольку в целом ряде случаев участие d-орбиталей в образовании химических связей у некоторых элементов остается спорным вопросом, возникает иллюзия невыполнения правила октетов. Классическими примерами выполнения правила 18-электронов являются молекулы Fe(CO)5, Ni(CO)4, Co2(C)8, Fe(C5H5)2 (ферроцен).
История
В конце XIX века стало известно, что координационные структуры формируются атомами или молекулами таким образом, чтобы максимально удовлетворить валентность задействованных атомов. В 1893 Альфред Вернер показал, что число атомов или их групп, ассоциированных с центральным, часто равно 4 или 6, реже 8. В 1904 году Ричард Абегг сформулировал правило (известное как правило Абегга), утверждавшее, что максимальная разница между положительной и отрицательной валентностью элемента часто равна 8. Используя его Гилберт Ньютон Льюис в 1916 году записал правило октета для своей теории кубического атома.
Обзор
Валентная оболочка элемента полна и наиболее устойчива, если содержит 8 электронов (что является причиной низкой химической активности благородных газов).
Объясните языком даунов, что такое правило Октета (химия)
Правило октета (октетная теория) — предложено Г. Н. Льюисом для объяснения причин образования ковалентных химических связей. Согласно этому правилу при образовании молекул атомы удовлетворяют свою потребность в достижении 8 электронной валентной оболочки, подобной электронной конфигурации благородных газов за счет попарного обобществления своих валентных электронов. По своей важности это фундаментальное открытие Льюиса стоит в одном ряду с такими открытиями, как Периодический закон элементов и теория строения органических соединений. Широко распространенное мнение, что правило октета выполняется лишь в ограниченном числе случаев также ошибочно, как и утверждение того, что Периодический закон элементов не имеет всеобщего характера. Все примеры «невыполнения» правила октетов можно подразделить на следующие три группы:
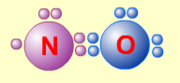
1. Сумма валентных электронов атомов, образующих молекулу, нечётна. Пример — молекула оксида азота NO.
Nitrogen oxide.png
В данном случае сумма валентных электронов атома азота (5) и кислорода (6) равна 11, поэтому в этой молекуле атом кислорода достигает восьмиэлектронной оболочки, а атом азота — нет. В данном случае изначально невозможно достижение обоими атомами восьмиэлектронной оболочки. Стремление атома азота заполнить свою электронную оболочку объясняет химическую реакционную способность этой молекулы.
2. Молекула образуется за счет трехцентровых связей, например KI3. В этой молекуле анион иода связан с молекулой иода трехцентровой четырехэлектронной связью. Аналогичные трехцентровые, но двухэлектронные связи присутствуют в молекуле B2H6.
3. В образовании химических связей принимают участие d-орбитали. В этом случае правило октетов (в пределе, то есть в случае участия всех пяти d-орбиталей) преобразуется в правило 18-электронов. Поскольку в целом ряде случаев участие d-орбиталей в образовании химических связей у некоторых элементов остается спорным вопросом, возникает иллюзия невыполнения правила октетов. Классическими примерами выполнения правила 18-электронов являются молекулы Fe(CO)5, Ni(CO)4, Co2(СО) 8, Fe(C5H5)2 (ферроцен) и многие другие.
Таким образом, главным в правиле октетов Льюиса является не цифра 8 (или 18), а обобществление электронов как основа образования ковалентной химической связи, и приближение за счет этого к электронной конфигурации инертного газа — восьмиэлектронной или восемнадцатиэлектронной.
«Согласно этому правилу при образовании молекул атомы удовлетворяют свою потребность в достижении 8 электронной валентной оболочки, подобной электронной конфигурации благородных газов за счет попарного обобществления своих валентных электронов. «
Правило октета
Атомы стремятся отдавать или принимать электроны до тех пор, пока в их внешнем слое не станет 8 электронов.
Расположение химических элементов в периодической системе Менделеева объясняется тем, как электроны заполняют доступные энергетические уровни, или слои, в атоме. Например, благородные газы, такие как неон, ксенон и аргон, имеют во внешнем слое по 8 электронов (то есть слой заполнен) — и поэтому они неохотно вступают в химические реакции. Самое низкое энергетическое состояние (и, следовательно, самое устойчивое) в большинстве случаев имеют атомы с заполненным внешним электронным слоем. На этом и построено правила октета.
Правило октета объясняет, как атомы образуют ионы. Рассмотрим в качестве примера натрий. В его атоме 11 электронов: два во внутреннем слое, восемь в следующем и один во внешнем слое. Этот внешний электрон очень подвижен, поэтому, если атому натрия передается энергия (например, в результате столкновения с другим атомом), он легко образует ион натрия с единичным положительным зарядом. Чтобы удалить электрон с внутреннего слоя, энергии потребуется в десять раз больше, поэтому ион натрия с двойным положительным зарядом — большая редкость. Точно так же кальций, имеющий 2 электрона во внешнем слое и 8 в следующем, более низком слое, образует ион, теряя 2 электрона. То есть, когда атомы превращаются в ионы, они по строению становятся похожи на атомы благородных газов.
Правило октета помогает нам понять, как устроены химические связи. Но оно работает далеко не для всех элементов. Например, олово имеет во внешнем незаполненном слое 14 электронов, но может отдавать только 2 или 4 электрона: отрыв большего количества электронов потребовал бы непомерных затрат энергии. Поэтому олово образует ионы с положительным зарядом 2 или 4.
Правило октета — одно из тех правил, которые отражают на первый взгляд случайные закономерности, выведенные химиками из опыта и наблюдений. Однако эти закономерности легко могут быть объяснены в терминах атомной теории строения вещества.
Правило октета. Почему образуется связь?
Химическая связь — это взаимодействие атомов, осуществляемое путем обмена электронами.
Причина образования химических связей – выигрыш в энергии системы связанных атомов по сравнению с изолированными атомами.
При образовании химической связи атомы стремятся приобрести устойчивую восьмиэлектронную (или двухэлектронную) внешнюю оболочку, соответствующую строению атома ближайшего инертного газа.
Движущей силой, заставляющей атомы соединяться между собой, является стремление принять, отдать или объединить электроны с тем, чтобы получить полностью заполненную внешнюю электронную оболочку. У водорода Н и гелия Не внешняя электронная оболочка представляет собой 1s-орбиталь, для заполнения которой требуется два электрона (вспомним, что первый электронный слой не имеет р-орбиталей).

Электронная конфигурация атома особенно стабильна (иными словами, имеет минимальный запас энергии, что всегда предпочтительно), когда внешняя электронная оболочка заполнена. Поэтому атомы склонны к таким превращениям, в результате которых во внешнем слое оказывается „магическое” число электронов — восемь. Исключение составляют атомы первых двух элементов периодической системы, для которых предпочтительно образование двухэлектронной внешней оболочки.
Правило октета объясняет, почему инертные газы (группа VIIIA) гелий, неон и аргон обычно не вступают в химические реакции. Их внешняя электронная оболочка уже заполнена, следовательно нет необходимости во взаимодействии с другими атомами с целью принять, отдать или объединить электроны.
Элементы 3—7-го периодов также обычно подчиняются правилу октета (т. е. склонны к заполнению s- и р-орбиталей, хотя могут иметься d- и f-орбитали).
Согласно правилу октета большинство атомов склонно принимать, отдавать или объединять электроны с тем, чтобы создать восьмиэлектронную внешнюю оболочку.