Методы исследования в химии
Цель курсовой или дипломной по химии — это конечная точка, к которой должен прийти студент в своём исследовании. Задачи — пункты, составляющие маршрут. А методы — способы, которые помогают успешно справиться со всеми вызовами в пути и достичь поставленной цели.
А какие именно теоретические и экспериментальные методы исследования чаще всего используют в химии? В чём их особенности и отличия от других? Обо всё этом расскажем в статье, а также приведём примеры, как применяют методы исследования в химии.
Не забудьте подписаться на наш информационный канал в Telegram — в нём мы публикуем актуальные и полезные новости. И следите за акциями и скидками от компании.
Доверь свою работу кандидату наук!
Узнать стоимость бесплатно
Методы исследования в химии: определение и классификация
Методы исследования: определение понятия
Прежде чем мы рассмотрим, какие современные методы исследования используют в химии, давайте дадим научное определение этому понятию:
Методы исследования — это способы познания в научно-исследовательских работах, которые включают в себя специфические методики, приёмы и подходы. Все методы, используемые в процессе, составляют методологическую базу исследования.
Классификация современных методов исследования в химии
Химия — практическая наука. Именно поэтому большинство работ по этой научной дисциплине имеют экспериментально-аналитический характер. Соответственно большинство методов исследования веществ, соединений, реакций и явлений в химии относятся к эмпирическим.
Для удобства мы разделили самые популярные методы исследования на три большие группы:
Проводя химические опыты, соблюдайте правила безопасности
Первые две группы методов встречаются в методологиях других наук, а специальные, или узкоспециализированные — только в химических исследованиях.
В химии применяют разные методы, в том числе и междисциплинарные. Это методологические приёмы, которые решают задачи смежных наук. Например, физико-химический анализ подходит для физических, химических, биологических и даже исторических исследований.
Методы научного исследования в химии: описание
Чтобы выбрать методы, которые лучше всего помогут раскрыть тему вашего исследования, стоит разобраться, что они из себя представляют и для каких задач применяются.
Общенаучные теоретические методы исследования в химии
Самыми востребованными теоретическими методами в химии являются:
Кстати! Для наших читателей сейчас действует скидка 10% на любой вид работы.
Метод наблюдения
Наблюдение — это внешнее изучение определённых химических явлений или веществ. Как правило, чтобы этот метод был эффективным, исследователь должен соблюдать следующие условия:
Только соблюдая условия, можно получить чёткие результаты и не запутаться в большом количестве данных.
Пример: провести наблюдение за химической реакцией сульфита меди и хлорида натрия.
Метод описания
Метод описания в химии чаще всего дополняет другие методы. С его помощью перечисляют основные признаки веществ и изображают химически проведённые опыты.
Пример: описать состав комплексных химических соединений тетрафторобериллат (II) калия и тетрагидридоалюминат (III) лития.
Метод моделирования
В химии далеко не все химические реакции можно провести в лаборатории. Для сложных явлений используют метод моделирования. С его помощью создают модели, по которым проверяют выдвинутые гипотезы.
Применяют две группы моделей:
Пример: провести молекулярное моделирование структурного состава атома водорода.
Метод абстрагирования
Метод абстрагирования применяют, когда необходимо отбросить несущественные показатели и более подробно исследовать общие закономерности химических веществ и явлений.
Пример: изучить общие свойства неорганических веществ.
Общенаучные эмпирические методы исследования в химии
К методам экспериментальных исследований в химии относят:
Метод эксперимента
Чем отличается эксперимент от наблюдения? Тем, что экспериментальные опыты — это всегда активное воздействие на изучаемый материал. Эксперимент проводят в контролируемых условиях и используют для практической части исследования.
Пример: провести химические опыты, позволяющие очистить загрязненную поваренную соль.
Метод измерений
Без метода измерений в химической науке никуда. Ведь мало просто провести научный эксперимент и описать реакцию. Надо понимать, какие показатели измерять и как их сравнивать, чтобы делать правильные выводы.
Пример: измерить физико-химические показатели горючего.
Важный этап любого опыта — записать выполненные измерения
Метод анализа
Аналитические методы в современных исследованиях химии очень важны. Они помогают изучать химические вещества с разных сторон, специально проводить нужные реакции и получать обоснованные выводы.
Пример: провести сравнительный анализ методов получения бутандиола-1,4.
В химии существует большое количество различных видов анализа. Их можно смело отнести к следующей группе методов — специальных.
Существует даже целая отдельная отрасль — аналитическая химия, в которой существуют собственные методы исследования: методы разделения и концентрирования, метод испарения, гравиметрический анализ, титриметрический анализ, хроматографические методы и так далее.
Метод синтеза
Метод синтеза в химии помогает получать новые вещества в процессе химических реакций. Он также важен, как и анализ. Его часто применяют в качестве метода исследования в органической химии.
Пример: описать историю химического синтеза и его важное значение для науки.
Специальные методы исследования в химии
К специальным в химии относятся методы исследования, которые обладают практическим характером. Их применение связано с изучением количественного состава и химических свойств различных соединений.
Таких методов довольно много, но условно их можно разделить на три большие группы:
Физические методы исследования в химии
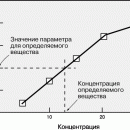
Физические методы в химии — это методы исследования, которые изучают физические параметры химических веществ. Среди наиболее часто встречающихся физических методов можно назвать:
Пример: определить, как изменилось излучение после воздействия на разные химические вещества.
Классические методы исследования в химии
Классические методы исследования помогают изучать химические растворы, газы, тела и другие элементы через различные виды реакций. Существует несколько разновидностей данных методических приёмов:
Пример: решить ряд химических уравнений, в ходе которых необходимо вычислить количество вещества, исходя из его объёма в газообразном состоянии.
Физико-химические методы исследования в химии
Физико-химические методы позволяют исследователю наблюдать и фиксировать, какие физические изменения происходят в веществах после того, как произошла химическая реакция. Среди них:
Резонансные методы исследования в химии
Самые известные методологические приёмы в этой группе — это резонансные методы исследования в химии:
Резонансные методы помогают изучить структурные и динамические изменения в молекулах, ионах и других элементах в различных химических фазах, например, в конденсированной или газообразной.
Пример: изучить, как распределяются электроны в молекулах с помощью резонансного метода исследования.
Магниторезонансный метод лежит в основе МРТ
Метод гигиенического исследования в химии
К физико-химическим методам также относится метод гигиенического исследования. Его применение связано с очень практическими целями:
Пример: провести санитарно-химический анализ воды, позволяющий оценить уровень хлора, сульфата и хлорида в составе.
Как выбирать методы исследования в химии
Практически любое грамотное химическое исследование строится на пяти основных этапах:
Поэтому и методологию стоит составлять из методов, которые помогут на каждом этапе всесторонне изучить объект и получить конкретные результаты.
Например, выбирая физико-химические методы исследования в органической химии, не забывайте об основе — теоретическом наблюдении и анализе химических материалов, полученных экспериментально.
Мы разобрали некоторые методы исследований, которые применяют в органической и неорганической химии. Теперь у вас есть хороший инструментарий, чтобы провести свою исследовательскую работу. А если нет времени писать лабораторную, курсовую или диплом по химии самостоятельно, обращайтесь в студенческий сервис. Наши специалисты помогут определиться с методами исследования и сдать работу даже по самой сложной теме точно в срок.
«Я видала такую чепуху, по сравнению с которой эта чепуха — толковый словарь» (Льюис Кэрролл «Алиса в стране чудес»). Любительница йоги, спиральной динамики и душевных разговоров 😊
ХИМИЯ
Смотреть что такое «ХИМИЯ» в других словарях:
ХИМИЯ — (греч. chymeia, от chymos сок). Отрасль естествоведения, исследующая природу и свойства простых тел, частичное влияние этих тел друг на друга и соединения, являющиеся следствием этого влияния. Словарь иностранных слов, вошедших в состав русского… … Словарь иностранных слов русского языка
ХИМИЯ — ХИМИЯ, наука о веществах, их превращениях, взаимодействии и о происходящих при этом явлениях. Выяснением основных понятий, к рыми оперирует X., как напр, атом, молекула, элемент, простое тело, реакция и др., учением о молекулярных, атомных и… … Большая медицинская энциклопедия
ХИМИЯ — (возможно от греч. Chemia Хемия, одно из древнейших названий Египта), наука, изучающая превращения веществ, сопровождающиеся изменением их состава и (или) строения. Химические процессы (получение металлов из руд, крашение тканей, выделка кожи и… … Большой Энциклопедический словарь
ХИМИЯ — ХИМИЯ, отрасль науки, изучающая свойства, состав и структуру веществ и их взаимодействие друг с другом. В настоящее время химия представляет собой обширную область знаний и подразделяется прежде всего на органическую и неорганическую химию.… … Научно-технический энциклопедический словарь
ХИМИЯ — ХИМИЯ, химии, мн. нет, жен. (греч. chemeia). Наука о составе, строении, изменениях и превращениях, а также об образовании новых простых и сложных веществ. Химию, говорит Энгельс, можно назвать наукой о качественных изменениях тел, происходящих… … Толковый словарь Ушакова
химия — – наука о составе, строении, свойствах и превращениях веществ. Словарь по аналитической химии [3] • аналитическая химия коллоидная химия неорганическая химия … Химические термины
ХИМИЯ — совокупность наук, предмет к рых составляют соединения атомов и превращения этих соединений, происходящие с разрывом одних и образованием других межатомных связей. Различные химия, науки отличаются тем, что они занимаются либо разными классами… … Философская энциклопедия
Химия — Наука * История * Математика * Медицина * Открытие * Прогресс * Техника * Философия * Химия Химия Кто не понимает ничего, кроме химии, тот и ее понимает недостаточно. •Лихтенберг Георг (Lichtenberg) (Источник: «Афоризмы со всего мира.… … Сводная энциклопедия афоризмов
Химия — наука о веществах, их составе, строении, свойствах и законах превращений: коллоидная наука о дисперсных системах и поверхностных явлениях на границах раздела взаимодействующих фаз; физическая наука, объясняющая химические явления и… … Энциклопедия терминов, определений и пояснений строительных материалов
ХИМИЯ
ХИМИЯ, наука о химических элементах, их соединениях и превращениях, происходящих в результате химических реакций. Она изучает, из каких веществ состоит тот или иной предмет; почему и как ржавеет железо, и почему олово не ржавеет; что происходит с пищей в организме; почему раствор соли проводит электрический ток, а раствор сахара – нет; почему одни химические изменения происходят быстро, а другие – медленно. Главная задача химии – выяснение природы вещества, главный подход к решению этой задачи – разложение вещества на более простые компоненты и синтез новых веществ. Используя этот подход, химики научились воспроизводить множество природных химических субстанций и создавать материалы, не существующие в природе. На химических предприятиях уголь, нефть, руды, вода, кислород воздуха превращаются в моющие средства и красители, пластики и полимеры, лекарства и металлические сплавы, удобрения, гербициды и инсектициды и т.д. Живой организм тоже можно рассматривать как сложнейший химический завод, на котором тысячи веществ вступают в точно отрегулированные химические реакции.
ЭЛЕМЕНТЫ И СОЕДИНЕНИЯ
Элементы
Исследование сложного вещества начинается с попыток разложить его на более простые. Простейшая форма материи, в которой сохраняется определенная совокупность физических и химических свойств, называется химическим элементом. Химические элементы – это частицы вещества, представляющие собой совокупность атомов с одинаковым зарядом ядра. Водород, кислород, хлор, натрий, железо – все это элементы. Элемент нельзя разложить на более простые составляющие обычными методами: с помощью тепла, света, электричества или под действием другого вещества. Для этого нужны колоссальное количество энергии, специальное оборудование (например, ускоритель частиц) или высокие температуры, сравнимые с температурами в недрах Солнца. Из 109 известных элементов в природе существует девяносто два элемента, остальные получены искусственно. Все они систематизированы в периодической таблице элементов, где каждому элементу соответствует свой порядковый номер, называемый атомным номером (см. ЭЛЕМЕНТЫ ХИМИЧЕСКИЕ; ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ). В табл. 1 перечислены первые 103 элемента в алфавитном порядке. Из этого ограниченного набора элементов и состоят миллионы химических веществ.
| Элемент | Символ | Атомный номер | Атомная масса |
| Азот | N | 7 | 14,0067 |
| Актиний | Ac | 89 | (227) |
| Алюминий | Al | 13 | 26,98154 |
| Америций | Am | 95 | (243) |
| Аргон | Ar | 18 | 39,948 |
| Астат | At | 85 | (210) |
| Барий | Ba | 56 | 137,33 |
| Бериллий | Be | 4 | 9,01218 |
| Берклий | Bk | 97 | (247) |
| Бор | B | 5 | 10,811 |
| Бром | Br | 35 | 79,904 |
| Ванадий | V | 23 | 50,9415 |
| Висмут | Bi | 83 | 208,9804 |
| Водород | H | 1 | 1,0079 |
| Вольфрам | W | 74 | 183,85 |
| Гадолиний | Gd | 64 | 157,25 |
| Галлий | Ga | 31 | 69,723 |
| Гафний | Hf | 72 | 178,49 |
| Гелий | He | 2 | 4,0026 |
| Германий | Ge | 32 | 72,59 |
| Гольмий | Ho | 67 | 164,9304 |
| Диспрозий | Dy | 66 | 162,50 |
| Европий | Eu | 63 | 151,96 |
| Железо | Fe | 26 | 55,847 |
| Золото | Au | 79 | 196,9665 |
| Индий | In | 49 | 114,82 |
| Иод | I | 53 | 126,9045 |
| Иридий | Ir | 77 | 192,22 |
| Иттербий | Yb | 70 | 173,04 |
| Иттрий | Y | 39 | 88,9059 |
| Кадмий | Cd | 48 | 112,41 |
| Калий | K | 19 | 39,0983 |
| Калифорний | Сf | 98 | (251) |
| Кальций | Ca | 20 | 40,078 |
| Кислород | O | 8 | 15,9994 |
| Кобальт | Co | 27 | 58,9332 |
| Кремний | Si | 14 | 28,0855 |
| Криптон | Kr | 36 | 83,80 |
| Ксенон | Xe | 54 | 131,29 |
| Кюрий | Cm | 96 | (247) |
| Лантан | La | 57 | 138,9055 |
| Лоуренсий | Lr | 103 | (260) |
| Литий | Li | 3 | 6,941 |
| Лютеций | Lu | 71 | 174,967 |
| Магний | Mg | 12 | 24,305 |
| Марганец | Mn | 25 | 54,9380 |
| Медь | Cu | 29 | 63,546 |
| Менделевий | Md | 101 | (258) |
| Молибден | Mo | 42 | 95,94 |
| Мышьяк | As | 33 | 74,9216 |
| Натрий | Na | 11 | 22,98977 |
| Неодим | Nd | 60 | 144,24 |
| Неон | Ne | 10 | 20,179 |
| Нептуний | Np | 93 | 237,0482 |
| Никель | Ni | 28 | 58,69 |
| Ниобий | Nb | 41 | 92,9064 |
| Нобелий | No | 102 | (259) |
| Олово | Sn | 50 | 118,710 |
| Осмий | Os | 76 | 190,2 |
| Палладий | Pd | 46 | 106,42 |
| Платина | Pt | 78 | 195,08 |
| Плутоний | Pu | 94 | (244) |
| Полоний | Po | 84 | (209) |
| Празеодим | Pr | 59 | 140,9077 |
| Прометий | Pm | 61 | (145) |
| Протактиний | Pa | 91 | 231,0359 |
| Радий | Ra | 88 | 226,0254 |
| Радон | Rn | 86 | (222) |
| Рений | Re | 75 | 186,207 |
| Родий | Rh | 45 | 102,9055 |
| Ртуть | Hg | 80 | 200,59 |
| Рубидий | Rb | 37 | 85,4678 |
| Рутений | Ru | 44 | 101,07 |
| Самарий | Sm | 62 | 150,36 |
| Свинец | Pb | 82 | 207,2 |
| Селен | Se | 34 | 78,96 |
| Сера | S | 16 | 32,066 |
| Серебро 2) | Ag | 47 | 107,8682 |
| Скандий | Sc | 21 | 44,9559 |
| Стронций | Sr | 38 | 87,62 |
| Сурьма | Sb | 51 | 121,75 |
| Таллий | Tl | 81 | 204,383 |
| Тантал | Ta | 73 | 180,9479 |
| Теллур | Te | 52 | 127,60 |
| Тербий | Tb | 65 | 158,9254 |
| Технеций | Tc | 43 | [97] |
| Титан | Ti | 22 | 47,88 |
| Торий | Th | 90 | 232,0381 |
| Тулий | Tm | 69 | 168,9342 |
| Углерод | C | 6 | 12,011 |
| Уран | U | 92 | 238,0289 |
| Фермий | Fm | 100 | (257) |
| Фосфор | P | 15 | 30,97376 |
| Франций | Fr | 87 | (223) |
| Фтор | F | 9 | 18,998403 |
| Хлор | Cl | 17 | 35,453 |
| Хром | Cr | 24 | 51,9961 |
| Цезий | Cs | 55 | 132,9054 |
| Церий | Ce | 58 | 140,12 |
| Цинк | Zn | 30 | 65,39 |
| Цирконий | Zr | 40 | 91,224 |
| Эйнштейний | Es | 99 | (252) |
| Эрбий | Er | 68 | 167,26 |
| 1) В расчете на атомную массу изотопа углерода 12 С, равную 12,0000. В круглых скобках указано массовое число наиболее долгоживущего нуклида. 2) См. также АТОМНАЯ МАССА. | |||
Соединения
Элементы, соединяясь друг с другом, образуют сложные вещества – химические соединения. Соль, вода, ржавчина, каучук – это примеры соединений. Соединение состоит из элементов, но обычно по своим свойствам и внешнему виду не напоминает ни один из них. Так, ржавчина образуется при взаимодействии газа – кислорода с металлом – железом, а сырьем для получения многих волокон служат уголь, вода и воздух. Именно индивидуальность свойств – одна из черт, отличающих соединение от простой смеси. Другая, и наиболее важная, характеристика соединения заключается в том, что элементы всегда соединяются между собой в определенных массовых соотношениях. Например, вода состоит из 2,016 массовых частей водорода и 16,000 массовых частей кислорода. Массовое соотношение между водородом и кислородом в водах Волги и льдах Антарктики одинаково и равно 1:8. Иными словами, каждое химическое соединение имеет вполне определенный состав, т.е. всегда содержит одни и те же элементы в одних и тех же массовых соотношениях. Это один из основных химических законов – закон постоянства состава.
Многие элементы образуют несколько соединений. Так, помимо воды известно еще одно соединение водорода и кислорода – пероксид водорода, который состоит из 2,016 частей водорода и 32 частей кислорода. Здесь водород и кислород находятся в массовом соотношении 1:16, что ровно вдвое отличается от их соотношения в воде. Этот пример иллюстрирует закон кратных соотношений: если два элемента образуют между собой несколько соединений, то массовые количества одного элемента, соединяющиеся с одним и тем же массовым количеством другого, относятся между собой как небольшие целые числа.
Атомы и молекулы
Понятия атомов и молекул – основные в химии. Атом – это мельчайшая частица элемента, обладающая всеми его свойствами, а молекула – мельчайшая частица соединения, обладающая его свойствами и способная к самостоятельному существованию. Атомистическая идея восходит к 6–5 вв. до н.э. и принадлежит древнегреческим философам Левкиппу и его ученику Демокриту. По их представлениям, вещество состоит из мельчайших неделимых частиц – атомов, созданных из одного и того же первичного материала. Правда, ни один из этих философов не определил, что это за материал. Впоследствии атомную теорию развил другой греческий философ, Эпикур (4–3 вв. до н.э.). Он утверждал, что атомы обладают весом и перемещаются в горизонтальном и вертикальном направлениях, взаимодействуя друг с другом. Аналогичные идеи высказывал римский поэт Лукреций в 1 в. до н.э., наблюдавший за пылинками, которые танцуют в солнечном луче. Наконец, в 1804–1810 английский химик и физик Дж.Дальтон разработал атомную теорию, которая включала законы кратных соотношений и постоянства состава. Однако убедительные доказательства существования атомов были получены только в 20 в. Когда Лукреций утверждал, что пылинки подталкиваются невидимыми потоками движущихся атомов, он был не так уж далек от истины: их танец действительно могут вызывать воздушные течения, но даже в неподвижном воздухе частички пыли или дыма находятся в постоянном движении. Этот эффект называют броуновским движением (см. также БРОУНОВСКОЕ ДВИЖЕНИЕ). Спустя два тысячелетия после Лукреция французский ученый Ж.Перрен, вооруженный микроскопом и математической теорией, изучил случайные блуждания суспендированных частичек краски и рассчитал число невидимых молекул, чьи удары заставляли их двигаться. После того, как атомы и молекулы удалось сосчитать, само их существование стало гораздо более убедительным.
Строение атома
Согласно современным представлениям, атом содержит центральное ядро, размеры которого очень малы по сравнению с атомом в целом. Ядро несет положительный электрический заряд и окружено диффузной оболочкой (облаком) из отрицательно заряженных электронов, которая и определяет размер атома. Диаметр атома – ок. 10 –8 см, диаметр ядра в 10 000 раз меньше и равен примерно 10 –12 см. У простейшего из атомов – атома водорода – в ядре всего одна частица – протон. Ядро атомов других элементов содержит более одного протона, а также нейтроны – частицы, близкие к протонам по массе, но не имеющие электрического заряда. Заряд ядра называют его атомным (или порядковым) номером. Атомный номер равен числу протонов в ядре и определяет химическую природу элемента. Так, атом с зарядом ядра +26 содержит 26 протонов в ядре и представляет собой элемент железо. Ядро атома железа окружают 26 электронов, поэтому атом в целом электронейтрален.
Суммарное число протонов и нейтронов в ядре называют массовым числом, поскольку в этих частицах сосредоточена практически вся масса атома. Число нейтронов, содержащихся в ядрах атомов данного элемента, в отличие от числа протонов, может варьировать. Атомы одного элемента, ядра которых содержат разное число нейтронов, называют изотопами. Слово «изотоп» греческого происхождения; оно означает «одно и то же место» – разные изотопы элемента занимают одну и ту же позицию в периодической таблице Менделеева (см. также ИЗОТОПЫ) и обладают очень близкими химическими свойствами. Так, у водорода (массовое число 1) есть изотоп дейтерий, в ядре которого один протон и один нейтрон (массовое число соответственно равно 2). Оба изотопа вступают в одни и те же химические реакции, но не всегда одинаково легко.
Термин «атомная масса» означает массу атома элемента, выраженную в единицах массы атома изотопа углерода 12 С, которую принято считать равной его массовому числу – 12,0000 (атомная масса изотопа близка к его массовому числу, но не равна ему, поскольку при образовании атомного ядра часть массы теряется в виде энергии). До 1961 атомные массы элементов определяли относительно среднего массового числа для смеси изотопов кислорода, равного 16,0000. Атомная масса элемента, существующего в природе в виде смеси изотопов, – это средняя величина атомных масс всех изотопов с учетом их распространенности в природе (см. также АТОМНАЯ МАССА). Молекулярная масса равна сумме масс атомов элементов, составляющих молекулу. Например, мол. масса воды равна сумме 2 · 1,008 (два атома водорода) + 16,0000 (один атом кислорода), т.е. 18,016.
Электронное облако
Физические и химические свойства атомов, а следовательно, и вещества в целом во многом определяются особенностями электронного облака вокруг атомного ядра. Положительно заряженное ядро притягивает отрицательно заряженные электроны. Электроны вращаются вокруг ядра так быстро, что точно определить их местонахождение не представляется возможным. Движущиеся вокруг ядра электроны можно сравнить с облаком или туманом, в одних местах более или менее плотным, в других – совсем разреженным. Форму электронного облака, а также вероятность нахождения электрона в любой его точке можно определить, решив соответствующие уравнения квантовой механики (см. также КВАНТОВАЯ МЕХАНИКА). Области наиболее вероятного нахождения электронов называют орбиталями. Каждая орбиталь характеризуется определенной энергией, и на ней может находиться не более двух электронов. Обычно вначале заполняются ближайшие к ядру самые низкоэнергетические орбитали, затем орбитали с более высокой энергией и т.д.
Существует четыре типа орбиталей, их обозначают s, p, d и f. На каждом уровне (слое) имеется одна s-орбиталь, которая содержит наиболее прочно связанные с ядром электроны. За ней следуют три p-орбитали, пять d-орбиталей и, наконец, семь f-орбиталей.