Что такое опсионплизированный эффект комплемента
Для защиты организма против внедрившихся агентов антитела действуют главным образом двумя путями: (1) прямой атаки патогенного агента; (2) активации системы комплемента, которая имеет множество своих собственных способов для разрушения внедрившегося в организм агента.
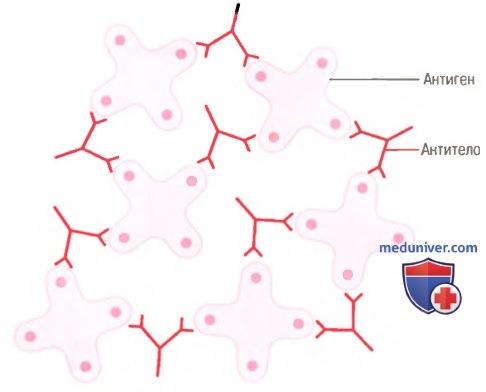
а) Прямое действие антител на внедрившиеся в организм агенты. На рисунке выше показаны антитела (обозначенные красными Y-образными полосками), реагирующие с антигенами (обозначенными затененными объектами). В связи с бивалентной природой антител и множеством антигенных участков на большинстве внедряющихся агентов антитела могут инактивировать их одним из следующих способов.
1. Агглютинация, при которой многочисленные крупные частицы с антигенами на их поверхности, например бактерии или красные клетки крови, связываются вместе, образуя комок.
2. Преципитация, при которой молекулярный комплекс растворимого антигена (например, столбнячный токсин) и антитела становится таким большим, что переходит в нерастворимое состояние и выпадает в осадок.
3. Нейтрализация, при которой антитела закрывают токсические участки антигенного агента.
4. Лизис, при котором некоторые сильнодействующие антитела способны непосредственно атаковать мембраны клеточных агентов и вызывать их разрушение.
Этих прямых действий антител, атакующих антигенные патогенные агенты, часто недостаточно, чтобы играть главную роль в защите организма против внедряющихся микроорганизмов. Более мощная защита обеспечивается путем усиливающих эффектов системы комплемента, изложенных далее.
Система комплемента при активации антител
Комплемент — собирательный термин для системы примерно из 20 белков, многие из которых являются предшественниками ферментов (проферментами). Главными действующими факторами этой системы являются 11 белков, обозначаемых С1-С9, В и D, показанные на рисунке выше. Все они присутствуют в норме среди белков плазмы крови, как и среди белков, просочившихся из капилляров в тканевые пространства. Проферменты в норме не активны, но они могут активироваться так называемым классическим путем.
а) Классический путь. Классический путь инициируется реакцией антиген-антитело. Это значит, что при связывании антитела с антигеном на константном участке антитела раскрывается или «активируется» специфическая реактивная зона. Эта зона, в свою очередь, непосредственно связывается с молекулой С1 системы комплемента, приводя в действие каскад последовательных реакций, показанных на рисунке, начиная с активации самого профермента С1. Сформированные при этом ферменты С1 активируют последовательно возрастающие количества ферментов более поздних этапов системы, и происходит чрезвычайно большое «умножение» реакции, незначительной в начале. Формируются множество конечных продуктов, как показано справа на рисунке, и некоторые из них вызывают важные эффекты, помогающие предупредить повреждение тканей тела внедрившимися микроорганизмами или токсинами.
Наиболее значимыми являются следующие эффекты.
1. Опсонизация и фагоцитоз. Один из продуктов каскада комплемента — С3b — мощно активирует фагоцитарную активность и нейтрофилов, и макрофагов, заставляя эти клетки поглощать бактерии, к которым прикрепляются комплексы антиген-антитело. Этот процесс, называемый опсонизацией, увеличивает в сотни раз число бактерий, которые могут быть разрушены.
2. Лизис. Одним из наиболее важных продуктов каскада комплемента является литинеский комплексу представляющий собой комбинацию многочисленных комплементарных факторов и обозначаемый как C5b6789. Он оказывает прямое действие, разрушающее клеточные мембраны бактерий или других патогенных организмов.
3. Агглютинация. Продукты комплемента также изменяют поверхности внедряющихся организмов, способствуя их прилипанию друг к другу.
4. Нейтрализация вирусов. Ферменты и другие продукты реакции комплемента могут атаковать структуры некоторых вирусов, в результате последние теряют свою вирулентность.
5. Хемотаксис. Фрагмент С5а инициирует хемотаксис нейтрофилов и макрофагов, заставляя большое количество этих фагоцитов мигрировать в тканевые области, прилежащие к антигенному агенту.
6. Активация тучных клеток и базофилов. Фрагменты С3а, С4а и С5а активируют тучные клетки и базофилы, заставляя их выделять гистамин, гепарин и некоторые другие вещества в местные ткани. Эти вещества, в свою очередь, ведут к увеличению локального кровотока, усилению просачивания жидкости и плазменных белков в ткань и другие местные тканевые реакции, способствующие инактивации или обездвиживанию антигенного агента. Те же факторы играют большую роль в воспалении и аллергических реакциях, которые мы обсудим далее.
7. Воспалительные эффекты. Кроме воспалительных эффектов, связанных с активацией тучных клеток и базофилов, вклад в местное воспаление вносят и некоторые другие продукты комплемента. Эти продукты ведут к:
(1) еще большему увеличению уже повышенного кровотока;
(2) усилению утечки белков из капилляров;
(3) коагуляции белков интер-стициальной жидкости в тканевых пространствах, что предотвращает движение внедрившихся организмов по тканям.
Видео схема классического пути активации комплемента
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Иммунная система Часть 7 Антитела, комплемент
Иммунная система Часть 7 Антитела, комплемент
Антитела
Антитела – главный молекулярный компонент гуморального иммунного ответа. Они секретируются плазматическими клетками, образованными из В-лимфоцитов. Распознают последовательности белков, полисахаридов и других структур конкретного антигена, точно соединяются с ним по поверхностным свойствам, подходя как ключ к замку. Благодаря наличию сходных структур, один и тот же вид антител перекрестно реагирует на разные антигены. По строению антитела представляют собой иммуноглобулины Ig нескольких классов.
Иммуноглобулин М IgM – первый вид антител, который формируется после встречи с новым антигеном. Циркулируя по крови, он связывает антиген и активирует комплемент, облегчая фагоцитоз. Каждый IgM связывает много антигенов, но эти связи непрочные. Он неидеально подходит к замку и больше похож на грубую заготовку ключа, поэтому часто бывают перекрестные реакции с другими антигенами.
Иммуноглобулин G IgG является наиболее распространенным иммуноглобулином в крови, но обнаруживается и в тканях. Это единственный иммуноглобулин, который проходит через плацентарный барьер во время беременности, обеспечивая иммунную защиту новорожденного в первые месяцы жизни. Для его формирования в первичном иммунном ответе требуется несколько дней и активная поддержка Т-лимфоцитов. Этот ключик более отточенный, причем чем больше проходит времени, тем идеальнее он подходит к замку. Свойство «идеальности» связывания с антигеном называется авидность. Именно поэтому при повторной встрече, высокоавидные IgG действуют более эффективно и быстро.
Иммуноглобулин А IgA присутствует в небольшом количестве в крови, но работает преимущественно в виде секреторного sIgA на поверхностях слизистых оболочек и в секретах (слюна, слезная жидкость, молозиво).
Иммуноглобулин D IgD связан с IgM на поверхности молодых В-лимфоцитов. Его уровни в крови очень низкие, а функция не известна.
Иммуноглобулин Е IgE присутствует в крови, на слизистых оболочках дыхательных путей и желудочно-кишечного тракта в небольшом количестве. Он обладает высоким сродством к рецепторам тучных клеток и базофилов. Если антиген взаимодействует с IgE на поверхности этих клеток, происходит их дегрануляция. Это выход содержимого гранул клеток, вызывающих острую аллергическую воспалительную реакцию.
Система комплемента
Система комплемента – это особый тип молекул (белки, ферменты и их предшественники), которые помогают в иммунном ответе. Система комплемента связывает врожденный и приобретенный иммунитет, т.к. участвует в фагоцитозе, выработке антител, уничтожении чужеродных клеток.
Компоненты системы комплемента выполняют множество функций: стимулируют хемотаксис (направленное движения лейкоцитов к антигенам), запускают дегрануляцию тучных клеток независимо от связывания антигена с IgE, помогают фагоцитирующим клеткам связывать антигены (опсонизация) и многое другое. Компоненты комплимента обозначаются буквой С и цифрой, обозначающей очередность их открытия (от С1 до С9), просто буквами (фактор B, фактор D) или имеют название (пропердин).
Активация комплимента происходит под действием иммунных комплексов, образованных связками антиген-антитело, либо же в ответ на крупные антигены и белки острой фазы.
Врожденный и приобретенный дефицит компонентов комплемента существенно снижает устойчивость организма к инфекционным агентам.
Белки воспаления
Воспаление – это местная и общая реакция организма в ответ на раздражитель. Его цель устранить причину повреждения и восстановить ткань в месте повреждения. Раздражители бывают механическими (травма), химическими (ожог, кислоты), инфекционными (бактерии, вирусы и их токсины), иммунными (комплексы антиген-антитело, комплемент).
Белки острой фазы – белки плазмы, уровень которых резко повышается или, в некоторых случаях, понижается при ответе на поражение тканей. Образуются они преимущественно в печени под действием высоких уровней ИЛ-1, ИЛ-6, ФНО-альфа в крови. Наиболее резко повышаются уровни:
Альфа-1 кислого гликопротеина
Сывороточного Р-компонента амилоида
Они повышаются через несколько часов после начала воспаления, способствуют активации комплемента, облегчают фагоцитоз, помогают ограничивать повреждение тканей, повышают сопротивляемость организма к инфекциям, способствуют заживлению тканей и прекращению воспаления. Альфа-1-кислый гликопротеин также является транспортным белком.
К белкам острой фазы воспаления относят фибриноген, ферритин, гаптоглобин, церулоплазмин и другие белки. Например, фибиронген помимо основной функции формирования тромба и остановки кровотечения, которые способствуют заживлению тканей, способен также усиливать фагоцитоз. Уровни фибриногена увеличиваются при воспалении и являются основной причиной повышения скорости оседания эритроцитов (СОЭ) в анализах.
Измерение уровней белков острой фазы указывают на воспаление, инфекцию или травму, но не помогают определить причину их возникновения.
В крови содержится еще много других молекулярных компонентов, которые участвуют так или иначе в воспалении и иммунном ответе. Дисбаланс их работы способствует либо чрезмерному ответу с поражением собственных тканей, развитием аутоиммунной патологии, либо наоборот, слабому ответу с развитием хронического воспалительного процесса.
Система комплемента
Из Википедии — свободной энциклопедии
Систе́ма комплеме́нта — комплекс защитных белков, постоянно присутствующих в крови. Это каскадная система протеолитических ферментов, предназначенная для гуморальной защиты организма от действия чужеродных агентов, она участвует в реализации иммунного ответа организма. Является важным компонентом как врождённого, так и приобретённого иммунитета. Выделяют три основных пути активации системы комплемента: классический, альтернативный и лектиновый. Для запуска классического пути комплемента необходима опсонизация чужеродной клетки антителами, а альтернативный и лектиновый пути могут активироваться в отсутствие антител. Поздние стадии у всех трёх путей активации системы комплемента одинаковы и включают образование мембраноатакующего комплекса, который нарушает целостность мембраны клетки-патогена и приводит к её гибели.
Система комплемента является эволюционно древним защитным механизмом, и некоторые её компоненты имеются даже у низших животных, таких как стрекающие. Многие патогены развили способность уклоняться от действия системы комплемента и стали устойчивы к ней. Недостаточность по многим компонентам комплемента или, наоборот, чрезмерная активность системы комплемента лежат в основе многих заболеваний человека.
Впервые система комплемента была описана в конце XIX века, а сам термин «комплемент» ввёл в употребление Пауль Эрлих.
Биологические последствия активации системы комплемента
Из приведенных выше данных видно, что активация системы комплемента приводит к образованию большого количества биологически активных компонентов. Какие же они? На схеме 3 представлены этапы активации комплемента по классическому и альтернативному пути и приведены ее основные биологические последствия.
Необходимо упомянуть о существовании так называемого С3-нефритического фактора, который представляет собой антитела против активированного С3bВb, т. е. С3-эстеразы альтернативного пути активации комплемента. Эти антитела, связываясь с С3-эстеразой, приводят к развитию гипокомплементемии, особенно у больных с ангиокапиллярным гломерулонефритом.
Среди биологически активных компонентов комплемента следует отметить комплекс С5b67, обладающий хемотаксической активностью. Однако в организме он быстро разрушается, поэтому нельзя утверждать, что этот хемотаксический эффект играет важную роль.
Следующий компонент комплемента – С4, продукты его расщепления выполняют важную биологическую функцию. Так, его субкомпонент С4b остается на мембране клетки-мишени, на которой происходит активация системы комплемента, и откладывается вблизи от активированного С1. Эти два компонента комплемента – С1 и С4 – обладают способностью связывать иммунный комплекс, в состав которого входит вирус, и приводить к нейтрализации вирусной активности. Предполагается, что таким образом молекула С4 (в частности С4b), предотвращает прикрепление вирусной частицы к клетке-мишени. С4а – еще один фрагмент активации С4, ко-торый переходит в растворимое состояние, также как СЗа и С5а, обладает анафилотоксической активностью, приводя к высвобождению гистамина из базофилов обоих типов.
Следующий компонент комплемента – С2. Известно, что при его расщеплении С2b переходит в растворимое состояние и тесно связан с продукцией кининоподобных молекул, которые в свою очередь усиливают сосудистую проницаемость без сокращения гладкой мускулатуры. Этот эффект и лежит в основе развития врожденного ангионевротического отека – заболевания, которое контролируется присутствием в организме ингибитора С1.
Следующий фактор – это фактор В альтернативного пути активации комплемента. Он расщепляется на два фрагмента: Ва и Вb. Фрагмент Ва, который переходит в растворенное состояние, является хемотаксическим фактором для нейтрофилов. Фрагмент Вb активирует макрофа-ги и способствует их прикреплению и распластыванию на поверхности клеток.
Конечные компоненты системы комплемента вызывают бактериолиз, цитолиз и виролиз, т. е. разрушение клеток, входящих в состав иммунных комплексов.
Важную роль играет система комплемента в патогенезе болезней иммунных комплексов, способствуя локализации и скорейшей элиминации антигена. Накопление же мелкодисперсных иммунных комплексов на базальных мембранах микроциркуляторного русла создает условия для длительной активации системы комплемента, приводит к отложению иммунных комплексов на мембранах и развитию воспаления.
В заключении раздела о системе комплемента следует более подробно охарактеризовать механизмы опсонизации, учитывая исключительно важное значение этого процесса в защитных реакциях организма.
Термин “опсонизация” означает процесс присоединения к микроорганизму различных молекул, выступающих впоследствии в роли лигандов (контррецепторов), к которым прикрепляются мононуклеарные клетки, имеющие на своей поверхности рецепторы к этим лигандам. Впервые процесс опсонизации был описан Райтом и Дугласом в 1903 г., однако, долгие годы его молекулярные основы оставались неизвестными. В настоящее время этот процесс представляется довольно сложным, в нем участвуют, по меньшей мере, две большие группы опсонинов; 1) молекулы некоторых иммуноглобулинов; 2) 3-й компонент комплемента (С3).
Таким образом, первая большая группа опсонинов – это молекулы иммуноглобулинов, прежде всего Ig G и его изотипов, а также Ig A.
Другая большая группа молекул опсонинов представлена С3 компонентом комплемента. В настоящее время описано, по крайней мере, три рецептора к С3. имеющиеся на мембране различных клеток (табл. 1), – CR1, CR2, и CR3. Доказано, что CR1, связывается с активированным С3 (СЗb); CR2 с C3d, a CR3 – с инактивированным С3 (С3bi). Но во всех случаях такое связывание приводит к усилению фагоцитоза опсонизированных микроорганизмов. Сложные взаимодействия между всеми этими опсонинами и соответствующими им рецепторами на клетках представляют собой главный защитный механизм, который играет важнейшую роль в антимикробном иммунитете. Антитела и комплемент проявляют как индивидуальную защиту, так и действуют синергически, дополняя друг друга и в некоторых случаях компенсируя недостаточность друг друга.
Кроме описанных выше механизмов опсонизации в последние годы открыт еще один, способствующий этому процессу. Он имеет отношение к маннозосвязывающему белку. Установлено, что маннозосвязывающий белок является кальцийзависимым лектином, который секретируется печенью некоторых видов животных, в том числе и человека. При полимеризации, по структуре он начинает напоминать первый субкомпонент системы комплемента – С1q. Подобно Clq, ман-нозосвязывающий белок способен взаимодействовать с Clr и С1s комплемента и активировать классический путь активации комплемента независимо от присутствия антител. Происходит это следующим образом: на мембране довольно большого количества различных инфекционных агентов, в том числе грамотрицательных бактерий, микобактерий, грибов, имеются манноза и N-ацетилглюкозоаминогликаны, к которым этот маннозосвязывающий белок за счет своей углеводородной группы может присоединяться. Кроме того, он может присоединяться и к сальмонеллам, на поверхности, которых также есть манноза. Присоединившись к указанным инфекционным агентам, маннозосвязывающий белок, который, как указано выше, структурно напоминает Clq. присоединяет Clr и Сls и таким образом запускает классический путь активации комплемента, что в конце концов приводит к опсонизации тех бактерий, к которым он присоединился.
В настоящее время считается, что активация классического пути комплемента за счет маннозосвязывающего белка представляет собой яркий пример неспецифических факторов защиты иммунной системы, в отсутствие которых могут развиваться различного рода нарушения в защитных реакциях организма. Например, в раннем послеродовом периоде, после того, как количество материнских имм уноглобули нов в орга низме ребенк а начинает сни жаться, он ста новится под вер-женным различного рода инфекциям. У него в организме имеется недостаточный репертуар (на¬бор) антител и сравнительно низкий уровень IgG, являющегося, как известно, опсонином и тем иммуноглобулином, который способен а кт ивироват ь систем у комплемента и усилить опсони чески й эффект. Если в этот период у ребенка будет еще и снижен уровень маннозосвязывающего белка, что явится дополнительным фактором риска, то у большинства таких детей возможно развитие различного рода инфекционных осложнений (средний отит, воспаление верхних дыхательных путей и др.), особенно в возрасте от 6 месяцев до 2 лет. Вполне возможно, что после этого транзиторного периода повышенной чувствительности к инфекционным агентам в организме ребенка появится достаточный репертуар зрелых антител, которые будут способны осуществить опсонический эффект. Тогда эффективность этих опсонических механизмов настолько повысится, что частота инфекционных осложнений у данного конкретного ребенка будет снижаться.
Существует еще один первичный дефект в иммунной системе (конкретно в системе комплемента), который, даже, несмотря на наличие в достаточном количестве опсонизирующих молекул иммуноглобулинов и маннозосвязывающего белка, будет проявляться у детей большей частотой инфекционных осложнений. Такой дефект выявлен приблизительно у 8% людей белой расы в виде недостаточности двух из четырех возможных функционирующих генов С4 комплемента, а стало быть недостаточности классического пути активации комплемента. Установлено, что продукты генного локуса С4b функционально работают в четыре раза активнее, чем белки, ассоциирующиеся с генным локусом С4а. Исходя из этого, гомозиготный дефицит по белковым продуктам С4b локусов будет реализовыватъся у детей в виде различных инфекционных осложнений, прежде всего бактериального менингита.
Существуют две гипотезы, объясняющие причины низкой сывороточной концентрации маннозосвязывающего белка. Согласно одной из них, нормальный белок синтезируется, однако в низких количествах, что связано с ненормальным контролем экспрессии гена маннозосвязывающего белка. В соответствии со второй гипотезой, ген маннозосвязывающего белка у больных кодирует дефективный белок.
В последнее время на основе изучения структуры гена маннозосвязывающего белка сделан вывод, что, он является белком острой фазы и, по всей вероятности, продуцируется в ответ на такие цитокины, как ИЛ-1 и ИЛ-6.
Для определения важных компонентов системы комплемента С3, С4 существуют современные лабораторные анализаторы, наиболее точными из которых являются нефелометры, способные оценивать низкие концентрации маркеров в сыворотке и плазме в течение короткого срока (30 мин.), представитель такого класса анализаторов – нефелометр Turbоx plus.
Активация системы комплемента при АНЦА-ассоциированных васкулитах: патогенетическая роль и перспективы для клинической практики
В течение длительного времени ведущим звеном патогенеза АНЦА-ассоциированных васкулитов (ААВ) считали опосредованную антителами к цитоплазме нейтрофилов (АНЦА) активацию нейтрофилов и моноцитов с после-дующим формированием активных форм кислорода и нейтрофильных внеклеточных ловушек. Однако в последние годы получено достаточное количество данных, свидетельствующих о значимой патогенетической роли активации системы комплемента, преимущественно по альтернативному пути, в развитии этой группы заболеваний. В обзоре проанализированы результаты экспериментальных и клинических исследований в этой области, а также представлены перспективные новые под-ходы к терапии ААВ в свете новых данных.
АНЦА-ассоциированные васкулиты (ААВ) – группа редких первичных васкулитов, характеризующихся некротизирующим воспалением стенки сосудов преимущественно мелкого калибра различной локализации и, как правило, появлением антител к цитоплазме нейтрофилов (АНЦА) в крови. АНЦА относятся к группе иммуноглобулинов класса G, мишенью которых являются первичные гранулы цитоплазмы нейтрофилов и лизосомы моноцитов. Согласно действующей классификации, принятой на конференции в Чапел Хилл в 2012 году, в группу ААВ входят гранулематоз с полиангиитом, микроскопический полиангиит, эозинофильный гранулематоз с полиангиитом и АНЦА-ассоциированный васкулит с изолированным поражением почек (АНЦА-ассоциированный гломерулонефрит) [1]. Длительное время ведущую роль в патогенезе ААВ отводили активации нейтрофилов и моноцитов, приводящей к развитию некротизирующего воспаления сосудистой стенки и инфильтрации окружающих тканей воспалительными клетками [2,3]. Следует отметить, что АНЦА, имеющие существенное значение для инициации каскада патологических реакций, удается выявить не у всех пациентов с ААВ. В частности, антитела в сыворотке крови не определяются у 60% пациентов с эозинофильным гранулематозом с полиангиитом и примерно у 10% пациентов с АНЦА-ассоциированным почечным васкулитом и системными формами гранулематоза с полиангиитом и микроскопического полиангиита 5. Эти данные позволяют предполагать многофакторную природу патогенеза ААВ, реализация которого происходит с вовлечением нескольких патологических механизмов.
Хорошо известно значение активации и дисрегуляции системы комплемента в развитии системной красной волчанки, криоглобулинемического васкулита и ряда других системных заболеваний соединительной ткани. Однако ее вклад в патогенез ААВ в течение длительного времени недооценивался в виду преимущественно скудного отложения компонентов системы комплемента в биоптатах, прежде всего ткани почки, полученных от пациентов с ААВ, а также низкой частоты гипокомплементемии у таких больных. Однако накопленные за последнее десятилетие данные экспериментальных и клинических исследований, свидетельствующие об активации системы комплемента при ААВ и ее существенной роли в формировании повреждения органов и тканей, позволили существенно расширить представления о патогенезе этой группы заболеваний и создали возможность для разработки новых подходов к ее лечению.
Экспериментальные модели
Роль АНЦА в патогенезе ААВ доказана в экспериментах in vitro, а также на мышиных моделях системного васкулита, ассоциированного с антителами к миелопероксидазе (МПО-АНЦА), а в клинической практике подтверждается наблюдениями новорожденных с почечно-легочным синдромом, который развился в результате трансплацентарной передачи антител от матери с активным васкулитом [7,8]. АНЦА направлены против гранул цитоплазмы нейтрофилов, содержащих МПО, протеиназу-3 (ПР-3) и ряд других веществ. В последнем случае речь идет об “атипичных” АНЦА, например, к гликопротеину-2 мембраны лизосом (lysosome-associated membrane protein 2), возможность применения которых в клинической практике для диагностики и оценки активности ААВ до конца не установлена, несмотря на доказательство их участия в патогенезе заболевания [9]. Основная функция АНЦА заключается в активации нейтрофилов и моноцитов, что приводит к повреждению ткани за счет дегрануляции протеаз, образования активных форм кислорода и нейтрофильных внеклеточных ловушек, а также к увеличению концентрации интерлейкина-1. Приме ча тельно, что экспозиция нейтрофилов in vitro с провоспалительными молекулами, в том числе C5а компонентом системы комплемента, приводит к появлению на мембране нейтрофилов таргетных молекул для АНЦА (“прайминг нейтрофилов”), что делает возможным взаимодействие аутоантител с клеткамимишенями, активацию нейтрофилов и реализацию перечисленных патологических механизмов [10]. В свою очередь, активированные нейтрофилы высвобождают факторы P и B системы комплемента, что поддерживает активацию петли амплификации и приводит к избыточной продукции C5a, который, помимо прочего, является мощным хемоаттрактантом, привлекающим еще большее количество нейтрофилов в очаг воспаления [11].
Следует отметить, что каскадная активация комплемента, запускаемая нейтрофилами через взаимодействие с клеточной мембраной и образование микрочастиц [16], может отчасти быть индуцирована и через классический путь при помощи C1q, активированного нейтрофильными внеклеточными ловушками [17,18], однако его вклад в патогенез заболевания остается неясным.
Активация системы комплемента при ААВ: клинические данные
Принято считать, что характерным для ААВ патоморфологическим изменением является некротизирующее воспаление стенки сосуда без накопления иммунных депозитов или с незначительным их количеством. При этом уже более 20 лет назад были опубликованы первые клинические наблюдения пациентов с АНЦА-ассоциированным гломерулонефритом, у которых при иммуногистохимическом исследовании ткани почки было выявлено отложение иммунных депозитов, в том числе C3 компонента комплемента [19]. Однако в то время подобные находки не были в полной мере интерпретированы. Впоследствии различными исследователями при морфологическом исследовании были выявлены депозиты C5b-9, С3d в почечных клубочках при помощи иммунофлуоресценции и электронной микро скопии [20,21]. В небольшом исследовании в нефробиоптатах 7 пациентов с активным АНЦА-ассоциированным гломерулонефритом было обнаружено отложение C5b-9, С3d, фактора В, в то время как у пациентов с болезнью минимальных изменений и в здоровой ткани почки эти депозиты практически отсутствовали. При этом в биоптатах пациентов с активным АНЦА-ассоциированным гломерулонефритом отсутствовали отложения маннозо-связывающего лектина и С4d компонента комплемента [22].
Изучение исходов заболевания показало, что отложение С3 компонента комплемента в ткани почки имеет неблагоприятное прогностическое значение. Это заключение было сделано группой Chen и соавт. на основании результатов наблюдения 112 пациентов с первичным АНЦА-ассоциированным гломерулонефритом. У пациентов с отложением депозитов С3с в биоптате средние значения суточной протеинурии и концентрации креатинина в сыворотке были достоверно выше, а расчетная СКФ – достоверно ниже, чем в группе пациентов без отложения C3c в биоптате (табл. 1). Частота развития диализзависимой почечной недостаточности в дебюте заболевания также была выше в группе пациентов с отложением С3с депозитов в ткани почки (48,6%), чем у пациентов без депозитов С3с (28,0%) [23]. Следует отметить, что частота выявления отложений С3с компонента комплемента в ткани почки среди обследованных больных достигала 33%, что позволяет пересмотреть сложившиеся представления о “малоиммунном” характере АНЦА-ассоциированного гломерулонефрита.
| Показатель | Пациенты с С3с в нефробиоптате, n=37 | Пациенты без С3с в нефробиоптате, n=75 | p |
|---|---|---|---|
| Суточная протеинурия, г | 1,8 (0,0–10,0) | 0,93 (0,0–13,4) | 0,01 |
| Креатинин сыворотки, мкмоль/л | 491,2±305,9 | 354,8±320,8 | 0,05 |
| рСКФ, мл/мин/1,73 м 2 | 9,9 (2,7–101,6) | 24,1 (1,87–153,6) | 0,05 |
При сравнении содержания компонентов комплемента в плазме у пациентов с активным ААВ (n=66) и в ремиссии (n=54) было выявлено, что концентрации С3а, C5а, растворимого C5b-9 и Bb были достоверно выше в первой группе, а концентрация пропердина в плазме – во второй. При этом имелись достоверные прямые корреляции между концентрацией компонента Bb в плазме крови и показателями активности заболевания, в частности количеством полулуний в нефробиоптате, величиной СОЭ и значением индекса Birmingham Vasculitis Activity Score (BVAS), а достоверные обратные корреляции – между концентрацией пропердина в плазме и количеством полулуний в нефробиоптате [24].
В другой работе было показано, что количество депозитов фактора Вb прямо коррелирует не только с процентом полулуний в нефробиоптате, но и выраженностью тубулоинтерстициального воспаления и фиброза [25]. При этом концентрация Bb в моче у пациентов с активным АНЦА-ассоциированным васкулитом была достоверно выше, чем у пациентов в ремиссии, а также прямо коррелировала с концентрацией креатинина сыворотки [25]. Сходные результаты были получены в более крупном исследовании, в котором было проанализировано 187 нефробиоптатов, полученных у пациентов с АНЦА-ассоциированным гломерулонефритом [26]. Отложение компонента C3d и пропердина в биоптате было ассоциировано скорее с формированием полулуний, нежели очаговым или смешанным типом гломерулонефрита, а отложение депозитов пропердина ассоциировалось с более высокой протеинурией. Примечательно, что при сопоставлении групп пациентов с различным серологическим профилем частота выявления депозитов С3с компонента комплемента была достоверно выше у пациентов с антителами к МПО (52,3%) по сравнению с таковой у носителей антител к ПР-3 (32,3%, р=0,006).
В исследовании Yuan и соавт. на мембранах нейтрофилов и макрофагов была выявлена экспрессия двух типов рецепторов к C5a: C5aR и C5L2. При этом у пациентов с активным ААВ экспрессия C5L2 была повышена, а экспрессия C5aR снижена, а ее выраженность имела обратную связь с концентрацией креатинина сыворотки и степенью интерстициального фиброза в ткани почки [27]. Предполагается, что этот феномен обусловлен эндоцитозом, которому подвергается C5aR после взаимодействия с C5a [28], что приводит к уменьшению его количества на клеточной мембране и служит косвенным свидетельством роли C5а в индукции воспалительных реакций [27].
Активность системы комплемента, в частности петли амплификации, в существенной степени определяется взаимодействием нескольких белков-регуляторов альтернативного пути (факторы H, I и др.). В частности, фактор H ингибирует амплификацию каскада комплемента в жидкой фазе и на поверхности клеток 30. Количественный дефицит этого белка или нарушение его функции вследствие генетических мутаций или выработки блокирующих антител приводят к дисрегуляции альтернативного пути комплемента, что является одним из хорошо изученных механизмов развития тромботической микроангиопатии и C3-гломерулопатии [32,33]. Однако возможный вклад этого сценария в патогенез ААВ остается малоизученным. В одном исследовании было показано, что концентрация фактора Н в плазме у пациентов с активным ААВ (n=82) была ниже, чем у пациентов в ремиссии, а ее величина обратно коррелировала со значением индекса BVAS, концентрацией креатинина сыворотки в дебюте и количеством полулуний в биоптате [34]. Более того, сог ласно многофакторному анализу выживаемости, концентрация фактора H плазмы была независимым предиктором развития терминальной почечной недостаточности или летального исхода. Однако недостатки исследования, в частности его ретроспективный и обсервационный характер, не позволяют оценить причины снижения уровня фактора Н и обосновывают проведение дополнительных клинических исследований. В недавней работе in vitro те же авторы показали, что фактор H способствует миграции нейтрофилов и их адгезии к клеткам гломерулярного эндотелия человека, но при этом подавляет индуцируемую АНЦА активацию нейтрофилов в клеточной культуре и препятствует повреждению эндотелиальных клеток [35]. Однако у пациентов с активным ААВ эти свойства фактора H были ослаблены по сравнению с образцами, полученными у здоровых добровольцев. Таким образом, фактор H, по всей видимости, обладает протективными свойствами в отношении эндотелия капилляров клубочка, но утрачивает эти свойства у пациентов с активным ААВ.
В большинстве представленных исследований для оценки активности системы комплемента были использованы лабораторные и иммуногистохимические методы, которые до настоящего времени не вошли в повседневную практику. В обычной лечебной работе врачам доступно преимущественно определение уровня C3 и C4 компонентов системы комплемента или ее общей активности (CH50). В последние годы были опубликованы результаты исследований, в которых оценивалась взаимосвязь этих тестов с особенностями течения ААВ. Согласно полученным данным, гипокомплементемия может быть фактором риска тяжелого поражения внутренних органов и худшего прогноза. В ретроспективном исследовании у 81 пациента с ААВ оценивали частоту развития гипокомплементемии, которую диагностировали на основании снижения уровня хотя бы одного из показателей: С3, С4 или СН50. У 16 (20%) пациентов была выявлена гипокомплементемия в дебюте заболевания. Ее формирование по сравнению с группой пациентов с нормокомплементемией (n=65) было ассоциировано с достоверно более частым развитием геморрагического альвеолита (38% и 8%, соответственно, p=0,006) и тромботической микроангиопатии (19% и 0%, р=0,007) и снижением общей выживаемости (p =0,033) [36]. В другом исследовании снижение концентрации С3 компонента комплемента, выявленное у 20% пациентов с ААВ, также сопровождалось снижением почечной и общей выживаемости [37]. Взаимосвязь гипокомплементемии с тяжестью течения ААВ была изучена в исследовании Crnogorac и соавт., в котором 75 пациентов были разделены на две группы в зависимости от концентрации С3 сыворотки: в первую группу вошли пациенты со снижением уровня C3 (менее 0,9 г/л), во вторую – с нормальной концентрацией С3 (0,9-1,8 г/л). В группе пациентов с низкой концентрацией С3 сыворотки частота летального исхода была почти в четыре раза выше (относительный риск 4,315, 95% доверительный интервал 1,350-13,799; p=0,014), чем у пациентов с нормокомплементемией [38].
Взаимосвязь тромбоэмболических осложнений и системы комплемента при ААВ
Пациенты с ААВ находятся в группе высокого риска развития тромбоэмболических осложнений [39]. Стиму ляция нейтрофилов C5а и АНЦА приводит к образованию активных форм кислорода, дегрануляции тканевых факторов и формированию нейтрофильных ловушек, что, в свою очередь, индуцирует активацию свертывающей системы крови и формирование тромбина. Различные компоненты свертывающей и противосвертывающей систем крови, включая тромбин, факторы XIa, Xa, IXa, плазмин, могут расщеплять С3 и C5, высвобождая биологически активные С3а и C5а [40, 41]. Другим потенциальным механизмом реализации протромбогенного потенциала при ААВ является воздействие системы комплемента на тромбоциты [42], приводящее к их активации [43]. Тромбоциты экспрессируют рецепторы к компонентам C3a и C5a [44], а взаимодействие с комплексом C5b-9 может стимулировать высвобождение из клеток альфа-гранул и микрочастиц [45]. В свою очередь, активированные тромбоциты могут инициировать запуск системы комплемента путем повышения синтеза С3а, С3b и формирования C5b-9 [46]. В пользу этой гипотезы свидетельствует и высокая частота развития тромбоцитоза у пациентов с активными формами ААВ, а также взаимосвязь числа тромбоцитов с показателями активности заболевания [47].
Система комплемента – потенциальная мишень терапевтического воздействия
Использование стандартных схем иммуносупрессивной терапии, в частности циклофосфамида (ЦФ) в сочетании с высокими дозами глюкокортикостероидов (ГКС), привело к значительному увеличению 5-летней выживаемости больных с ААВ – примерно с 20% до 80% [48,49]. В качестве альтернативы возможно применение ритуксимаба (моноклональные антитела к CD20+ лимфоцитам) в сочетании с ГКС. Эффективность этой схемы индукционной терапии была сопоставимой с таковой ЦФ и ГКС в двух рандомизированных исследованиях (RAVE и RITUXVAS) [50,51].
Однако, несмотря на очевидные успехи в терапии ААВ, нельзя игнорировать тот факт, что в настоящее время в числе причин летального исхода осложнения иммуносупрессивной терапии по частоте не уступают проявлениям самого заболевания. Так, при ретроспективном анализе структуры причин смерти у пациентов с ГПА частота нежелательных эффектов проводимого лечения была сопоставима с вкладом поражения легких в рамках основного заболевания – 35,1% и 37,8%, соответственно, а в проспективной группе значительно превышала их – 47,1% и 17,6%, соответственно [52]. Основные нежелательные эффекты терапии ЦФ (инфекционные осложнения, гемор рагический цистит и рак мочевого пузыря, лимфопролиферативные заболевания, миелодисплазия, бесплодие) обусловлены его высокой токсичностью 52. Применение ритуксимаба также сопряжено с высокой частотой нежелательных явлений (46%), в основном за счет развития инфекций [55]. При этом существенный вклад в развитие инфекционных осложнений вносит длительный прием и/или использование высоких доз ГКС. Поэтому одним из наиболее перспективных направлений является разработка новых схем лечения ААВ с использованием препаратов принципиально иного механизма действия, обладающих потенциальным стероидосберегающим эффектом.
В настоящее время существует несколько препаратов, способных подавлять активность системы комплемента при аутоиммунных заболеваниях. Одним из первых в клинической практике был использован экулизумаб для лечения пароксизмальной ночной гемоглобинурии и атипичного гемолитико-уремического синдрома. Однако эффективность этого препарата в лечении ААВ в клинических исследованиях не изучалась. Тем не менее, нами был описан опыт успешного использования экулизумаба в сочетании с иммуносупрессивной терапией у пациентки с сочетанием микроскопического полиангиита и атипичного гемолитико-уремического синдрома [56].
Непосредственно для лечения ААВ был разработан препарат для перорального использования, блоки рующий рецепторы C5а (ССХ168, авакопан), эффективность и безопасность которого изучались в много центровом клиническом исследовании CLEAR (NCT01363388) у 67 пациентов с ААВ. Одной из целей исследования было изучить возможность использования ССХ168 в сочетании с низкими дозами ГКС или без ГКС. Первичной конечной точкой было снижение активности васкулита (индекса BVAS по крайней мере на ≥50%) через 12 недель после начала терапии. Доля пациентов, достигших первичной конечной точки, была сопоставимой в группах пациентов, получавших авакопан в сочетании с низкими дозами ГКС и иммуносупрессивными препаратами (86,4%), авакопан в сочетании с иммуносупрессивными препаратами без ГКС (81,0%) и стандартную иммуносупрессивную терапию с высокими дозами ГКС (70,0%). У значительного числа пациентов, получавших ССХ168, была достигнута ранняя ремиссия уже на 4-й неделе лечения с сохранением низкой активности заболевания к 12-й неделе. В частности, альбуминурия снизилась у 47% пациентов, получавших препарат без ГКС, и у 40% пациентов, получавших препарат в сочетании с низкими дозами ГКС (рис. 1). Степень снижения СКФ была сопоставимой в обеих группах пациентов, получавших авакопан. Полученные данные позволили сделать вывод о стероидсберегающем эффекте препарата.

В исследовании CLASSIC (NCT02222155), в котором оценивали безопасность использования ССХ168 в дозах 10 мг и 30 мг два раза в день в сочетании с полной дозой ГКС и ЦФ или ритуксимаба в течение 12 недель, частота и структура нежелательных явлений не отличались от таковой в контрольной группе [57]. Таким образом, авакопан представляется перспективным препаратом, который, вероятно, позволит снизить бремя нежелательных явлений, ассоциированных с применением ГКС, у пациентов с ААВ при сохранении высокой эффективности терапии.




