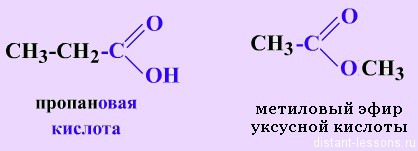
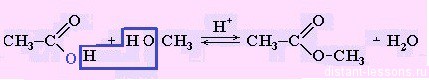Органические кислоты

Эти соединения выступают промежуточными элементами и основными компонентами метаболического преобразования энергии, основанного на производстве аденозинтрифосфата, цикле Кребса.
Концентрация органических кислот в организме человека отражает уровень функционирования митохондрий, окисления жирных кислот и обмена углеводов. Помимо этого, соединения способствуют восстановлению кислотно-щелочного баланса крови. Дефекты метаболизма митохондрий вызывают отклонения в обменных реакциях, развитие нервно-мышечных патологий и изменение концентрации глюкозы. Более того, они могут повлечь гибель клетки, что связано с процессами старения и появлением бокового амиотрофического склероза, болезнями Паркинсона, Альцгеймера.
Классификация
Наибольшее содержание органических кислот в продуктах растительного происхождения, из-за этого их часто называют «фруктовыми». Они придают характерные вкус плодам: кислый, терпкий, вяжущий, поэтому часто используются в пищевой промышленности в качестве консервантов, влагоудерживающих агентов, регуляторов кислотности, антиокислителей. Рассмотрим распространенные органические кислоты и номера пищевых добавок, под которыми они зафиксированы: муравьиная (Е236); яблочная (Е296); винная (Е335 – 337, Е354); молочная (Е326 – 327); щавелевая; бензойная (Е210); сорбиновая (Е200); лимонная (Е331 – 333, Е380); уксусная (Е261 – 262); пропионовая (Е280); фумаровая (Е297); аскорбиновая (Е301, Е304); янтарная (Е363).
Органические кислоты человеческий организм получает не только из продуктов питания в процессе переваривания пищи, но и вырабатывает самостоятельно. Такие соединения растворимы в спирте, воде, выполняют обеззараживающую функцию, улучшая самочувствие, восстанавливают здоровье.
Роль органических кислот
Главная функция карбоновых соединений – поддержание кислотно-щелочного равновесия в организме.
Органические вещества увеличивают уровень рh среды, что улучшает поглощение питательных веществ внутренними органами и выведение шлаков. Дело в том, что иммунная система, полезные бактерии в кишечнике, химические реакции, клетки лучше функционируют в щелочной среде.
Закисление организма, наоборот, – это идеальные условия для процветания болезней, в основе которых лежат следующие причины: агрессивное воздействие кислот, нарушающее работу клеток, деминерализация, ферментативная недостаточность. В результате человек испытывает недомогание, постоянную усталость, повышенную эмоциональность; появляются кислая слюна, отрыжка, спазмы, гастрит, трещины на эмали, гипотония, бессонница, неврит. В итоге ткани пытаются за счет внутренних резервов нейтрализовать лишнюю кислоту. Человек теряет мышечную массу, ощущает нехватку жизненных сил.
Органические кислоты участвуют в следующих процессах пищеварения, ощелачивая организм:
Функции некоторых органических соединений:
Органические кислоты – вкусовые компоненты, которые в свободном состоянии или в виде солей входят в состав пищевых продуктов, определяя их вкус. Данные вещества увеличивают срок годности продуктов, улучшают усвояемость и переваривание пищи. Энергетическая ценность органических кислот – три килокалории энергии на грамм. Карбоновые и сульфоновые соединения могут образовываться во время производства продуктов переработки или быть природной частью сырья. Для улучшения вкуса, запаха органические кислоты добавляют в блюда в процессе приготовления (в выпечку, джемы). Помимо этого, они снижают pH среды, тормозят процессы гниения в ЖКТ, активируют перистальтику кишечника, стимулируют сокоотделение в желудке, оказывают противовоспалительное, антимикробное действия.
Суточная норма, источники
Для сохранения кислотно-щелочного баланса в пределах нормы (рН 7,36-7,42) важно ежедневно употреблять продукты, содержащие органические кислоты.
Для большинства овощей (огурцы, болгарский перец, капуста, лук репчатый) количество соединения на 100 грамм съедобной части составляет 0,1-0,3 грамма. Повышенное содержание полезных кислот в ревене (1 грамм), грунтовых томатах (0,8 грамма), щавеле (0,7 грамма), фруктовых соках, квасе, творожной сыворотке, кумысе, кислых сортах вин (до 0,6 грамм). Лидерами по уровню органических веществ выступают ягоды и фрукты:
До 0,5 грамм органических кислот содержат молоко, кисломолочные продукты. Их количество зависит от свежести и вида изделия. При длительном хранении происходит закисление такой продукции, в результате она становится непригодной к употреблению в диетическом питании.
Учитывая, что каждый вид органической кислоты обладает особым действием, суточная надобность организма во многих из них варьирует в пределах от 0,3 до 70 грамм. При хронической усталости, пониженной секреции желудочного сока, авитаминозах потребность возрастает. При заболеваниях печени, почек, повышенной кислотности желудочного сока, наоборот, снижается. Показания к дополнительному приему природных органических кислот: низкая выносливость организма, хроническое недомогание, снижение тонуса скелетной мускулатуры, головные боли, фибромиалгия, спазмы в мышцах.
Вывод
Органические кислоты – группа соединений, которая ощелачивает организм, участвует в энергетическом обмене и содержится в растительных продуктах (корнеплодах, зелени, ягодах, фруктах, овощах). Недостаток данных веществ приводит к серьезным заболеваниям. Повышается кислотность, снижается усвоение жизненно необходимых минералов (кальция, натрия, калия, магния). Возникают болезненные ощущения в мышцах, суставах; развиваются остеопороз, болезни мочевого пузыря, сердечно-сосудистой системы, падает иммунитет, нарушается обмен веществ.
При повышенной кислотности (ацидозе) в мышечной ткани накапливается молочная кислота, возрастает риск наступления сахарного диабета, образования злокачественной опухоли. Избыток фруктовых соединений приводит к появлению проблем с суставами, пищеварением, нарушает работу почек.
Органические кислоты нормализуют кислотно-щелочное равновесие организма, сохраняют здоровье и красоту человека, оказывая благотворное влияние на кожу, волосы, ногти, внутренние органы. Поэтому в природном виде они должны ежедневно присутствовать в вашем рационе.
Больше свежей и актуальной информации о здоровье на нашем канале в Telegram. Подписывайтесь: https://t.me/foodandhealthru
Органические кислоты

Всего получено оценок: 176.
Всего получено оценок: 176.
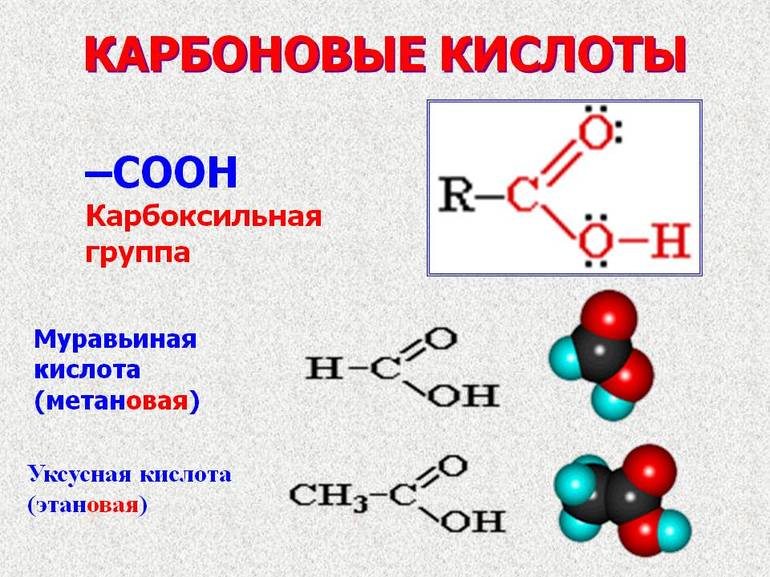
Карбоновые кислоты
Карбоновыми кислотами называют производные углеводородов, в молекулах которых один или несколько углеродных атомов образуют карбоксильную группу. Карбоновые кислоты классифицируются по основности (числу карбоксильных групп) и по виду радикала:
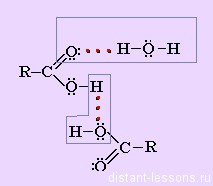
наличие водородных связей делает температуры кипения и плавления карбоновых кислот даже более высокими, чем в случае спиртов близкой молекулярной массы. Кислоты даже в парах существуют в виде димеров.
Низшие кислоты хорошо растворимы в воде. Чем больше длина цепи, тем растворимость меньше вследствие возрастания влияния неполярной части молекулы. Высшие кислоты в воде нерастворимы, ароматические растворимы очень мало, причем все являются кристаллическими.
Сульфоновые кислоты
Сульфоновые кислоты имеют общую формулу RSO3H или R-SO2-OH. Низшие сульфокислоты являются кристаллическими веществами, которые хорошо растворяются в воде.
Самой сильной сульфокислотой является трифторметансульфокислота CF3SO3H. Главными свойствами сульфокислот является способность реагировать с основаниями и со спиртами. получают эти кислоты путем сульфирования ароматических углеводородов и их производных.
Что мы узнали?
Понятие кислота
В 1877 году химик из Швеции Сванте Аррениус предложил разделять ряд веществ на основания и кислоты. Согласно его теории, если при растворении в воде элемент высвобождает протон водорода Н+, его нужно относить к кислоте, а если гидроксид-иона (ОН-), то к основанию. Это правило позволило объяснить нейтрализацию веществ при взаимодействии друг с другом. Позже учёный дал уточнение, что сталкивание гидроксид-иона с ионом водорода образовывает воду H2O.
В начале двадцатого века британец Томас Лаури и датчанин Йоханнсен Брёнстед расширили определение. Они предложили относить к кислотам любую молекулу (ион), способную отдавать протон. Это позволило описать реакции, проходящие c водой, например, хлорид аммония.
В 1923 году американец Льюис на основании двух определений сформулировал своё правило. Его формулировка и стала использоваться повсеместно. По нему, кислота — это химическое соединение, принимающее электронную пару и образовывающее ковалентную связь. Основание же, напротив — соединение, способное избавляться от электронной пары.
Все кислоты в химии принято разделять на 2 типа:
Кроме этого, соединения могут быть одноосновными, двухосновными или трёхосновными. Все кислоты, за исключением кремниевой, отлично растворяются в воде. При взаимодействии с основаниями образуют соль, воду и кислотный остаток. Протекание реакции при соприкосновении с металлами происходит не всегда. Взаимодействие возможно лишь элементов, которые располагаются левее водорода. При этом кислотное соединение должно быть не только сильным, но и способным отдавать частицы водорода, которые выделяются во время взаимодействия.
Кислотные растворы могут изменять цвет. Так, лакмус становится красным. Соединение при взаимодействии имеет кислый вкус, появляется электрическая проводимость.
Если же в кислотный раствор добавить спирт, образуется сложный эфир. Все приведенные свойства характерны как для органических соединений, так и неорганических.
Особенности органического класса
Органическая химия изучает синтезирование углеводородов и их производство. Производные соединения углерода и водорода в молекулах относятся к карбоксильной группе (- COOH). Название веществ состоит из двух элементов: карбонита и гидроксила. Свойства же группы определяется смещением электронной плотности к карбонильному кислороду и образованной поляризацией связи O-H.
Другое название карбонатных кислот — органические. Их свойства определяются строением. Особенности группы из-за диссоциации с образованием частиц водорода в том, что её свойства совпадают с минеральными кислотами. Некоторые соединения, например, уксусная кислота (СН3СОOН) в своей молекуле имеют углеводородный радикал, поэтому возможны реакции, сопровождающиеся выбиванием водорода галогеном. Этот процесс приводит к повышению степени диссоциации, и кислота становится сильнее.
Из свойств органических соединений можно выделить:
Так как карбоновые кислоты распадаются на ионы, степень растворимости и достаточно большая температура кипения определяют межмолекулярные водородные связи. При этом с возрастанием молекулярной массы растворимость соединения уменьшается.
Карбоновые кислоты принято разделять и по природе углеводородного радикала: они бывают алифатическими, ароматическими и алициклическими. Если же в первом типе содержится более шести атомов углерода, соединение называют жирной кислотой. Это происходит из-за того, что в виде сложных эфиров они являются частью природных жиров и масел.
Ароматическая представляет собой бензойную и дикарбоновую кислоту, а алициклическая – циклопропан-карбоновую и циклогексанкарбоновую кислоты. Из структуры соединений выделяют радикалы (ацилы). Подписывают их используя суффикс – ил., например, бутрил, формил.
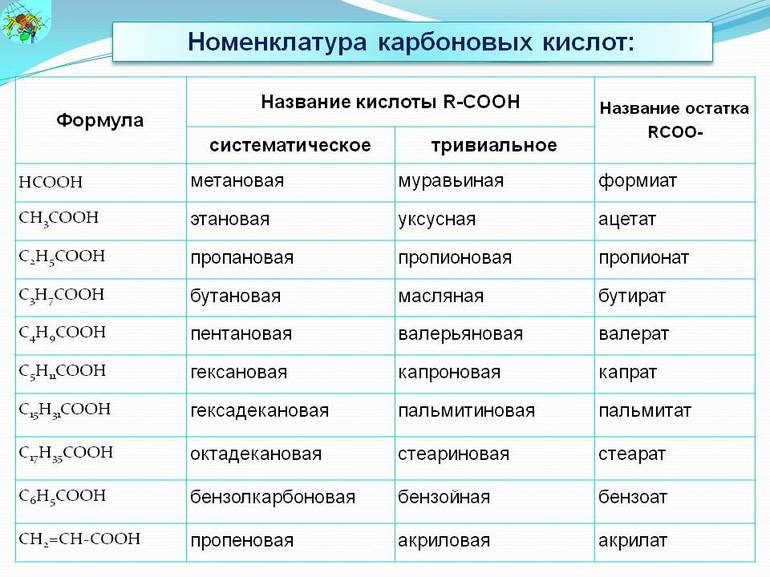
Таблица соединений
Существует две системы обозначений для карбоновых соединений. Их классификация допускает использование тривиального названия и по ИЮПАК. В то же время применение систематической номенклатуры считается более предпочтительной. Всё дело в том, что тривиальные имена не содержат сведений о составе и строении соединений, а некоторые сложные эфиры и соли вовсе не имеют сокращённых наименований.
В мире насчитывается более сотни различных видов органических кислот. Они входят в компоненты природных вод и связаны с жизнедеятельностью человека, животных и растений. Общую формулу для всей группы можно изобразить как R—COOH. Из наиболее популярных соединений можно выделить:
| Тривиальное имя | Название по ИЮПАК | Содержащиеся соли и эфиры | Номер регистрации по CAS |
| Адипиновая | Гександиовая | Адипинаты | 124-04-9 |
| Акриловая | Пропеновая | Акрилаты | 79-10-7 |
| Аспарагин | 4-амид-2-аминобутандиовая | 70-47-3 | |
| Бензиловая | Гидроксидифенилуксусная | 76-93-7 | |
| Валериановая | Пентановая | Валераты | 109-52-4 |
| Ванилиновая | 4-гидрокси-3-метоксибензойная | 121-34-6 | |
| Винная | 2,3-дигидроксибутандиовая | Тартраты | 133-37-9 |
| Виноградная | DL-винная | 526-83-0 | |
| Гистидин | 2-амино-3-(4-имидазолил)пропановая | 351-50-8 | |
| Глицин | Аминоуксусная | 56-40-6 | |
| Изоянтарная | Метилмалоновая | 516-05-2 | |
| Камфорная | цис-1,2,2-триметилциклопентан-1,3-дикарбоновая кислота | 560-09-8 | |
| Кофейная | 3-(3,4-дигидроксифенил)пропеновая | 331-39-5 | |
| Лимонная | 2-гидрокси-1,2,3-пропантрикарбоновая | Цитраты | 77-92-9 |
| Лимонно-яблочная | 2-гидрокси-2-метилбутандиовая | 597-44-4 | |
| Мелиссовая | Триаконтановая | Мелиссаты | 506-50-3 |
| Молочная | 2-гидроксипропановая | Лактаты | 50-21-5 |
| Никотиновая | Пиридин-3-карбоновая | Никотинаты | 59-67-6 |
| Оксаминовая | Моноамид щавелевая | 471-47-6 | |
| Пенициллиновая | (2Z)-3-метокси-5-метил-4-оксо-2,5-гексадиеновая | 90-65-3 | |
| Пробковая | Октандиовая | Субераты | 505-48-6 |
| Салициловая | 2-гидроксибензойная | Салицилаты | 69-72-7 |
| Травматиновая | 2-додецендиовая | 64-02-36-4 | |
| Уксусная | Этановая | Ацетаты | 64-19-7 |
| Фенантровая | 1-фенантренкарбоновая | 27875-89-4 | |
| Фолиевая | 59-30-3 | ||
| Яблочная | Малаты | 6915-15-7 |
Отдельно нужно выделить муравьиную кислоту (HCOOH). Это одноосновное соединение. В природе она вырабатывается у пчёл, муравьёв, содержится в крапиве и хвое. Проявляет восстановительные свойства. Эта кислота очень востребована как антибактериальное средство.
Происхождение и получение
Получение HOOC-соединений связано с окислением спиртов. Протекающую реакцию окисления этилового спирта можно записать как CH3 – CH2 – OH → CH3 – C = O (-OH) + H2O. Окисление же уксусного альдегида выглядит следующим образом: CH3 – C = O (H) → CH3 – C =O (-OH). Образование возможно и гидролизом нитрилов. Побочным продуктом является аммиак: CH3 – C = N + H2O → CH3 – C = O (-OH) + NH3.
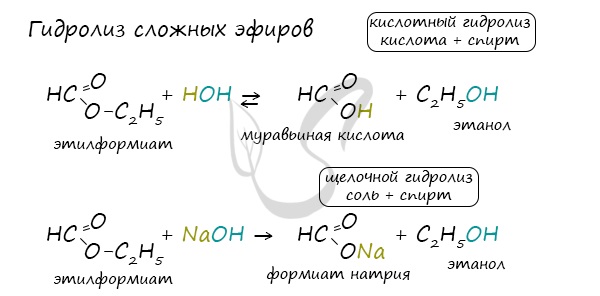
Карбоновую кислоту можно создать гидролизом сложного эфира. В результате реакции получается спирт. Что интересно, если в реакции использовать щёлочь, продуктом станет соль. Но если её поместить в минеральную кислоту, получится органическая. Реакция имеет вид: СH3 – C = O (-CH3) + H2O → CH3 – C = O (-OH) – CH3OH. Этот способ применяется для получения высших соединений: пальмитинового ( C 16 H 32 O 2), стеаринового ( c17h35cooh), олеинового ( c17h33cooh). При этом в воде они не растворяются.
Всего же можно выделить следующие способы:
Химия, Биология, подготовка к ГИА и ЕГЭ
Органические кислоты
Карбоновые кислоты
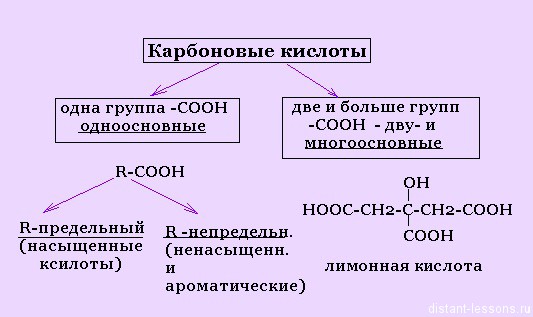
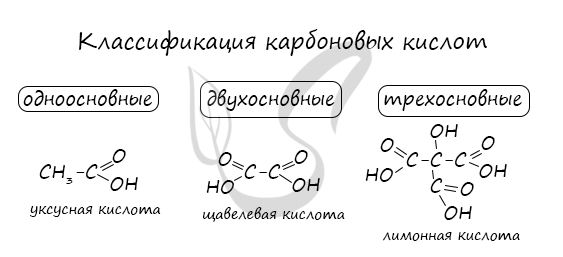
Классификация органических кислот
Здесь все просто — деление по числу карбоксильных групп и по составу радикала.
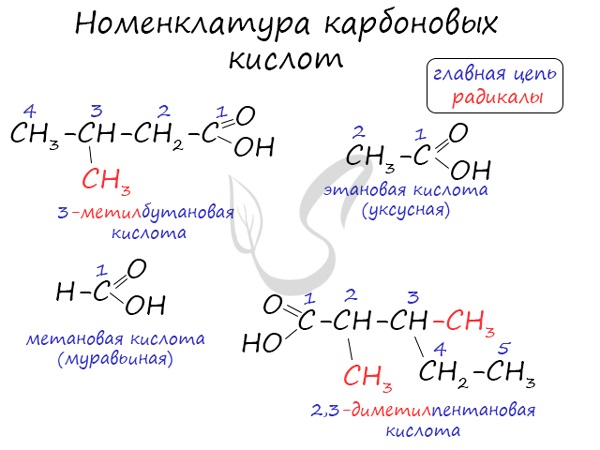
Номенклатура
Номенклатура карбоновых кислот достаточно проста:
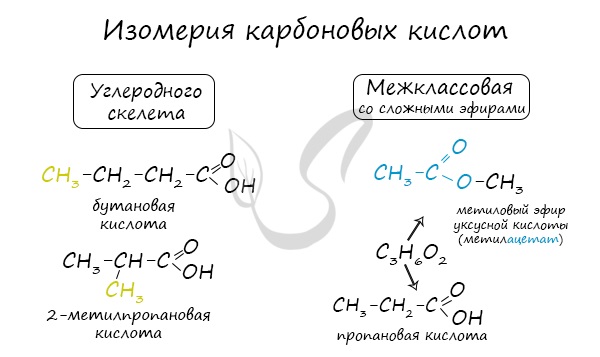
Изомерия органических кислот
Физические свойства:
Химические свойства карбоновых кислот
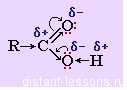
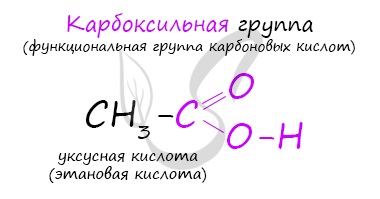
Карбоксильная группа устроена таким образом, что молекула достаточно легко может отщеплять водород — проявлять свойства кислоты. Кислород карбонильной группы тянет электронную плотность на себя, поэтому связь O-H в гидроксильной группе поляризуется, и H становится более подвижным.
Важно понимать, что органические кислоты НАМНОГО слабее неорганических (но: угольная H2CO3 и кремниевая H2SiO3 — слабее органических).
Соответственно, органические кислоты реагируют с
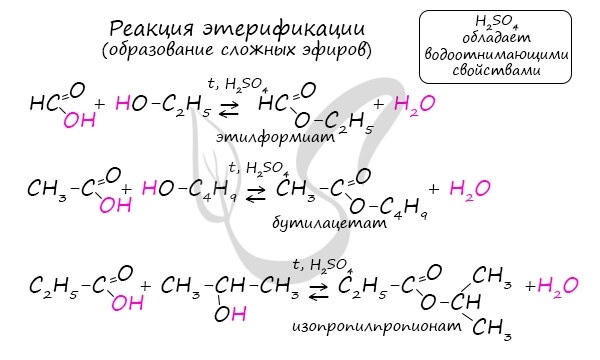
CH3COOH + CH3OH = CH3COOCH3 + H2O
Получение кислот
Карбоновые кислоты
Классификация карбоновых кислот
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав которых они входят.
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными эфирами.
Получение карбоновых кислот
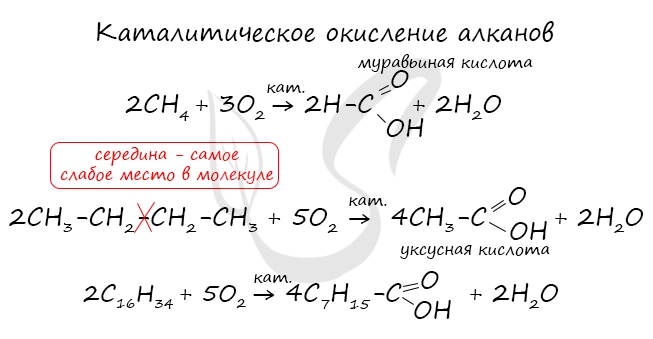
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого образуются кислоты.
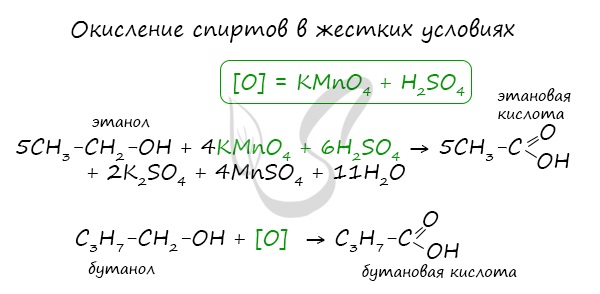
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются до соответствующих кислот.
Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.
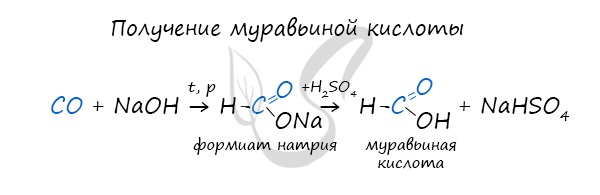
При дальнейшей обработке формиата серной кислотой образуется муравьиная кислота.
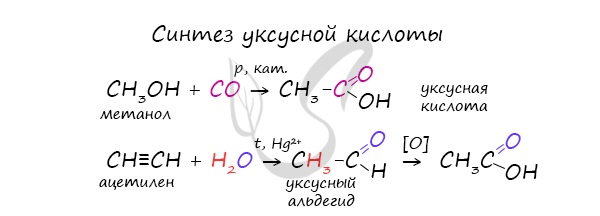
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид. Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты.
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.
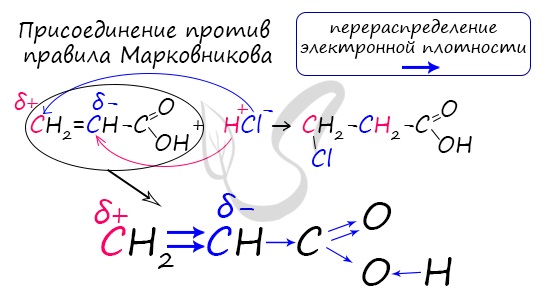
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.
Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот, способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.
При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
Сложные эфиры
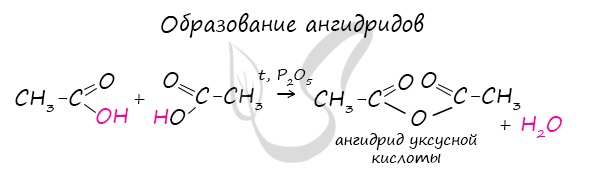
Ангидриды
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.
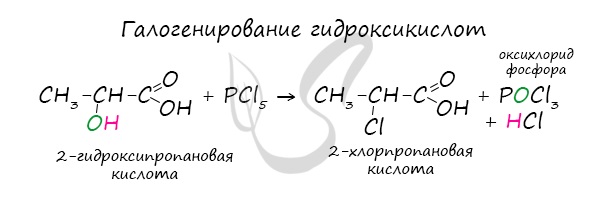
Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания. Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
Непредельные карбоновые кислоты
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.