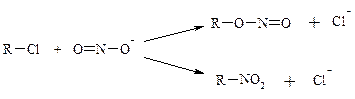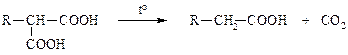Ориентации правила
Полезное
Смотреть что такое «Ориентации правила» в других словарях:
Правила полётов по приборам — Правила полётов по приборам, ППП (англ. Instrument flight rules, IFR) совокупность авиационных правил и инструкций, предусматривающих выполнение полетов в условиях, при которых местонахождение, пространственное положение и параметры… … Википедия
ПБ 10-611-03: Правила устройства и безопасной эксплуатации подъемников (вышек) — Терминология ПБ 10 611 03: Правила устройства и безопасной эксплуатации подъемников (вышек): 7.19. Аварийный останов двигателя Предохранительное устройство, предназначенное для аварийного останова двигателя из люльки или с нижнего пульта… … Словарь-справочник терминов нормативно-технической документации
Устройство ориентации люльки — 7.12. Устройство ориентации люльки Специальная система, предназначенная для обеспечения ориентации пола люльки в горизонтальном положении при изменении положений колен подъемника Источник: ПБ 10 611 03: Правила устройства и безопасной… … Словарь-справочник терминов нормативно-технической документации
ПБ 10-11-92: Правила устройства и безопасной эксплуатации подъемников (вышек) — Терминология ПБ 10 11 92: Правила устройства и безопасной эксплуатации подъемников (вышек): 7.16. Аварийное опускание люльки (площадки) Устройство, предназначенное для аварийного опускания люльки (площадки) при отказе гидросистемы или двигателя… … Словарь-справочник терминов нормативно-технической документации
СТО 70238424.27.100.063-2009: Ветроэлектростанции (ВЭС). Охрана труда (правила безопасности) при эксплуатации и техническом обслуживании. Нормы и требования — Терминология СТО 70238424.27.100.063 2009: Ветроэлектростанции (ВЭС). Охрана труда (правила безопасности) при эксплуатации и техническом обслуживании. Нормы и требования: 3.1.1 аварийная защита электроагрегата (электростанции): Комплекс… … Словарь-справочник терминов нормативно-технической документации
Электронные теории в органической химии — теории, рассматривающие строение, физические свойства и реакционную способность (См. Реакционная способность) органических соединений на основе представлений о распределении электронной плотности в атомах и молекулах, а также о смещениях… … Большая советская энциклопедия
Нитрование — введение нитрогрупп NO2 в молекулы органических соединений при действии различных нитрующих агентов. В зависимости от строения нитруемого соединения и условий реакции Н. может сопровождаться введением в молекулу др. функциональных групп,… … Большая советская энциклопедия
Органическая химия — раздел химии (См. Химия), естественнонаучная дисциплина, предметом изучения которой являются соединения углерода с др. элементами, называемые органическими соединениями, а также законы превращения этих веществ. Углерод образует соединения … Большая советская энциклопедия
Реакции химические — превращения одних веществ в другие, отличные от исходных по химическому составу или строению. Общее число атомов каждого данного элемента, а также сами химические элементы, составляющие вещества, остаются в Р. х. неизмененными; этим Р. х … Большая советская энциклопедия
Реакционная способность — характеристика химической активности веществ, учитывающая как разнообразие реакций, возможных для данного вещества, так и их скорость. Например, благородные металлы (Au, Pt) и инертные газы (Не, Ar, Kr, Xe) химически инертны, т. е. у них… … Большая советская энциклопедия
Что такое ориентация в химии
В молекуле бензола π-электронное облако распределено равномерно между всеми атомами углерода. Но если в бензольное кольцо ввести какой-нибудь заместитель, то равномерность распределения π-электронной плотности нарушается. В результате этого бензольное кольцо становится частично поляризованным, и место вступления нового заместителя определяется природой уже имеющегося заместителя.
По своему направляющему действию все заместители делятся на две группы: ориентанты I рода и ориентанты II рода.
Ориентанты I рода (орто-пара-ориентанты) – это группировка атомов, способных отдавать электроны (электродоноры):
– R, – ОН, – OR, – OCOR, –SH, – SR, – NH2, – NHR, – NHCOR, –N=N–, – CH3, – CH2R, – CR3, – Hal (F, Cl, Br, I)
Электродонорные заместители проявляют +М и/или +I-эффект и повышают электронную плотность в сопряженной системе, например:
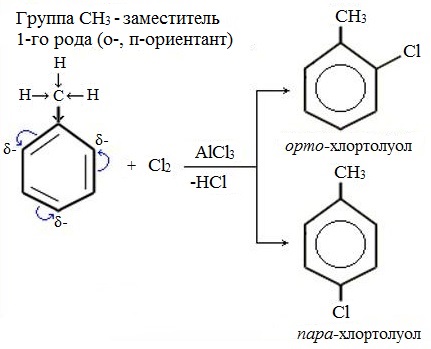
Эти заместители смещают электронную плотность в сторону бензольного кольца. Облегчая вхождение электрофильных реагентов в бензольное кольцо, они ориентируют новый заместитель в орто- и пара-положения.
Ориентанты I рода, повышая электронную плотность в бензольном кольце, увеличивают его активность в реакциях электрофильного замещения по сравнению с незамещенным бензолом.
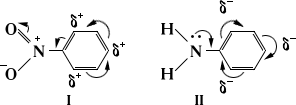
Электроноакцепторные заместители проявляют –М-эффект и/или –I-эффект и снижают электронную плотность в сопряженной системе, например:
Эти заместители смещают электронную плотность от бензольного кольца, особенно в орто- и пара-положениях на себя, создавая частичный отрицательный заряд в мета-положении.
Поэтому электрофил атакует атомы углерода не в этих положениях, а в мета-положении, где электронная плотность несколько выше.
Все ориентанты II рода, уменьшая в целом электронную плотность в бензольном кольце, снижают его активность в реакциях электрофильного замещения.
Таким образом, легкость электрофильного замещения для соединений ниже, уменьшается в ряду:
Помимо ориентирующего действия заместители оказывают влияние и на реакционную способность бензольного кольца: ориентанты I-го рода (кроме галогенов) облегчают вступление второго заместителя; ориентанты II-го рода (и галогены) затрудняют его.
Правила ориентации в бензольном кольце.
Основным фактором, который определяет химические свойства молекулы, является распределение электронной плотности. Характер распределения зависит от взаимного влияния атомов.
Влияние атомов осуществляется через индуктивный эффект (по σ-связи). В молекулах, предоставляющих собой сопряженный системы, имеет место мезомерный эффект: влияние заместителей, передающееся по сопряженной системе π-связей.
Если в кольцо ввести какой-нибудь заместитель, то равномерное распределение нарушается и происходит перераспределение электронной плотности в кольце. Место вступления второго заместителя в бензольном кольце определяется природой заместителя.
Заместители делят на 2 группы в зависимости от проявляемого эффекта (мезомерного и индуктивного): электронодонорного и электроноакцепторные.
В результате электронная плотность сосредотачивается в орто- и пара- положениях:
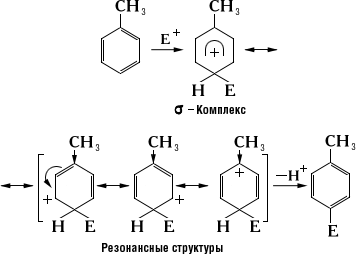
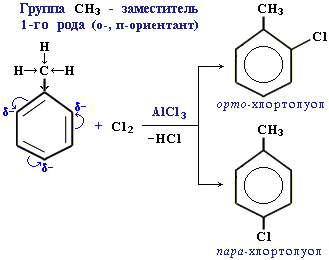
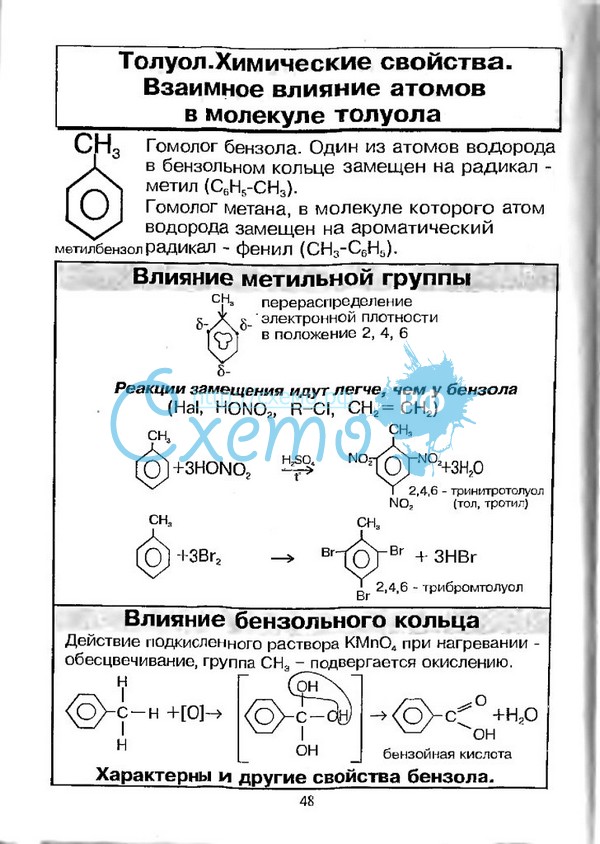
Алкильные группы проявляют +I—эффект, под действием которого наблюдается перераспределение π-электронной плотности.
Такие заместители образуют сопряженную систему, но электронная система сдвигается в сторону этих групп. Поэтому электронная плотность уменьшается и в большей степени – в мета-положении:
Галогены проявляют –I-эффект, что также способствуют понижению электронной плотности кольца.
Такие закономерности носят названия правил ориентации в бензольном кольце.
Заместители, которые проявляют +I— эффект или +М – эффект, направляют замещение в орто- и пара-положения бензольного кольца, и называются такие заместители – ориентантами (заместителями) первого рода:
Заместители, обладающие –I и –М –эффектами, направляют замещение в мета-положение бензольного кольца, и называются заместителями второго рода:
Ориентанты 1го рода облегчают вступление второго заместителя, ориентанты 2го – затрудняют его.
Ориентации правила
Ориент а ции пр а вила, в органической химии определяют порядок замещения в ароматическом кольце при наличии в нём заместителя (ориентанта). При электрофильном ароматическом замещении (см. Замещения реакции, Нуклеофильные и электрофильные реагенты) ориентанты I рода (OH, OR, OCOR, SH, SR, NH2, NHR, NR2, алкилы, галогены) направляют замещение в орто- и пара-положения кольца, ориентанты II рода (SO3H, NO2, COOH, COOR, CN, CF3, 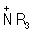
В возникающем переходном состоянии наблюдается прямое взаимодействие заместителя с положительным зарядом, в результате чего его энергия становится меньше, чем переходного состояния в случае мета-замещения в толуоле.
Более сложно поведение галогенных ориентантов, у которых —I- и +М-эффекты действуют в противоположных направлениях. В нереагирующей молекуле из-за —I-эффекта галоген служит отрицательным концом диполя. В образующемся переходном состоянии при орто- и пара-замещении благодаря возможности частичного погашения заряда за счёт +М-эффекта заместитель направляется именно в эти положения. Однако электрофильное замещение происходит труднее, чем в бензоле. Для заместителей, обладающих такой же комбинацией эффектов, например для аминогруппы (NH2), +М-эффект перекрывает действие —I-эффекта. Протонирование аминогруппы в растворах приводит к изменению характера ориентанта, т.к. 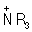
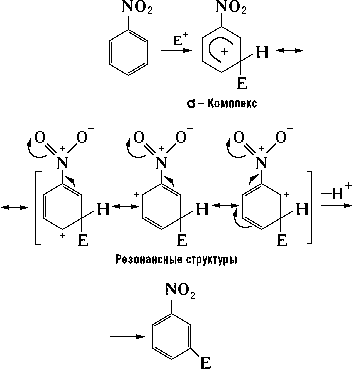
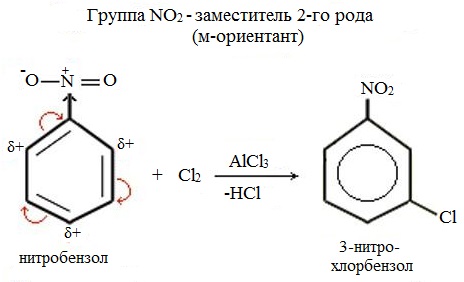
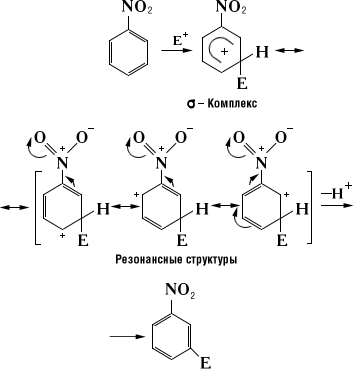
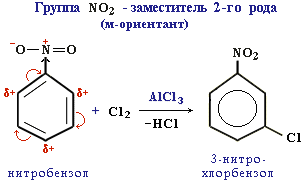
Ориентанты II рода за счет действия тех же эффектов в обратном направлении (—I- и —М-эффекты) затрудняют вступление электрофила во все положения бензольного кольца, но особенно (за счет эффекта сопряжения) в орто- и пара-положения, поэтому в этом случае замещение в основном осуществляется в мета-положение, например как в нитробензоле:
В возникающем переходном состоянии отсутствует прямое взаимодействие заместителя с положительным зарядом.
При наличии нескольких заместителей в ароматическом кольце возможны случаи согласованной и несогласованной ориентации, как, например, в n- и м-нитротолуолах. Относительная реакционная способность и эффект ориентации (избирательность реакции) в значительной степени зависят от характера электрофильного агента. Обратное влияние рассмотренных заместителей (как на активацию замещения, так и на ориентацию) наблюдается при нуклеофильном ароматическом замещении.
Лит.: Ингольд К., Теоретические основы органической химии, пер. с англ., М., 1973.
Правила ориентации
1. Заместители, имеющиеся в бензольном ядре, направляют вновь вступающую группу в определенные положения, т.е. оказывают ориентирующее действие.
2. По своему направляющему действию все заместители делятся на две группы: ориентанты первого рода и ориентанты второго рода.
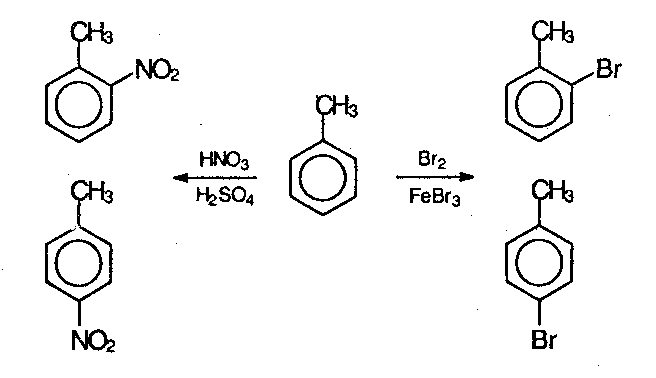
Ориентанты 1-го рода (орто-пара-ориентанты) направляют последующее замещение преимущественно в орто— и пара-положения.
К ним относятся электронодонорные группы (электронные эффекты групп указаны в скобках):
Ориентанты 1-го рода повышают электронную плотность в бензольном кольце, особенно на углеродных атомах в орто— и пара-положениях, что благоприятствует взаимодействию с электрофильными реагентами именно этих атомов.
Пример:
Ориентанты 1-го рода, повышая электронную плотность в бензольном кольце, увеличивают его активность в реакциях электрофильного замещения по сравнению с незамещенным бензолом.
Ориентанты 2-го рода уменьшают электронную плотность в бензольном кольце, особенно в орто— и пара-положениях. Поэтому электрофил атакует атомы углерода не в этих положениях, а в мета-положении, где электронная плотность несколько выше.
Пример:
Все ориентанты 2-го рода, уменьшая в целом электронную плотность в бензольном кольце, снижают его активность в реакциях электрофильного замещения.
Таким образом, легкость электрофильного замещения для соединений (приведенных в качестве примеров) уменьшается в ряду:
17)
18) Классификация реагентов и реакций
Вещества, участвующие в реакции, называются реагентом и субстратом.
Когда реакция проходит между органическими и неорганическими соединениями, реагентом называется неорганическое, а субстратом – органическое вещество. В случае реакции между органическими соединениями субстратом называется вещество с более сложной структурой.
Реакционный центр – атом, у которого происходит разрыв или образование связей.
Если в реагенте имеется 2 реакционных центра, он называется амбидентным :
Механизм реакции – это детальное описание пути, ведущего от исходных веществ к продуктам реакции, включающее как можно более полную характеристику состава, строения и других свойств промежуточных соединений и активированных комплексов, а также предположения, касающиеся смещения электронов в ходе последовательных превращений частицы.
I. Классификация реакций по изменениям углеродного скелета
1) Конденсации – реакции, сопровождающиеся увеличением числа атомов углерода за счёт образования новых С–С-связей :
2) Деградации – реакции, сопровождающиеся уменьшением числа атомов углерода за счёт разрыва С–С-связей :
3) Перегруппировки – реакции, в которых число связей С–С остаётся тем же, но изменяется относительное расположение атомов:
4) Изменение функциональных групп (изменяется природа функциональных групп с сохранением углеродного скелета):
Радикал (буквально: «коренной» от лат. radix — «корень») — термин, используемый в разных отраслях человеческих знаний, каждый раз со своим значением.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет