Что такое осмос физиология
Поддержание адекватного объема одной или обеих (внутри- и внеклеточной) жидких сред организма является частой проблемой при лечении тяжелобольных. Распределение внеклеточной жидкости между плазмой и межклеточным пространством в основном зависит от уравновешивания сил гидростатического и коллоидно-осмотического давления, которые действуют на мембрану капилляров.
Распределение жидкости между внутри- и внеклеточной средами в основном определяется осмотическими силами мелких молекул растворенных веществ, преимущественно натрия, хлора и других электролитов, действующих по разные стороны мембраны. Причина этого распределения обусловлена свойствами мембран, проницаемость которых для воды высока, а для ионов даже очень небольшого диаметра, таких как натрий и хлор, практически равна нулю. Следовательно, вода быстро проникает через мембрану, а внутриклеточная жидкость, тем не менее, остается изотоничной по отношению к внеклеточной.
В следующем разделе рассмотрим взаимосвязь между внутри- и внеклеточной жидкостями и причины осмотического характера, способные влиять на перенос жидкости между этими средами.
В статье мы рассмотрим только наиболее важные теоретические положения, касающиеся регуляции объемов жидкости.
Теоретические основы осмоса и осмотического давления
Основы осмоса и осмотического давления изложены в отдельной статье на сайте (просим вас пользоваться формой поиска выше). В этой статье мы рассмотрим только наиболее важные теоретические положения, касающиеся регуляции объемов жидкости.
Осмос — процесс диффузии воды через полупроницаемую мембрану. Он происходит из области с высокой концентрацией воды в область с ее низкой концентрацией. Растворение вещества в воде приводит к снижению концентрации воды в данном растворе. Следовательно, чем больше концентрация вещества в растворе, тем ниже в нем содержание воды. Кроме того, вода диффундирует из области с низкой концентрацией вещества (высоким содержанием воды) в область с высокой концентрацией вещества (низким содержанием воды).
Поскольку проницаемость мембраны клеток избирательна (она относительно низка для большинства растворенных веществ, но высока для воды), то при повышении концентрации вещества с одной стороны мембраны вода проникает в эту область путем диффузии. Если растворенное вещество, такое как NaCl, добавить во внеклеточную жидкость, вода будет быстро выходить из клетки до тех пор, пока концентрации молекул воды по обе стороны мембраны не уравняются. Если, напротив, концентрация NaCl во внеклеточной жидкости снизится, вода из внеклеточной жидкости устремится в клетки. Интенсивность, с которой вода диффундирует в клетку, называют осмотической силой.
а) Соотношение молей и осмолей. Поскольку концентрация воды в растворе зависит от количества в нем частиц вещества, под термином «концентрация вещества» (независимо от его химического состава) понимают общее число частиц вещества в растворе. Это число измеряют в осмолях. Один осмоль (осм) соответствует одному молю (1 моль, 6,02×10 23 ) частиц растворенного вещества. Следовательно, каждый литр раствора, содержащий 1 моль глюкозы, соответствует концентрации 1 осм/л. Если молекула диссоциирует на 2 иона, т.е. возникают две частицы (например, NaCl распадается на ионы Na+ и Сl-), то одномолярный раствор (1 моль/л) будет иметь осмолярность 2 осм/л. Аналогично раствор, содержащий 1 моль вещества, которое диссоциирует на 3 иона, например сульфат натрия Na2SО4, будет содержать 3 осм/л. Поэтому термин «осмоль» определяют, ориентируясь не на молярную концентрацию вещества, а на число растворенных частиц.
В целом осмоль — слишком большая величина, чтобы использовать ее в качестве единицы измерения осмотической активности жидких сред организма. Обычно используют 1/1000 осмоли — миллиосмолъ (моем).
б) Осмоляльность и осмолярность. Осмолялъностью называют осмоляльную концентрацию вещества в растворе, которая выражается в количестве осмолей на килограмм растворителя. Когда же речь идет о количестве осмолей в литре раствора, эту концентрацию называют осмолярностью. Для сильно разведенных растворов, которыми являются жидкие среды организма, справедливо использовать оба термина, т.к. разница значений невелика. Во многих случаях сведения о жидких средах организма легче выражать в литрах, чем в килограммах, поэтому в большинстве расчетов, используемых в клинике, а также в следующих главах, за основу принята не осмоляльность, а осмолярность.
в) Осмотическое давление. Осмос молекул воды через избирательно проницаемую мембрану может быть уравновешен силой, приложенной в направлении, обратном осмосу. Величину давления, необходимую для прекращения осмоса, называют осмотическим давлением. Таким образом, осмотическое давление является непрямой характеристикой содержания воды и концентрации веществ в растворе. Чем оно выше, тем меньше в растворе содержание воды и выше концентрация растворенного вещества.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Осмос
О́смос (от греч. ὄσμος — толчок, давление) — процесс односторонней диффузии через полупроницаемую мембрану молекул растворителя в сторону бо́льшей концентрации растворённого вещества (меньшей концентрации растворителя).
Более широкое толкование явления осмоса основано на применении Принципа Ле Шателье — Брауна: если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия.
Содержание
История
Впервые осмос наблюдал А. Нолле в 1748, однако исследование этого явления было начато спустя столетие.
Суть процесса
Явление осмоса наблюдается в тех средах, где подвижность растворителя больше подвижности растворённых веществ. Важным частным случаем осмоса является осмос через полупроницаемую мембрану. Полупроницаемыми называют мембраны, которые имеют достаточно высокую проницаемость не для всех, а лишь для некоторых веществ, в частности, для растворителя. (Подвижность растворённых веществ в мембране стремится к нулю). Как правило, это связано с размерами и подвижностью молекул, например, молекула воды меньше большинства молекул растворённых веществ. Если такая мембрана разделяет раствор и чистый растворитель, то концентрация растворителя в растворе оказывается менее высокой, поскольку там часть его молекул замещена на молекулы растворённого вещества (см. Рис. 1). Вследствие этого, переходы частиц растворителя из отдела, содержащего чистый растворитель, в раствор будут происходить чаще, чем в противоположном направлении. Соответственно, объём раствора будет увеличиваться (а концентрация вещества уменьшаться), тогда как объём растворителя будет соответственно уменьшаться.
Например, к яичной скорлупе с внутренней стороны прилегает полупроницаемая мембрана: она пропускает молекулы воды и задерживает молекулы сахара. Если такой мембраной разделить растворы сахара с концентрацией 5 и 10 % соответственно, то через нее в обоих направлениях будут проходить только молекулы воды. В результате в более разбавленном растворе концентрация сахара повысится, а в более концентрированном, наоборот, понизится. Когда концентрация сахара в обоих растворах станет одинаковой, наступит равновесие. Растворы, достигшие равновесия, называются изотоническими. Если принять меры, чтобы концентрации не менялись, осмотическое давление достигнет постоянной величины, когда обратный поток молекул воды сравняется с прямым.
Осмос, направленный внутрь ограниченного объёма жидкости, называется эндосмосом, наружу — экзосмосом. Перенос растворителя через мембрану обусловлен осмотическим давлением. Это осмотическое давление возникает соответственно Принципу Ле Шателье из-за того, что система пытается выравнять концентрацию раствора в обоих средах, разделенных мембраной, и описывается вторым законом термодинамики. Оно равно избыточному внешнему давлению, которое следует приложить со стороны раствора, чтобы прекратить процесс, то есть создать условия осмотического равновесия. Превышение избыточного давления над осмотическим может привести к обращению осмоса — обратной диффузии растворителя.
В случаях, когда мембрана проницаема не только для растворителя, но и для некоторых растворённых веществ, перенос последних из раствора в растворитель позволяет осуществить диализ, применяемый как способ очистки полимеров и коллоидных систем от низкомолекулярных примесей, например электролитов.
Значение осмоса
Осмос играет важную роль во многих биологических процессах. Мембрана, окружающая нормальную клетку крови, проницаема лишь для молекул воды, кислорода, некоторых из растворённых в крови питательных веществ и продуктов клеточной жизнедеятельности; для больших белковых молекул, находящихся в растворённом состоянии внутри клетки, она непроницаема. Поэтому белки, столь важные для биологических процессов, остаются внутри клетки.
Осмос участвует в переносе питательных веществ в стволах высоких деревьев, где капиллярный перенос не способен выполнить эту функцию.
Осмос широко используют в лабораторной технике: при определении молярных характеристик полимеров, концентрировании растворов, исследовании разнообразных биологических структур. Осмотические явления иногда используются в промышленности, например при получении некоторых полимерных материалов, очистке высоко-минерализованной воды методом обратного осмоса жидкостей.
Клетки растений используют осмос также для увеличения объёма вакуоли, чтобы она распирала стенки клетки (тургорное давление). Клетки растений делают это путём запасания сахарозы. Увеличивая или уменьшая концентрацию сахарозы в цитоплазме, клетки могут регулировать осмос. За счёт этого повышается упругость растения в целом. С изменениями тургорного давления связаны многие движения растений (например, движения усов гороха и других лазающих растений). Пресноводные простейшие также имеют вакуоль, но задача вакуолей простейших заключается лишь в откачивании лишней воды из цитоплазмы для поддержания постоянной концентрации растворённых в ней веществ.
Осмос также играет большую роль в экологии водоёмов. Если концентрация соли и других веществ в воде поднимется или упадёт, то обитатели этих вод погибнут из-за пагубного воздействия осмоса.
Использование в промышленности
Первая в мире электростанция — прототип, использующая для выработки электричества явление осмоса, запущена компанией Statkraft 24 ноября 2009 года в Норвегии вблизи города Тофте. Солёная морская и пресная вода на электростанции разделены мембраной; так как концентрация солей в морской воде выше, между солёной водой моря и пресной водой фьорда развивается явление осмоса, — постоянный поток молекул воды через мембрану в сторону солёной воды. В результате чего давление солёной воды возрастает. [1] Это давление соответствует давлению столба воды в 120 метров высотой, то есть достаточно высокому водопаду. Поток воды достаточен, чтобы приводить в действие гидротурбину, вырабатывающую энергию. [2] Производство носит ограниченный характер, основная цель — тестирование оборудования. Самый проблематичный компонент электростанции — мембраны. По оценкам специалистов Statkraft мировое производство может составить от 1 600 до 1 700 TWh, что сравнимо с потреблением Китая в 2002. Ограничение связано с принципом действия — подобные электростанции могут быть построены только на морском побережье. [3] Это не вечный двигатель, источником энергии является энергия солнца. Солнечное тепло отделяет воду от моря при испарении и посредством ветра переносит на сушу. Потенциальная энергия используется на гидроэлектростанциях, а химическая энергия долго оставалась без внимания.
ОСМОС, ЕГО БИОЛОГИЧЕСКАЯ РОЛЬ
Движущей силой процесса является разность концентраций растворителя по обе стороны мембраны. Осмос, направленный внутрь ограниченного объёма жидкости, называется эндосмосом, наружу – экзосмосом. Перенос растворителя через мембрану обусловлен осмотическим давлением. Это осмотическое давление возникает соответственно Принципу Ле-Шателье из-за того, что система пытается выровнять концентрацию раствора в обеих средах, разделенных мембраной, и описывается вторым законом термодинамики. Оно равно избыточному внешнему давлению, которое следует приложить со стороны раствора, чтобы прекратить процесс, то есть создать условия осмотического равновесия. Превышение избыточного давления над осмотическим может привести к обращению осмоса – обратной диффузии растворителя.
Осмос играет важную роль во многих биологических процессах. Мембрана, окружающая нормальную клетку крови, проницаема лишь для молекул воды, кислорода, некоторых из растворённых в крови питательных веществ и продуктов клеточной жизнедеятельности; для больших белковых молекул, находящихся в растворённом состоянии внутри клетки, она непроницаема. Поэтому белки, столь важные для биологических процессов, остаются внутри клетки. Осмос участвует в переносе питательных веществ в стволах высоких деревьев, где капиллярный перенос не способен выполнить эту функцию. Осмос широко используют в лабораторной технике: при определении молярных характеристик полимеров, концентрировании растворов, исследовании разнообразных биологических структур. Осмотические явления иногда используются в промышленности, например при получении некоторых полимерных материалов, очистке высокоминерализованной воды методом обратного осмоса жидкостей.
Человечество с древних времен, использовало эффект осмоса в процессе засаливания пищи. В результате происходил плазмолиз клеток патогена.
Осмос также играет большую роль в экологии водоёмов. Если концентрация соли и других веществ в воде поднимется или упадёт, то обитатели этих вод погибнут из-за пагубного воздействия осмоса.
Осмос всегда широко использовался в лабораторных исследованиях. С помощью лабораторной техники, использующей явление осмоса, специалисты могут определить молярную характеристику полимеров, концентрацию растворов. Также с помощью осмоса проводят исследования над разнообразными биологическими структурами. Осмотические явления довольно часто используют в промышленности для получения разнообразных полимерных материалов. Совсем недавно осмос начали использовать для выработки электроэнергии. В последнее время очень популярными стали системы по очистке жидкостей и воды, использующие осмос и обратный осмос. Такие системы могут эксплуатироваться как в промышленных объемах, так и на бытовом уровне. В наше время, в каждом магазине бытовой техники можно встретить фильтры для очистки воды, использующих технологию обратного осмоса. Роль осмоса и его значение в будущем будет еще большей, так как проблема очистки воды становится все более острой.
ЛИТЕРАТУРА
Осмос
Резюме
Исторический
Феномен
Осмос демонстрируется прохождением молекул или ионов через мембрану (проницаемую или полупроницаемую), которая разделяет два раствора разного состава (или концентрации). Мембрана должна быть проницаемой для воды (или для растворителя в целом) и непроницаемой для растворенных веществ (идеальные полупроницаемые, селективные или диализирующие мембраны).
Пока два раствора не содержат одинакового количества растворенных частиц в единице объема, происходит движение воды (или растворителя) из наименее концентрированного отсека (называемого гипотонической средой) в наиболее концентрированный отсек (средний гипертонический), который стремится уравновесить концентрации.
Химический потенциал
Осмотическое давление
Осмотическое давление пропорционально концентрациям растворенных веществ по обе стороны от мембраны и температуре; когда один находится в присутствии нескольких растворенных веществ, необходимо учитывать все растворенные вещества (как в случае сложного газа, сумма парциальных давлений ).
Уравнение, применяемое к действительным решениям, со своей стороны,
Поэтому мы можем упростить уравнение:
Мы также можем написать это так:
Заметим аналогию с законом идеального газа
Рассмотрим два водных раствора 1 и 2 осмотического давления, а затем, если вода переходит от 2 к 1; 2 концентрируются ( увеличивается) и 1 разбавляется ( уменьшается) до тех пор, пока осмотическое давление не сравняется. Π 1 <\ displaystyle \ Pi _ <1>> 



Осмотическое давление и гидростатическое давление
Биологическое значение и связь с клеткой
В биологии существует три типа осмотических отношений: гипертоническая, изотоническая и гипотоническая.
Изотоническое соотношение соответствует ситуации, когда раствор в ячейке и раствор в среде имеют сбалансированные концентрации. Размер ячеек остается стабильным и не колеблется.
Осмос, «болезнь» полиэстера
«Фальсифицированные» пероксиды
Фактически, причина находится на уровне растворителей, используемых для разбавления пероксидов (катализаторов). Одному из производителей перекиси пришла неудачная идея использовать нелетучие и растворимые в воде растворители на основе этиленгликоля. Таким образом, катализируемые таким образом полиэфирные смолы содержат смешивающиеся с водой растворители. Конечное количество растворителя было небольшим, но со временем вода абсорбировалась и вызывала образование пузырей. Эти пузыри возникли из-за наличия действительно непроницаемого слоя смолы (т.е. отсутствия смешивающихся с водой растворителей). Явление потребовалось достаточно времени, чтобы заявить и понять, что производитель перекиси успел принять участие в строительстве большого количества лодок. Поскольку был обеспокоен только один производитель, это объясняет, почему не все лодки были затронуты. Соли кобальта, которые являются активаторами перекиси, напрямую не затрагиваются: они представляют собой соли органических кислот (например, октоат кобальта) и не растворяются в воде.
Осмос и осмотическое давление



Если разделить раствор и растворитель при помощи полупроницаемой перегородки (мембраны), пропускающей свободно молекулы растворителя и задерживающей молекулы растворенного вещества, то наблюдается односторонняя диффузия растворителя.
Такого рода диффузия обусловливается тем, что число молекул растворителя в единице объема больше, чем в таком же объеме раствора, так как в растворе часть объема занимают молекулы растворенного вещества. В результате молекулярного движения перемещение молекул растворителя через мембрану из растворителя в раствор преобладает над перемещением их в обратном направлении.
Односторонняя диффузия растворителя к раствору называется осмосом, а сила, обусловливающая осмос, отнесенная к единице поверхности полупроницаемой мембраны, называется осмотическим давлением.
Механизм осмоса нельзя объяснить только тем, что полупроницаемые мембраны играют роль сита с ячейками, через которые свободно проходят молекулы растворителя, но не проходят молекулы растворенного вещества.
По-видимому, механизм осмоса значительно сложнее. Здесь большую роль играют строение и состав мембраны.
В зависимости от природы мембраны механизм осмоса будет различен. В одних случаях через мембрану свободно проходят только те вещества, которые в ней растворяются, в других случаях мембрана взаимодействует с растворителем, образуя промежуточные непрочные соединения, которые легко распадаются, и, наконец, она может представлять и пористую перегородку с определенными размерами пор.
Для измерения осмотического давления в сосуд с полупроницаемыми стенками наливают исследуемый раствор и плотно закрывают пробкой, в которую вставлена трубка, соединенная с манометром. Такой прибор для измерения осмотического давления называется осмометром.
Осмометр с раствором погружают в сосуд с растворителем. В начале процесса растворитель из наружного сосуда диффундирует в осмометр с большей скоростью, чем из него, поэтому уровень жидкости в трубке осмометра поднимается, что создает в ней гидростатическое давление, которое постепенно увеличивается. По мере увеличения гидростатического давления скорости диффузии растворителя в осмометр и из осмометра уравниваются, в результате чего наступает состояние динамического равновесия, подъем жидкости в трубке осмометра прекращается.
Гидростатическое давление, установившееся в результате осмоса, служит мерой осмотического давления.
Измерение осмотического давления при помощи осмометра не всегда возможно с достаточной точностью, так как не существует мембран, способных задерживать все частицы растворенного вещества. Измеряемое значение осмотического давления для одного и того же раствора будет, следовательно, в какой-то мере зависеть от природы мембраны.
Осмотическое давление возникает лишь на границе между раствором и растворителем (или раствором другой концентрации), если эта граница образована полупроницаемой перегородкой. Раствор, содержащийся в обыкновенном сосуде, не оказывает на его стенки никакого иного давления, кроме обычного гидростатического. Поэтому осмотическое давление надо рассматривать не как свойство растворенного вещества, или растворителя, или самого раствора, а как свойство системы из растворителя и раствора с полупроницаемой перегородкой между ними.
Зако́ны Ра́уля — общее название открытых французским химиком Ф. М. Раулем в 1887 г. количественных закономерностей, описывающих некоторые коллигативные (зависящие отконцентрации, но не от природы растворённого вещества) свойства растворов.
Первый закон Рауля [править]
Первый закон Рауля связывает давление насыщенного пара над раствором с его составом; он формулируется следующим образом:
· Парциальное давление насыщенного пара компонента раствора прямо пропорционально его мольной доле в растворе, причём коэффициент пропорциональности равен давлению насыщенного пара над чистым компонентом.

Для бинарного раствора, состоящего из компонентов А и В (компонент А считаем растворителем) удобнее использовать другую формулировку:
· Относительное понижение парциального давления пара растворителя над раствором не зависит от природы растворённого вещества и равно его мольной доле в растворе.
На поверхности оказывается меньше способных испаряться молекул растворителя, ведь часть места занимает растворённое вещество.
Растворы, для которых выполняется закон Рауля, называются идеальными. Идеальными при любых концентрациях являются растворы, компоненты которых очень близки по физическим и химическим свойствам (оптические изомеры, гомологи и т. п.), и образование которых не сопровождается изменением объёма и выделением либо поглощением теплоты. В этом случае силы межмолекулярного взаимодействиямежду однородными и разнородными частицами примерно одинаковы, и образование раствора обусловлено лишь энтропийным фактором.
Отклонения от закона Рауля [править]
Растворы, компоненты которых существенно различаются по физическим и химическим свойствам, подчиняются закону Рауля лишь в области очень малых концентраций; при больших концентрациях наблюдаются отклонения от закона Рауля. Случай, когда истинные парциальные давления паров над смесью больше, чем вычисленные по закону Рауля, называют положительными отклонениями. Противоположный случай, когда парциальные давления паров компонентов оказываются меньше вычисленных — отрицательные отклонения.
Причиной отклонений от закона Рауля является то обстоятельство, что однородные частицы взаимодействуют друг с другом иначе, чем разнородные (сильнее в случае положительных и слабее в случае отрицательных отклонений).
Реальные растворы с положительными отклонениями от закона Рауля образуются из чистых компонентов с поглощением теплоты (ΔНраств > 0); объём раствора оказывается больше, чем сумма исходных объёмов компонентов (ΔV > 0). Растворы с отрицательными отклонениями от закона Рауля образуются с выделением теплоты (ΔНраств −1 ·кг соответственно. Поскольку одномоляльный раствор не является бесконечно разбавленным, второй закон Рауля для него в общем случае не выполняется, и величины этих констант получаютэкстраполяцией зависимости из области малых концентраций до m = 1 моль/кг.
Для водных растворов в уравнениях второго закона Рауля моляльную концентрацию иногда заменяют молярной. В общем случае такая замена неправомерна, и для растворов,плотность которых отличается от 1 г/см³, может привести к существенным ошибкам.
Второй закон Рауля даёт возможность экспериментально определять молекулярные массы соединений, неспособных к диссоциации в данном растворителе; его можно использовать также для определения степени диссоциации электролитов.
Растворы электролитов [править]
Законы Рауля не выполняются для растворов (даже бесконечно разбавленных), которые проводят электрический ток — растворов электролитов. Для учёта этих отклонений Вант-Гоффвнёс в приведённые выше уравнения поправку — изотонический коэффициент i, неявно учитывающий диссоциацию молекул растворённого вещества:
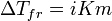
Неподчинение растворов электролитов законам Рауля и принципу Вант-Гоффа послужили отправной точкой для создания С. А. Аррениусом теории электролитической диссоциации.
Эбуллиоскопическая константа– разница между температурой кипения раствора и температурой чистого растворителя.
Криоскопическая константа– разница между температурой замерзания раствора и температурой чистого растворителя.
74. Явление осмоса, его роль в биологических системах. Осмотическое давление. Закон Вант-Гоффа.
Растворы изотонические, гипо- и гипертонические.
Явление осмоса наблюдается в тех средах, где подвижность растворителя больше подвижности растворённых веществ. Важным частным случаем осмоса является осмос через полупроницаемую мембрану. Полупроницаемыми называют мембраны, которые имеют достаточно высокую проницаемость не для всех, а лишь для некоторых веществ, в частности, для растворителя. (Подвижность растворённых веществ в мембране стремится к нулю). Как правило, это связано с размерами и подвижностью молекул, например, молекула воды меньше большинства молекул растворённых веществ. Если такая мембрана разделяет раствор и чистый растворитель, то концентрация растворителя в растворе оказывается менее высокой, поскольку там часть его молекул замещена на молекулы растворённого вещества (см. Рис. 1). Вследствие этого, переходы частиц растворителя из отдела, содержащего чистый растворитель, в раствор будут происходить чаще, чем в противоположном направлении. Соответственно, объём раствора будет увеличиваться (а концентрация вещества уменьшаться), тогда как объём растворителя будет соответственно уменьшаться.
Значение осмоса [править]
Осмос играет важную роль во многих биологических процессах. Мембрана, окружающая нормальную клетку крови, проницаема лишь для молекул воды, кислорода, некоторых из растворённых в крови питательных веществ и продуктов клеточной жизнедеятельности; для больших белковых молекул, находящихся в растворённом состоянии внутри клетки, она непроницаема. Поэтому белки, столь важные для биологических процессов, остаются внутри клетки.
Осмос участвует в переносе питательных веществ в стволах высоких деревьев, где капиллярный перенос не способен выполнить эту функцию.
Осмос широко используют в лабораторной технике: при определении молярных характеристик полимеров, концентрировании растворов, исследовании разнообразных биологических структур. Осмотические явления иногда используются в промышленности, например при получении некоторых полимерных материалов, очистке высоко-минерализованной воды методом обратного осмоса жидкостей.
Клетки растений используют осмос также для увеличения объёма вакуоли, чтобы она распирала стенки клетки (тургорное давление). Клетки растений делают это путём запасания сахарозы. Увеличивая или уменьшая концентрацию сахарозы в цитоплазме, клетки могут регулировать осмос. За счёт этого повышается упругость растения в целом. С изменениями тургорного давления связаны многие движения растений (например, движения усов гороха и других лазающих растений). Пресноводные простейшие также имеют вакуоль, но задача вакуолей простейших заключается лишь в откачивании лишней воды из цитоплазмы для поддержания постоянной концентрации растворённых в ней веществ.
Осмос также играет большую роль в экологии водоёмов. Если концентрация соли и других веществ в воде поднимется или упадёт, то обитатели этих вод погибнут из-за пагубного воздействия осмоса.
Осмотическое давление (обозначается π) — избыточное гидростатическое давление на раствор, отделённый от чистого растворителя полупроницаемой мембраной, при котором прекращается диффузия растворителя через мембрану. Это давление стремится уравнять концентрации обоих растворов вследствие встречной диффузии молекул растворённого вещества и растворителя.
ЗАКОН ВАНТ-ГОФФА описывает зависимость ОСМОТИЧЕСКОГО ДАВЛЕНИЯ разбавленных растворов от температуры и молярной концентрации раствора:
Вант-Гофф пришел к заключению, что закон Авогадро справедлив и для разбавленных растворов. Он экспериментально установил, что осмотическое давление, представляющее собой меру стремления двух различных растворов по обе стороны мембраны к выравниванию концентрации, в слабых растворах зависит не только от концентрации, но и от температуры и, следовательно, подчиняется законам термодинамики газов. Вант-Гофф выразил осмотическое давление формулой РV = iRT, где Р означает осмотическое давление вещества, растворенного в жидкости; V – объем; R – газовую постоянную; Т – температуру и i – коэффициент, который для газов часто равен 1, а для растворов, содержащих соли, – больше единицы. Вант-Гофф смог объяснить, почему изменяется значение i, связав этот коэффициент с числом ионов, находящихся в растворе. Проведенные Вант-Гоффом исследования разбавленных растворов явились обоснованием теории электролитической диссоциации С.Аррениуса. Впоследствии Аррениус приехал в Амстердам и работал вместе с Вант-Гоффом.
Гипотонические растворы отличаются от изотонического меньшей концентрацией и соответственно меньшим осмотическим давлением. При контакте с тканями вода из гипотонических растворов поступает в клетки тканей. Вследствие этого они набухают, а при чрезмерном накоплении в них воды наступает разрыв клеточных оболочек, т. е. лизис клеток.
Применение гипотонических растворов натрия хлорида в практике очень ограничено. В ряде случаев они используются для приготовления растворов веществ, применяемых для инфильтрационной анестезии. Действиеанестетиков в гипотонических растворах усиливается, так как последние способствуют более глубокому проникновению веществ в ткани.
Гипертонические растворы, растворы, осмотическое давление которых выше осмотического давления в растительных или животных клетках и тканях. В зависимости от функциональной, видовой и экологической специфики клеток осмотическое давление в них различно, и раствор, гипертоничный для одних клеток, может оказаться изотоничным или даже гипотоничным для др. При погружении растительных клеток в Г. р. он отсасывает воду из клеток, которые уменьшаются в объёме, а затем дальнейшее сжатие прекращается и протоплазма отстаёт от клеточных стенок (см. Плазмолиз). Эритроциты крови человека и животных в Г. р. также теряют воду и уменьшаются в объёме. Г. р. в сочетании с гипотоническими растворами иизотоническими растворами применяют для измерения осмотического давления в живых клетках и тканях.