13 лучших примеров осмоса в повседневной жизни
Что такое осмос?
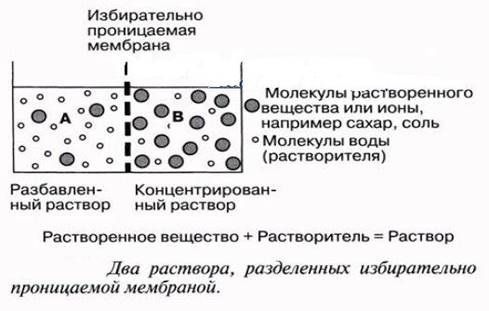
Но что такое полупроницаемая мембрана? Что ж, это своего рода барьер, через который проходят одни молекулы или вещества, но не другие. Например, пластиковая пленка позволяет водяному пару и воздуху проходить через нее, но не пище или воде. Точно так же мембраны клеток пропускают воду и определенные растворенные вещества (крошечные молекулы, растворенные в растворителе), блокируя при этом другие растворенные вещества.
Этот процесс был впервые задокументирован французским физиком Жаном-Антуаном Нолле в 1748 году. Более века спустя немецкий химик изобрел высокоселективные осаждающие мембраны, продвигая искусство и технику измерения осмотического потока.
Как это работает?
Осмос всегда пытается уравнять концентрацию по обе стороны мембраны. Поскольку растворенное вещество не может проходить через мембрану, перемещаться должен только растворитель (вода). По мере приближения к равновесию раствор становится более стабильным. Таким образом, осмос поддерживает законы термодинамики.
Виды осмоса
Обычно бывает два типа осмоса:
Чтобы лучше объяснить это явление, мы перечислили несколько очень хороших примеров осмоса, с которыми мы сталкиваемся в повседневной жизни.
13. Изюм в воде
Тип: Эндосмос
Поскольку растворитель (чистая вода) входит в клетку изюма, это является примером эндосмоса.
12. Картофель в сахарном растворе
Тип: Экзосмос
Если положить картофель в сахарный раствор, он со временем сожмется. Это связано с тем, что в клетках картофеля концентрация воды намного выше, чем в растворе сахара, поэтому вода выходит из картофеля через его мембрану в раствор сахара.
Поскольку растворитель выходит из клеток картофеля и попадает в раствор сахара, пытаясь достичь равновесия, это пример экзосмоса.
11. Растения поглощают воду из почвы
Тип: Эндосмос
В то время как растения поглощают воду по всей своей поверхности (листья, стебли и корни), большая часть воды поглощается корневыми волосками. Эти корневые волоски действуют как полупроницаемый барьер, позволяя молекулам воды (растворителю) перемещаться от высокой концентрации (почва) к низкой концентрации (корни).
В результате корневые волосковые клетки становятся более набухшими, а их осмотическое давление (способность впитывать растворители) падает.
Затем молекулы воды перемещаются в трубки, называемые сосудами ксилемы, и транспортируются к листьям. Внутри клеток ксилемы молекулы воды оказывают сильное влияние друг на друга за счет водородных связей. Когда вода испаряется через устьица (крошечные поры на листьях), через клетки ксилемы корня выводится больше воды, чтобы заменить то, что было потеряно.
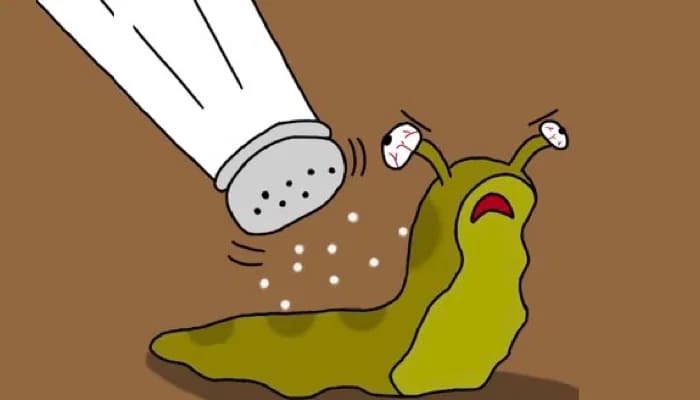
10. Соль на слизнях
Тип: Экзосмос
Соль и слизни плохо сочетаются. Вы когда-нибудь задумывались, почему соль убивает слизней и улиток? Влажная кожа слизняка действует как полупроницаемая мембрана. Высокая концентрация соли на коже слизняка вытягивает воду из его клеток посредством осмоса.
Вода выходит наружу, потому что это уравновешивает концентрацию соли между внешней и внутренней стороной кожи слизняка. Как и большинству других живых организмов, слизням для обслуживания нужна вода. А когда они теряют слишком много воды, они сморщиваются и умирают.
9. Красные кровяные тельца, помещенные в пресную воду
Тип: Эндосмос
При помещении в пресную воду вода попадает в клетки посредством осмоса, вызывая набухание клеток. Это происходит потому, что концентрация ионов и других растворенных частиц внутри эритроцита выше, чем вне его.
Количество воды, которая может попасть в клетки, контролируется давлением клеточной мембраны, действующим на содержимое клетки. В большинстве случаев клетка потребляет больше воды, чем может выдержать ее мембрана, что приводит к взрыву клетки. Это явление называется гемолизом.
Однако, когда красные кровяные тельца помещаются в раствор с более высокой концентрацией растворенного вещества, вода выходит из клетки. В результате клетки становятся меньше и имеют зубчатую форму.
8. Рыбы впитывают воду через кожу и жабры
Тип: эндосмос или экзосмос в зависимости от вида рыб.
Если поместить морскую или пресноводную рыбу в воду с разной концентрацией соли, она погибнет из-за попадания или выхода воды в ее клетки.
Кровь и физиологические жидкости пресноводных рыб намного соленее, чем вода, в которой они плавают. Таким образом, вода проходит через их жабры. Точно так же рыба, обитающая в океане, имеет тенденцию терять воду через жабры.
Как и человеческое тело, рыбьему телу для наилучшего функционирования необходима определенная концентрация соли. Они не могут противостоять слишком большому количеству воды, втекающей или вытекающей через жабры. Пресноводная рыба лопнет, а морская засохнет.
Однако этого не происходит, потому что их жабры содержат специализированные клетки, которые выборочно перекачивают соль в кровь или из нее. Клетки пресноводных рыб регулярно переносят соль, а клетки морских рыб регулярно ее выкачивают. А поскольку океанская вода очень соленая, рыба откачивает излишки соли через жабры и почки.
7. Полоскание горла с соленой водой избавляет от боли в горле
Тип: экзосмос (избыток жидкости выбрасывается из тканей горла).
Соленая вода на самом деле не лечит боль в горле, но помогает уменьшить боль и дискомфорт. Это потому, что соленая вода содержит более высокую концентрацию растворенного вещества (соли), чем то, что присутствует в тканях нашего горла.
Более конкретно, осмотическое давление соленой воды больше, чем давление в жидкости окружающих клеток. Поэтому, когда мы полощем горло, избыток жидкости выходит из тканей горла, уменьшая отек и облегчая боль.
6. Сахар на клубнике
Тип: Экзосмос
Наружная мембрана клубники действует как полупроницаемый слой между ее внутренней и внешней частью. Внутренняя часть уже содержит воду и натуральный сахар. При посыпании сахара на срезанную клубнику, большее количество сахара за пределами клеток плода (в сочетании со способностью сахара притягивать воду) вызывает движение воды наружу к поверхности клубники.
Этот процесс можно использовать для приготовления вкусных продуктов, таких как мацерированная клубника, желе и джемы. Его также можно использовать для продления срока хранения фруктов.
5. Консервирование продуктов питания
Тип: Экзосмос (клетки бактерий теряют воду)
Они действуют не только как усилители вкуса, но и как отличные консерванты, убивая бактерии и предотвращая рост других вредных микроорганизмов.
Высокая концентрация сахара и соли гипертонически воздействует на клетки бактерий. Клетки бактерий теряют воду из-за более высоких концентраций снаружи и становятся менее проводящими для поддержания роста микроорганизмов.
4. Переваренная пища всасывается в тонком и толстом кишечнике
Тип: Эндосмос
Когда вы пьете воду или едите пищу, она движется изо рта по пищеводу в желудок. Внутри желудка пища распадается на множество мелких частей, которые смешиваются с желудочными жидкостями. Смесь образует густую полужидкую массу, называемую химусом. Когда химус попадает в тонкий кишечник, происходит осмос.
Клетки кишечного эпителия (которые образуют слизистую оболочку кишечника) имеют более низкую концентрацию, чем химус. Таким образом, чтобы достичь равновесия, растворитель (вода) проникает в эти клетки через полупроницаемые мембраны, забирая с собой некоторые питательные вещества.
Рядом с эпителиальными клетками находятся капилляры. И питательные вещества, и вода проходят через клетки капилляров в кровоток.
3. Патогенные бактерии мешают кишечным клеткам
Бактерии холеры, полученные с помощью сканирующего электронного микроскопа
Тип: Экзосмос
Некоторые патогенные бактерии, такие как Vibrio cholerae, способны вмешиваться в каналы транспорта ионов кишечных клеток человека. Они производят энтеротоксины, которые изменяют проницаемость эпителиальных клеток кишечной стенки за счет образования пор.
В результате осмоса вода и другие жидкие соединения выводятся из организма, что приводит к сильному обезвоживанию и диарее. Эти бактерии могут крепко держаться за клетки кишечника, в то время как обычные бактерии, живущие в нашем желудке, вымываются. Таким образом, бактерии холеры получают достаточно области для роста и размножения. Умный крошечный микроб, не так ли?
2. Вызванная контактными линзами сухость глаз
Тип: Экзосмос
Знаете ли вы, почему мы помещаем контактные линзы в физиологический раствор? Почему не чистая вода? Это связано с тем, что физиологический раствор для контактных линз содержит такую же концентрацию соленой воды, как и ваш глаз.
Когда вы держите линзы внутри раствора, они остаются влажными, мягкими и удобными. В противном случае они имеют тенденцию впитывать влагу из глаз посредством осмоса, поскольку теряют воду во время носки.
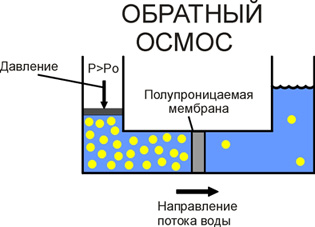
1. Очистка воды
Этот процесс широко используется для удаления из воды распространенных загрязняющих веществ, в том числе пестицидов свинца, нитратов, фтора, сульфатов, мышьяка, бактерий и многого другого.
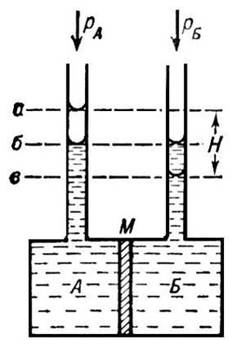
Осмотическое давление
Осмотическое давление (обозначается π) — избыточное гидростатическое давление на раствор, отделённый от чистого растворителя полупроницаемой мембраной, при котором прекращается диффузия растворителя через мембрану. Это давление стремится уравнять концентрации обоих растворов вследствие встречной диффузии молекул растворённого вещества и растворителя.
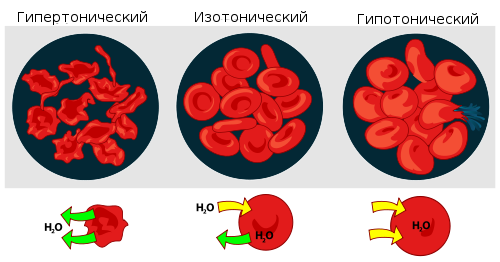
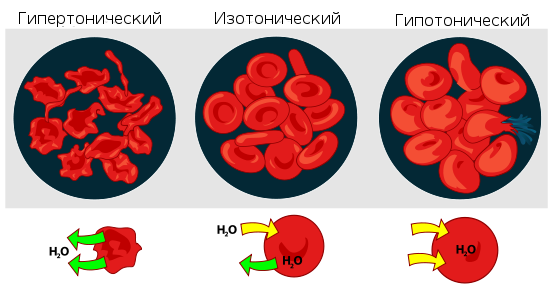
Мера градиента осмотического давления, то есть различия водного потенциала двух растворов, разделённых полупроницаемой мембраной, называется тоничность. Раствор, имеющий более высокое осмотическое давление по сравнению с другим раствором, называется гипертоническим, имеющий более низкое — гипотоническим.
Осмотическое давление может быть весьма значительным. В дереве, например, под действием осмотического давления растительный сок (вода с растворёнными в ней минеральными веществами) поднимается по ксилеме от корней до самой верхушки. Одни только капиллярные явления не способны создать достаточную подъёмную силу — например, секвойям требуется доставлять раствор на высоту до 100 метров. При этом в дереве движение концентрированного раствора, каким является растительный сок, ничем не ограничено.
Если же подобный раствор находится в замкнутом пространстве, например, в клетке крови, то осмотическое давление может привести к разрыву клеточной мембраны. Именно по этой причине лекарства, предназначенные для введения в кровь, растворяют в изотоническом растворе, содержащем столько хлорида натрия (поваренной соли), сколько нужно, чтобы уравновесить создаваемое клеточной жидкостью осмотическое давление. Если бы вводимые лекарственные препараты были изготовлены на воде или очень сильно разбавленном (гипотоническом по отношению к цитоплазме) растворе, осмотическое давление, заставляя воду проникать в клетки крови, приводило бы к их разрыву. Если же ввести в кровь слишком концентрированный раствор хлорида натрия (3-5-10 %, гипертонические растворы), то вода из клеток будет выходить наружу, и они сожмутся. В случае растительных клеток происходит отрыв протопласта от клеточной оболочки, что называется плазмолизом. Обратный же процесс, происходящий при помещении сжавшихся клеток в более разбавленный раствор, — соответственно, деплазмолизом.
Величина осмотического давления, создаваемая раствором, зависит от количества, а не от химической природы растворенных в нём веществ (или ионов, если молекулы вещества диссоциируют), следовательно, осмотическое давление является коллигативным свойством раствора. Чем больше концентрация вещества в растворе, тем больше создаваемое им осмотическое давление. Это правило, носящее название закона осмотического давления, выражается простой формулой, очень похожей на некий закон идеального газа:

Это показывает также схожесть свойств частиц растворённого вещества в вязкой среде растворителя с частицами идеального газа в воздухе. Правомерность этой точки зрения подтверждают опыты Ж. Б. Перрена (1906): распределение частичек эмульсии смолы гуммигута в толще воды в общем подчинялось закону Больцмана.
Осмотическое давление, которое зависит от содержания в растворе белков, называется онкотическим (0,03 — 0,04 атм.). При длительном голодании, болезни почек концентрация белков в крови уменьшается, онкотическое давление в крови снижается и возникают онкотические отёки: вода переходит из сосудов в ткани, где πОНК больше. При гнойных процессах πОНК в очаге воспаления возрастает в 2-3 раза, так как увеличивается число частиц из-за разрушения белков. В организме осмотическое давление должно быть постоянным (≈ 7,7 атм.). Поэтому пациентам вводят изотонические растворы (растворы, осмотическое давление которых равно πПЛАЗМЫ ≈ 7,7 атм. (0,9 % NaCl — физиологический раствор, 5 % раствор глюкозы). Гипертонические растворы, у которых π больше, чем πПЛАЗМЫ, применяются в медицине для очистки ран от гноя (10 % NaCl), для удаления аллергических отёков (10 % CaCl2, 20 % глюкоза), в качестве слабительных лекарств (Na2SO4∙10H2O, MgSO4∙7H2O).
Закон осмотического давления можно использовать для расчёта молекулярной массы данного вещества (при известных дополнительных данных).
Осмотическое давление
Из Википедии — свободной энциклопедии
Осмотическое давление (обозначается π) — избыточное гидростатическое давление на раствор, отделённый от чистого растворителя полупроницаемой мембраной, при котором прекращается диффузия растворителя через мембрану (осмос). Это давление стремится уравнять концентрации обоих растворов вследствие встречной диффузии молекул растворённого вещества и растворителя.
Мера градиента осмотического давления, то есть различия водного потенциала двух растворов, разделённых полупроницаемой мембраной, называется тоничностью. Раствор, имеющий более высокое осмотическое давление по сравнению с другим раствором, называется гипертоническим, имеющий более низкое — гипотоническим.
Если же подобный раствор находится в замкнутом пространстве, например, в клетке крови, то осмотическое давление может привести к разрыву клеточной мембраны. Именно по этой причине лекарства, предназначенные для внутривенного введения, растворяют в изотоническом растворе, содержащем столько хлорида натрия (поваренной соли), сколько нужно, чтобы уравновесить создаваемое клеточной жидкостью осмотическое давление. Если бы вводимые лекарственные препараты были изготовлены на воде или очень сильно разбавленном (гипотоническом по отношению к цитоплазме) растворе, осмотическое давление, заставляя воду проникать в клетки крови, приводило бы к их разрыву. Если же ввести в кровь слишком концентрированный раствор хлорида натрия (3—10 %, гипертонические растворы), то вода из клеток будет выходить наружу, и они сожмутся. В случае растительных клеток происходит отрыв протопласта от клеточной оболочки, что называется плазмолизом. Обратный же процесс, происходящий при помещении сжавшихся клеток в более разбавленный раствор, — соответственно, деплазмолизом.
Реферат: Осмос, осмотическое давление и его биологическая роль
| Название: Осмос, осмотическое давление и его биологическая роль Раздел: Рефераты по химии Тип: реферат Добавлен 07:25:32 20 мая 2011 Похожие работы Просмотров: 21767 Комментариев: 23 Оценило: 9 человек Средний балл: 5 Оценка: 5 Скачать |