Анемия: симптомы, степени, лечение
Анемия, или малокровие, – состояние, при котором уменьшается концентрация гемоглобина (переносчика кислорода) в крови. Часто сопровождается понижением количества эритроцитов (красных кровяных телец). Это не самостоятельное заболевание, а синдром других болезней.
Анемия у женщин диагностируется, если гемоглобин опускается ниже 120 г/л (при беременности – ниже 110 г/л), а у мужчин, если показатель понижается до 130 г/л.
При малокровии клетки и ткани не получают достаточного количества кислорода, что приводит к нарушению функционирования внутренних органов, способствует развитию других заболеваний.
Виды анемии
В зависимости от причины различают 4 группы патологии:
Известно несколько разновидностей дефицитной патологии:
Самые распространенные формы гемолитической анемии:
Вид анемии определяется врачом — терапевтом или гематологом на основе анализов крови.
Симптомы анемии
Признаки патологии зависят от ее вида и степени тяжести. Легкая форма часто протекает бессимптомно. Возможны общая слабость, повышенная утомляемость, ослабление внимания. В тяжелых случаях (при понижении гемоглобина ниже 50 г/л) может развиться ацидоз (закисление крови), сердечная недостаточность.
К общим признакам, сопровождающим все виды анемии, принадлежат:
Для железодефицитной формы характерны наличие трещин и заед в углах рта, поперечная исчерченность, слоистость и ломкость ногтей, сечение и выпадение волос, искажение вкусовых предпочтений (желание есть мел, землю), понижение артериального давления, обмороки.
При В12-дефицитной анемии человек ощущает покалывание и онемение в пальцах, чувство ползания мурашек, скованность и отечность конечностей, кожа приобретает желтоватый оттенок, а язык – малиновый, походка становится шаткой.
При апластическом малокровии в грудной области возникают колющие боли, физические усилия сопровождаются одышкой. На коже появляются мелкие кровоизлияния (петехии) в виде красной сыпи, кровоточат десны, менструации становятся длительными и обильными.
При фолиеводефицитной форме затрудняется пережевывание и глотание пищи, атрофируются слизистые оболочки ЖКТ, развивается непереносимость кислой пищи.
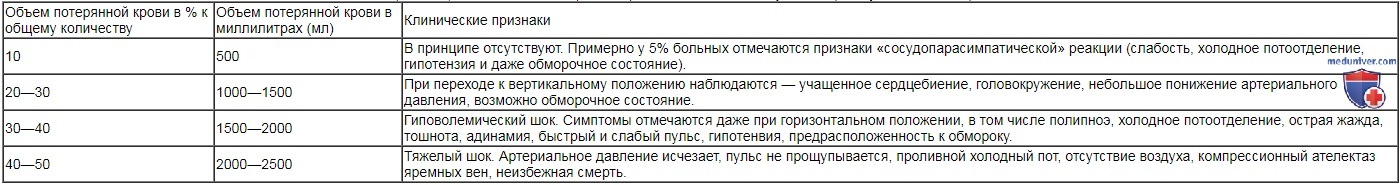
При постгеморрагической анемии кружится голова, понижаются давление и температура тела, учащается (но становится слабым) пульс, появляется холодный пот. Если кровотечение обильное, то возможны судороги, коматозное состояние и даже остановка сердца.
Для гемолитического малокровия характерны желтушность кожи и слизистых оболочек, потемнение мочи и кала, повышенная температура тела, увеличение размеров печени или селезенки.
При гипопластической форме усиливается кровоточивость десен, в ротовой полости образуются язвы, на коже появляются синяки, развивается тахикардия, постоянно хочется спать.
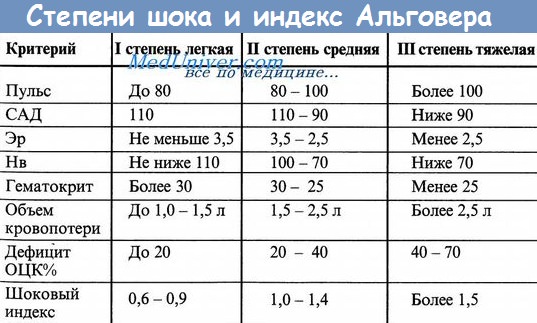
Степени анемии
В зависимости от уровня гемоглобина различают 3 степени анемии:
Причины возникновения анемии
Спровоцировать развитие анемии способны различные факторы:
Часто анемия развивается при:
В группу риска входят вегетарианцы, доноры, профессиональные спортсмены, беременные женщины.
Основная причина анемии у детей – быстрый рост, требующий усиленного питания, и несовершенство механизмов кроветворения. В результате ослабляется иммунная система, усиливается восприимчивость к инфекционным заболеваниям.
Лечение анемии
Метод терапии врач подбирает индивидуально в зависимости от причины малокровия и тяжести состояния.
При железодефицитной анемии доктор порекомендует включить в свой рацион продукты, богатые железом. При необходимости назначит железосодержащие препараты.
Если малокровие вызвано инфекцией или интоксикацией, то необходимо избавиться от возбудителя болезни и провести детоксикацию организма.
При постгеморрагической анемии следует остановить кровотечение. Дополнительно приписывают лекарства, нормализующие объем крови и количество кровяных клеток. Если возникает угроза для жизни, переливают кровь, вводят кровезаменители.
Гемолитическую анемию лечат анаболическими гормонами и глюкокортикоидами. Дополнительно назначают витамины. Если консервативное лечение оказывается неэффективным, то прибегают к операции, во время которой удаляют селезенку.
При гипопластической форме стимулируют процессы кроветворения, выполняют переливание крови, делают пересадку костного мозга.
Серповидно-клеточную анемию лечат вливанием кровезаменителей или эритроцитарной массы.
Что такое острая постгеморрагическая анемия тяжелой степени
Острая постгеморрагическая анемия развивается после резкой и разовой потери крови за счет внешнего или внутреннего кровоизлияния.
При небольших, повторяющихся в течение длительного периода времени геморрагиях, развивающаяся анемия представляется как результат деплеции тканевого железа.
В большинстве случаев место кровоизлияния нетрудно установить. Частные, связанные с этим проблемы возникают при внутреннем кровоизлиянии. В таких случаях следует не забывать, что наиболее частые острые геморрагии отмечаются у мужчин в желудочно-кишечном тракте, в то время как у женщин — в половых органах.
Большое практическое значение представляет также уточнение причины явления — местного ли она характера или составляет проявление кровоточивости.
Клинические признаки острой постгеморрагической анемии
Обнаруживаемые у больного признаки зависят от величины и скорости кровотечения, его локализации, общего состояния больного (состояния сердечно-сосудистой системы, наличия сопутствующих заболеваний и пр.), прошедшего от кровоизлияния времени.
Исходные клинические проявления относятся за счет быстрого развития гиповолемии. Их интенсивность пропорциональна объему потерянной крови. На следующем за восстановлением объема сосудистой крови этапе развиваются собственно признаки анемии.
Количество потерянной крови не получает точной оценки по цифровым показателям гемоглобина или гематокрита, в связи с компенсаторными колебаниями общего объема сосудистой крови. Клиницисту предстоит решить эту проблему по интенсивности функциональных признаков.
Толкование признаков, связанных с наличием гиповолемии необходимо связать с сопутствующими патологическими условиями и возрастом больного.
После восстановления объема сосудистой крови (самопроизвольно или в результате проведения терапевтических мероприятий) на первый план выступают признаки, связанные с деплецией, находящихся в сосудистой крови эритроцитов. К таковым относятся бледность, общая слабость, одышка при физической нагрузке, сердцебиение, головокружения, анемические шумы.
Выраженность этих признаков зависит от степени анемии, состояния работы сердечно-сосудистой системы и приспособления организма больного к созданным недостатком кислорода условиям.
Признаки, связанные с быстрым сокращением объема сосудистой крови у молодого здорового
Лабораторные признаки острой постгеморрагической анемии
Тромбоцитоз (значения которого достигают 1 млн/мм3) развивается в течение первого часа от начала геморрагии (Hillman). Спустя 2—6 часов отмечается лейкоцитоз (10—30 тыс. на мм3) за счет мобилизации запасов зрелых гранулоцитов (Wintrobe и сотр.). Через 3—5 день после кровоизлияния развивается ретикулоцитоз, максимальные значения которого (10—15%) достигаются за 6—11 дней (Hillman). Гематокрит медленно понижается в ближайшие после прекращения геморрагии 2—3 дня.
У человека в норме, до кровоизлияния, красные кровяные клетки нормоцитные и нормохромные. После развития ретикулоцитоза наблюдается макроцитоз и полихроматофилия.
В формах, сопровождающихся острой анемией, выявляется наличие эритробластов. Обнаружение гипохромии наиболее часто свидетельствует о предшествующем геморрагическому явлению железодефиците. Формула белой крови отражает сдвиг влево.
В костном мозге определяется развитие гиперплазии эритробластов спустя 3—5 дней от геморрагии.
При внутриполостных кровоизлияниях развивается гипербилирубинемия за счет рассасывания разлитой крови. Кровоизлияние в кишечник может сопровождаться повышением показателя азотемии (Попеску,
Патофизиология острой постгеморрагической анемии
Резкое понижение объема сосудистой крови и давления в ней кислорода приводят в действие компенсационные механизмы. Потеря сосудистой крови до 20—30% возмещается, по началу, сужением глубоких и кожных вен, в дальнейшем — сердцебиением и перераспределением крови спланхнических зон в направлении сердечной мышцы и мозга. Когда же объем потерянной крови превышает 40%, отмечается провал артериального давления.
На весьма ранних сроках присоединяется компенсирующее разжижение крови за счет подвоза воды и белков из внесосудистого пространства. Тканевая недостаточность кислорода, в развитии которой участвуют все отмеченные факторы, способствует выделению сосудоактивных веществ и кислых метаболитов, ускоряющих развитие коллапса (Киотан и Кристя).
Линейному сокращению гематокрита соответствует логарифмический рост синтеза эритропоэтина (Адамсон). Эффекты влияния эритропоэтина следующие:
а) ускорение выделения кислорода из эритроцитов;
б) ранний диабез ретикулоцитов;
в) рост костномозгового эритропоэза.
Реакция костного мозга зависит от интенсивности анемии, структурной целостности костного мозга, запаса железа и катализаторов.
Течение острой постгеморрагической анемии
Нормальный костный мозг может восстановить объем красных кровяных клеток примерно за 33 дня (Wintrobe и сотр.). Спустя 10—14 дней от прекращения геморрагии признаки активного восстановления эритроцитов исчезают. Лейкоцитоз нормализуется за 3—4 дня. Дальнейшие наличие гипертромбоцитоза и/или ретикулоцптоза подсказывает мысль о продолжающемся кровоизлиянии. В одинаковой мере сохраняющийся лейкоцитоз свидетельствует о непрекратившейся геморрагии, в частности в той или иной полости организма, или о развитии инфекции.
Диагностирование острой постгеморрагической анемии
В принципе определение механизма развития геморрагии не ставит каких-либо проблем. Лишь появившуюся после внутриполостной геморрагии с дальнейшей желтухой и лихорадкой анемию можно принять за анемию, развившуюся за счет резкого расплавления крови. Вопрос решает определение места кровоизлияния.
Терапия острой постгеморрагической анемии
Проводимое лечение задается целью качественного и количественного восстановления сосудистой крови. В порядке их значения проводятся следующие мероприятия:
а) восстановление объема сосудистой крови;
б) пресечение кровотечения;
в) восстановление массы эритроцитов.
Вместе с тем подбор терапевтического подхода делается в соответствии с количеством потерянной крови, по приведенным ниже критериям. Количество жидкостей, необходимых восстановлению объема сосудистой крови, оценивается из расчета общего количества последней по следующим данным Кривда и Манолеску:
| У мужчин (к % веса тела) | У женщин (к % веса тела) | |
| С развитой мускулатурой. | 7,5% | 7,0% |
| В норме. | 7,0% | 6,5% |
| Худых. | 6,5% | 6,0% |
| Ожирелых. | 6,0% | 5,5% |
Для восстановления общего количества сосудистой крови применяются следующие средства: расствор декстрана, раствор белковой плазмы, кристаллоидный раствор, цельная кровь. Капельное вливание декстрана и крови составляет наиболее полезный способ восстановления массы сосудистой крови. Кровь показана лишь в случае потери более 20% кровяной массы. Назначение сосудопрессорных средств в принципе противопоказано.
Реакция на проводимое лечение оценивается по окраске и температуре покровов, наполнению вен (в основном яремных), исчезновению явлений аноксии, росту артериального давления.
В принципе, после преодоления исходного критического периода лечение анемии сводится к гигиено-диетическим мероприятиям. При нормальном костном мозге и адекватном количестве железа, восстановление всегда может быть самопроизвольным.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Лечение постгеморрагических анемий при язвенных гастродуоденальных кровотечениях
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Гастродуоденальные кровотечения в последнее десятилетие лидируют среди осложнений язвенной болезни [1,4,5]. Большое число работ по этой теме посвящено вопросам гемостаза, прогнозированию повторных кровотечений, выбору метода гемостаза, способам медикаментозной профилактики рецидива [1,4,6]. В этих же источниках отмечен факт поздней госпитализации с момента первого эпизода кровотечения, особенно в тех случаях, когда оно немассивное. Постгеморрагические анемии наблюдаются у большинства больных с длительными сроками неинтенсивного желудочно–кишечного кровотечения (ЖКК), нередко служат веским аргументом в пользу госпитализации пациентов без угрозы рецидива ЖКК и диктуют выбор способа лечения.
При успешном консервативном лечении на фоне первичного эндоскопического гемостаза и отсутствии рецидивов в ранние (до 5 сут.) и поздние сроки актуальным является восстановление гемостазиологических показателей крови, которые влияют на сроки заживления и качество рубцевания язвенного дефекта. Особенно важно это у тех пациентов, у которых язвенное ЖКК появляется на фоне хронической анемии или другой патологии [2,3,9]. Активность регенерации слизистой при язвенных поражениях зависит от транспорта кислорода к тканям эритроцитами. Ведущим патогенетическим звеном постгеморрагических анемий является уменьшение общего объема крови, особенно ее циркулирующей фракции, что ведет к гипоксии, сдвигам кислотно–основного состояния, дисбалансу ионов в клетках и вне их. В зависимости от скорости кровопотери выделяют острую и хроническую постгеморрагические анемии [8,10].
Наблюдения за пациентами показывают, что анемия, связанная с кровопотерей, выявляется не сразу, а спустя день–два, когда возникает гидремическая фаза компенсации кровопотери, выражающаяся в обильном поступлении в кровеносную систему тканевой жидкости (лимфы), в результате чего в сосудистом русле циркулирует первоначальный объем. Эта фаза длится несколько дней в зависимости от величины кровопотери, и наблюдается прогрессирующее равномерное снижение показателей красной крови — гемоглобина и эритроцитов без снижения цветового показателя. Анемия носит нормохромный характер. Спустя 4–5 дней после кровопотери в крови появляются в большом количестве образованные в костном мозгу эритроциты и ретикулоциты. Это костномозговая фаза компенсации анемии. Сроки восстановления нормальной картины крови после однократной или многократной кровопотери различны, зависят от величины кровопотери, индивидуальных особенностей организма, регенераторной способности костного мозга и содержания железа в организме.
Таким образом, при выполнении первичного гемостаза любым способом (как при консервативном лечении, так и после хирургического вмешательства) требуется применение компонентов крови и кровезаменителей в ближайшие сроки после остановки кровотечения. После компенсации объема потерянной крови за счет жидкости необходима коррекция качественного состава циркулирующей крови за счет полноценных компонентов – эритроцитов, лейкоцитов, тромбоцитов. Поэтому в процессе лечения постгеморрагической анемии используют препараты железа, витамины группы В и другие средства, стимулирующие гемопоэз. Отсюда целью нашей работы являлся анализ использования в лечении анемии при язвенных кровопотерях кровезаменителей и различных препаратов железа.
Материал и методы
Нами проведен ретроспективный анализ лечения в течение 4 лет 473 пациентов с кровотечениями из хронических язв желудка и двенадцатиперстной кишки (12 п.к.), среди которых было 340 (71,9%) мужчин и 133 (28,1%) женщины. Всем пациентам при госпитализации в течение 2–4 ч выполнена ЭГДС, при которой в случаях активного кровотечения проводился гемостаз инъекционными, а также электротермическими способами, такими как электрокоагуляция, лазерная коагуляция, микроволновая или аргоноплазменная. У большинства больных применялся комбинированный гемостаз – сочетание инъекционных и термических способов. Для оценки кровоточащих язв пользовались классификацией Forrest. В случаях с нестабильным гемостазом F IIА и F IIВ применяли профилактику рецидива, используя те же способы гемостаза. По локализации источника кровотечения все пациенты разделены на три основные группы, представленные в таблице 1.
Возраст пациентов, включенных в анализ, варьировал от 15 до 97 лет. Существенных различий по возрасту в сформированных группах не обнаружено.
Среди 9 пациентов с послеоперационными язвами у 3–х кровотечение возникло в поздние сроки после операции ваготомии с пилоропластикой, у 2–х – после ушивания перфоративной язвы, у 3–х – после резекций желудка по Б–2, у одной пациентки – после гастроэнтероанастомоза. Малые сроки госпитализации этой группы пациентов связаны с тем, что у них уже имелись осложнения, по поводу которых выполнялись операции, поэтому при начальных проявлениях осложнения они рано обращались за медицинской помощью.
У 26 пациентов кровотечение началось в стационаре, где они проходили лечение по поводу сопутствующей патологии, поэтому у них наблюдались самые короткие сроки верификации источника кровотечения. Основные различия в сроках госпитализации в выделенных группах показаны на рисунке 1.
Срок госпитализации с момента ЖКК колебался от получаса (при появлении его у стационарных пациентов) до 14 сут. в группе ЯБ 12 п.к., до 7 сут. – при ЯБЖ и до 3 сут. – при послеоперационных язвах. Наблюдалась слабая отрицательная корреляция (r=–0,2 при р=0,02) между сроком заболевания и уровнем Нb при поступлении в группах пациентов с язвенными поражениями желудка и 12 п.к. и высокая корреляция (r=0,7 при р=0,02) в группе пациентов с послеоперационными язвами.
Степень тяжести кровопотери оценивали по шкале А.И. Горбашко (1974). Согласно ей на основании клинико–лабораторных показателей были выделены 3 группы пациентов: с легкой, средней и тяжелой кровопотерей. Значимых различий в сроках с момента первого эпизода ЖКК в этих группах не выявлено, потому что они зависят от интенсивности кровотечения, числа рецидивов при поздней обращаемости, имеющейся анемии на фоне другой соматической патологии. Поэтому для выделения группы пациентов с анемией проведено сравнение клинического понятия тяжести кровотечения с лабораторными показателями гемоглобина, гематокрита и эритроцитов при поступлении и в первые сутки лечения. Результаты представлены в таблицах 2 и 3.
В группах пациентов с различной степенью кровопотери имеются существенные различия по уровню Нb (при р 101 г/л препараты железы применялись у 19. В большинстве случаев использовались пероральные препараты 2–валентного железа, у 6 – Феррум Лек внутримышечно. У 9 больных к моменту выписки наблюдалось полное рубцевание язвы либо поверхностный эпителизирующийся язвенный дефект. Оперированных и умерших в группе получавших препараты железа не было. Оценка сроков заживления язв у 19 больных, принимавших препараты железа, и без него у 225 больных в группе с уровнем Нb>101 г/л показала, что существенных различий в заживлении язвы к концу госпитализации не выявлено (χ2=0,139 при р=0,709). Таким образом, процесс заживления язвенного дефекта при нормальных уровнях Нb зависит от других факторов, рассмотрение которых не является целью нашего исследования.
Способы лечения постгеморрагической анемии у 215 больных другой группы представлены в таблице 4.
У пациентов с постгеморрагической анемией в 97 (45,1%) случаях для коррекции анемии применяли препараты железа. В группу с легкой кровопотерей включены больные с признаками хронической анемии на фоне давних эпизодов ЖКК, среднее значение Нb у которых было равно 85,2 г/л (СО – 18,2 г/л). Четверо из них получали Фенюльс. К концу стационарного лечения стадия заживления язвы с поверхностным дефектом наблюдалась только у больного с уровнем Нb 100 г/л, в остальных 3–х случаях язвенный дефект оставался открытым.
У 210 больных со средней и тяжелой кровопотерей (медиана значений Нb составляла 80 г/л; СО – 17,2; ДИ 95% – от 63 до 90) в 93 (44,3%) случаях наряду с гемо– и плазмотрансфузиями применяли препараты железа после стабилизации гемостаза консервативными или хирургическими методами. 46 больных получали Сорбифер или Ферроплекс перорально, а 47 – парентеральные препараты железа: 40 человек – Феррум Лек, 7 человек – Венофер. Средние сроки стационарного лечения больных с тяжелой и средней кровопотерей составляли от 2 до 4 нед., препараты железа применялись 10–14 сут., в дальнейшем рекомендован амбулаторный прием. Различий в уровне показателей красной крови, Нb, гематокрита и эритроцитов в момент госпитализации у больных, получавших разные препараты железа, отмечено не было. Также в группах, получавших пероральные и парентеральные препараты железа, различий в объеме, числе гемо– и плазмотрансфузий не было (χ2=0,052 при р=0,819). Данные об основных показателях красной крови при выписке у пациентов, получавших препараты железа, представлены в таблице 5.
Полученные результаты показывают, что существенных различий (независимо от способа применения препарата) показателей красной крови к концу стационарного лечения не получено. Возможно, это связано с малыми сроками применения препаратов, когда не происходит насыщение организма железом, или при постгеморрагических анемиях (в нашем анализе не наблюдался железодефицит). Оценка зависимости сроков рубцевания язвы при консервативном лечении и приеме препаратов железа у пациентов со средней и тяжелой кровопотерей к концу стационарного лечения показала, что существенных различий в количестве заживших язв к концу лечения не обнаружено (χ2=0,004 при р=0,948). Также не выявлено различий в количестве заживших язв у больных, получавших препараты железа, и без них (χ2=0,734 при р=0,391). У больных, не получавших препараты крови путем проведения инфузионной терапии, как применявших препараты железа, так и без них, мы не выявили существенных различий в заживлении язвы к концу госпитализации (χ2=0,105 при р=0,746).
Данные о влиянии гемотрансфузий на показатели крови и заживление язв представлены в таблице 6.
В ней же представлены данные о выживших пациентах без оперативного лечения кровотечения, у которых была проведена контрольная ЭГДС для оценки рубцевания язвы в поздние сроки. Наблюдаются явные различия уровня Нb у пациентов в группах с переливанием компонентов крови и без переливания. Отмечается тенденция снижения уровня Нb в конце лечения у больных без переливания крови, хотя достоверных отличий не выявлено. У больных, которым были проведены гемотрансфузии, в конце стационарного лечения уровень Нb повысился, однако он не достиг нормальных показателей и достоверно не отличался от исходного. В то же время мы выявили положительное влияние гемотрансфузий на заживление язвенного дефекта, различия в группах по рубцеванию язвы достоверны (χ2=17,39 при р
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Постгеморрагическая анемия
Постгеморрагическая анемия – это комплекс патологических гематологических и клинических изменений в организме больного, который развивается как следствие обильной острой или хронической потери крови. Последняя проявляет себя бледностью кожных покровов, головокружениями, пониженной температурой тела, а в тяжёлых случаях – ощущением заторможенности, шоковыми состояниями и даже потерей сознания. Причина кроется в серьёзном снижении объёма циркулирующей крови, снижении уровня эритроцитов ниже 3,3×1012 клеток/л, но, как правило, без снижения уровня гемоглобина. Сам по себе данный комплекс может протекать как в острой, так и в хронической форме. Вторая – вариант железодефицитного состояния, поскольку механизм её развития и клинические проявления появляются из-за прогрессирующего недостатка железа в организме.
Пройти диагностику и лечение постгеморрагической анемии в Москве приглашает отделение гематологии ЦЭЛТ. Наша многопрофильная клиника одна из первых в России начала предлагать платные медицинские услуги и делает это уже более четверти столетия. Мы располагаем современной лечебно-диагностической базой, которая позволяет точно и правильно ставить диагнозы и проводить лечение в соответствии с международными стандартами. В отделении гематологии ведут приём кандидаты и доктора медицинских наук, профессоры с опытом научной и практической работы от тридцати лет. Ознакомиться с нашими ценами на лечение можно перейдя на вкладку «Услуги и цены». Во избежание недоразумений просим уточнять цифры у операторов нашей информационной линии или на приёме у врача.
Этиология постгеморрагической анемии
Как уже упоминалось, причины развития постгеморрагической анемии кроются в кровопотере, которая развилась из-за внутреннего или наружного кровотечения. Принято выделять:
| Форма | Отличительные особенности |
| Острая постгеморрагическая анемия |