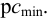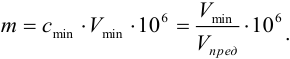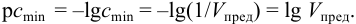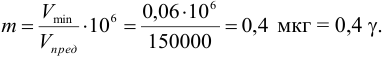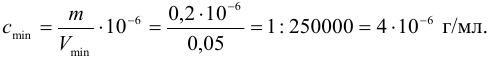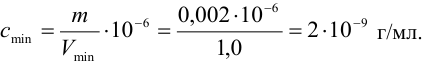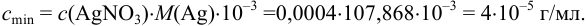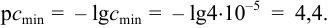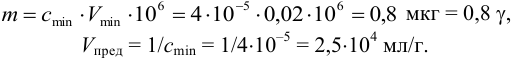ХАРАКТЕРИСТИКА АНАЛИТИЧЕСКИХ РЕАКЦИЙ
Качественный химический анализ большей частью основан на реакциях, которые сопровождаются каким-либо характерным внешним эффектом. При этом не имеет большого значения количественная сторона химического процесса и стехиометрическое соотношение элементов, входящих в состав образующихся соединений. Существенными являются две характеристики химических реакций: чувствительность и избирательность.
Чувствительность реакций
Чувствительность реакции выражается двумя взаимно связанными величинами: чувствительностью определения (минимальная концентрация, или предельное разбавление) и абсолютной чувствительностью (открываемый минимум):
где m — открываемый минимум, мкг, с — минимальная концентрация, т. е. та наименьшая концентрация, которую еще удается обнаружить данным методом, мкг/мл, мкг/г, % и т. п.; V—объем пробы, мл; g — масса пробы, г.
Предельное разбавление характеризуется отношением одной весовой части обнаруживаемого иона или вещества к числу весовых частей анализируемого вещества (основы) или указывается как отношение числа весовых частей обнаруживаемого иона или вещества к 106 весовых частей анализируемого вещества (млн-1, международное обозначение, ррт.). Чувствительность выражается также в %
Значения тис могут изменяться в широких пределах в зависимости от условий реакции. Чувствительность реакции может быть повышена изменением концентрации реагентов, рН среды, порядка смешивания реагентов, экстракцией, флотацией, соосаждением, образованием смешанных соединений, а также путем использования различных методов проведения реакций (капельный анализ, пирохимический анализ и др.) и способов наблюдения продуктов реакции (в обычном световом или электронном микроскопе, в потоке ультрафиолетового света и т. д.). Ниже приведены границы чувствительности различных методов качественного анализа (в %):
Чувствительность аналитических реакций с примерами решения
Чувствительность аналитических реакций
Аналитическими реакциями, пригодными для качественного анализа, являются реакции, сопровождающиеся каким-нибудь внешним эффектом: выпадением и растворением осадка, выделением газообразных веществ, изменением окраски. Выбирая реакции для химического анализа, руководствуются законом действующих масс и представлениями о химическом равновесии в растворах. Для успешного проведения аналитической реакции необходимо соблюдать ряд тех или иных условий, обеспечивающих получение достоверных результатов. Такими условиями являются pH раствора, температура, маскирование или удаление мешающих ионов. Однако даже при соблюдении всех этих условий аналитическая реакция может не дать положительного эффекта, если недостаточна концентрация обнаруживаемого иона в растворе. С концентрацией обнаруживаемого иона в растворе связано понятие «чувствительность» аналитической реакции.
Чувствительность аналитических реакций характеризуется пределом обнаружения 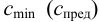
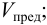
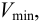
Предел обнаружения 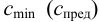
Предел обнаружения m (мкг) — открываемый минимум; это наименьшая масса определяемого компонента, с заданной доверительной вероятностью обнаруживаемая данной аналитической реакцией в минимальном объеме предельно разбавленного раствора.
Предельное разбавление, 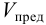
Минимальный объем предельно разбавленного раствора, 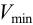
Эти характеристики чувствительности связаны между собой соотношением:
В качественном анализе обычно используют реакции с 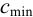
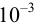
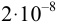
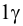
Показатель чувствительности, 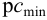
В количественном химическом анализе показателем чувствительности является нижняя граница определяемых содержаний 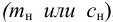
Пример 1.6.
Предельное разбавление ионов 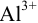
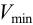
Решение:
По формуле (1.1) находим:
Пример 1.7.
Для обнаружения ионов меди действием раствора аммиака 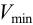
Решение:
С учетом формулы (1.1) рассчитываем 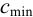
Пример 1.8.
Предельно допустимая концентрация (ПДК) иона аммония в питьевой воде 2,0 мг/л. Предел обнаружения его по реакции с реактивом Несслера составляет 0,002 мкг. Проверьте расчетами возможность обнаружения иона аммония в 1,0 мл воды при содержании, равном ПДК.
Решение:
Рассчитаем минимальную концентрацию иона аммония в растворе, при которой реакция с реактивом Несслера дает положительный эффект:
Сравнивая полученное значение 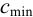
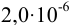
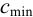
Пример 1.9.
Катионы серебра 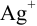
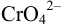
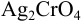
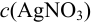
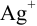
Решение:
Найдем 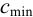
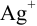
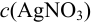
Вычислим показатель чувствительности:
Используя формулу (1.1), найдем 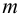
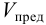
Эти примеры взяты со страницы примеров решения задач по аналитической химии:
Возможны вам будут полезны эти страницы:
Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Основы аналитической химии. ( предел обнаружения, открываемый минимум, предельное разбавление)
Качественная реакция определяется чувствительностью. Её характеризуют три основные параметра:
Спред. = 1 / Vmin [г/мл ]
Все эти параметры связаны между собой.
Сmin = m / Vmin * 0,0000001 => m = Сmin * Vmin * 1000000 => Vmin * 1000000 /W
Техника лабораторного эксперимента. ( Весы и взвешивание, химическая посуда, калибрование посуды, фильтрование.)
Весы́ — устройство или прибор для определения массы тел по действующему на них весу, приближёно считая его равным силе тяжести. Вес тела может быть определён как через сравнение с весом эталонной массы (как в рычажных весах), так и через измерение этой силы через другие физические величины.
Согласно ГОСТ весы можно подразделить на следующие группы:
По точности взвешивания:
По способу установки на месте эксплуатации:
По виду уравновешивающего устройства:
По способу достижения положения равновесия:
По классу точности
Основные параметры весов
Наибольший предел взвешивания (НПВ) — верхняя граница предела взвешивания, определяющая наибольшую массу, измеряемую при одноразовом взвешивании.
Наименьший предел взвешивания (НмПВ) — нижняя граница предела взвешивания, определяется минимальным грузом, при одноразовом взвешивании которого относительная погрешность взвешивания не должна превышать допустимого значения.
Цена деления d — разность значений массы, соответствующих двум соседним отметкам шкалы весов с аналоговым отсчетным устройством, или значение массы, соответствующее дискретности отсчета цифровых весов.
Цена поверочного деления e — условная величина, выраженная в единицах массы, используемая при классификации весов и нормировании требований к ним.
Разновес
Наборы гирь для определённых весов называются разновесом. В зависимости от максимальной и минимальной массы, взвешиваемой на весах, разновес может состоять из большего или меньшего числа элементов.
Современная, наиболее распространённая система численного ряда для разновесов была предложена Д. И. Менделеевым. Она обеспечивает минимальное число операций наложения/снятия гирь на чашки весов при подборе навески.
Точное взвешивание. — С большою точностью можно взвешивать только вполне не изменяемое в отношении веса тело, т. е. негигроскопичное (не притягивающее паров воды), не сгущающее газов в порах, не испаряющееся, или защищенное от изменений на время взвешивания помещением в легкие стеклянные или иные сосуды, закрытые или даже запаянные. Но так как гигроскопичность стеклянной поверхности может еще произвести ощутительную погрешность при взвешивании, то в химических работах тигли с осадками после прокаливания должны быть охлаждены в аппарате для высушивания (эксикатор) или под колоколом воздушного насоса.
изделия из стекла, кварца, фарфора, платины и др. материалов, применяемые для препаративных и химико-аналитических работ. Химическая посуда должна быть устойчива к воздействию химических реагентов, легко отмываться от загрязнений, а материал её должен быть термоустойчив и обладать малым коэффициентом теплового расширения. По назначению она может быть разделена на мерную, немерную и специального применения.
Мерная химическая посуда имеет точную градуировку, её нельзя нагревать. Мерная посуда, как и вся химическая, лабораторная посуда различается по ёмкости, диаметру и формам. К ней относятся: пипетки — для отбора жидкостей (0,1—100 мл) и газов (от 100 мл и выше); бюретки (1—100 мл) — для титрования, измерения точных объёмов (различают микробюретки, бюретки объёмные, весовые, поршневые, газовые); мерные колбы (10—2000 мл) — для отмеривания и хранения определённых объёмов жидкостей: мерные мензурки и цилиндры (градуированы менее точно).
К немерной, или общего назначения, химической посуде относятся: изделия, употребляемые с нагревом, — пробирки (5—25 мл), стаканы (5—1000 мл), колбы (10—1000 мл, плоскодонные, круглодонные, конические), реторты (до 3 л): употребляемые без нагрева — пробирки (из толстостенного стекла) для центрифугирования, воронки для переливания и фильтрования жидкостей и делительные воронки (от 25 мл и выше, цилиндрические, грушевидные и шарообразные), кристаллизаторы (плоскодонные сосуды), холодильники для охлаждения и конденсации паров и собирания конденсата (специальные и универсальные), сифоны (различных форм и размеров, применяются для переливания жидкостей), водоструйные насосы (ускоряют фильтрование, создают при перегонке вакуум над кипящей жидкостью), склянки (служат в качестве резервуара, из которого жидкость поступает в др. сосуд, например в бюретки при титровании), бюксы с пришлифованными крышками (для хранения веществ), капельницы различного устройства (для дозировки жидкости).
К химической посуде специального назначения относятся: колбы для дистилляции, аллонжи — изогнутые трубки (для соединения холодильника с приёмником), дефлегматоры (насадки, представляющие собой трубки с расширением и отводом в верхней части; применяются при фракционированной перегонке); колбы грушевидной формы, применяющиеся для определения азота («колбы Кьельдаля»), эксикаторы для медленного высушивания и сохранения веществ, легко поглощающих влагу из воздуха, различного вида склянки для промывания газов с целью освобождения их от примесей, Киппа аппарат для получения лабораторных количеств газов (CO2, H2S и др.), трубки различной формы (например, хлоркальциевые U-образные) для сушки и очистки газов от механических загрязнений.
Наиболее распространённый материал для химической посуды — стекло; во многих случаях применяются и др. материалы. Кварцевая химическая посуда необходима при работе с особо чистыми веществами, а также для нагрева до 1200 °С, в том числе и под вакуумом. Платиновая химическая посуда используется главным образом при работе с фтористоводородной (плавиковой) кислотой. Платиновую химическую посуду не рекомендуется применять при работе с PbSO4, PbO2, SnO2, Bi2O3, Sb2O3, др. соединениями, способными легко восстанавливаться, при работе с серу- и фосфорсодержащими соединениями в присутствии восстановителей, при сплавлении богатых железом веществ, а также веществ, выделяющих галогены в присутствии окислителей, например царской водки. Тигли из золота и серебра удобны для сплавления различных веществ со щелочами при 900—1000 °C. Фарфоровая химическая посуда. по сравнению со стеклянной более прочна и термостойка, но непрозрачна и тяжела. Помимо стаканов, чашек (для выпаривания) и тиглей, из фарфора изготовляют ступки, воронки Бюхнера, ложки-шпатели для отбора вещества, лодочки для прокаливания в печи. Для нагревания при 1200—3000 °С применяют тигли из высокоогнеупорных материалов (алунд, глинозём, корунд и др.).
· Калибрование посуды.
Мерную посуду при выполнении точных измерений необходимо калибровать. Вследствие неодинакового внутреннего диаметра бюретки по всей длине неравномерной толщины стенок пипетки, а иногда в результате ошибок, допущенных на фабрике-изготовителе, показания мерной посуды могут не соответствовать действительной вместимости. Перед проверкой бюретки, пипетки, пикнометры, мерные колбы тщательно моют, высушивают и охлаждают до комнатной температуры. Проверку пипеток, бюреток следует проводить при температуре, указанной на них. Взвешивание производят с точностью, соответствующей вместимости мерной посуды. Так, при калибровании бюреток, пипеток, мерных колб вместимостью 10. 100 мл массу
Для проверки пипетки ее наполняют дистиллированной водой до метки, затем эту воду сливают в заранее’ взвешенный бюкс и вновь взвешивают. При слнванни воды ее нельзя выдувать, меняя скорость истечения жидкости. Все измерения откалиброван-ной пипеткой проводят одинаково, точно так же, как это делалось при калибровании. Проверку проводят 3-4 раза, берут среднюю массу воды, находят в таблице ее плотность при температуре измерений и вычисляют объем.
У бюретки сначала проверяют полную вместимость, а затем уменьшают по 1 или по 5 мл. Например, у бюретки вместимостью 25 мл определяют массу всего объема, а затем 24, 23 мл и т. д., либо 20, 15 мл и т. д. в зависимости от требуемой точности. По полученным данным из 2-3 измерений составляют таблицу поправок.
· Фильтрование
— это процесс разделения неоднородных систем (например, суспензия, аэрозоль) при помощи пористых перегородок, пропускающих дисперсионную среду и задерживающих дисперсную твёрдую фазу. Целью фильтрования в широком смысле слова является отделение жидкости от самых различных твердых примесей.
Все современные способы очистки можно разделить укрупненно на две группы: механические фильтры, являющиеся перфорированной перегородкой той или иной конструкции, и очистители в силовых полях (гравитационные, центробежные, магнитные, электростатические). Недостатком первых является малая грязеемкость, увеличение перепада давления по мере забивания отверстий или пор в перегородке, наличие байпасного клапана, перепускающего без очистки часть жидкости из линии загрязненной жидкости в линию очищенной жидкости, ограничения по степени загрязненности, подаваемой на очистку жидкостей, большие габаритные размеры, увеличивающиеся по мере увеличения пропускной способности или тонкости очистки, и др. Все это приводит к необходимости периодической замены или регенерации фильтрующего элемента, встройки сигнальных устройств и т.п. Следует попутно отметить, что запыленность окружающей среды зачастую настолько велика, что простая замена фильтроэлементов в гидросистемах вносит загрязнений больше, чем изнашивание за все время эксплуатации.
Фильтрующие материалы
Разделение суспензий или аэрозолей производят с помощью пористых перегородок, пропускающих жидкость или газ.
В качестве фильтрующего материала применяют специальные лабораторные фильтры из фильтровальной бумаги.
В промышленности используют фильтровальные ткани (напр. бельтинг), пористые вещества (например, фильтры из прессованного титана, асбеста, пористого стекла и др.).
Качественный анализ
Качественный анализ предназначен для качественного обнаружения веществ, элементов (ионов), функциональных групп, а также включает задачи идентификации веществ – установление их аналогии с определенным эталоном (стандартом). Для идентификации используют комплекс методов, выясняя сходство состава, строения, физических свойств вещества и эталона.
Задача по идентификации может быть решена при помощи физических и химических методов. Физические методы позволяют проводить анализ, используя различия в оптических, магнитных, тепловых и других свойствах анализируемых элементов или ионов.
Химические методы основаны на химических реакциях, позволяющих обнаружить элемент или ион. Анализ можно провести сухим путем, без растворения анализируемого вещества, и мокрым путем, т.е. после предварительного растворения веществ.
Для проведения анализа мокрым путем анализируемое вещество обязательно должно быть переведено в раствор. При химических методах качественного анализа открываемый ион переводят в соединение, дающее видимый эффект (образование осадка, изменение цвета раствора, образование газообразных веществ).
Дробный анализ – применяя специфические реакции (реагенты), можно идентифицировать ионы непосредственно в отдельных порциях раствора. При этом порядок определения отдельных ионов не имеет значения. Этот анализ применяется редко из-за недостатка регентов, малого количества специфических реакций.
Систематический анализ – часто применяемый анализ, суть которого состоит в том, что сначала проводят предварительные испытания, отобрав часть раствора, а затем делят на группы катионов, используя групповой регент; основан на применении одной из аналитических классификаций. Его применяют при исследовании минералов, горных пород, сложных смесей неорганических веществ.
Наиболее часто групповое отделение катионов и анионов осуществляется в виде трудно растворимых соединений, а в некоторых случаях действие группового реагента заключается в растворении осадка.
В основе каждой классификации подбор группового реагента, с помощью которого можно выделить определяемую группу ионов.
Требования, предъявляемые к групповому реагенту:
2) осаждаемые ионы должны быть далее легко растворимы;
3) избыток реагента не мешает определению других ионов.
Известно несколько классификаций катионов:
1) аммиачно-фосфатная – основана на растворимости фосфатов в воде, в щелочах, кислотах и аммиаке;
2) бифталатная – основана на использовании в качестве группового реагента бифталата калия (HOOCC6H4COOK), который проявляет буферные свойства, т.е. создает определенное значение pH, при котором в осадок выпадает группа катионов;
3) сульфидная – суть состоит в том, что при добавлении группового реагента выпадают в осадок определенные сульфиды, в качестве групповых реагентов используются (NH4)2S – сульфидно-основной, тиоацетамид CH3CSNH2 – тиоацетамидный метод, H2S – сероводородный метод;
4) кислотно-основная – основана на отношении соединений к кислотам, основаниям и аммиаку, проста и удобна в использовании.
Согласно кислотно основной классификации катионы делят на 6 групп:
Аналитические классификации катионов базируются на химических свойствах их соединений и тесно связаны с местоположением элементов в периодической системе Д.И. Менделеева, их строением и физико-химическими характеристиками.
Аналитические классификации создавались на основе эмпирического опыта аналитической химии. По мере расширения и углубления теории химии стала возможной их интерпретация с позиции периодического закона.
Большинство из солей растворимо в воде вследствие высокой полярности связи, близкой к ионной. В периодической системе они располагаются в IА – группе.
Во всех классификациях сходны группы катионов, осаждаемые серной кислотой, карбонатом аммония и гидрофосфатом натрия в присутствии аммиака. Это катионы
Амфолиты обладают небольшой элеткроотрицательностью, высокими поляризующими свойствами, и их соединения способны в зависимости от условий проявлять себя и как основания и как кислоты.
Аналитические классификации логически вытекают на основе этого из периодического закона.
Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим.