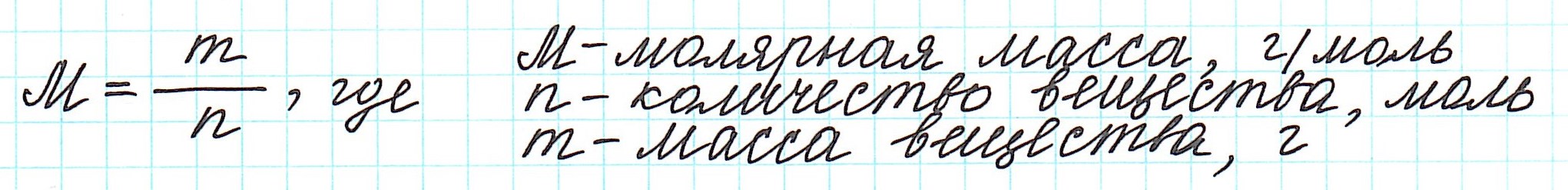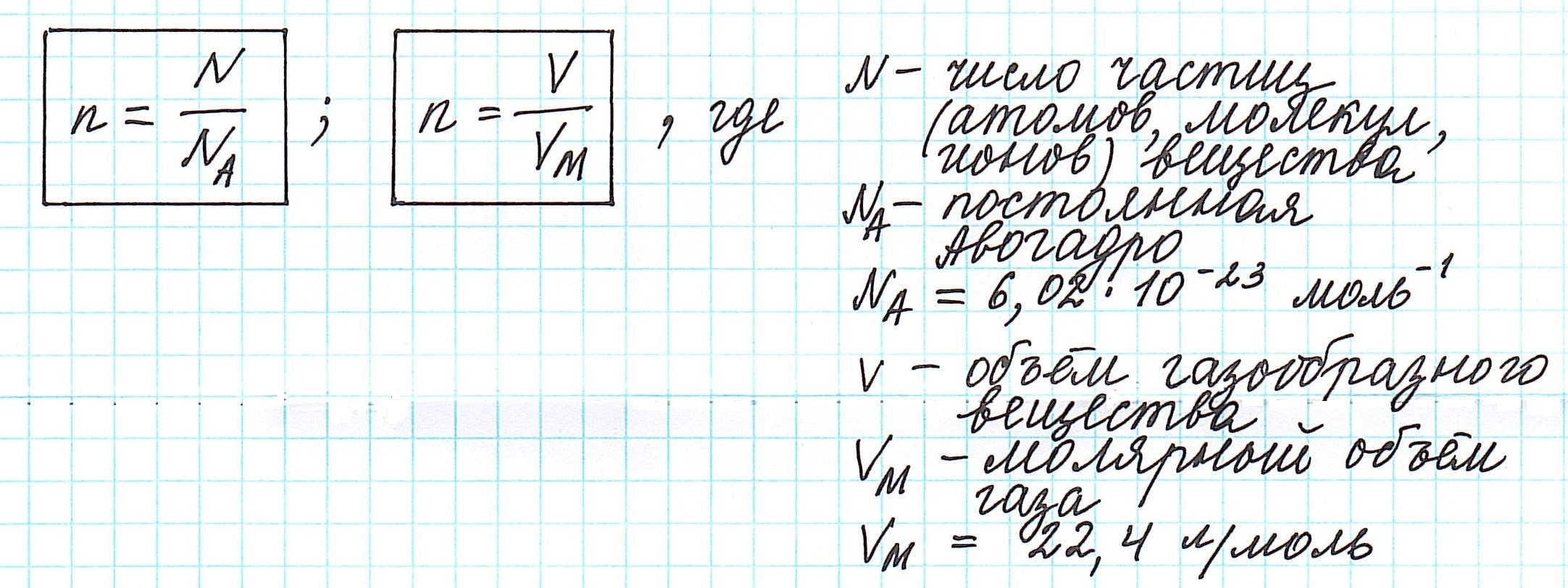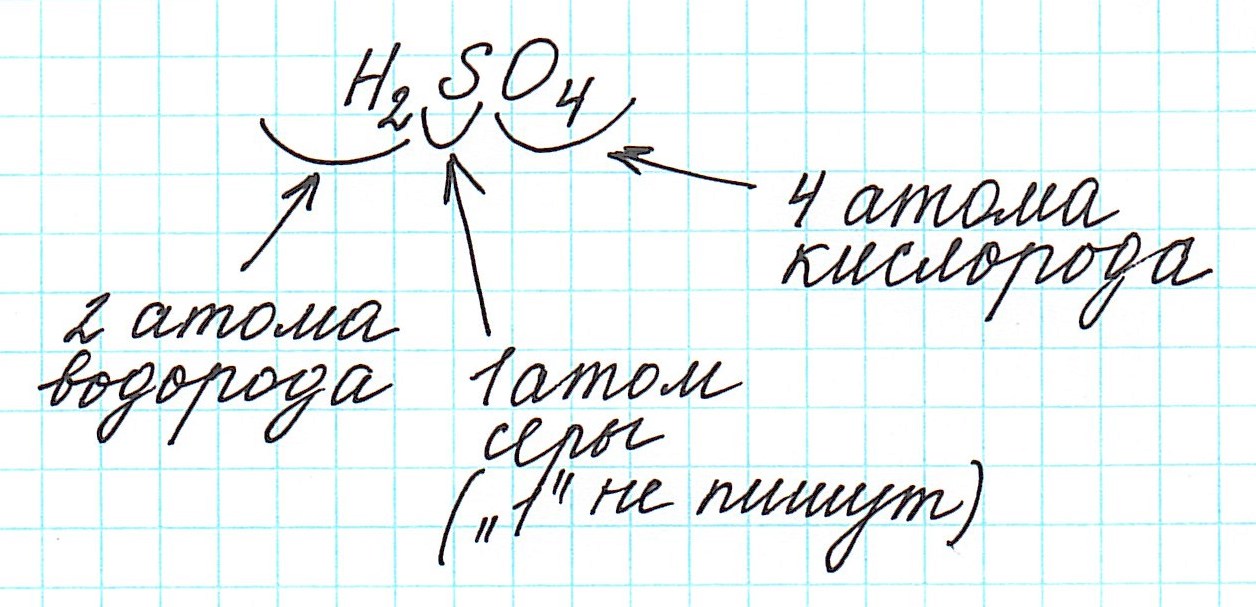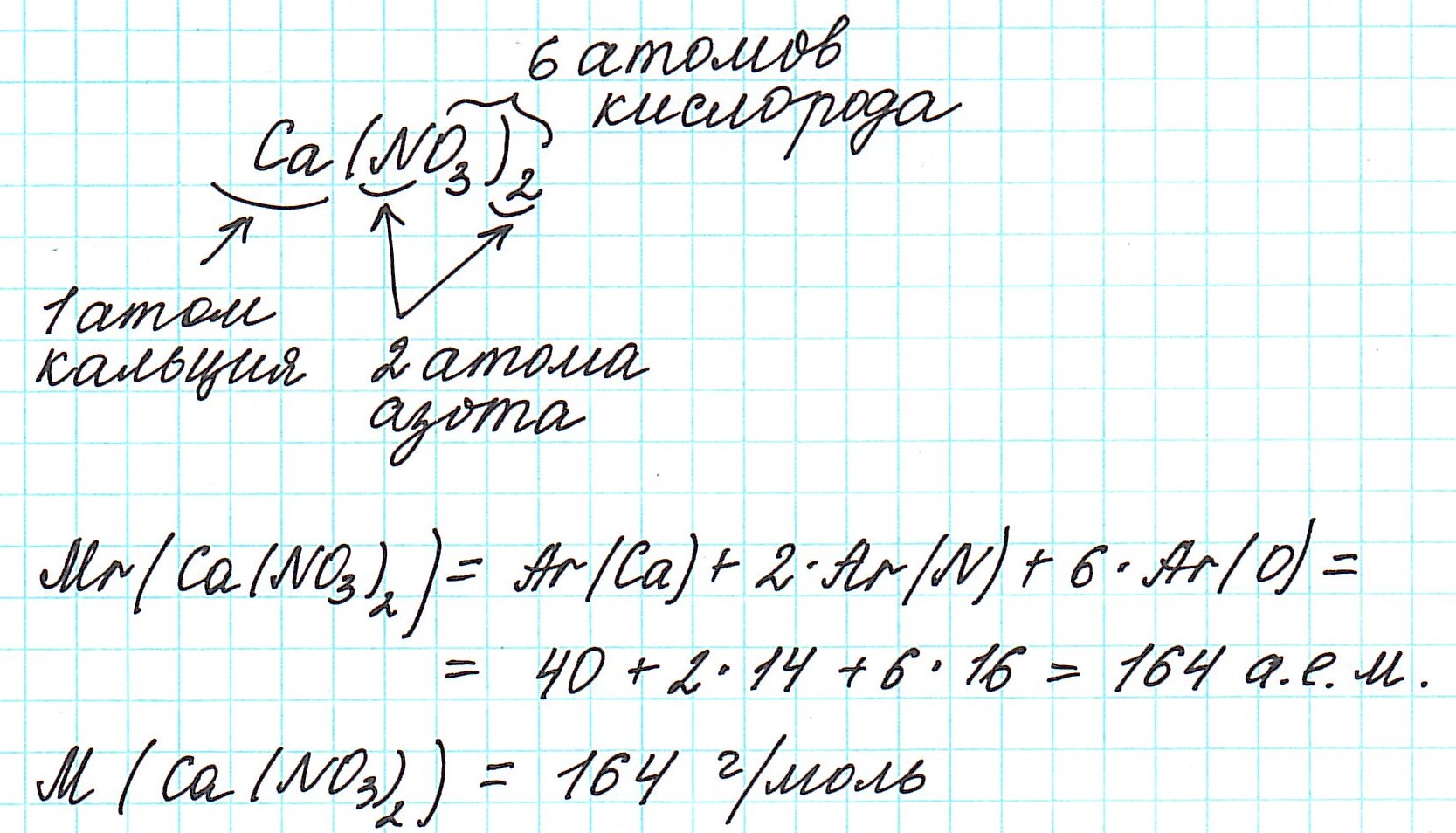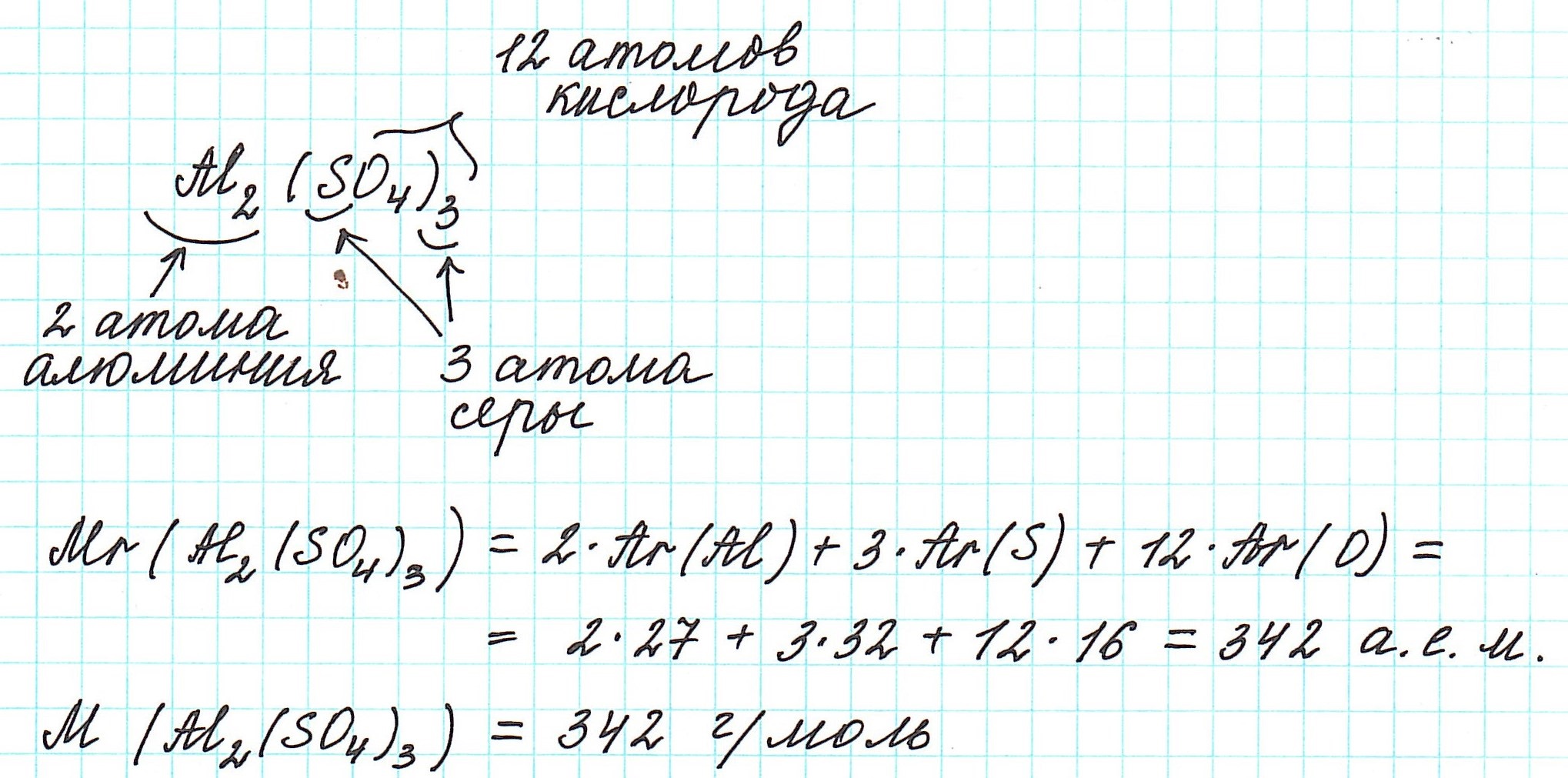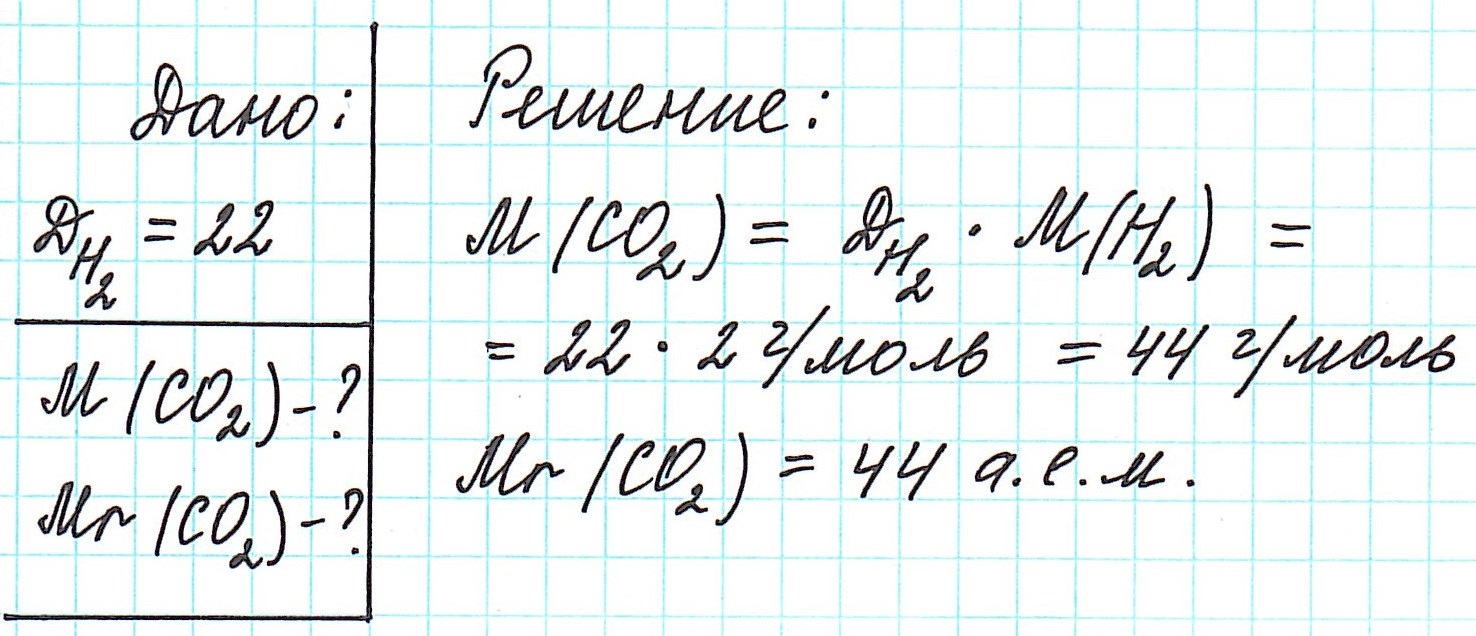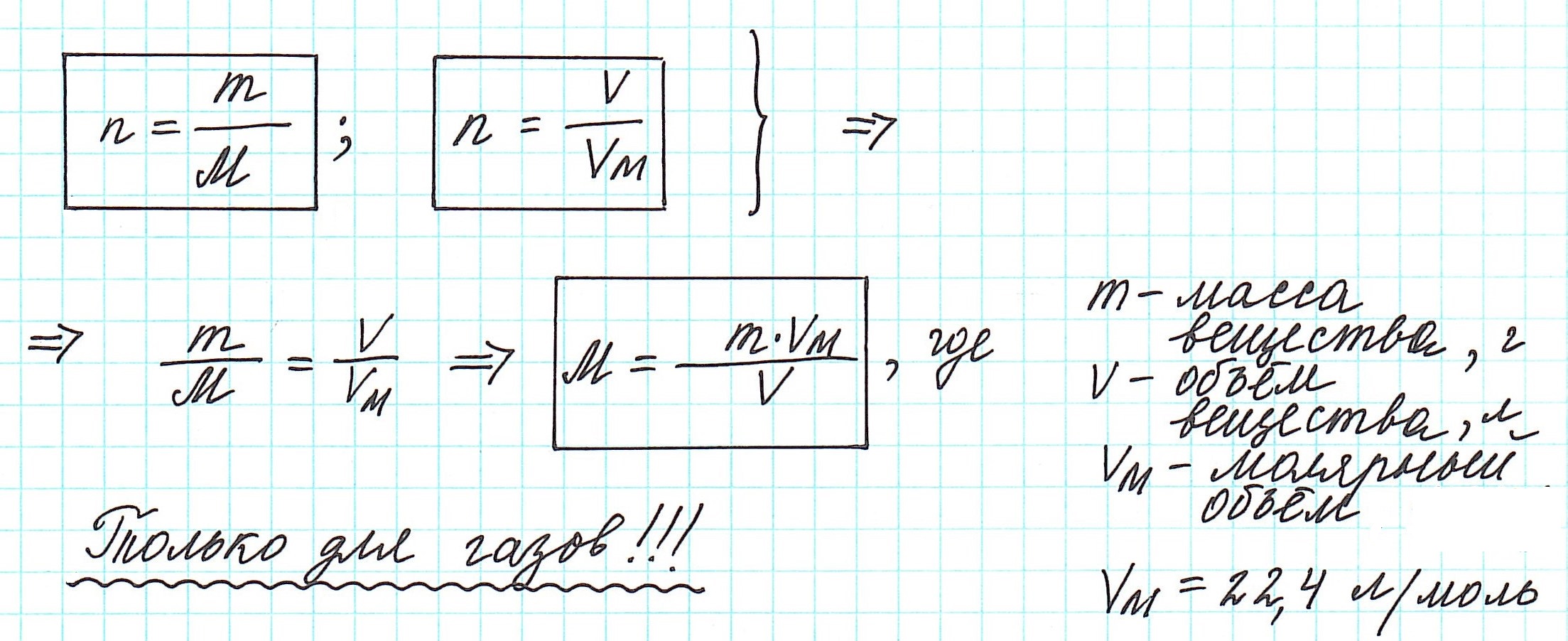Масса молекул (относительная молекулярная масса)
Отношение массы молекулы данного вещества m0 к 1/12 массы атома углерода m0C называют относительной молекулярной массой вещества Mr:
Чтобы определить относительную молекулярную массу вещества, необходимо по структурной формуле сложить относительные атомные массы его составляющих. Например, относительная молекулярная масса воды равна 18, поскольку атомные массы водорода и кислорода равны 1 и 16 соответственно. Из формулы воды H2O имеем: 2 x 1 + 16 = 18 а. е. м.
Множитель 1/12 введен для того, чтобы относительные молекулярные массы были близки к целым числам. Например, относительная молекулярная масса молекулы кислорода O2 равна приблизительно 32 а. е. м., а молекулы водорода — 2 а. е. м.
Итак, размеры и масса молекул очень маленькие, тем не менее их количество в макроскопическом теле огромное. Например, в 1 г воды приблизительно 3,3 • 10 22 молекул. Чтобы упростить расчеты, в физике и химии количество атомов, молекул или других структурных единиц в данном теле принято сравнивать с количеством атомов в 12 г углерода.
Для измерения массы вещества молекулярная физика использует относительную молекулярную (атомную) массу. Относительные атомные массы всех известных химических элементов приведены в Периодической таблице химических элементов Д. И. Менделеева.
Молекулярная масса
Молекуля́рная ма́сса (менее правильный термин: молекулярный вес) — масса молекулы, выраженная в атомных единицах массы. Численно равна молярной массе. Однако следует чётко представлять разницу между молярной массой и молекулярной массой, понимая, что они равны лишь численно и различаются по размерности.
Молекулярные массы сложных молекул можно определить, просто складывая относительные атомные массы входящих в них элементов. Например, молекулярная масса воды (H2O) есть
См. также
Смотреть что такое «Молекулярная масса» в других словарях:
МОЛЕКУЛЯРНАЯ МАССА — значение массы молекулы, выраженное в атомных единицах массы. Практически М. м. равна сумме масс входящих в неё атомов (см. АТОМНАЯ МАССА). Физический энциклопедический словарь. М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1983 … Физическая энциклопедия
МОЛЕКУЛЯРНАЯ МАССА — (молекулярный вес) масса молекулы, выраженная в атомных единицах массы. Практически равна сумме масс всех атомов, из которых состоит молекула. Величины молекулярной массы используются в химических, физических и химико технических расчетах … Большой Энциклопедический словарь
МОЛЕКУЛЯРНАЯ МАССА — (масса моля), термин ранее использовался для обозначения ОТНОСИТЕЛЬНОЙ МОЛЕКУЛЯРНОЙ МАССЫ … Научно-технический энциклопедический словарь
Молекулярная масса М м — Молекулярная масса, М. м. * малекулярная маса, М. м. * molecular mass or M. m. масса молекулы, не имеющая собственных единиц измерения, поэтому обычно в этом смысле используют термин «молекулярный вес» (см.) … Генетика. Энциклопедический словарь
молекулярная масса — — [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN molecular mass … Справочник технического переводчика
Молекулярная масса — – относительная величина, отношение массы молекулы данного вещества к 1/12 части массы атома Изотопа углерода С12. [Ушеров Маршак А. В. Бетоноведение: лексикон. М.: РИФ Стройматериалы. 2009. – 112 с.] Рубрика термина: Общие термины… … Энциклопедия терминов, определений и пояснений строительных материалов
МОЛЕКУЛЯРНАЯ МАССА — сумма масс атомов, входящих в состав данной молекулы; выражается в атомных единицах массы (а. е. м.). Поскольку 1 а. е. м. (иногда называемая дальтон, D) равна 1/12 массы атома нуклида 12 С и в единицах массы СИ составляет 1,66057.10 27 кг, то… … Химическая энциклопедия
молекулярная масса — santykinė molekulinė masė statusas T sritis Standartizacija ir metrologija apibrėžtis Molekulės vidutinės masės arba tiksliai apibrėžto medžiagos darinio masės ir nuklido ¹²C atomo masės 1/12 dalies dalmuo. atitikmenys: angl. molecular mass;… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
молекулярная масса — santykinė molekulinė masė statusas T sritis Standartizacija ir metrologija apibrėžtis Molekulę sudarančių atomų santykinių atominių masių suma, skaitine verte lygi medžiagos molio masei. atitikmenys: angl. molecular mass; molecular weight;… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
молекулярная масса — santykinė molekulinė masė statusas T sritis chemija apibrėžtis Molekulę sudarančių atomų santykinių atominių masių suma, skaitine verte lygi vieno medžiagos molio masei. atitikmenys: angl. molecular mass; molecular weight; relative molecular mass … Chemijos terminų aiškinamasis žodynas
молекулярная масса — (молекулярный вес), масса молекулы, выраженная в атомных единицах массы. Практически равна сумме масс всех атомов, из которых состоит молекула. Величины молекулярной массы используются в химических, физических и химико технологических расчётах. * … Энциклопедический словарь
Что такое относительная молекулярная масса в физике
Основные положения молекулярно-кинетической теории (МКТ)
Основные утверждения МКТ
1. Вещество состоит из частиц (молекул и атомов).
2. Между частицами есть промежутки.
3. Частицы беспорядочно и непрерывно движутся.
4. Частицы взаимодействуют друг с другом (притягиваются и отталкиваются).
Подтверждение МКТ:
1. экспериментальное
— механическое дробление вещества; растворение вещества в воде; сжатие и расширение газов; испарение; деформация тел; диффузия; опыт Бригмана: в сосуд заливается масло, сверху на масло давит поршень, при давлении 10 000 атм масло начинает просачиваться сквозь стенки стального сосуда;
— диффузия; броуновское движение частиц в жидкости под ударами молекул;
— плохая сжимаемость твердых и жидких тел; значительные усилия для разрыва твердых тел; слияние капель жидкости;
2. прямое
— фотографирование, определение размеров частиц.

Броуновское движение
Броуновское движение стало доказательством непрерывного и хаотичного (теплового) движения молекул вещества.
— открыто английским ботаником Р. Броуном в 1827 г.
— дано теоретическое объяснение на основе МКТ А. Эйнштейном в 1905 г.
— экспериментально подтверждено французским физиком Ж. Перреном.
Масса и размеры молекул
Размеры частиц
Диаметр любого атома составляет около 

Число молекул в веществе
Масса одной молекулы
Единица измерения массы в СИ: [m]= 1 кг
В атомной физике массу обычно измеряют в атомных единицах массы (а.е.м.).
Условно принято считать за 1 а.е.м. :
Относительная молекулярная масса вещества

Относительная атомная масса химического элемента

Относительная атомная масса каждого химического элемента дана в таблице Менделеева.
Другой способ определения относительной молекулярной массы вещества
Относительная молекулярная масса вещества равна сумме относительных атомных масс химических элементов, входящих в состав молекулы вещества.
Относительную атомную массу любого химического элемента берем из таблицы Менделеева!)
Количество вещества
Количество вещества (ν) определяет относительное число молекул в теле.
Единица измерения количества вещества в системе СИ: [ν]= 1 моль
Запомни!
В 1 моле любого вещества содержится одинаковое число атомов или молекул!
Но!
Одинаковые количества вещества для разных веществ имеют разную массу!
Постоянная Авогадро
Число атомов в 1 моле любого вещества называют числом Авогадро или постоянной Авогадро:
Молярная масса


Единица измерения молярной массы: [M]=1 кг/моль.
Формулы для решения задач
Эти формулы получаются в результате подстановки вышерассмотренных формул.
Масса любого количества вещества
и формула для 7 класса
Количество вещества
Число молекул в веществе
Молярная масса
Масса одной молекулы
Связь между относительной молекулярной массой и молярной массой

Относительная атомная и относительная молекулярная массы
Определение и формула атомной массы
Массы атомов и молекул очень малы, поэтому в качестве единицы измерения удобно выбрать массу одного из атомов и выражать массы остальных атомов относительно нее. Именно так и поступал основоположник атомной теории Дальтон, который составил таблицу атомных масс, приняв массу атома водорода за единицу.
До 1961 года в физике за атомную единицу массы (а.е.м. сокращенно) принимали 1/16 массы атома кислорода 16 О, а в химии – 1/16 средней атомной массы природного кислорода, который является смесью трех изотопов. Химическая единица массы была на 0,03% больше, чем физическая.
В настоящее время за в физике и химии принята единая система измерения. В качестве стандартной единицы атомной массы выбрана 1/12 часть массы атома углерода 12 С.
Относительная атомная масса элемента (Ar) – это безразмерная величина, равная отношению средней массы атома элемента к 1/12 массы атома 12С.
При расчете относительной атомной массы учитывается распространенность изотопов элементов в земной коре. Например, хлор имеет два изотопа 35 Сl (75,5%) и 37 Сl (24,5%).Относительная атомная масса хлора равна:
Ar(Cl) = (0,755×m( 35 Сl) + 0,245×m( 37 Сl)) / (1/12×m( 12 С) = 35,5.
Из определения относительной атомной массы следует, что средняя абсолютная масса атома равна относительной атомной массе, умноженной на а.е.м.:
Видео
Сколько атомов в грамме вещества?
В одном грамме хлора содержится 93,03 × 10 23 молекул, опять же для удобства расчётов была введена единица измерения «моль». Моль — это 6,022 140 857(74) × 10 23 единиц. В молях можно измерять что угодно, 1 моль людей — это 6,022 140 857(74) × 10 23 людей. Данное число называется числом Авогадро, оно было рассчитано как количество атомов в 12 граммах углерода.
Поскольку а.е.м. и моль были рассчитаны исходя из массы углерода, следует запомнить следующие соотношения:
Как можно использовать данные соотношения? Если мы возьмём атомную массу любого элемента, отношение грамм/моль будет численно равно данному числу: масса серы — 32,066 а.е.м., значит один моль серы весит 32,066 грамм.
Атомная единица массы
Пользоваться такими маленькими величинами масс атомов при расчетах неудобно. К тому же, когда в XIX в. начало формироваться атомно- молекулярное учение, ученые еще не представляли реальных размеров и масс атомов. Поэтому на практике вместо истинных масс атомов стали применять их относительные значения. Они рассчитывались по массовым отношениям простых веществ в реакциях друг с другом. Химики предположили, что эти отношения пропорциональны массам соответствующих атомов. Именно так в начале XIX в. Дж. Дальтон ввел понятие относительной атомной массы, приняв за единицу сравнения массу самого легкого атома — водорода.
В настоящее время в качестве такой единицы сравнения используется 1/12 часть массы атома углерода (рис. 33). Она получила название атомной единицы массы (а. е. м.). Ее международное обозначение — u (от английского слова «unit» — единица):
Атомная единица массы — это 1/12 часть массы атома углерода, которая равна 1,66·10 −27 кг.
Нахождение атомной массы
Определить атомное число для выбранного элемента можно при помощи таблицы Менделеева. Номер элемента в таблице всегда совпадает с количеством протонов в ядре. К примеру, упомянутый выше водород имеет первый номер в таблице и в его составе содержится всего 1 протон. Ниже в таблице всегда указан средний атомный вес элемента, который для расчетов требуется округлить до ближайшего целого числа.
Таблица Менделеева изначально отображает всю информацию по количеству протонов и электронов в атоме, а также его атомной массе. Именно поэтому в школьных задачах на определение атомной массы достаточно использовать периодическую таблицу и не вычислять ничего специально.
Обычно на уроках по химии ставится обратная задача: как определить количество нейтронов в конкретном изотопе? В этом случае действует простая формула:
Количество нейтронов = атомная масса – порядковый номер.
К примеру, атом водорода-1 не содержит нейтронов, так как его атомное число равняется также единице. А вот тритий — это уже водород с одним протоном и двумя нейтронами. Тритий — нестабильный изотоп. Он легко распадается на атомы гелия, свободные электроны и антинейтрино, при этом выделяется некоторое количество энергии. Нестабильные изотопы носят название радиоактивных.
Наша программа позволяет рассчитать атомную массу конкретного изотопа, если известно его количество протонов и нейтронов. Для этого достаточно ввести в ячейки соответствующие числа и получить мгновенный результат.
Как вычислить абсолютную массу, формулы, примеры
Найти абсолютную массу молекулы C2H6. Решение Исходя из утверждения, что абсолютная масса молекулы равняется произведению ее относительной молекулярной массы на атомную единицу массы, получаем: m(C2H6)=Mr(C2H6)·1,661·10-27=49,82·10-27кг=49,82·10-24г
Найти молекулярную массу серной кислоты, используя таблицу Менделеева. Решение Известно, что молекулярная масса вещества равна сумме атомных масс веществ, входящих в состав молекулы. Поэтому: Mr(H2SO4)=1·2+32+16·4=98г/моль
МОЛЯРНАЯ МАССА И ОТНОСИТЕЛЬНАЯ МОЛЕКУЛЯРНАЯ МАССА: В ЧЕМ ОТЛИЧИЕ И ПОЧЕМУ ОНИ ЧИСЛЕННО РАВНЫ
Как вычислить молярную массу вещества? В каких единицах она измеряется?
А еще есть относительная молекулярная масса. Почему она относительная и численно равна молярной массе? Может быть это одно и то же?
Вот сколько вопросов возникает сразу в отношении такого простого на первый взгляд понятия, как молярная масса.
Разберемся по порядку и научимся ее определять.
Относительная атомная масса
Огромнейший вклад в развитие и обоснование понятия относительная атомная масса внесли в разное время французский ученый Гей-Люссак, итальянский ученый А.Авогадро и шведский ученый Й.Я. Берцелиус.
Не углубляясь в историю вопроса, вспомним, что любой химический элемент представляет собой определенную разновидность атомов. Сегодня мы знаем, что атомы химических элементов имеют свои особые характеристики.
И самая главная из них, определяющая практически все остальные, это заряд ядра. А так как заряд ядра обусловлен присутствием в нем протонов, а заряд одного протона равен +1, то и количество протонов, соответственно, также является важнейшей характеристикой атомов химических элементов.
Основную массу атома составляет ядро, которое кроме протонов содержит еще и нейтроны. Масса последних сопоставима с массой первых. Оболочку атома составляют электроны.
По числу частиц в атоме, а точнее, по их суммарной массе, атомы химических элементов можно условно разделить на тяжелые и легкие. Например, легким элементом является водород, так как его атомы имеют самую маленькую массу. А свинец — это уже тяжелый элемент. Масса его атома в 302 раза тяжелее массы атома водорода.
Но тем не менее, как бы мы не делили все атомы на тяжелые или легкие, абсолютная масса (mA) каждого из них ничтожно мала, как мала и масса составляющих их частиц. Например,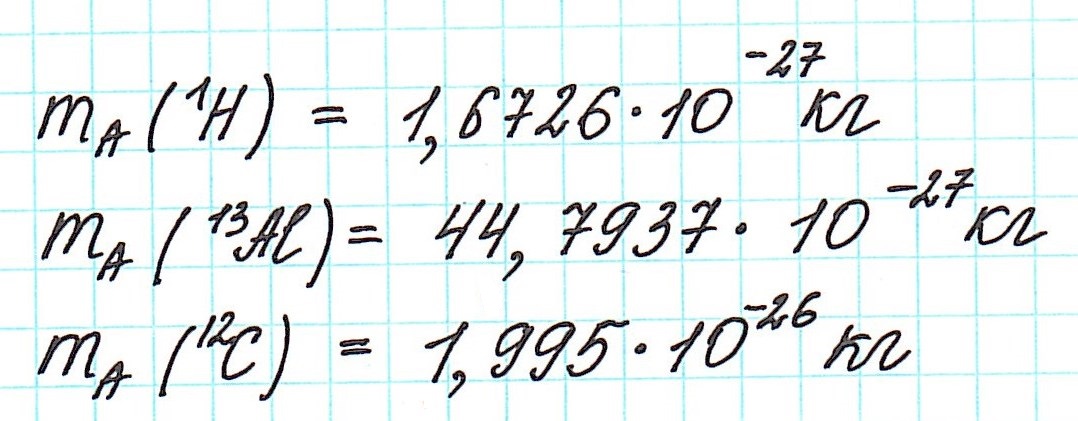
Величина, с которой сравнивают массу атома
Первоначально еще Дальтон сравнивал массы атомов с массой атома водорода, как самого легкого. Позднее появилась так называемая кислородная единица, равная 1/16 части массы атома кислорода. К ней перешли потому, что большинство атомов химических элементов образуют соединения с кислородом.
Однако, с развитием атомной физики и эта единица стала крайне неудобной. Все потому, что кислород в природе имеет несколько изотопов (а именно 3 устойчивых, всего же их 16). А изотопы, как известно, отличаются своей атомной массой. Из-за большого разнообразия изотопов и их различной устойчивости кислородная единица утратила свою актуальность.
Почему именно углерод? Да потому, что:
— у углерода всего 2 изотопа: 12 С и 13 С; причем первого 98,9%;
— количество органических веществ (их основу составляет, как известно, именно углерод) в сотни раз больше, чем неорганических;
— при переходе от кислородной единицы к углеродной уже посчитанные относительные атомные массы всех элементов изменились не существенно, что оказалось очень удобным.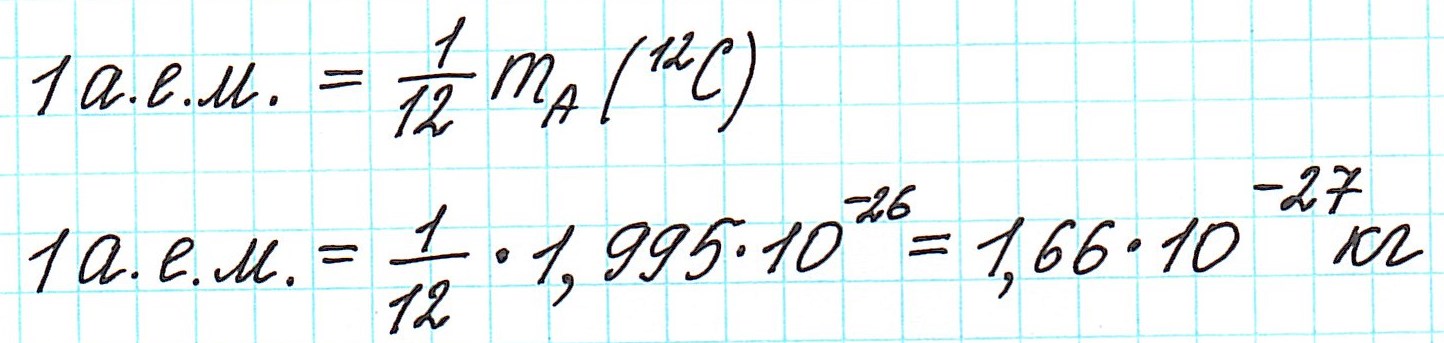
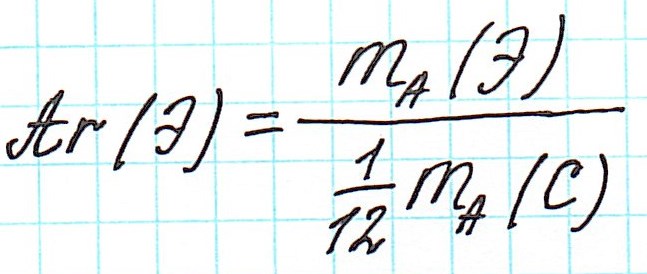
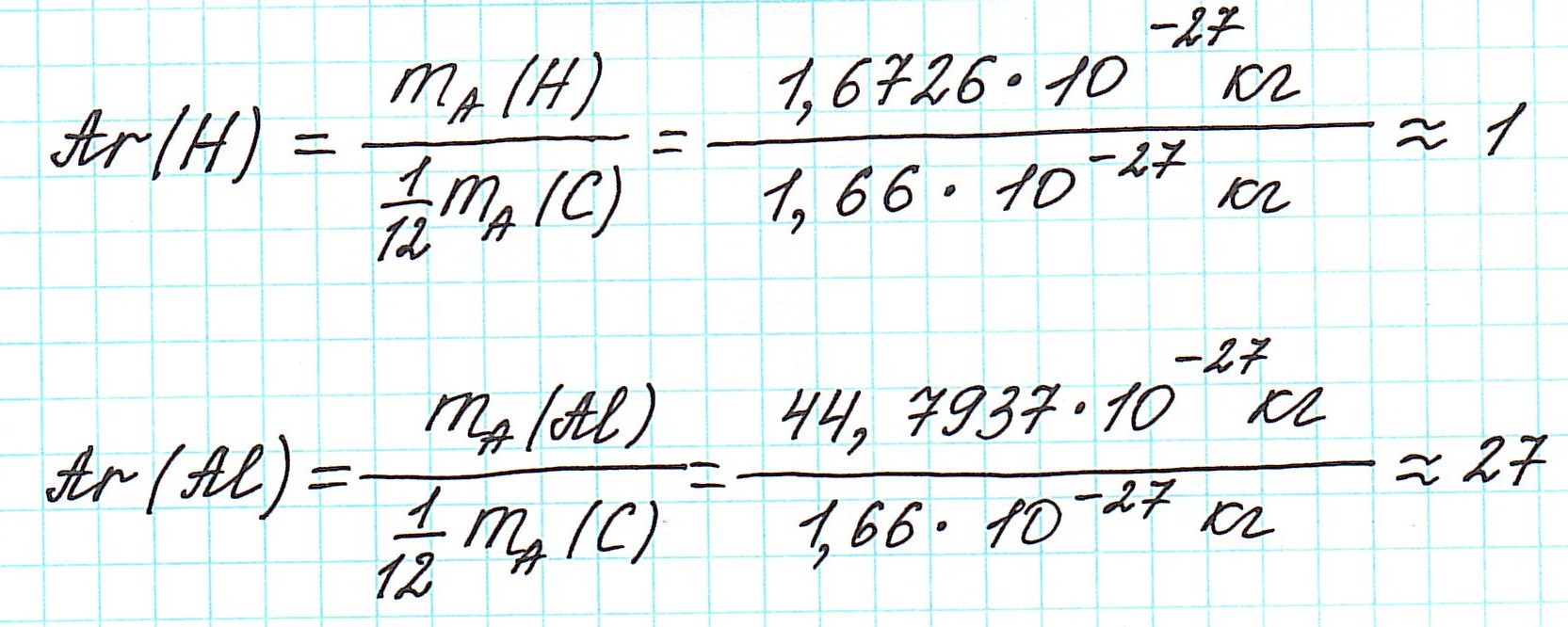
Почему атомная масса дробная?
Вернемся к строению атома.
Масса атома складывается из массы всех составляющих его частиц.
Массы протона и нейтрона приняты равными 1. А вот массой электрона обычно пренебрегают (по крайней мере в химии), так как даже относительная она безнадежно мала (0,0005485799090659(16) а.е.м.). То есть можно сказать, что масса атома определяется массой его ядра.
В составе ядра целое количество частиц. Например, в атоме одного из изотопов кислорода 8 протонов и 8 нейтронов. Значит, его Ar должна быть равна 16. Так почему же Ar представлена в периодической системе химических элементов в виде десятичной дроби? Для кислорода это Ar(О)=15,9994.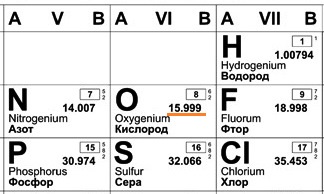
Например, химический элемент кислород в природе состоит на 99,76% из изотопа 16 О, на 0,04% из изотопа 17 О и на 0,20% из изотопа 18 О. Таким образом, Ar для кислорода является средним значением, учитывающим относительное содержание его изотопов.
Относительная молекулярная масса
А как же найти относительную молекулярную массу?
Дело в том, что молекулы характерны для веществ с ковалентными связями: вода H2O, серная кислота H2SO4, глюкоза C6H12O6 и т.д. И к ним в полной мере можно применить термин «относительная молекулярная масса».
Так как молекулы состоят из атомов, то относительная молекулярная масса (Mr) будет складываться из их относительных атомных масс. Например: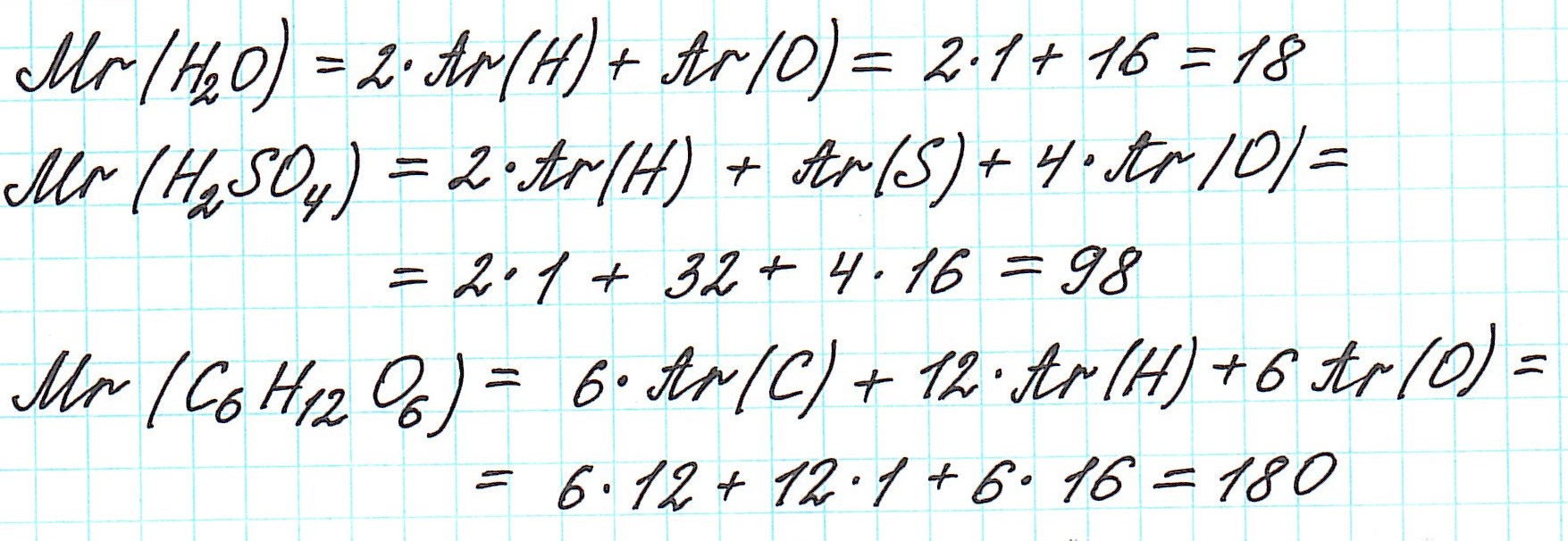
Точно так же, как относительную атомную массу (Ar), относительную молекулярную массу (Mr) будем сопоставлять с 1/12 частью атома изотопа углерода 12 С.
В последующем говорим о Mr.
Количество вещества и молярная масса
В практических расчетах все-таки требуется вычислять массы, взятые в граммах, килограммах ато и в тоннах (если речь идет о каком-то производстве, например).
Как же поступают тогда?
Количество вещества, которое содержит столько же частиц (атомов, ионов, молекул – в зависимости от строения), что и 12 г изотопа углерода 12 С, назвали молем.
Один моль вещества (любого!) всегда содержит 6,02·10 23 его частиц ( постоянная Авогадро ).
Ну, а так как атомы элементов отличаются по своей массе, то и 1 моль вещества тоже будет отличаться по массе.
Массу одного моля вещества называют молярной массой (М) и вычисляют в г/моль.
Таким образом, молярная масса и количество вещества связаны соотношением:
Можно также определить и такие отношения, связанные с количеством вещества:
Почему же относительная молекулярная и молярная массы равны?
Итак, относительная молекулярная и молярная массы, как следует из их определений – это не одно и то же.
Докажем, каким образом обе массы численно могут быть равны:
Как вычислить молярную массу вещества
Мы уже знаем, что относительная молекулярная масса складывается из относительных атомных масс.
При нахождении относительной молекулярной массы (Mr), а значит и молярной (М), выполняем следующие действия :
1) правильно записываем формулу вещества;
2) анализируем качественный состав (атомы каких элементов составляют вещество) и количественный состав (в каких количествах находятся эти атомы – смотрим по индексам, которые стоят справа внизу от знака химического элемента);
3) в периодической системе химических элементов находим элементы, атомы которых составляют вещество, и округляем относительную атомную массу, стоящую рядом со знаком элемента, до целого числа (! у хлора – до 35,5);
4) складываем относительные атомные массы всех элементов с учетом количества атомов.
Рассмотрим еще примеры:
Как вычислить молярную массу вещества, находящегося в газообразном состоянии
Это означает, что в данных условиях отношение масс газов друг к другу является отношением их молярных масс:


Вычислить молярную массу вещества (а, значит, и относительную молекулярную), находящегося в газообразном состоянии, можно, используя молярный объем газа (VM):
Итак, подведем итог:
Без вычисления молярной массы не обходится решение практически ни одной задачи. Если вы поняли, что такое молярная и относительная молекулярная массы и как их вычислять, но еще не умеете решать задачи с их применением, то самое время научиться.
Разбор простых типовых задач по химии в книге, которую вы можете совершенно БЕСПЛАТНО скачать здесь.