Что такое парциальное давление кислорода
Кислород постоянно абсорбируется из альвеол в кровь легочных капилляров, и также постоянно поступают из атмосферы в альвеолы новые порции кислорода. Чем быстрее абсорбируется кислород, тем ниже становится его концентрация в альвеолах. И наоборот, чем быстрее вдыхается кислород из атмосферы, тем выше становится его концентрация в альвеолах.
Таким образом, концентрация кислорода в альвеолах, а также его парциальное давление контролируются: (1) скоростью абсорбции кислорода в кровь; (2) скоростью доставки новых порций кислорода в легкие путем вентиляции.
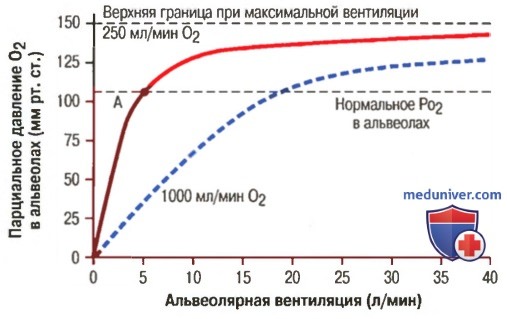
На рисунке выше показано влияние альвеолярной вентиляции и скорости абсорбции кислорода в кровь на альвеолярное парциальное давление кислорода (PO2). Одна кривая представляет абсорбцию кислорода со скоростью 250 мл/мин, другая — со скоростью 1000 мл/мин.
При нормальной величине вентиляции (4,2 л/мин) и потреблении кислорода 250 мл/мин рабочей точкой на рисунке выше является точка А. На рисунке выше также видно, что при абсорбции кислорода в кобольшое увеличение альвеолярной вентиляции не может поднять PO2 в альвеолах выше 149 мм рт. ст., если человек дышит нормальным атмосферным воздухом на уровне моря, т.к. для увлажненного воздуха при таком давлении это значение PO2 является пределом возможного.
На рисунке выше также показано, что даже очень большое увеличение альвеолярной вентиляции не может поднять PO2 в альвеолах выше 149 мм рт. ст., если человек дышит нормальным атмосферным воздухом на уровне моря, т.к. для увлажненного воздуха при таком давлении это значение PO2 является пределом возможного. Если человек дышит газовой смесью с парциальным давлением кислорода, превышающим 149 мм рт. ст., то при высокой скорости вентиляции PO2 в альвеолах может сравниться с PO2 вдыхаемой смеси.
б) Концентрация и парциальное давление двуокиси углерода в альвеолах. Двуокись углерода образуется в организме человека постоянно и переносится кровью в альвеолы; из альвеол она также постоянно удаляется путем вентиляции. На рисунке ниже показано влияние альвеолярной вентиляции и двух разных уровней выделения двуокиси углерода (200 и 800 мл/мин) на парциальное давление двуокиси углерода в альвеолах.
Нормальная скорость выделения двуокиси углерода составляет 200 мл/мин, и на соответствующей кривой на рисунке при альвеолярной вентиляции в 4,2 л/мин альвеолярное PCO2 определяется точкой А, т.е. составляет 40 мм рт. ст.
На рисунке выше показаны еще два факта. Во-первых, альвеолярное PCO2 растет прямо пропорционально скорости выделения двуокиси углерода, т.к. при скорости выделения CO2, равной 800 мл/мин, кривая поднимается выше в 4 раза. Во-вторых, альвеолярное PCO2 снижается обратно пропорционально альвеолярной вентиляции, поэтому концентрация и парциальное давление личестве 1000 мл/мин, как это бывает при умеренной физической нагрузке, для поддержания нормального PO2 в альвеолах (104 мм рт. ст.) скорость альвеолярной вентиляции должна увеличиться в 4 раза.
Выдыхаемый воздух
Выдыхаемый воздух является смесью воздуха мертвого пространства и альвеолярного воздуха, поэтому его состав определяется:
(1) количеством воздуха мертвого пространства;
(2) количеством альвеолярного воздуха в этой смеси.
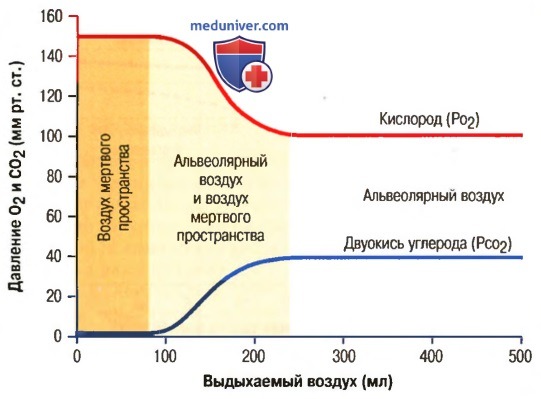
В последующих порциях к воздуху мертвого пространства примешивается все большее количество альвеолярного воздуха, пока из мертвого пространства не вымывается весь воздух, содержавшийся там до начала выдоха. В конце выдоха выходит только альвеолярный воздух, поэтому для сбора альвеолярного воздуха можно просто собрать последнюю порцию выдыхаемого воздуха после форсированного выдоха, вытолкнувшего из мертвого пространства весь воздух, содержащийся там до начала выдоха.
При нормальном выдохе выдыхаемый воздух содержит воздух как из мертвого пространства, так и из альвеол, т.е. они находятся в диапазоне между данными состава альвеолярного воздуха и увлажненного атмосферного воздуха.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «Физиология человека.»
Что такое парциальное давление кислорода
а) Влияние вентиляционно-перфузионного коэффициента на концентрацию газа в альвеолах. PO2 и PCO2 в альвеолах определяется двумя факторами:
(1) скоростью альвеолярной вентиляции;
(2) скоростью перехода кислорода и двуокиси углерода через дыхательную мембрану.
Предполагают, что все альвеолы вентилируются в равной степени и кровоток в альвеолярных капиллярах одинаков во всех альвеолах. Однако некоторые участки легких при хорошей вентиляции почти лишены кровотока, а другие — могут иметь великолепный кровоток при малой или отсутствующей вентиляции.
Это в некоторой степени возможно даже в нормальных условиях, но чаще выявляется при различных болезнях легких. В обоих случаях серьезно пострадает газообмен через дыхательную мембрану и человек может испытывать тяжелое нарушение дыхания, несмотря на нормальные показатели общей вентиляции и общего кровотока в легких, наряду с различными показателями вентиляции и кровотока в разных частях легких.
Для лучшего понимания изменений дыхания, возникающих при нарушении соответствия альвеолярной вентиляции и альвеолярного кровотока, была выработана специальная количественная концепция, названная вентиляционно-перфузионным коэффициентом.
Вентиляционно-перфузионный коэффициент обозначают количественно как VA/Q. Если VA (альвеолярная вентиляция) для данной альвеолы и Q (кровоток) в этой же альвеоле имеют нормальную величину, то вентиляционно-перфузионный коэффициент VA/Q также называют нормальным. Если альвеолярная вентиляция (Уд) равна нулю, но в альвеоле имеется перфузия (Q), то VA/Q тоже равняется нулю.
Если же при адекватной вентиляции (VA) наблюдается нулевая перфузия, то VA/Q равняется бесконечности. При коэффициенте, равном нулю или бесконечности, в этих альвеолах нет газообмена через дыхательную мембрану. Перейдем к разъяснению процесса дыхания в этих крайних случаях.
б) Парциальное давление кислорода и двуокиси углерода в альвеоле в случае, когда VA/Q равно нулю. При VA/Q, равном нулю, т.е. при отсутствии какой-либо альвеолярной вентиляции, воздух в альвеоле приходит в равновесие с кислородом и двуокисью углерода, находящимися в крови, т.к. эти газы распределяются между кровью и альвеолярным воздухом.
Кровь в капиллярах является венозной кровью, возвращающейся к легким из системного кровообращения, поэтому альвеолярные газы уравновешиваются с газами венозной крови. В главе 40 мы узнаем, что в нормальной венозной крови (v) P02 составляет 40 мм рт. ст. и PCO2 — 45 мм рт. ст., поэтому величины парциального давления этих двух газов являются нормальными для альвеол, в которых имеется кровоток, но нет вентиляции.
в) Парциальное давление кислорода и двуокиси углерода в альвеоле в случае, когда VA/Q равно бесконечности. Влияние парциальных давлений альвеолярного газа в случае, когда VA/Q равно бесконечности, полностью отличается от их влияния в случае, когда VA/Q равно нулю, поскольку теперь отсутствует капиллярный кровоток, уносящий кислород из альвеол и приносящий двуокись углерода в альвеолы.
Вместо уравновешивания альвеолярных газов с венозной кровью альвеолярный воздух заменяется увлажненным вдыхаемым воздухом, т.е. кислород из вдыхаемого воздуха не уходит в кровь и двуокись углерода не переходит из крови во вдыхаемый воздух. В нормальном вдыхаемом увлажненном воздухе PO2 равняется 149 мм рт. ст. и PCO2 — 0 мм рт. ст., поэтому такими будут и парциальные давления этих двух газов в альвеоле.
г) Газообмен и парциальные давления газов в альвеолах при нормальном VA/Q. В случае, когда в альвеоле присутствуют и нормальная вентиляция, и нормальный капиллярный кровоток (нормальная альвеолярная перфузия), обмен кислорода и двуокиси углерода через дыхательную мембрану является почти оптимальным, и альвеолярное PO2 составляет обычно 104 мм рт. ст., т.е. находится в диапазоне между величинами Рог вдыхаемого воздуха (149 мм рт. ст.) и венозной крови (40 мм рт. ст.).
Альвеолярное PCO2 также расположено между двумя экстремальными значениями; в норме оно составляет 40 мм рт. ст., в то время как в венозной крови PCO2 имеет величину 45 мм рт. ст. и во вдыхаемом воздухе — 0 мм рт. ст. Таким образом, в нормальных условиях в альвеолярном воздухе PO2 составляет 104 мм рт. ст. и PCO2 — 40 мм рт. ст.
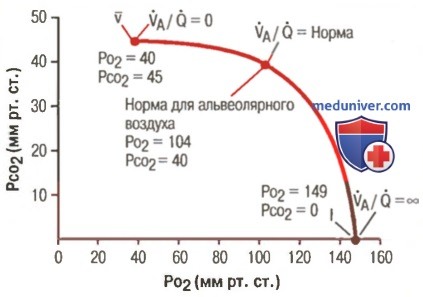
д) Диаграмма PO2-PCO2, VA/Q. Приведенные в предыдущих разделах концепции могут быть представлены в графическом виде. На рисунке выше изображена диаграмма PO2-PCO2, VA/Q. Кривая на диаграмме представляет все возможные комбинации PO2 и PCO2 в пределах значений VA/Q между нулем и бесконечностью в случае, когда давления газов в венозной крови нормальны и человек дышит воздухом на уровне моря. Так, точка v определяет значения PO2 и PCO2 при VA/Q равном нулю. PO2 в этой точке равно 40 мм рт. ст. и PCO2 — 45 мм рт. ст., что соответствует их величине в венозной крови.
На другом конце кривой, где VA/Q равен бесконечности, точка I обозначает вдыхаемый воздух — PO2 здесь равно 149 мм рт. ст., а PCO2 — 0 мм рт. ст. На кривой обозначена и точка, представляющая нормальный альвеолярный воздух при нормальном VA/Q PO2 равняется здесь 104 мм рт. ст. и PCO2 — 40 мм рт. ст.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Парциальное давление кислорода в крови
Диффузия газов в легких
В обычных условиях человек дышит обычным воздухом, имеющим относительно постоянный состав (табл. 1). В выдыхаемом воздухе всегда меньше кислорода и больше углекислого газа. Меньше всего кислорода и больше всего углекислого газа в альвеолярном воздухе. Различие в составе альвеолярного и выдыхаемого воздуха объясняется тем, что последний является смесью воздуха мертвого пространства и альвеолярного воздуха.
Альвеолярный воздух является внутренней газовой средой организма. От его состава зависит газовый состав артериальной крови. Регуляторные механизмы поддерживают постоянство состава альвеолярного воздуха. Состав альвеолярного воздуха при спокойном дыхании мало зависит от фаз вдоха и выдоха. Например, содержание углекислого газа в конце вдоха всего на 0,2-0,3% меньше, чем в конце выдоха, так как при каждом вдохе обновляется лишь 1/7 часть альвеолярного воздуха. Кроме того, газообмен в легких протекает непрерывно, при вдохе и при выдохе, что способствует выравниванию состава альвеолярного воздуха. При глубоком дыхании зависимость состава альвеолярного воздуха от вдоха и выдоха увеличивается.
Таблица 1. Состав воздуха (в %)
Название газа
Воздух
вдыхаемый
выдыхаемый
альвеолярный
Газообмен в легких осуществляется в результате диффузии кислорода из альвеолярного воздуха в кровь (около 500 л в сутки) и углекислого газа из крови в альвеолярный воздух (около 430 л в сутки). Диффузия происходит вследствие разности парциального давления этих газов в альвеолярном воздухе и их напряжений в крови.
Парциальное давление газа: понятие и формула
Парциальное давленые газа в газовой смеси пропорционально процентному содержанию газа и общему давлению смеси:
Для воздуха: Ратмосферное = 760 мм рт. ст.; Скислорода = 20,95%.
Оно зависит от природы газа. Всю газовую смесь атмосферного воздуха принимают за 100%, она обладает давлением 760 мм рт. ст., а часть газа (кислорода — 20,95%) принимают за х. Отсюда парциальное давление кислорода в смеси воздуха равно 159 мм рт. ст. При расчете парциального давления газов в альвеолярном воздухе необходимо учитывать, что он насыщен водяными парами, давление которых составляет 47 мм рт. ст. Следовательно, на долю газовой смеси, входящей в состав альвеолярного воздуха, приходится давление не 760 мм рт. ст., а 760 — 47 = 713 мм рт. ст. Это давление принимается за 100%. Отсюда легко вычислить, что парциальное давление кислорода, который содержится в альвеолярном воздухе в количестве 14,3%, будет равно 102 мм рт. ст.; соответственно, расчет парциального давления углекислого газа показывает, что оно равно 40 мм рт. ст.
Парциальное давление кислорода и углекислого газа в альвеолярном воздухе является той силой, с которой молекулы этих газов стремятся проникнуть через альвеолярную мембрану в кровь.
Диффузия газов через барьер подчиняется закону Фика; так как толщина мембраны и площадь диффузии одинакова, диффузия зависит от диффузионного коэффициента и градиента давления:
Qгаза — объем газа, проходящего через ткань в единицу времени; S — площадь ткани; DK-диффузионный коэффициент газа; (Р1, — Р2) — градиент парциального давления газа; Т — толщина барьера ткани.
Если учесть, что в альвеолярной крови, притекающей к легким, парциальное напряжение кислорода составляет 40 мм рт. ст., а углекислого газа — 46-48 мм рт. ст., то градиент давления, определяющий диффузию газов в легких, будет составлять: для кислорода 102 — 40 = 62 мм рт. ст.; для углекислого газа 40 — 46(48) = минус 6 — минус 8 мм рт. ст. Поскольку диффузный коэффициент углекислого газа в 25 раз больше, чем у кислорода, то углекислый газ более активно уходит из капилляров в альвеолы, чем кислород в обратном направлении.
В крови газы находятся в растворенном (свободном) и химически связанном состоянии. В диффузии участвуют только молекулы растворенного газа. Количество газа, растворяющегося в жидкости, зависит:
Чем выше давление данного газа и температура, тем больше газа растворяется в жидкости. При давлении 760 мм рт. ст. и температуре 38 °С в 1 мл крови растворяется 2,2% кислорода и 5,1 % углекислого газа.
Растворение газа в жидкости продолжается до наступления динамического равновесия между количеством растворяющихся и выходящих в газовую среду молекул газа. Сила, с которой молекулы растворенного газа стремятся выйти в газовую среду, называется напряжением газа в жидкости. Таким образом, в состоянии равновесия напряжение газа равно парциальному давлению газа в жидкости.
Если парциальное давление газа выше его напряжения, то газ будет растворяться. Если парциальное давление газа ниже его напряжения, то газ будет из раствора выходить в газовую среду.
Парциальное давление и напряжение кислорода и углекислого газа в легких приведены в табл. 2.
Таблица 2. Парциальное давление и напряжение кислорода и углекислого газа в легких (в мм рт. ст.)
Название газа
Венозная кровь
Альвеолярный воздух
Парциальное давление и напряжение газов
Если над жидкостью находится смесь газов, то каждый газ растворяется в ней соответственно его парциальному давлении, в смеси, т. е. тому давлению, которое приходится на его долю. Парциальное давление любого газа в газовой смеси можно вычислить, зная общее давление газовой смеси и ее процентный состав. Так, при атмосферном давлении воздуха 700 мм рт.ст. парциальное давление кислорода составляет примерно 21% от 760 мм, т. е. 159 мм, азота — 79% от 700 мм, т. е. 601 мм.
При расчете парциального давления газов в альвеолярном воздухе следует учесть, что он насыщен водяными парами, парциальное давление которых при температуре тела равно 47 мм рт. ст. Поэтому на долю остальных газов (азота, кислорода, углекислого газа) приходится уже не 700 мм, а 700—47 — 713 мм. При содержании кислорода в альвеолярном воздухе, равном 14,3%, парциальное давление его будет равно только 102 мм; при содержании углекислого газа, равном 5,6%, парциальное давление его равно 40 мм.
Если жидкость, насыщенная газом при определенном парциальном давлении придет в соприкосновение с тем же газом, но имеющим меньшее давление, то часть газа выйдет из раствора и количество растворенного газа уменьшится. Если же давление газа будет выше, тогда в жидкости растворится большее количество газа.
Растворение газов зависит от парциального давления, т. е. давления именно данного газа, а не общего давления газовой смеси. Поэтому, например, кислород, растворенный в жидкости, будет выходить в атмосферу азота так же, как и в пустоту, даже в том случае, когда азот находится под очень большим давлением.
При соприкосновении жидкости с газовом смесью определенного состава количество газа, поступившего в жидкость или вышедшего из нее, зависит не только от соотношения давлений газа в жидкости и в газовой смеси, но и от их объемов. Если большой объем жидкости соприкасается с большим объемом газовой смеси, давление которой резко отличается от давления газов в жидкости, то из последней могут выйти или могут войти в нее большие количества газа. Напротив, если достаточно большой объем жидкости соприкасается с газовым пузырьком малого объема, то из жидкости выйдет или войдет в нее очень небольшое количество газа в газовый состав жидкости практически не изменится.
Для газов, растворенных в жидкости, употребляется термин « напряжение », соответствующий термину «парциальное давление» для свободных газов. Напряжение выражается в тех же единицах, что и давление, т.е.в атмосферах или в миллиметрах ртутного или водяного столба. Если напряжение газа равно 1,00 мм рт. ст., то это означает, что растворенная в жидкости газ находится в равновесии со свободным газом, находящихся под давлением 100 мм.
Если напряжение растворенного газа не равно парциальному давлению свободного газа, то равновесие нарушается. Оно восстанавливается, когда эти две величины снова станут равны друг другу. Например, если напряжение кислорода в жидкости замкнутого сосуда равно 100 мм, а давление кислорода в воздухе этого сосуда 150 мм, то кислород будет входить а жидкость.
При этом напряжение кислорода в жидкости будет уволичиваться, а его давление вне жидкости уменьшаться, пока не установится новое динамическое равновесие и обе эти величины не сравняются, получив какое-то новое значение между 150 и 100 мм. Как изменится в данном оучае давление и напряжение, зависит от относительных объемов газа и жидкости.
Алексей Павлюц
Личный сайт
Дайвинг, газы. Понимание принципов за 10 минут (keynotes)
Хотелось бы обобщить информацию о принципах дайвинга в части газов для дыхания в формате keynotes, т.е. когда понимание нескольких принципов избавляет от необходимости запоминания множества фактов.
Итак, для дыхания под водой необходим газ. Как наиболее простой вариант — запас воздуха, представляющий собой смесь кислорода (∼21%), азота (∼78%) и других газов (∼1%).
Главным фактором является давление окружающей среды. Из всех возможных единиц измерения давления мы будем использовать «абсолютную техническую атмосферу» или АТА. Давление на поверхности составляет ∼1 АТА, каждые 10 метров погружения в воду добавляют к нему ∼1 АТА.
При погружении давление воздействует на нас всеобъемлюще. Регулятор поддерживает давление воздуха в системе дыхания, примерно равное давлению окружающей среды, меньшее ровно на столько, на сколько необходимы для «вдыхания». Так, на глубине в 10 метров вдыхаемый из баллона воздух имеет давление около 2 АТА. Аналогичное абсолютное давление будет наблюдаться во всем нашем организме. Таким образом, парциальное давление кислорода на этой глубине составит ∼0,42 АТА, азота ∼1,56 АТА
Воздействие давления на организм заключается в следующих ключевых факторах.
1. Механическое воздействие на органы и системы
Его мы рассматривать подробно не будем, вкратце — человеческий организм имеет ряд заполненных воздухом полостей и резкое изменение давления в любую сторону вызывает нагрузку на ткани, мембраны и органы вплоть до механических повреждений — баротравм.
2. Насыщение тканей газами
При погружении (увеличении давления) парциальное давление газов в дыхательном тракте — выше чем в тканях. Таким образом газы насыщают кровь, а через кровоток насыщаются все ткани организма. Скорость насыщения различна для разных тканей и характеризуется «периодом полунасыщения», т.е. временем, в течение которого при постоянном давлении газа разница парциальных давлений газа и тканей уменьшается вдвое. Обратный процесс называют «рассыщением», он происходит при всплытии (уменьшении давления). В этом случае парциальное давление газов в тканях выше, чем давление в газа в легких, идет обратный процесс — газ из крови выделяется в легких, кровь с уже меньшим парциальным давлением циркулирует по организму, из тканей газы переходят в кровь и снова по кругу. Газ всегда движется от большего парциального давления к меньшему.
Принципиально важно, что разные газы имеют разную скорость насыщения/рассыщения, обусловленную их физическими свойствами.
Растворимость газов в жидкостях тем больше, чем выше давление. В случае, если количество растворенного газа больше предела растворимости при данном давлении — происходит выделение газа, в том числе концентрация в виде пузырьков. Мы это наблюдаем каждый раз, как вскрываем бутылку газированной воды. Так как скорость выведения газа (рассыщения тканей) ограничена физическими законами и газовым обменом через кровь, слишком быстрое падение давления (быстрое всплытие) может привести к образованию пузырьков газа непосредственно в тканях, сосудах и полостях организма, нарушая его работу вплоть до летального исхода. Если давление падает медленно, то организм успевает вывести «лишний» газ за счет разницы парциальных давлений.
Для расчетов этих процессов используются математические модели тканей организма, наиболее популярной является модель Альберта Бюльмана, которая учитывает 16 видов тканей (компартментов) со временем полунасыщения/полурассыщения от 4 до 635 минут.
Наибольшую опасность представляет инертный газ, имеющий максимально большое абсолютное давление, чаще всего это — азот, который составляет основу воздуха и не участвует в метаболизме. По этой причине основные расчеты в массовом дайвинге проводятся по азоту, т.к. воздействие кислорода в плане насыщения на порядки меньше, при этом оперируют понятием «азотная нагрузка», т.е. остаточное количество растворенного в тканях азота.
«Продвинутые» дайверы используют дайв-компьютеры, которые динамически рассчитывают насыщение по моделям в зависимости от газа и давления, в том числе рассчитывают «компрессионный потолок» — глубину, всплытие выше которой потенциально опасно исходя из текущего насыщения. При сложных погружениях компьютеры дублируются, не говоря уже о том, что одиночные погружения как правило не практикуются.
3. Биохимическое воздействие газов
Наш организм максимально адаптирован к воздуху при атмосферном давлении. При увеличении давления газы, даже не участвующие в метаболизме воздействуют на организм самым разным образом, при этом воздействие зависит от парциального давления конкретного газа. Для каждого газа существуют свои пределы безопасности.
Кислород
Являясь ключевым участником нашего метаболизма, кислород — единственный газ, имеющий не только верхний, но и нижний предел безопасности.
Нормальное парциальное давление кислорода ∼0,21 АТА. Потребность в кислороде сильно зависит от состояния организма и физических нагрузок, теоретический минимально необходимый уровень для поддержания жизнедеятельности здорового организма в состоянии полного покоя оценивается в ∼0,08 АТА, практический — в ∼0,14 АТА. Снижение уровня кислорода от «номинального» в первую очередь сказывается на способности к физической активности и может вызвать гипоксию, или кислородное голодание.
В то же время высокое парциальное давление кислорода вызывает широкий спектр негативных последствий — кислородное отравление или гипероксию. Особую опасность при погружении имеет ее судорожная форма, выражающуюся в поражении нервной системы, судорогах, что влечет за собой риск утопления.
Для практических целей дайвинга принято считать пределом безопасности ∼1,4 АТА, пределом умеренного риска — ∼1,6 АТА. При давлении выше ∼2,4 АТА в течение длительного времени вероятность кислородного отравления стремиться к единице.
Таким образом, несложным делением предельного уровня кислорода 1,4 АТА на парциальное давление кислорода в смеси можно определить максимальное безопасное давление среды и установить, что абсолютно безопасно дышать чистым кислородом (100%, 1 АТА ) можно на глубинах до ∼4 метров (. ), сжатым воздухом (21%, 0,21 АТА) — до ∼57 метров, стандартным «нитрокс-32» с содержанием кислорода 32% (0,32 АТА) — до ∼34 метров. Аналогично можно посчитать пределы для умеренного риска.
Необходимо принимать во внимание, что повышенное парциальное давление кислорода в любом случае оказывает воздействие на нервную систему и легкие, причем это разные виды воздействия. Кроме того, воздействие имеет свойство накапливаться при серии погружений. Для учета воздействия на ЦНС используется понятие «кислородного лимита» как расчетной единицы, с помощью которой определяются безопасные лимиты для разового и суточного воздействия. Подробно с таблицами и расчетами можно ознакомиться здесь.
Помимо этого, повышенное давление кислорода негативно воздействует на легкие, для учета этого явления используются «единицы кислородной выносливости», которые рассчитываются по специальным таблицам, соотносящим парциальное давление кислорода и количество «единиц в минуту». Для примера, 1.2 АТА дает нам 1.32 OTU в минуту. Признанный лимит безопасности составляет 1425 единиц в сутки.
Из вышесказанного в частности должно быть понятно, что для безопасного пребывания на больших глубинах требуется смесь с пониженным содержанием кислорода, которая непригодна для дыхания при меньшем давлении. Например, на глубине 100 метров (11 АТА) концентрация кислорода в смеси не должна превышать 12%, а на практике будет еще ниже. Дышать такой смесью на поверхности невозможно.
Азот не метаболизируется организмом и не имеет нижней границы. При повышенном давлении азот оказывает отравляющее воздействие на нервную систему, сходное с наркотическим или алкогольным опьянением, известное как «азотный наркоз«.
Механизмы воздействия точно не выяснены, границы воздействия сугубо индивидуальны, и зависят как от особенностей организма, так и от его состояния. Так, известно, что усиливает воздействие состояние усталости, похмелья, все виды угнетенного состояния организма типа простудных заболеваний и т.д.
Незначительные проявления в виде состояния, сравнимого с легким опьянением возможны на любых глубинах, действует эмпирическое «правило мартини», согласно которому воздействие азота сравнимо с бокалом сухого мартини натощак на каждые 10 метров глубины, что не представляет опасности и добавляет хорошего настроения. Накопленный при регулярных погружениях азот так же влияет на психику сродни легким наркотикам и алкоголю, чему автор сам свидетель и участник. Проявляется в ярких и «наркотических» снах, в частности, действует в пределах нескольких часов. И таки да, дайверы — немного наркоманы. Азотные.
Опасность представляют сильные проявления, которые характеризуются стремительным нарастанием вплоть до полной потери адекватности, ориентации в пространстве и времени, галлюцинаций, что может привести к гибели. Человек может запросто рвануть на глубину, потому что там клево или он там что-то якобы увидел, забыть, что он под водой и «вдохнуть полной грудью», выплюнув загубник и т.д. Само по себе воздействие азота не летально и даже не вредно, однако последствия в условиях погружения могут быть трагичны. Характерно, что при снижении давления эти проявления так же стремительно проходят, иногда достаточно подняться всего на 2..3 метра чтобы «резко протрезветь».
Вероятность сильного проявления на глубинах, принятых для рекреационного дайвинга начального уровня (до 18 м, ∼2,2 АТА ) оценивается как очень низкая. По имеющейся статистике случаи тяжелого отравления становятся довольно вероятны с 30 метров глубины (∼3,2 АТА), и далее вероятность растет по мере роста давления. В то же время люди с индивидуальной устойчивостью могут не испытывать проблем и на куда больших глубинах.
Единственным способом противодействия является постоянный самоконтроль и контроль напарника с немедленным уменьшением глубины в случае подозрения на азотное отравление. Использование «нитрокса» снижает вероятность азотного отравления, естественно, в пределах ограничений по глубинам, обусловленных кислородом.
Гелий и другие газы
В техническом и профессиональном дайвинге используют и другие газы, в частности, гелий. Известны примеры использования в глубинных смесях водорода, и даже неона. Эти газы отличаются высокой скорость насыщения/рассыщения, отравляющие эффекты гелия наблюдаются при давлении более 12 АТА и могут быть, как ни парадоксально, компенсированы азотом. Однако широкого применения они не имеют за счет высокой стоимости, поэтому столкнуться с ними дайверу средней руки фактически невозможно, а уж если читателя действительно интересуют такие вопросы — то ему уже надо использовать профессиональную литературу, а не этот скромный обзор.
При использовании любых смесей логика расчетов остается такой же, как описано выше, только используются специфические для каждого газа лимиты и параметры, а для глубоких технических погружений обычно используются несколько разных составов: для дыхания на пути вниз, работы внизу и поэтапного пути вверх с декомпрессией, составы этих газов оптимизируются исходя из описанной выше логики их движения в организме.
Практическое заключение
Понимание этих тезисов позволяет придать осмысленность многим даваемым на курсах ограничениям и правилам, что совершенно необходимо как для дальнейшего развития, так и для правильного их нарушения.
Нитрокс рекомендован к использованию при обычных погружениях, ибо он снижает азотную нагрузку на организм даже если Вы остаетесь полностью в пределах ограничений рекреационного дайвинга, это лучшее самочувствие, больше удовольствия, легче последствия. Однако, если Вы собираетесь нырять глубоко и часто — надо помнить не только о его преимуществах, но и о возможной кислородной интоксикации. Всегда лично проверяйте уровни кислорода и определяйте свои лимиты.
Азотное отравление — наиболее вероятная из проблем, с которыми можно столкнуться, всегда будьте внимательны к себе и партнеру.
Отдельно хотелось бы обратить внимание, что прочтение данного текста не означает, что читатель освоил полный набор информации для понимания работы с газами при сложных погружениях. Для практического применения этого совершенно недостаточно. Это только стартовая точка и базовое понимание, не более того.
Всегда оставайтесь в пределах своих знаний и физических возможностей! Удачи!















