ПГД эмбриона

Наши преимущества
У вас в семье есть наследственные заболевания? Вы хотите, чтобы у будущего ребенка не было хромосомных аномалий? Нужно повысить шансы на успех ЭКО? Поможет преимплантационное генетическое тестирование (ПГД)!
Такой подход позволяет предупредить патологии, которые невозможно определить визуально, ведь генетические нарушения могут иметь даже эмбрионы хорошего качества.
Чтобы определить наличие показаний к ПГТ (ПГД), нужно записаться на консультацию к генетику. Специалист также сможет решить, какой метод диагностики будет наиболее эффективным именно в вашем случае.
ПГТ хромосомных аномалий (ПГТ-А) предполагает проведение преимплантационного генетического тестирования (ПГД), позволяющего выявить лишние или недостающие хромосомы в ядре клетки, а также участки, на которых генетический материал утрачен или же, напротив, удвоен. Важно, что современная методика позволяет провести анализ по всем 46 хромосомам и не ограничена обнаружением наиболее вероятных нарушений.
ПГТ моногенных заболеваний (ПГТ-М) позволяет выявить определенное наследственное заболевание. Этот метод может быть рекомендован в том случае, если присутствует высокий риск генных мутаций у будущего ребенка.
Показания к ПГТ (ПГД)
Преимплантационное генетическое тестирование (ПГД) может потребоваться в следующих случаях:
Каких целей позволяет достичь ПГТ (ПГД)
ПГТ на анеуплоидии (ПГТ-А) дает возможность:
ПГТ моногенных заболеваний (ПГТ-М), если в семье присутствует наследственная патология, дает возможность:
Как проводится преимплантационное генетическое тестирование эмбрионов (ПГД эмбрионов)
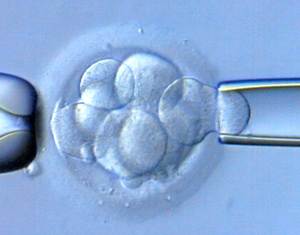
Сначала специалисты должны получить материал для исследования. С этой целью осуществляется биопсия нескольких клеток эмбриона.
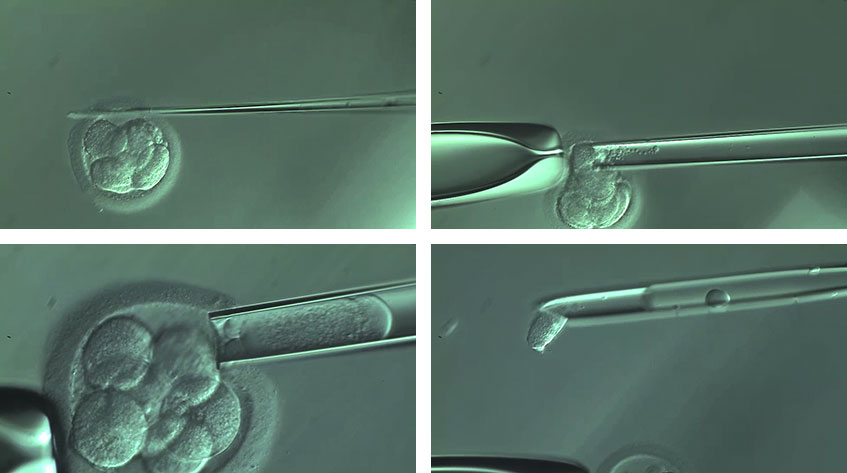
На первом этапе нужно разрушить блестящую оболочку, а уже затем с помощью специального микрокапилляра извлечь клетку и зафиксировать ее для проведения дальнейшего генетического тестирования.
ПГТ эмбриона может осуществляться с применением следующих методик:
Раньше преимплантационное генетическое тестирование эмбрионов проводилось, как правило, на 3 день, однако сейчас доказано, что проведение биопсии на этом этапе заметно снижает жизнеспособность эмбрионов. В то же время забор клеток на 5 день после оплодотворения не влияет на их дальнейшее развитие.
Запишитесь на прием к специалисту «Нова Клиник» в Москве и узнайте больше о преимплантационном генетическом тестировании эмбрионов. Цена консультации указана на сайте.
Преимплантационная генетическая диагностика (ПГД, ПГС) в Москве
Метод, который выявляет у эмбрионов, полученных в результате ЭКО, генные и хромосомные патологии, и позволяет переносить в полость матки пациентки только нормальные образцы.
| Цена | 27 500 руб. |
| Срок исполнения | до 60 рабочих дней |
| Исследуемый материал | Биопсия клеток наружного слоя бластоцисты |
| Метод исследования | Исследование генов эмбрионов |
Что такое ПГД?
Для семей, которые точно знают о наличии проблем, связанных с хромосомными перестройками и генными мутациями, ПГД особенно актуальна и является единственной диагностикой, благодаря которой можно родить здорового ребенка в рамках протокола экстракорпорального оплодотворения. Тест дает возможность выявить изменения в хромосомном наборе, нарушения структуры хромосом и генетического аппарата, мутации генов до этапа переноса эмбрионов. То есть врачи смогут обнаружить нездоровые эмбрионы до их подсадки в маточную полость пациентки. Для переноса отбирается самый жизнеспособный здоровый материал. Поэтому будущие мать и отец могут не переживать о том, что у них может появиться ребенок с синдромом Дауна или другими тяжелыми наследственными заболеваниями.
ПГТ-А (ПГД хромосомных аномалий) позволяет обнаружить:
ПГТ-М (ПГД моногенных заболеваний) позволяет идентифицировать конкретную наследственную патологию. Исследование рекомендовано при высоком риске мутагенеза у будущего ребенка.
Показания к ПГТ эмбриона
Основания к проведению преимплантационной диагностики определяет генетик. После консультации и детального изучения анамнеза пациентов врач индивидуально назначает оптимальный метод исследования.
Преимплантационный генетический анализ эмбрионов
Каждая из 100 триллионов клеток в организме человека (за исключением красных кровяных клеток) содержит весь человеческий геном. Хромосомы – это струноподобные элементы внутри ядра (в центре) каждой клетки вашего тела. Они содержат генетическую информацию, ДНК. Ген занимает определенное место на хромосоме. В норме, есть 23 идентичных пары хромосом (2 метра ДНК) в каждой клетке, в общей сложности 46 хромосом. Каждый партнер во время оплодотворения обычно предоставляет 23 хромосомы. Если яйцеклетка или сперматозоид имеют аномальную упаковку хромосом, эмбрион, который они создают, также будет иметь хромосомные аномалии. Иногда это связано с перестройкой хромосом, или недостатком части хромосомы. В некоторых случаях есть отсутствующие хромосомы, или дополнительная хромосома (анеуплоидии), ведущие к наследственным заболеваниям. Любой эмбрион, в котором отсутствует хромосома (моносомия) перестанет расти до имплантации (фатальная аномалия). Если анеуплоидии включают хромосомы 13, 18, 21, Х или Y, беременность может дойти до родов. Наиболее распространенной из этих несмертельных аномалий является трисомия 21, или синдром Дауна, при которой присутствует дополнительная 21-я хромосома. Другие включают синдром Тернера у женщин и синдром Клайнфельтера у мужчин.
История преимплантационной генетической диагностики (ПГД)
Первые живорождения после ПГД были зарегистрированы в Лондоне в 1989 году. Две двойни девочек-близнецов родились от пяти пар с риском передачи связанного с Х-хромосомой заболевания. В настоящее время с помощью методов генетического анализа или ПГД могут быть обнаружены около 90% аномальных эмбрионов. Не все хромосомные или генетические заболевания могут быть определены этими процедурами, так как в ходе одной процедуры может быть диагностировано только ограниченное число хромосом. Многочисленные исследования на животных и некоторые исследования на человеке показывают, что микрохирургия эмбриона (биопсия), необходимая для удаления клеток, не влияет на нормальное развитие ребенка. Эта процедура, однако, была выполнена относительно небольшому числу пациентов во всем мире, поэтому точные негативные последствия, если таковые имеются, неизвестны. Несмотря на то, что после генетического анализа для выявления анеуплоидии всем мире на сегодняшний день было рождено уже много детей, эта процедура все еще относительно нова. В исследованиях на животных не было обнаружено никаких очевидных проблем и предварительные данные с эмбрионами человека позволяют предположить справедливость этого вывода. В исследовании, проведенном в Университетском колледже Лондона, исследователи недавно рассмотрели 12 преимплантационных эмбрионов с новой техникой, которая сочетает в себе амплификацию всего генома (WGA) и сравнительную гибридизацию генома (CGH). В результате в 8 из 12 изученных эмбрионов были обнаружены значительные хромосомные аномалии. Это может объяснить, почему люди имеют в лучшем случае 25% шансов на достижение жизнеспособной беременности в месяц при естественном зачатии.
Как передаются по наследству генетические заболевания
В диаграммах ниже, D или d представляет дефектный ген, а N или n представляет нормальный ген. Мутации не всегда приводят к болезни.
Доминантные заболевания:
Один из родителей имеет один дефектный ген, который доминирует над своей нормальной парой. Так как потомки наследуют половину своего генетического материала от каждого из родителей, есть 50% риск наследования дефектного гена, и, следовательно, заболевания.
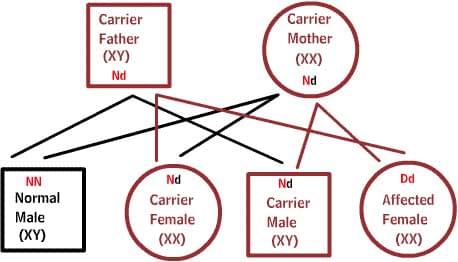
Рецессивные заболевания:
Оба родителя являются носителями одного дефектного гена, но при этом имеют нормальную пару гена. Для наследования заболевания необходимы две дефектных копии гена. Каждый потомок имеет 50% шанс быть носителем, и 25% шанс унаследовать заболевание.
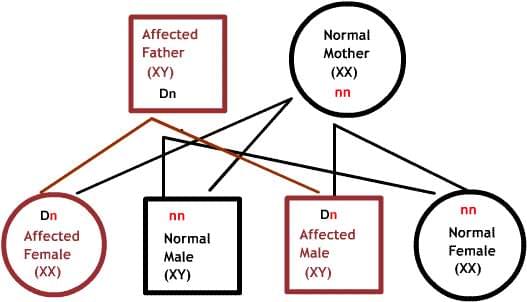
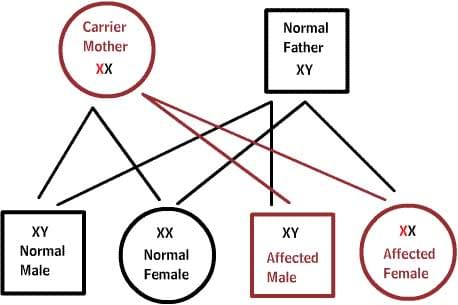
X-сцепленные заболевания:
Нормальные женщины имеют XX хромосомы, а нормальные мужчины XY. Женщины, которые имеют нормальный ген на одной из Х-хромосом, защищены от дефектного гена на их другой Х-хромосоме. Однако, у мужчины отсутствует такая защита в связи с наличием только одной Х-хромосомы. Каждый мужской потомок от матери, которая несет в себе дефект, имеет 50% шанс унаследовать дефектный ген и заболевание. Каждый женский потомок имеет 50% шанс быть носителем, как и ее мать. (на рисунке ниже X представляет нормальный ген а X представляет дефектный ген)
Возможные преимущества генетического анализа
Преимплантационная генетическая диагностика позволяет отобрать и перенести не измененные (хромосомно нормальные) эмбрионы, которые могут привести к большей частоте имплантации на эмбрион, сокращению потерь беременности и рождению большего числа здоровых детей. Генетическая диагностика предлагает парам альтернативу мучительному выбору по поводу того, чтобы прервать пострадавшую беременность после пренатальной диагностики, производимой путем амниоцентеза или биопсии ворсин хориона (CVS) на более поздних стадиях беременности. Почти все генетически связанные заболевания, которые могут быть диагностированы в перинатальном периоде либо амниоцентезом или CVS, могут быть обнаружены и ПГД. Процедура должна уменьшить психологическую травму для пар, которые несут повышенный риск генетических заболеваний для потомства.
Преимущества преимплантационной генетической диагностики (ПГД) могут включать в себя:
Возможные риски генетического анализа
Кандидаты для биопсии эмбриона и ПГД
Кандидаты для биопсии эмбриона и ПГД включают в себя:
Пары с повторными неудачами ЭКО.
Используемые методы
Для анализа на наличие генетических дефектов эмбриона, из него необходимо удалить либо первое полярное тельце из неоплодотворенной яйцеклетки и/или 1 или 2 клетки от каждого эмбриона. Это называется биопсией яйцеклетки или эмбриона и обычно делается перед тем, как происходит оплодотворение, или через 3 дня после оплодотворения. Биопсия на 6-10 клеточной стадии не оказывает отрицательного влияния на преимплантационное развитие. На этом этапе каждая клетка имеет полный набор хромосом. Обычно из эмбриона удаляется только одна клетка, так как ожидается, что будут одинаковыми со всеми другими клетками в эмбрионе. Иногда необходимо удалить вторую клетку из эмбриона, например, если сигнал в первой не обнаружен. Для диагноза предрасположенности с помощью первого и второго полярных телец, как показателей генетического статуса яйцеклетки, используется анализ методом FISH. Недостатком анализа полярных телец заключается в том, что он не принимает во внимание отцовские анеуплоидии.
Анализ биопсированной клетки использует один из двух методов:
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.
Клиника «Центр ЭКО»
Бесплодным считается брак, в котором отсутствует беременность у женщины при регулярной половой жизни партнеров без использования каких-либо противозачаточных средств. Ошибочно полагается, что бесплодие относится только к женщинам. В 45 процентах случаев это патология со стороны женщин, а в 40 процентах – у мужчин. Еще в 5-10 процентах случаев нарушения обнаруживаются сразу у обоих партнеров.
Клиническое бесплодие бывает:
Наиболее распространены следующие формы бесплодия:
В клинике бесплодия первой жалобой пациентов является отсутствие беременности либо выкидыши с невозможностью выносить и родить малыша. Также выявляются жалобы, связанные с первичной или сопутствующей патологией. Анамнез также подтверждает нарушения менструального цикла, перенесенные операции и аборты, воспалительные заболевания, или заболевания щитовидной железы, надпочечников, либо травму головного мозга. При физикальном обследовании могут выявиться ожирение, клиника синдрома Иценко-Кушинга, который также провоцирует бесплодие, признаки гиперандрогении (повышение андрогенов – мужских половых гормонов), либо нервная анорексия, клинически также приводящая к бесплодию.
Почему стоит выбрать клинику «Центр ЭКО»?
Преимущества клиники «Центр ЭКО»:
Комфорт и удобство клиники «Центр ЭКО»
Подробно узнать о ВРТ-программах клиники «Центр ЭКО» вы можете в разделе «Наши услуги».
Мы поможем вам осуществить вашу мечту о детях!
Преимплантационная генетическая диагностика эмбриона
До последнего времени единственным способом предотвратить рождение больного ребенка было прерывание беременности после того, как в результате диагностических процедур (пренатальная диагностика) получали подтверждение генетической патологии у плода. В случае преимплантационного генетического тестирования есть возможность отобрать эмбрионы без генетических аномалий еще до стадии переноса.
Как правило, у одной женщины получают несколько яйцеклеток, и почти всегда есть возможность выбрать хотя бы одну здоровую, которая даст жизнь здоровому ребенку. Полученные яйцеклетки сначала оплодотворяют, затем делают биопсию эмбрионов, отбирают с помощью генетического анализа здоровые эмбрионы и переносят их в матку женщины. Болезни, которые ребенок может получить от отца, можно определить только путем биопсии эмбриона.
Преимплантационная диагностика является единственной альтернативой методам пренатальной диагностики.
Типы ПГТ (Преимплантационная генетическая диагностика)
ПГТ разделяют на несколько типов по целевому направлению диагностики.
ПГТ-А – анализ анеуплоидий, направлен на выбор эмбриона с нормальным количеством хромосом. Чаще всего данный подход применяется для увеличения шансов на имплантацию при переносе. Он позволяет быстрее получить желаемую беременность (повышает шансы до 70-75%) и позволяет избежать переноса анеуплоидных эмбрионов, например, с синдромом Дауна.
ПГТ-М – тестирование на конкретную мутацию, выявленную у родственников. Это возможность исключения моногенных (обусловленных одним геном) заболеваний у переносимых эмбрионов. Необходима дополнительная предварительная диагностика родителей для уточнения, в каком именно участке гена могла произойти мутация. Стоит отметить, что диагностика проводится только на конкретную мутацию и гарантирует ее отсутствие в переносимом эмбрионе, но совершенно ничего не говорит об отсутствии других нарушений в его геноме.
ПГТ – SR – тестирование эмбрионов на наличие специфических перестроек в их ДНК, которые так же могут приводить к различным заболеваниям и передаваться по наследству.
Наши врачи
Показания к ПГД (ПГТ)
Какие болезни выявляет ПГТ-М? Уже сегодня возможна «выбраковка» до беременности эмбрионов с такими наследственными заболеваниями, как муковисцидоз, гемофилия А, болезнь Тей-Сакса, дефицит 1-антитрипсина, миатрофия Дюшена и др. (см. список).
Список некоторых наиболее распространенных наследственных заболеваний:
Наши преимущества
ребенка родилось благодаря нашим специалистам
Как правило, у одной женщины получают несколько яйцеклеток, и почти всегда есть возможность выбрать хотя бы одну лучшую, которая даст жизнь здоровому ребенку. Полученные яйцеклетки сначала оплодотворяют, затем эмбрионы культивируют и на 5-6-й день делают биопсию трофэктодермы – клеток, которые участвуют в формировании плаценты.
Такой подход меньше всего сказывается на жизнеспособности эмбрионов и, в отличие от биопсии на 3-й день, наименее травматичен. Полученные клетки под микроскопом помещают в специальные пробирки и передают в генетическую лабораторию. Среди всех биоптатов, отбирают с помощью генетического анализа те эмбрионы, что не несут патологии и именно их переносят в матку женщины.
Что дальше? ПГТ методом NGS
Секвенирование нового поколения – NGS (Next Generation Sequencing) – это метод определения последовательности нуклеотидов в ДНК.
Технология позволяет проводить анализ последовательности ДНК одновременно в большом количестве участков хромосомы, что дает возможность значительного ускорения всего процесса и снижает себестоимость. Для определения последовательности нуклеотидов (структур ДНК) необходимо создать копию исследуемой ДНК.
Существует несколько путей определения последовательности нуклеотидов в интересующей нас ДНК при помощи NGS. Эту последовательность можно определить с помощью измерения кислотности среды (ph) при удлинении копируемой цепочки; второй путь заключается в использовании «меченых» нуклеотидов: их считывает светочувствительная матрица, а компьютер обрабатывает информацию и строит цепочку ДНК.
Оба метода требуют получения достаточного для анализа последовательности количества ДНК. В случае работы с биоптатом трофэктодермы (при проведении ПТГ) речь идет о тонком процессе выделения ДНК из единичных клеток. Для увеличения количества ДНК и возможности безошибочной диагностики применяют метод т.н. «полногеномной амплификации» (WGA), позволяющей в миллионы раз увеличить копии всей ДНК в образце. Трудность в том, что WGA не идентифицирует отдельно источник ДНК, то есть одинаково эффективно будет удваивать и ДНК клеток эмбриона и ДНК, занесенную в реакцию извне.
Поэтому чистота выполнения всех процедур биопсии и подготовки пробы к анализу критична для адекватного ответа генетической лаборатории и проверяется множественными контролями. Например, в нашей лаборатории–партнере всегда проводится контроль чистоты вновь приготовленного «буфера» (среды с ДНК), контроль его функциональной работы, контроль правильного раскапывания буфера в пробирки для анализа, контроль чистоты индивидуально для каждого образца, контроль работоспособности буфера с единичными клетками. Эмбриологи нашей лаборатории, в обязательном порядке, проходят тестовую биопсию, позволяющую минимизировать человеческий фактор ошибок.
После WGA возможно проведение уже самого анализа последовательности полученной ДНК. Все описанные этапы автоматизированы и проходят в специальном приборе под контролем компьютерной программы. На первом этапе создается так называемая библиотека случайных последовательностей ДНК – геном режется на небольшие фрагменты длиной от 25 до 20 000 нуклеотидов, каждый из которых присоединяется к специальным адаптерным участкам с известной последовательностью.
Второй этап — создание копий этих последовательностей при помощи эмульсионной ПЦР (когда в каждой капельке масла в суспензии ферментов амплифицируется индивидуальная молекула ДНК). Третий этап — определение первичной структуры всех фрагментов тем или иным способом. И в заключении, обработка полученных данных, их анализ и интерпретация.
Нажимая кнопку “Отправить заявку”, Вы даете согласие на обработку Ваших персональных данных в соответствии с условиями
Очевидно, что точность определения последовательности ДНК будет зависеть от количества прочтений – ридов (сколько раз один и тот же участок прошел анализ) матрицы – чем их больше – тем точнее. В современных протоколах для ПГТ-А используют сотни тысяч таких ридов, а при анализе единичных мутаций конкретного гена ( ПГТ-М ) – миллионы. За счет этого удается добиться поразительной точности анализа и исключить ошибки неправильного прочтения нуклеотидов.
Заключительным этапом является т.н. биоинформатический анализ полученных данных. Зачастую именно анализ и выявление клинически-значимых отклонений последовательности ДНК и определение критериев их значимости занимает больше времени само определение последовательности. Метод NGS в практике ПГТ дает практически неограниченные возможности; определение хромосомных поломок – лишь незначительная толика того, что может дать этот метод. Достаточно упомянуть о том, что с помощью NGS можно расшифровать весь геном человека!
Выбор правильного подхода и цели исследования определяются на этапе генетического консультирования (желательно до начала процедуры ЭКО!) и может потребовать дополнительных подготовительных исследований ДНК родителей или родственников в случае программ ПГТ при подозрении на наследственное заболевание. Как правило, в большинстве случаев ПГТ достаточно довольно поверхностного анализа генетической информации эмбриона или его родителей.