Пероксид ацетона
| Пероксид ацетона | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | 3,3,6,6-тетраметил-1,2,4,5-тетраоксан (димер) 3,3,6,6,9,9-гексаметил-1,2,4, 5,7,8-гексаоксациклононан (тример) |
| Химическая формула | C6H12O4 (димер) C9H18O6 (тример) |
| Физические свойства | |
| Молярная масса | (димер) 148,157 г/моль (тример) 222,24 г/моль |
| Термические свойства | |
| Температура плавления | 91 °C |
| Температура кипения | 97–160 °C |
| Классификация | |
| Рег. номер CAS | 17088-37-8 |
| SMILES | CC1(OOC(OOC(OO1)(C)C)(C)C)C |
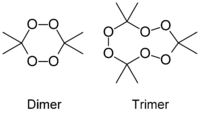
Пероксид ацетона (перекись ацетона, триперекись ацетона, диперекись ацетона, трициклоацетонпероксид, ТА, ДА, ТЦАП, киса, (3,3,6,6,9,9-гексаметил-1,2,4,5,7,8-гексаоксонан)) — инициирующее взрывчатое вещество, впервые получено в 1885 году Вольфенштейном. Существует в виде тримера и димера. Иногда можно встретить утверждения о существовании мономера и полимера, однако достоверные подтверждения этого неизвестны. В большинстве случаев образуется триперекись, иногда с небольшими примесями диперекиси. Чистая диперекись получается лишь при использовании специальных кислот. Часто можно встретить ошибку, когда триперекись называют диперекисью. Название «киса» является жаргонным, произошло, по всей видимости, от «перекись ацетона», или из-за сильной чувствительности к трению («против шерсти лучше не гладить»).
Содержание
Физические свойства
Представляет собой мелкодисперсное вещество, похожее на муку. После многомесячного хранения или перекристаллизации из растворителя образуются крупные прозрачно-белые кристаллы неправильной формы. Вещество практически нерастворимо в воде, растворимо в ацетоне, эфире. Температура плавления триперекиси — 97 °С, диперекиси — 132 °С.
При комнатной температуре улетучивается с разложением, в открытом сосуде большие количества перекиси могут полностью испариться за десятки минут. При хранении даже в приоткрытом сосуде происходит кристаллизация из паров, что ведёт к росту высокочувствительных кристаллов.
Взрывчатые свойства
Скорость детонации при плотности 0,92 г/см³ — 3750 м/с, 1,2 г/см³ — 5290 м/с. Способна к перепрессовке, то есть спрессованная под давлением около 2000 кгс/см² уже горит, а не детонирует.
По бризантности превосходит азид свинца и ГМТД, по инициирующей способности превосходит гремучую ртуть, но уступает ГМТД и азиду свинца.
Инициирующая способность для тетрила 0,09;г, для тротила 0,18;г.
Уравнение взрывчатого разложения:
Небольшие количества на открытой поверхности сгорают большим, объёмным пламенем, с глухим звуком хлопка. В количествах более 10 г и/или запрессованная в бумажный корпус оглушительно детонирует.
Не взаимодействует с большинством металлов, однако свинец является катализатором разложения перекисей и может привести к самоподрыву, поэтому контакт перекисей ацетона с ним опасен. Соли переходных металлов (железо, хром, марганец) также являются катализаторами разложения перекиси ацетона.
Получение
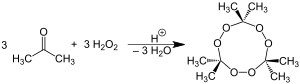
Перекись ацетона получают путём воздействия пероксида водорода на ацетон в кислой среде. Реакция отличается малой требовательностью к условиям. Для получения кислой среды используются разнообразные минеральные кислоты. Как правило, рекомендуется использование соляной кислоты, однако реакция идёт и при использовании азотной, ортофосфорной, серной, надсерной и других кислот. В случае использования серной кислоты образуется триперекись с примесями диперекиси, в случае надсерной кислоты — диперекись. В остальных случаях образуется триперекись ацетона
Применение
C 9 H 18 O 6 (тример)
C 12 H 24 O 8 (тетрамер)
222,24 г / моль (тример)
91 ° C (тример)
17 384 фут / с
3,29 миль в секунду
СОДЕРЖАНИЕ
История
Работа над этой методологией и над различными полученными продуктами была дополнительно исследована в середине 20 века Миласом и Голубовичем.
Химия
Продукт, полученный с использованием соляной кислоты, считается более стабильным, чем продукт, полученный с использованием серной кислоты. Известно, что следы серной кислоты, захваченные внутри образовавшихся кристаллов пероксида ацетона, приводят к нестабильности. Фактически, захваченная серная кислота может вызывать детонацию при температурах до 50 ° C (122 ° F), это наиболее вероятный механизм случайных взрывов пероксида ацетона, которые происходят во время сушки на нагретых поверхностях.
Трипероксид триацетона образуется в 2-пропаноле при длительном стоянии на воздухе.
Для анализа следов ТАТФ можно использовать несколько методов, включая газовую хроматографию / масс-спектрометрию (ГХ / МС), высокоэффективную жидкостную хроматографию / масс-спектрометрию (ВЭЖХ / МС) и ВЭЖХ с постколоночной производной.
Пероксид ацетона растворим в толуоле, хлороформе, ацетоне, дихлорметане и метаноле. Перекристаллизация первичных взрывчатых веществ может давать большие кристаллы, которые самопроизвольно взрываются из-за внутренней деформации.
Промышленное использование
Перекись ацетона используется в качестве отбеливателя муки для отбеливания и «зрелой» муки.
Использование в самодельных взрывных устройствах
Избыточное давление ударной волны ТАТФ составляет 70% от давления ТНТ, импульс положительной фазы составляет 55% от эквивалента ТНТ. ТАТФ при 0,4 г / см 3 имеет примерно одну треть бризантности TNT (1,2 г / см 3 ), измеренной с помощью теста Гесса.
В Европейском Союзе приняты законодательные меры по ограничению продажи концентрированной перекиси водорода до 12% и выше.
C 9 H 18 O 6 (тример)
C 12 H 24 O 8 (тетрамер)
222,24 г / моль (тример)
91 ° C (тример)
17 384 фут / с
3,29 миль в секунду
СОДЕРЖАНИЕ
История
Работа над этой методологией и над различными полученными продуктами была дополнительно исследована в середине 20 века Миласом и Голубовичем.
Химия
Продукт, полученный с использованием соляной кислоты, считается более стабильным, чем продукт, полученный с использованием серной кислоты. Известно, что следы серной кислоты, захваченные внутри образовавшихся кристаллов пероксида ацетона, приводят к нестабильности. Фактически, захваченная серная кислота может вызывать детонацию при температурах до 50 ° C (122 ° F), это наиболее вероятный механизм случайных взрывов пероксида ацетона, которые происходят во время сушки на нагретых поверхностях.
Трипероксид триацетона образуется в 2-пропаноле при длительном стоянии на воздухе.
Для анализа следов ТАТФ можно использовать несколько методов, включая газовую хроматографию / масс-спектрометрию (ГХ / МС), высокоэффективную жидкостную хроматографию / масс-спектрометрию (ВЭЖХ / МС) и ВЭЖХ с постколоночной производной.
Пероксид ацетона растворим в толуоле, хлороформе, ацетоне, дихлорметане и метаноле. Перекристаллизация первичных взрывчатых веществ может давать большие кристаллы, которые самопроизвольно взрываются из-за внутренней деформации.
Промышленное использование
Перекись ацетона используется в качестве отбеливателя муки для отбеливания и «зрелой» муки.
Использование в самодельных взрывных устройствах
Избыточное давление ударной волны ТАТФ составляет 70% от давления ТНТ, импульс положительной фазы составляет 55% от эквивалента ТНТ. ТАТФ при 0,4 г / см 3 имеет примерно одну треть бризантности TNT (1,2 г / см 3 ), измеренной с помощью теста Гесса.
В Европейском Союзе приняты законодательные меры по ограничению продажи концентрированной перекиси водорода до 12% и выше.
Что такое перекись ацетона
Что такое перекись ацетона?
Строение молекулы перекиси водорода
Перекись водорода (3% раствор)
Цистерна с перекисью водорода
Перекись водорода проявляет окислительные свойства. Некоторые горючие органические материалы (например, бумага, солома, метанол) при контакте с крепкой перекисью водорода могут воспламеняться. От действия 30% раствора перекиси водорода кожа и волосы человека становятся белыми. Разбавленные водные растворы перекиси водорода гораздо более стабильны. Трехпроцентная перекись водорода продается в аптеках как антисептик.
Другие неорганические перекиси также проявляют окислительные свойства, многие из них довольно неустойчивы и легко отщепляют кислород.
Однако, некоторые неорганические перекиси достаточно стабильны. Например, перекись натрия Na2O2 образуется при горении натрия на воздухе. Данное вещество плавится без разложения при 675°C. Более того: при нагревании оксида натрия Na2O на воздухе образуется пероксид Na2O2.
Если в перекиси водорода Н-О-О-Н заместить один или оба атома водорода на органический радикал R, то мы получим органические гидроперекиси R-О-О-Н и перекиси R-О-О-R соответственно.
Органические гидроперекиси
Органические перекиси
Органические перекиси неустойчивы и легко разлагаются, иногда разложение происходит со взрывом. Например, перекись ацетона и перекись бензоила при нагревании взрываются.
Молекулы органических перекисей способны распадаться, образуя свободные радикалы. Некоторые перекиси используют в промышленности как инициаторы радикальной полимеризации (перекись бензоила, перекись метилэтилкетона).
Органические пероксопроизводные очень разнообразны, в частности, существуют перекиси, которые являются производными карбоновых кислот RC(O)OOH (пероксокислоты или надкислоты), сложных эфиров RC(O)OOR, альдегидов.
Пероксокислоты (надкислоты)
Пероксопроизводные сложных эфиров
Диперекись и триперекись ацетона
В большинстве случаев при осаждении из водных растворов образуется триперекись ацетона, однако, нельзя исключить, что она не содержит примеси диперекиси. Диперекись ацетона получить гораздо сложнее, чем триперекись: для этого необходимо проводить синтез в строго определенных условиях (методика получения диперекиси изложена в приложении ко второй части статьи, однако она дается в основном для ознакомления).
Есть также сообщение о получении тетраперекиси ацетона (ссылка), однако относиться к таким статьям следует с большой осторожностью: много подобных открытий было со временем опровергнуто.
Перекись ацетона представляет собой белое кристаллическое вещество. Практически нерастворима в воде, растворима в ацетоне, эфире. Температура плавления триперекиси 97 °C, диперекиси 132 °C. Даже при комнатной температуре перекись ацетона легко сублимируется.
С другой стороны, перекись ацетона окружена своеобразным ореолом таинственности, в результате находится немало молодых людей, которые хотят познакомиться с этим веществом поближе, не всегда осознавая опасности.
Что такое перекись ацетона
Ниже приведены рассказы химиков про случаи, связанные с перекисью ацетона. Независимо от правдоподобия историй, многие из них заставляют серьезно задуматься.
«Эту историю рассказал один из участников форума химик.ру. Подробностей точно не помню, но смысл примерно такой.
Когда химик спустился, он увидел, что пакет с перекисью ацетона упал в снег, это и уберегло его от взрыва.»
«Другой случай закончился не так удачно.
Молодой человек начитался «Поваренной книги анархиста» и получил несколько сот грамм перекиси ацетона. Потом он не нашел ничего лучшего, чем расплавить вещество и залить его в металлические корпуса из-под конденсаторов.
Один из корпусов взорвался, «несостоявшегося анархиста» убило на месте. Остальные корпуса с перекисью ацетона не сдетонировали.
На место трагедии приехали сотрудники милиции, которые собрали оставшиеся корпуса с перекисью ацетона в кулек, взяли распечатанные страницы из «Поваренной книги анархиста» и привезли все это в свою лабораторию.
В лаборатории оперативники просто выложили на стол корпуса с перекисью ацетона и сказали: «Проанализируйте, что это. Ах да: вот еще какие-то страницы, найденные у погибшего. «
Когда их химик это увидел, у него глаза на лоб полезли: «Ребята, очень осторожно возьмите корпуса с перекисью ацетона, отвезите их на полигон и уничтожьте как неразорвавшийся боеприпас». «
«Перекись ацетона? Брр.. ненавижу эту штуку. У моего друга 150 осколков с лица доставали 2 года назад, глаза хорошо хоть не задело. Чудо вообще, что я легко отделался: всего 2 крупных осколка в ноге (по 3-4 мм). Правда, этот «нехороший человек» сам виноват: он кинул банку с перекисью ацетона в забор. «
«Как я впервые увидел перекись ацетона.
На первом курсе одногруппник принес небольшую пробирку с белым порошком. Он отсыпал немного порошка на ладонь и поджег. Произошла моментальная желтая вспышка, ладонь осталась абсолютно целой. Одногруппник сказал, что это за вещество, но я не запомнил название. В голове осталась только структурная формула, которую он нарисовал. У меня довольно плохая зрительная память, но формула отложилась, потому что она была красивой:
Как видите, это диперекись ацетона. Почти наверняка в пробирке была не диперекись, а триперекись, но не стоит цепляться к деталям.
В статье уже упоминалось, как хлорацетон (лакриматор) действует на незадачливых экспериментаторов [ ]. Можете себе представить, что случилось, когда у меня в ванной «кипело» 3 литра реакционной смеси. «
«Странный случай произошел со мной, когда я был еще юным химиком. Случилось это в 1977 году.
Уже позже, учась в КХТИ, пытался выяснить, бывает ли напряженный фарфор. Оказалось очень даже бывает.
В заключении предлагаем вниманию читателей переписку с юным химиком, которая была частично опубликована в журнале Химия и Жизнь в далеком 1981 году.
Вызвал скорую, попал в больницу. В справке написали: «Множественные раны обеих рук, повреждение сухожилий-сгибателей, травматическая ампутация первой фаланги среднего пальца правой руки».
Кстати, нелишне бы писать в книгах по органической химии об опасности механических воздействий на органические перекиси. Ведь взрывчатая сила огромна, фарфоровая ступка превратилась в пыль, газовая плита из стального листа пробита фарфоровым осколком почти насквозь. Так что мне еще очень и очень повезло. Вы как-то писали в «Переписке» о перекиси ацетона, что она «весьма взрывчата»; не заменить ли «весьма» на «чрезвычайно»? Не завидую тому собирателю этого вещества, которому вы отвечали через журнал [ 1 ].
Надо предостеречь читателей и вот еще почему. Два года назад на олимпиадах о перекиси ацетона и слуха не было, а в прошлом году многие участники олимпиады знали упрощенный, но безотказный способ ее получения.
Зная ваше отношение к консультациям по поводу взрывчатых и вообще опасных веществ, обращаюсь все же к вам с просьбой ответить.
Олег В., гор. Грозный
____________________________________________
1 Имеется ввиду ответ на письмо читателя, опубликованный в двенадцатом номере Химии и Жизни за 1976 год:
«С. ГУДЗЕНКО, Ессентуки: Белый порошок, который вы получаете и по неведению копите,- это, по всей видимости, взрывчатая триперекись ацетона; пока не поздно, растворите ее осторожно в ацетоне и вылейте по частям в канализацию.»
________________________________________________
. К сожалению, перекись ацетона не впервые становится причиной несчастных случаев. Поэтому я предложу редакции напечатать (конечно, с вашего согласия) письмо, не указывая метода синтеза.
Консультант редакции кандидат химических наук
И. ЛЕЕНСОН
Уважаемый товарищ консультант,
большое спасибо за обстоятельный ответ. Я неплохо знаю правила работы с такого рода веществами, но, во-первых, о перекисях кетонов мало где подробно написано и, во-вторых, я азартен, работая, теряю представление о времени и о многом забываю. Надо исправляться; этот случай меня многому научил. Чрезмерная увлеченность, неосторожность, излишняя самоуверенность стали причиной несчастья. А ведь всего через пять дней надо было лететь на Всесоюзную олимпиаду во Фрунзе.
Нельзя ли передать привет через журнал юным химикам, с которыми я в этом году не смог увидеться? Надеюсь взять реванш на олимпиаде-82. Очень постараюсь. Олег В. «
_____________________________________________
Комментарий редакции ХиХ.
Как видите, недостаток информации о свойствах опасных веществ не приводят к добру.
К сожалению, некоммерческие сайты также иногда грешат неточной информацией, которая может стать причиной серьезных проблем. Например, в Википедии в статье «Перекись ацетона» (вариант на 1 марта 2010) было написано:
Для пластификации ТА используется водяная баня, притом исходное вещество может быть влажным и содержать примеси изначальных веществ (кислот и ацетона). При переходе в жидкое состояние оседает на дне, а после охлаждения и последующей кристаллизации, все жидкие вещества будут отделены от ТА. Таким образом решаются две задачи: промывка ТА и относительно безопасная кристаллизация. «
Во-вторых, в предыдущих разделах статьи уже было показано, что попытки плавить перекись ацетона могут иметь самые трагические последствия [ ]. Одна из таких печальных историй описана выше.
Слава богу, что упомянутая неточность в Википедии уже исправлена.
Общество мечется между двумя крайностями: раньше многие сведения просто скрывали, и за этим строго следила цензура. Теперь же информация доступна. Более того, она в избытке.
Однако достоверные сведения часто тонут в море некомпетентной информации. А результат один и тот же: несчастные случаи продолжаются.