Пероксид натрия
| Пероксид натрия | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | пероксид натрия |
| Химическая формула | Na2O2 |
| Физические свойства | |
| Состояние (ст. усл.) | желтоватый порошок |
| Отн. молек. масса | 78 а. е. м. |
| Молярная масса | 78 г/моль |
| Плотность | 2.8 г/см³ |
| Термические свойства | |
| Температура плавления | 675 °C |
| Энтальпия образования (ст. усл.) | -513 кДж/моль |
| Химические свойства | |
| Растворимость в воде | реагирует |
| Классификация | |
| Рег. номер CAS | [1313-60-6] |
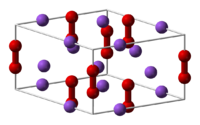
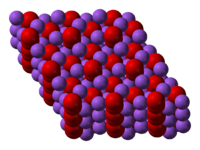
Пероксид натрия (перекись натрия), Na2O2 — желтовато-белые кристаллы с ионной кристаллической решеткой.
Содержание
Свойства
Энергично реагируют с водой со значительным выделением тепла:
Для пероксида натрия характерно образование хорошо кристаллизующихся гидратов и аддуктов с пероксидом водорода. Так, быстрой кристаллизацией пероксида натрия из ледяной воды легко осаждается гидрат Na2O2•8H2O.
Пероксид натрия является сильным оксилителем. С восстановителями, такими, как сера, порошок алюминия, эфиры реагирует с образованием пламени. С монооксидом углерода реагирует менее активно, образуя карбонат:
Окисление аммиака пероксидом натрия приводит к образованию нитрата натрия:
Получение
Пероксид натрия образуется при сгорании натрия в кислороде:
Применение
Применяют для отбеливания тканей, шерсти, шелка, древесной и вискозной массы, соломы. Для получения кислорода, поглощения угарного и углекислого газа используется в регенерационных установках и изолирующих противогазах:
Литература
Полезное
Смотреть что такое «Пероксид натрия» в других словарях:
Натрия пероксид — Пероксид натрия Общие Систематическое наименование Пероксид натрия Химическая формула … Википедия
Пероксид — (ранее перекись) вещество, содержащее пероксогруппу О О (например, пероксид водорода Н2О2, пероксид натрия Na2O2). Пероксид легко выделяет кислород. Для неорганических веществ рекомендуется использовать термин пероксид, для… … Википедия
Натрия фосфаты — Известны следующие фосфаты натрия: Дигидрофосфат натрия NaH2PO4 Гидрофосфат натрия Na2HPO4 Ортофосфат натрия Na3PO4 Применение Употребляются для буферных растворов различного назначения, как эмульгаторы в пищевой промышленности … Википедия
Пероксид водорода — Пероксид водорода … Википедия
Пероксид рения — Общие Систематическое наименование Пероксид рения Традиционные названия Перекись рения Химическая формула ReO4 Физические свойства Состояние ( … Википедия
натрия пероксид — natrio peroksidas statusas T sritis chemija formulė Na₂O₂ atitikmenys: angl. sodium peroxide rus. натрия перекись; натрия пероксид ryšiai: sinonimas – dinatrio dioksidas … Chemijos terminų aiškinamasis žodynas
натрия пероксид — Na2O2, бесцветные кристаллы (технический продукт слабо жёлтый). Сильный окислитель, при нагревании выше 300°C разлагается с выделением О2; содержание так называемого активного кислорода 20,5%. Применяют для отбеливания тканей, бумаги, для… … Энциклопедический словарь
НАТРИЯ СУПЕРОКСИД — (гипероксид натрия, надпероксид натрия) NaO2, желтые кристаллы; выше Ч 50 °С устойчива фаза I кубич. сингонии ( а =0,549 нм, z= 4, пространств. группа Рт3 т), в интервале от Ч50 до Ч 77 °С кубич. фаза II (а= 0,546 нм, пространств. группа… … Химическая энциклопедия
натрия перекись — natrio peroksidas statusas T sritis chemija formulė Na₂O₂ atitikmenys: angl. sodium peroxide rus. натрия перекись; натрия пероксид ryšiai: sinonimas – dinatrio dioksidas … Chemijos terminų aiškinamasis žodynas
Перекись натрия
Смотреть что такое «Перекись натрия» в других словарях:
натрия перекись — natrio peroksidas statusas T sritis chemija formulė Na₂O₂ atitikmenys: angl. sodium peroxide rus. натрия перекись; натрия пероксид ryšiai: sinonimas – dinatrio dioksidas … Chemijos terminų aiškinamasis žodynas
Натрия пероксид — Пероксид натрия Общие Систематическое наименование Пероксид натрия Химическая формула … Википедия
Натрия перекись — Na2O2, см. Перекись натрия … Большая советская энциклопедия
натрия пероксид — natrio peroksidas statusas T sritis chemija formulė Na₂O₂ atitikmenys: angl. sodium peroxide rus. натрия перекись; натрия пероксид ryšiai: sinonimas – dinatrio dioksidas … Chemijos terminų aiškinamasis žodynas
ПЕРЕКИСЬ ВОДОРОДА — (Hydrogenium hy peroxy datum, Hydrogenium peroxy datum), H202, сиропообразная жидкость, прозрачная, в тонких слоях бесцветная, в толстых голубого цвета, в 1х/2 раза тяжелее воды, металлического острого вкуса, растворяется в любых отношениях в… … Большая медицинская энциклопедия
Перекись водорода — I (техн.) находит в последнее время применение в довольно широких размерах для беления шелковых и шерстяных изделий, а также перьев. По сравнению с сернистой кислотой, которая издавна употребляется для этой цели, перекись водорода отбеливает… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Перекись водорода (хим.) — (Wasserstoffsuperoxyd; Peroxyde d hydrogène ou eau oxygéné e; Hidrogen peroxyde). Это вещество, H 2O2, открыто в 1818 г. Тенаром, который получил его при действии разведенной соляной кислоты на П. бария: ВаО 2 + 2HCl = BaCl2 + H2O2;… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Перекись водорода — Пероксид водорода Общие Систематическое наименование Пероксид водорода Химическая формула … Википедия
Перекись — Пероксид (ранее перекись) вещество, содержащее пероксогруппу О О (например, пероксид водорода Н2О2, пероксид натрия Na2O2). Пероксид легко выделяет кислород. Для неорганических веществ рекомендуется использовать термин пероксид, для… … Википедия
перекись — ПЕРЕКИСЬ, и, ж Спец. Соединение химического элемента с двумя атомами кислорода, связанными между собой, например, перекись водорода, натрия, марганца. Перекись водорода это бесцветная вязкая жидкость, легко разлагается на воду и кислород,… … Толковый словарь русских существительных
не растворим в основании
реагирует с этиловый спирт
Перекись натрия это неорганическое соединение с формулой Na2О2. Это желтоватое твердое вещество является продуктом воспламенения натрия в избытке кислорода. [3] Это прочная база. Этот перекись металла существует в нескольких гидраты и пероксигидраты, включая Na2О2· 2H2О2· 4H2На2О2· 2H2На2О2· 2H2О2, а Na2О2· 8H2О. [4] Октагидрат, который легко приготовить, имеет белый цвет в отличие от безводного материала. [5]
Содержание
Характеристики
Пероксид натрия кристаллизуется с гексагональной симметрией. [6] При нагревании гексагональный форма претерпевает переход в фазу неизвестной симметрии при 512 ° C. [7] При дальнейшем нагревании выше температуры кипения 657 ° C соединение разлагается до Na2O, отпуская O2. [8]
Подготовка
Октагидрат получают путем обработки гидроксида натрия перекисью водорода. [5]
Пероксид натрия можно получить в больших масштабах реакцией металлического натрия с кислородом при 130–200 ° C, в процессе, который приводит к оксид натрия, который в отдельной стадии поглощает кислород: [7] [9]
Его также можно получить путем пропускания газообразного озона над твердым йодид натрия внутри платина или же палладий трубка. Озон окисляет натрий с образованием пероксида натрия. В йод можно сублимировать мягким нагреванием. Платина или палладий катализируют реакцию и не подвергаются воздействию пероксида натрия.
Использует
Перекись натрия гидролизует давать едкий натр и пероксид водорода согласно реакции [9]
Перекись натрия использовалась для отбеливания древесной массы при производстве бумаги и текстиля. В настоящее время он в основном используется для специализированных лабораторных операций, например, для добычи полезных ископаемых из различных руд. Перекись натрия может продаваться под торговыми названиями Solozone [7] и Flocool. [8] В химических препаратах в качестве окислителя используется перекись натрия. Он также используется в качестве источника кислорода, реагируя с углекислым газом с образованием кислорода и карбоната натрия:
Таким образом, он особенно полезен для акваланга, подводных лодок и т. Д. Перекись лития имеет аналогичное использование.
не растворим в основании
реагирует с этиловый спирт
Перекись натрия это неорганическое соединение с формулой Na2О2. Это желтоватое твердое вещество является продуктом воспламенения натрия в избытке кислорода. [3] Это прочная база. Этот перекись металла существует в нескольких гидраты и пероксигидраты, включая Na2О2· 2H2О2· 4H2На2О2· 2H2На2О2· 2H2О2, а Na2О2· 8H2О. [4] Октагидрат, который легко приготовить, имеет белый цвет в отличие от безводного материала. [5]
Содержание
Характеристики
Пероксид натрия кристаллизуется с гексагональной симметрией. [6] При нагревании гексагональный форма претерпевает переход в фазу неизвестной симметрии при 512 ° C. [7] При дальнейшем нагревании выше температуры кипения 657 ° C соединение разлагается до Na2O, отпуская O2. [8]
Подготовка
Октагидрат получают путем обработки гидроксида натрия перекисью водорода. [5]
Пероксид натрия можно получить в больших масштабах реакцией металлического натрия с кислородом при 130–200 ° C, в процессе, который приводит к оксид натрия, который в отдельной стадии поглощает кислород: [7] [9]
Его также можно получить путем пропускания газообразного озона над твердым йодид натрия внутри платина или же палладий трубка. Озон окисляет натрий с образованием пероксида натрия. В йод можно сублимировать мягким нагреванием. Платина или палладий катализируют реакцию и не подвергаются воздействию пероксида натрия.
Использует
Перекись натрия гидролизует давать едкий натр и пероксид водорода согласно реакции [9]
Перекись натрия использовалась для отбеливания древесной массы при производстве бумаги и текстиля. В настоящее время он в основном используется для специализированных лабораторных операций, например, для добычи полезных ископаемых из различных руд. Перекись натрия может продаваться под торговыми названиями Solozone [7] и Flocool. [8] В химических препаратах в качестве окислителя используется перекись натрия. Он также используется в качестве источника кислорода, реагируя с углекислым газом с образованием кислорода и карбоната натрия:
Таким образом, он особенно полезен для акваланга, подводных лодок и т. Д. Перекись лития имеет аналогичное использование.
Пероксид водорода
Из Википедии — свободной энциклопедии

наименование
(при 20 °C)

Перокси́д водоро́да (пе́рекись водоро́да), H2O2 — простейший представитель пероксидов. Бесцветная тяжёлая полярная жидкость с «металлическим» вкусом, неограниченно растворимая в воде, спирте и эфире. Концентрированные водные растворы взрывоопасны. Пероксид водорода является хорошим растворителем. Из воды выделяется в виде неустойчивого кристаллогидрата H2O2∙2H2O.
Молекула пероксида водорода имеет следующее строение:
Вследствие несимметричности молекула H2O2 сильно полярна (μ = 0,7⋅10 −29 Кл·м). Относительно высокая вязкость жидкого пероксида водорода обусловлена развитой системой водородных связей. Поскольку атомы кислорода имеют неподелённые электронные пары, молекула H2O2 также способна образовывать донорно-акцепторные связи.











