Перекись водорода : инструкция по применению
Описание
Бесцветная прозрачная жидкость.
Состав
Флакон 40 мл содержит:
действующее вещество: перекись водорода – 1,2 г;
вспомогательные вещества: натрия бензоат, вода очищенная.
Флакон 100 мл содержит:
действующее вещество: перекись водорода – 3 г;
вспомогательные вещества: натрия бензоат, вода очищенная.
Флакон 200 мл содержит:
действующее вещество: перекись водорода – 6 г;
вспомогательные вещества: натрия бензоат, вода очищенная.
Флакон 400 мл содержит:
действующее вещество: перекись водорода – 12 г;
вспомогательные вещества: натрия бензоат, вода очищенная.
Фармакотерапевтическая группа
Прочие антисептические и дезинфицирующие средства.
Фармакологическое действие
Антисептическое средство из группы оксидантов. При контакте перекиси водорода с поврежденной кожей или слизистыми оболочками высвобождается активный кислород, который обладает противомикробным, дезодорирующим, депигментирующим свойством, при этом происходит механическое очищение и инактивация органических веществ (протеины, кровь, гной). Антисептическое действие не является стерилизующим, при его применении происходит лишь временное уменьшение количества микроорганизмов. Обильное пенообразование способствует тромбообразованию и остановке кровотечений из мелких сосудов.
Показания к применению
Дезинфектант для обработки небольших порезов, ран (в том числе гнойных), изъязвлений кожи, ожогов.
Для остановки незначительных кровотечений (поверхностных, носовых).
Для полоскания полости рта и горла (при стоматите, ангине).
При гинекологических заболеваниях с целью дезинфекции.
Способ применения и дозы
Для наружного применения используют раствор 30 мг/мл; для полоскания полости рта и горла, нанесения на слизистые оболочки – раствор 2,5 мг/мл (раствор 30 мг/мл разводят водой в соотношении 1:11). Неразбавленный раствор не применяют для обработки слизистых оболочек. Поврежденные участки кожи или слизистой оболочки обрабатывают ватным или марлевым тампоном, смоченным раствором лекарственного средства. Тампоны следует держать пинцетом. Возможно струйное орошение раневой поверхности.
Побочное действие
При обработке раны возможно возникновение чувства жжения.
При длительном применении для полосканий возможна гипертрофия сосочков языка, потеря чувствительности.
Возможно проявление местных аллергических реакций при индивидуальной непереносимости лекарственного средства.
В случае возникновения побочных реакций, в т.ч. не указанных в данной инструкции, необходимо обратиться к врачу.
Противопоказания
Повышенная чувствительность к компонентам лекарственного средства.
Не используется в закрытых полостях тела и хирургических ранах из-за опасности газовой эмболии, как следствия поступления свободного кислорода в циркуляцию.
Не используется для дезинфекции хирургических инструментов (частей эндоскопов) и клизм.
Передозировка
Случайное попадание внутрь может стать причиной болезненности в глотке, желудочных сокращений и рвоты. Внезапное поступление свободного кислорода в желудочно-кишечный тракт может вызвать острое раздувание желудка и внутреннее кровотечение. Разрешается пить воду. Поступление больших объемов перекиси может привести к газовой эмболии, являющейся следствием высвобождения кислорода в желудок.
Меры предосторожности
Только для наружного применения. Не рекомендуется использовать лекарственное средство под окклюзионные повязки. Следует избегать попадания в глаза. Не применять для орошения закрытых полостей и проникающих ран во избежание высвобождения свободного кислорода в циркуляцию и возникновения газовой эмболии.
Не стабилен в щелочной среде, в присутствии щелочей металлов, сложных радикалов некоторых оксидантов, а также на свету и в тепле. Осветляет ткань.
Обработка раны раствором перекиси водорода не гарантирует защиту от заражения столбняком и др. раневой инфекцией.
Применение в педиатрической практике.
Для полоскания полости рта и горла применяется у детей с 12 лет. Применение у детей младшего возраста допускается только по показаниям врача.
Применение в гериатрической практике.
Нет достоверных данных.
Применение у лиц с нарушением функции печени и почек.
Нет достоверных данных.
Применение во время беременности и в период лактации
Нет достоверных данных. Перед применением лекарственного средства во время беременности и в период лактации необходимо проконсультироваться с врачом.
Перекись водорода: помощь или вред?
Перекись водорода была впервые получена химиком Луисом Тенеро в 1818 году и уже очень скоро стала применяться в промышленности. Сейчас ее повсеместно используют в хозяйстве и быту.
1 Что такое перекись водорода: химическая формула и свойства
Перекись водорода это простейший представитель пероксидов. Он представляет собой прозрачную жидкость со своеобразным металлическим вкусом и слабым запахом, способную неограниченно растворяться в спирте, воде и эфире.
Химическая формула

Химические свойства
При взаимодействии с определенными металлами, такими например, как Mn или Fe, происходит активная химическая реакция
Распад вещества быстрее происходит в щелочной среде, кислотная же среда наоборот замедляют процесс. Именно поэтому в раствор часто добавляют фосфорную кислоту. В термических условиях H2O2 быстро разлагается, поэтому не рекомендуется хранить его на свету.
Пероксид водорода хорошо смешивается с C2H5OH (спиртом) и H2O (водой) в любых пропорциях.
Реакция распада перокисда водорода
Кислотная среда более подходящаая среда для распада. Щелочная же более подходит для восстановления
Пример реакции восстановления мы можем наблюдать при взаимодействии H2O2 с серебром
Аналогично, по существу, протекает его взаимодействие с озоном (О3 + Н2О2 = 2 Н2О + 2 О2) и с перманганатом калия в кислой среде:
Последняя реакция применяется для количественного определения пероксида водорода.
2 Основные лечебные свойства
3 Способы применения
Уже многие годы перекись водорода используется в различных областях применения благодаря своей эффективности и доступности. Его применение основывается в первую очередь на его окисляющих свойствах.
В традиционной медицине
В косметологии
Препарат используется на коже, склонной к излишней жирности и появлению акне, черных точек, благодаря способности уничтожать возбудителей инфекции. Для этого 5 капель 3% раствора добавляют к 50 мл тоника. Косметологи советуют его наносить не более 2 раз в неделю.
Людям с веснушками и пигментными пятнами вещество также подойдет за счет его отбеливающего свойства. Чтобы провести процедуру, применяют специальные маски. Взять ст. л. 20% творога, сырой желток и 5 капель перекиси. Все ингредиенты перемешиваются до однородной структуры, а затем кисточкой наносятся на кожный покров. Слегка массируют, оставляя маску на 15 мин. По истечении времени масса смывается, а на лицо накладывают увлажняющий крем.
Применение в быту
Благодаря полезным свойствам Н2О2 можно не только устранить желтые пятна, разводы с белой материи и удалить налет на кафельной плитке, но и избавиться от грибка и плесени.
Чтобы почистить плитку в ванной комнате, взять 40 мл пероксида, ч. л. жидкого мыла и полстакана пищевой соды. Компоненты хорошо перемешать и нанести на влажную губку, которой оттереть проблемные участки. Если загрязнений много, нужно оставить массу на 10 минут, чтобы они растворились.
Для очистки материала берут 3% раствор, который вливают на пятна. Оставляют на 20-30 минут, а затем смывают с поверхности.
Перекись водорода в народной медицине
4 Польза или вред?
Если человек хорошо переносит пероксид и правильно им пользуется, он не должен вызвать каких-либо неблагоприятных последствий.
Нельзя употреблять вещество внутрь, это опасно появлением отравления. При полоскании рта иногда теряется чувствительность языка и могут гипертрофироваться его сосочки.
Также не стоит использовать при наличии у человека индивидуальной непереносимости. Это может повлечь за собой развитие аллергической реакции.
5 Форма выпуска и возможные противопоказания препарата
Изготавливается в виде 3% раствора для наружного местного нанесения.
6 Метод Неумывакина: что это?
Это лечение с успехом применяется в нетрадиционной медицине. Профессор Неумывакин считал перекись панецеей от всех заболеваний. Принцип действия он объяснял укрепляющим эффектом лекарства: при взаимодействии с кровью и ферментом каталазой оно распадается до воды и кислорода, который разжижает кровь, нормализует обменные процессы и улучшает деятельность органов и систем.
Если ожидаемый эффект не достигался, профессор считал, что организм чрезмерно зашлакован. Поэтому он рекомендовал проводить полную очистку.
Метод не признан официальной медициной, так как его противники утверждают, что перекись не только неэффективна, но и может причинить опасность при использовании не по назначению.
В нашей следующей статье мы поговорим об особенностях применения каустической соды.
Пероксид водорода
| Пероксид водорода | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Пероксид водорода |
| Химическая формула | H2O2 |
| Физические свойства | |
| Состояние (ст. усл.) | жидкость |
| Отн. молек. масса | 34,01 а. е. м. |
| Молярная масса | 34,01 г/моль |
| Плотность | 1.4 г/см³ |
| Термические свойства | |
| Температура плавления | −0,432 °C |
| Температура кипения | 150,2 °C |
| Энтальпия образования (ст. усл.) | -136.11 кДж/моль |
| Химические свойства | |
| pKa | 11.65 |
| Растворимость в воде | неограниченная |
| Классификация | |
| Рег. номер CAS | 7722-84-1 |
| SMILES | OO |
| Регистрационный номер EC | 231-765-0 |
Перокси́д водоро́да (перекись водорода), H2O2 — простейший представитель пероксидов. Бесцветная жидкость с «металлическим» вкусом, неограниченно растворимая в воде, спирте и эфире. Концентрированные водные растворы взрывоопасны. Пероксид водорода является хорошим растворителем. Из воды выделяется в виде неустойчивого кристаллогидрата H2O2•2H2O.
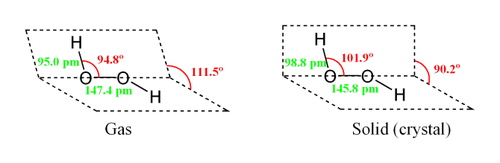
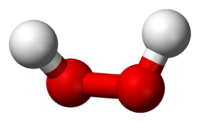
Молекула пероксида водорода имеет следующее строение:
Вследствие несимметричности молекула H2O2 сильно полярна (μ = 0,7·10 −29 Кл·м). Относительно высокая вязкость жидкого пероксида водорода обусловлена развитой системой водородных связей. Поскольку атомы кислорода имеют неподелённые электронные пары, молекула H2O2 также способна образовывать донорно-акцепторные связи.
Содержание
Химические свойства
Оба атома кислорода находятся в промежуточной степени окисления −1, что и обуславливает способность пероксидов выступать как в роли окислителей, так и восстановителей. Наиболее характерны для них окислительные свойства:

При взаимодействии с сильными окислителями пероксид водорода выступает в роли восстановителя, окисляясь до кислорода:
Молекула пероксида водорода сильно полярна, что приводит к возникновению водородных связей между молекулами. Связь O—O непрочна, поэтому H2O2 — неустойчивое соединение, легко разлагается. Так же этому может поспособствовать присутствие ионов переходных металлов. В разбавленных растворах пероксид водорода тоже не устойчив и самопроизвольно диспропорционирует на H2O и O2.Реакция диспропорционирования катализируется ионами переходных металлов, некоторыми белками:
Однако очень чистый пероксид водорода устойчив.
Пероксид водорода проявляет слабые кислотные свойства (К = 1,4·10 −12 ), и поэтому диссоциирует по двум ступеням:
При действии концентрированного раствора Н2O2 на некоторые гидроксиды в ряде случаев можно выделить пероксиды металлов, которые можно рассматривать как соли пероксида водорода (Li2O2, MgO2 и др.):

Пероксид водорода может проявлять как окислительные, так и восстановительные свойства. Например, при взаимодействии с оксидом серебра он является восстановителем:
В реакции с нитритом калия соединение служит окислителем:
Пероксидная группа [—O—O—] входит в состав многих веществ. Такие вещества называют пероксидами, или пероксидными соединениями. К ним относятся пероксиды металлов (Na2O2, BaO2 и др.). Кислоты, содержащие пероксидную группу, называют пероксокислотами, например, пероксомонофосфорная H3PO5 и пероксидисерная H2S2O8 кислоты.
Окислительно-восстановительные свойства
Пероксид водорода обладает окислительными, а также восстановительными свойствами. Он окисляет нитриты в нитраты, выделяет иод из иодидов металлов, расщепляет ненасыщенные соединения по месту двойных связей. Пероксид водорода восстанавливает соли золота и серебра, а также кислород при реакции с водным раствором перманганата калия в кислой среде.
При восстановлении Н2O2 образуется Н2O или ОН-, например:
При действии сильных окислителей H2O2 проявляет восстановительные свойства, выделяя свободный кислород:
Реакцию KMnO4 с Н2O2 используют в химическом анализе для определения содержания Н2O2:
Окисление органических соединений пероксидом водорода (например, сульфидов и тиолов) целесообразно проводить в среде уксусной кислоты.
Биологические свойства
Перекись водорода относится к реактивным формам кислорода и при повышенном образовании в клетке вызывает оксидативный стресс. Некоторые ферменты, например глюкозоксидаза, образуют в ходе окислительно-восстановительной реакции пероксид водорода, который может играть защитную роль в качестве бактерицидного агента. В клетках млекопитающих нет ферментов, которые бы восстанавливали кислород до перекиси водорода. Однако, несколько ферментных систем (ксантиноксидаза, НАД(Ф)H-оксидаза, циклоксигеназа и др.) продуцируют супероксид, который спонтанно или под действием супероксиддисмутазы превращается в перекись водорода.
Получение
Пероксид водорода получают в промышленности при реакции с участием органических веществ, в частности, каталитическим окислением изопропилового спирта:
Ценным побочным продуктом этой реакции является ацетон.
В промышленных масштабах пероксид водорода получают электролизом серной кислоты, в ходе которого образуется надсерная кислота, и последующим разложением последней до пероксида и серной кислоты.
В лабораторных условиях для получения пероксида водорода используют реакцию:
Концентрирование и очистку пероксида водорода проводят осторожной перегонкой.
Применение
Благодаря своим сильным окислительным свойствам пероксид водорода нашёл широкое применение в быту и в промышленности, где используется, например, как отбеливатель на текстильном производстве и при изготовлении бумаги. Применяется как ракетное топливо — в качестве окислителя или как однокомпонентное (с разложением на катализаторе). Используется в аналитической химии, в качестве пенообразователя при производстве пористых материалов, в производстве дезинфицирующих и отбеливающих средств. В промышленности пероксид водорода также находит свое применение в качестве катализатора, гидрирующего агента, как эпоксидирующий агент при эпоксидировании олефинов.
Хотя разбавленные растворы перекиси водорода применяется для небольших поверхностных ран, исследования показали что этот метод обеспечивая антисептический эффект и очищение и удлиняет время заживления. [1] [2] Обладая хорошими очищающими свойствами, перекись водорода на самом деле не ускоряет заживление ран. Достаточно высокие концентрации, обеспечивающие антисептический эффект, могут также удлинять время заживления из-за повреждения прилегающих к ране клеток. [3] Более того, перекись водорода может мешать заживлению и способствовать образованию рубцов из-за разрушения новообразующихся клеток кожи. [4] Однако, в качестве средства для очистки глубоких ран сложного профиля, гнойных затеков, флегмон, и других гнойных ран санация которых затруднена, перикись водорода остается препаратом выбора. Так как она обладает не только антисептическим эффектом, но и продуцирует большое количество пены, при взаимодействии с ферментом пероксидазой. Что в свою очередь позволяет размягчить и отделить от тканей некротизированные участки, сгустки крови, гноя, которые буду легко смыты последующим введением в полость раны антисептического раствора. Без предварительной обработки перекисью водорода, антисептический раствор не сможет удалить данные патологические образования, что приведет значительному увеличению времени заживления раны, и ухудшит состояние больного.
В пищевой промышленности растворы пероксида водорода применяются для дезинфекции технологических поверхностей оборудования, непосредственно соприкасающихся с продукцией. Кроме того, на предприятиях по производству молочной продукции, соков, растворы перекиси водорода используются для дезинфекции упаковки (технология «Тетра Пак»). Для технических целей пероксид водорода применяют в производстве электронной техники.
В быту применяется также для выведения пятен MnO2, получившихся при взаимодействии перманганата калия «марганцовки» с предметами (ввиду его окислительных свойств).
Пероксид водорода в аквариумистике
3%-ный раствор пероксида водорода используется в аквариумистике для оживления задохнувшейся рыбы, а также для очистки аквариумов и борьбы с нежелательной флорой и фауной в аквариуме (гидры, планарии, паразиты, водоросли, бактерии и др.)
Формы выпуска
Выпускается в виде водных растворов, стандартная концентрация 1-6 %, 30, 38, 50, 60, 85, 90 и 98 %. 30 % водный раствор пероксида водорода, стабилизированный добавлением фосфатов натрия, называется пергидролем.
Опасность применения
Несмотря на то, что пероксид водорода не токсичен, его концентрированные растворы при попадании на кожу, слизистые оболочки и в дыхательные пути вызывают ожоги. В больших концентрациях недостаточно чистый пероксид водорода может быть взрывоопасен. Опасен при приёме внутрь концентрированных растворов. Вызывает выраженные деструктивные изменения, сходные с действиями щелочей. Летальная доза 30%-го раствора пероксида водорода (пергидроля) — 50—100 мл. [7]
Купить перекись водорода. Продажа пергидроль 37%. Высший сорт. Цена, свойства, применение, транспортировка.
Внимание! При использовании концентрированных растворов перекиси водорода соблюдать осторожность. Избегать попадания на кожу и в глаза. Использовать резиновые перчатки, защитные очки. Перекись водорода 37% не надо покупать на авито или на юле, все гораздо ближе, чем вы думаете, поиск закончен, Вы нашли её. Купить перекись водорода в Нижнем Новгороде можно в компании ХимЭксперт. Характеристика вещества Водорода пероксид. Прозрачная бесцветная жидкость без запаха или со слабым своеобразным запахом, слабокислой реакции; быстро разлагается под действием света, при нагревании или соприкосновении со щелочью, окисляющими или восстанавливающими веществами, с выделением кислорода.
Технические условия перекись водорода
Применение перекиси водорода в отраслях
Перекисью водорода можно
Применение перекиси водорода в медицине
Перекись водорода в медицине. Данный химикат широко используется при медикаментозном лечении различных заболеваний. Чаще для этих целей применяют 3%-ный раствор вещества, механизм действия которого кратко можно описать следующим образом. При непосредственном соприкосновении химиката с повреждённой эпителиальной тканью человеческого организма, вещество распадается с обильным выделением кислорода. При этом создаются негативные условия для развития микроорганизмов (особенно анаэробного и гнилостного характера). Это сопровождается образованием пены и удалением из поражённого участка посторонних тел и загрязняющих элементов. Польза перекиси водорода в этом случае заключается в том, что помимо непосредственной нейтрализации возможных источников заражения раны, образовывающийся слой пены создаёт защитную прослойку, останавливающую кровотечение из повреждённых сосудов. Кроме этого, перекись водорода может использоваться в качестве эффективного антидота при отравлении калия перманганатом. В этом случае 3%-ный раствор вещества комбинируют с 3%-ным раствором уксусной кислоты.
Применение перекиси водорода для бассейнов и водоемов
Перекись водорода для бассейна (очистка бассейна перекисью) Одним из наиболее распространённых направлений использования этого химиката является санитарная обработка бассейнов и прочих резервуаров для воды большого объёма. При добавлении пероксида водорода в воду для бассейнов частного или промышленного пользования быстро и эффективно подавляется развитие патогенной микрофлоры, характерной для водоёмов замкнутого типа, вода не темнеет под прямыми солнечными лучами, не наблюдается рост количества водорослей и прочих видов растительности на стенках и на дне резервуара. Применяются для этих целей водные растворы вещества в различной концентрации. Сколько перекиси лить в бассейн Если для обработки воды вы используете 35%-ный раствор, то рекомендованная доза 0,75 л химиката на 1 м³ воды. При этом рекомендуют обработку производить при температуре воды в бассейне не выше 28 ºC, с показателями рН в пределах 7,2 – 7,4. Периодичность проведения обработки зависит от частоты использования, количества купающихся и прочих показателей. Средний показатель периодичности рекомендуется в пределах 30 – 40 дней. В тех же случаях, если для этих целей используется раствор с 50%-ной концентрацией вещества, то дозировку рекомендуют на уровне 0,5 л из расчёта на тот же объём воды. А рекомендации по периодичности обработки можно применить указанные выше.
Применение перекиси водорода в растениеводстве
Удобрение перекисью водорода. Применение данного химиката с такой целью основано на нестабильности вещества. Как уже было сказано выше, атомы кислорода имеют ковалентную связь, вследствие чего в случае распада выделяется вода и свободный кислород, необходимый для дыхания растениям. Подкормка перекисью водорода помогает обильно снабжать кислородом корневую систему культуры. При этом структура вещества не содержит никаких хлорсодержащих компонентов, тяжёлых металлов и прочих вредных веществ. Кроме этого, известно, что этот химикат губителен для различной патогенной микрофлоры, следовательно, обработка пероксидом водорода стеблей и листьев растений способна помочь избавиться от вредоносных микроорганизмов и некоторых насекомых вредителей. В частности, таких как мучнистые червецы, паутинные клещи, тля, щитовики, трипсы и прочие. Практикуется и обработка семян посредством протравочного состава, одним из компонентов которого может быть пероксид водорода. Перекись водорода для цветов и комнатных растений Простота применения, доступность и неизменно качественные результаты использования послужили большой популярности этого средства для обработки различных декоративных культур. Все преимущества подпитки перекисью водорода могут быть применены в отношении домашних растений и цветов в горшках или небольших палисадниках на придомовой территории. Перекись водорода для цветов и растений. Пропорции и способы применения Возможно использование данного химиката в качестве питательной добавки к поливной воде. В этом случае 20 миллилитров 3%- ной перекиси водорода добавляют из расчёта на 1 литр поливной воды и используют для обычного полива. В том случае, если есть потребность в борьбе с вредителями домашних растений, то приготавливается смесь, состоящая из: 1 литра воды, 30 капель медицинского спиртового раствора йода и 45 мл пероксида водорода. Данным средством следует тщательно опрыскать листья, ветки и стволы растений. А, если есть потребность протравить семена, то посадочный материал нужно в течение 4 часов выдержать в смеси следующего состава: на 1 литр воды 40 мл 3%-ной перекиси водорода. Такие семена менее чувствительны к большинству заболеваний и проявляют более высокий уровень всхожести.
Применение перекиси водорода в быту
Кроме традиционного применения в медицинских целях и при выращивании домашних растений существует ещё несколько распространённых направлений использования этого химиката. Пероксид водорода может быть эффективным моющим и чистящим средством для целого ряда полезных бытовых приспособлений. Во многих случаях ещё и с антисептическим эффектом. В перекиси водорода можно вымачивать разделочные доски для кухни, зубные щётки, губки и мочалки для мытья посуды. Обработка этим химикатом овощей и фруктов является не только превосходной санитарной обработкой этих продуктов питания, но и способствует их более длительному хранению без признаков порчи. А также выводят плесень в труднодоступных местах, очищают нагар на кастрюлях и сковородах, чистят керамическую плитку и используют в качестве отбеливающего средства при стирке. Выведение пятен перекисью водорода В предыдущей части статьи было сказано, что данный химикат может использоваться в текстильном производстве для обработки тканей. Также это химическое вещество может использоваться в быту в качестве пятновыводителя высокой эффективности. С его помощью удаляются пятна крови, чернил, жира, чая, вина, кофе и прочих загрязнителей. Рекомендуется обработать удаляемое пятно с помощью небольшого количества перекиси водорода, потерев его смоченной салфеткой или слегка обрызгав химикатом. Далее дать «отбеливателю» поработать, а потом отправить отбеленную одежду в обычную стирку. Эффект будет особенно хорош в случае, если обрабатываемая одежда белого цвета. Продажа технической перекиси водорода оптом с розливом в канистры, бочки, еврокубы и автоналивом. Пероксид водорода – неустойчивый кристаллогидрат H2O2+2H2O, бесцветная жидкость. В неограниченном количестве растворяется в воде, эфире, спирте. В концентрированном виде взрывоопасен, образует ожоги.Перекись водорода медицинская PEROXID 37% 1л/1.3кг, 1 кг = 48 руб.Перекись водорода медицинская выпускается согласно ГОСТ 177-88 Дезинфицирующее средство «Перекись водорода медицинская»выпускается согласно ТУ 2123-001-25665344-2008 Перекись водорода медицинская ГОСТ 177-88 используется в медицинской и фармацевтической промышленности, как асептическое, кровоостанавливающее вещество. ТУ 2123-001-25665344-2008 как дезинфицирующая жидкость для изделий медицинского и стоматологического назначения.Купить перекись водорода медицинскую можно в канистрах 1л/1.3кг. 10л/12кг. 20л/24кг. 30л/34кг.
Перекись водорода: условия хранения и срок годности. Срок хранения перекиси водорода
Стабилизация как способ продления срока годности С другой стороны, для продления срока годности перекиси, в неё сразу после изготовления добавляют стабилизаторы, которые никак не влияют на потребительские свойства вещества, но значительно замедляют процессы распада. В качестве стабилизаторов обычно используются салициловая кислота, пирофосфорнокислый натрий или однозамещённый фосфорнокислый натрий, концентрации которых в растворе перекиси водорода составляют 0,5-0,6%. Что о сроках хранения говорит ГОСТ 177-88? Пероксид водорода 3% и 6% продаётся в аптеках, в небольших пузырьках или бутылочках, и обычно используется в качестве местного дезинфицирующего средства. Свойства вещества в этом случае сохраняются от года до трех лет (это указано на этикетке), если ёмкость не открывалась. После вскрытия пергидроль будет эффективна в течение 30-45 дней. Гарантийный срок хранения раствора перекиси водорода концентрацией от 30% до 40% ГОСТу — 6 месяцев от даты изготовления, а рабочих растворов — всего 1 сутки. Но это не означает, что ровно через 180 дней пергидроль превратиться в обычную воду. Шесть месяцев – это срок, в течение которого, при условии правильного хранения, производитель гарантирует минимальное изменение всех заявленных параметров. А что дальше, после окончания гарантийного срока хранения? Перекись водорода будет медленно (в течение нескольких лет) разлагаться на воду и кислород, концентрация раствора будет постепенно снижаться.
По опыту наших клиентов, у некоторых из них пероксид работал «как надо» и через три года хранения в тёмном помещении. Правила хранения перекиси водорода Ёмкости более 200 мл, в которых хранится пергидроль, должны быть снабжены специальными пробками, обеспечивающими выход образующегося газа. Помещение для хранения должно быть тёмным, также желательно использовать посуду из тёмного стекла или непрозрачного пластика. Температура хранения не должна превышать +25 градусов Цельсия, а в идеале – быть не выше нескольких градусов тепла. Если вам нужна только часть перекиси или нужно смочить тряпку или вату – аккуратно отлейте необходимый объём в другую чистую ёмкость. Любые загрязнения и посторонние вещества, попавшие в пергидроль (в том числе и с чистой на вид ватки), заметно снижают срок её хранения.
Особенности хранения перекиси водорода
Для пероксида водорода, а тем более пергидроля, имеет немаловажное значение, в какой емкости он хранится. Наиболее подходящий вариант хранения – в оригинальных емкостях из затемненного стекла или непрозрачных пластиковых бутылях. Главный фактор влияния на хранение – свойство вещества легко разлагаться на воду и газообразный кислород. В связи с этим емкость вместимостью свыше 200 мл не подлежит герметичной закупорке. Не рекомендуется вскрывать пероксид заблаговременно и без особой надобности, а также переливать из оригинальной емкости, тем более в прозрачную тару. Перекись водорода: срок годности после вскрытия флакона, условия хранения, показания к применению Среди самых доступных лекарств выделяется пероксид водорода, который является универсальным медикаментом для лечения разных недугов и отличается многофункциональностью, простотой и низкой ценой. Что такое перекись водорода? Химический состав перекиси содержит по 2 атома кислорода и водорода. В продажу она поставляется в форме водного раствора с концентрациями активного элемента 3 или 5 %. С виду это бесцветная жидкость, не имеющая запаха. Отличается перекись неустойчивой формулой, при свете разлагается с высвобождением кислорода. Иными концентрированными формами выступают гидроперит в виде таблеток и пергидроль – применяется как осветлитель для волос или для дезинфекции помещений. Показания к применению перекиси водорода будут описаны ниже. Лечебные свойства Положительные свойства перекиси водорода для людей весьма широки, потому что этот медикамент универсален и используется во многих целях. Уровень активности до 0,3 % воздействует бактериостатически, а до 3 % – как бактерицидное вещество.Такая же концентрация оказывает дезодорирующий эффект, а если воздействовать на кожный покров чистым концентратом, можно получить раздражение, ожоги и депигментацию.
Дозировка перекиси водорода при доливке в бассеин
Перекись водорода является идеальным средством для очистки, дезинфекции и профилактики воды в бассейне. Эффективность и простота в применении, доступная цена, экологичность для окружающей среды и безопасность купающихся людей, вот причины по которым перекись водорода набирает популярность из года в год. В применении хорошо известные средства для очистки бассейнов, такие как хлор и бром, наносят не поправимый урон коже, слизистой глаз и дыхательных путей, волосам, а так же возникает не простой вопрос с утилизацией воды, после сезона купания. Перекись водорода создает комфортную и безопасную среду в вашем бассейне, а вода становится чистой и сверкающей.
Применение, рекомендованная дозировка перекиси водорода для бассеина
Дозировка для зеленой, застоявшейся воды с образовавшимися водорослями: пергидроль 37% 1200-1400 мл на 1000 литров воды (1 м³); пергидроль 60% 700-900 мл на 1000 литров воды (1 м³);