Состав и структура белков
Вопрос 1. Какие вещества называются белками или протеинами?
Белки (протеины) — это гетерополимеры, состоящие из 20 различных мономеров — природных альфа-аминокислот. Белки — нерегулярные полимеры.
Общее строение аминокислоты может быть представлено следующим образом:
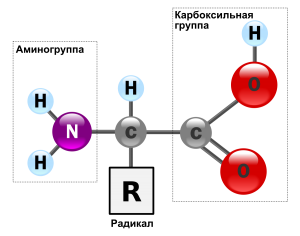
R—С(NH2)—СООН. Все аминокислоты имеют аминогруппу (—МН2) и карбоксильную группу (—СООН) и различаются строением и свойствами радикалов. Аминокислоты в белке связаны пептидной
связью —N(Н)—С(=О), поэтому белки ещё называют пептидами.
Вопрос 2. Что такое первичная структура белка?
В молекуле белка аминокислоты связаны друг с другом пептидной связью между атомами углерода и азота. В строении молекулы белка различают первичную структуру — последовательность аминокислотных остатков.
Вопрос 3. Как образуются вторичная, третичная и четвертичная структуры белка?
Вторичная структура белка — как правило, это спиральная структура (альфа-спираль), которая удерживается множеством водородных связей, возникающих между находящимся близко друг от друга С=О и NН-группами. Другой тип вторичной структуры — это бета-слой, или складчатый слой; это две параллельные полипептидные цепи, связанные водородными связями, перпендикулярными цепям.
Третичная структура белковой молекулы — это пространственная конфигурация, напоминающая компактную глобулу. Она поддерживается ионными, водородными и дисульфидными (S=S) связями, а также гидрофобными взаимодействиями.
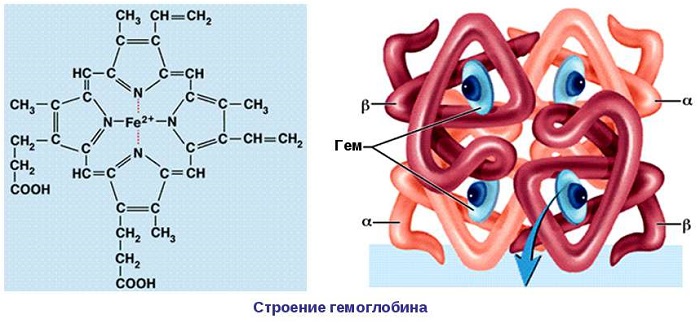
Четвертичная структура белка образуется при взаимодействии нескольких глобул, которые объединяются в комплекс (например, молекула гемоглобина состоит из четырех таких субъединиц).
Вопрос 4. Что такое денатурация белка?
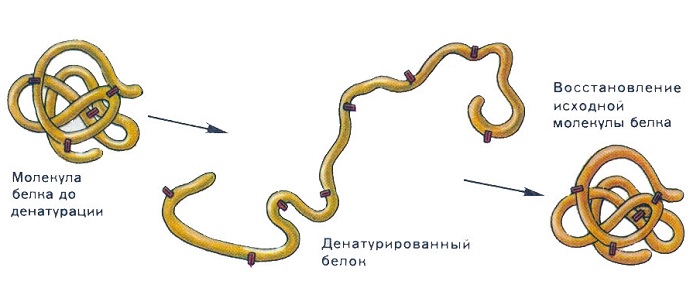
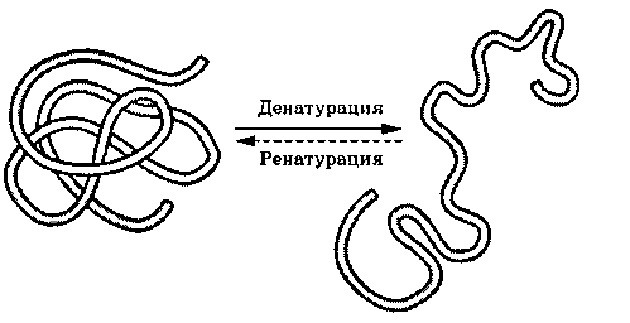
Утрата белковой молекулой своей структуры называется денатурацией; она может быть вызвана повышением температуры, обезвоживанием, облучением и т.д. Если при денатурации первичная структура не нарушается, то при восстановлении нормальных условий полностью воссоздается структура белка. Если же действие фактора нарастает, разрушается и первичная структура белка — полипептидная цепь. Это уже необратимый процесс — восстановить структуру белок не может. Например, при высокой температуре (выше 42oС) в организме человека многие белки денатурируют необратимо.
Вопрос 5. По какому признаку белки делятся на простые и сложные?
Простые белки (протеины) состоят исключительно из аминокислот (альбумины, глобулины, кератин, коллаген, гистон и другие). В состав сложных белков могут входить другие органические вещества: углеводы (тогда они называются гликопротеидами), жиры (липопротеиды), нуклеиновые кислоты (нуклеопротеиды), фосфорная кислота (фосфопротеиды), при сочетании белка с каким-либо окрашенным веществом образуются так называемые хромопротеиды. Из хромопротеидов наиболее изучен гемоглобин – красящее вещество красных кровяных шариков (эритроцитов).
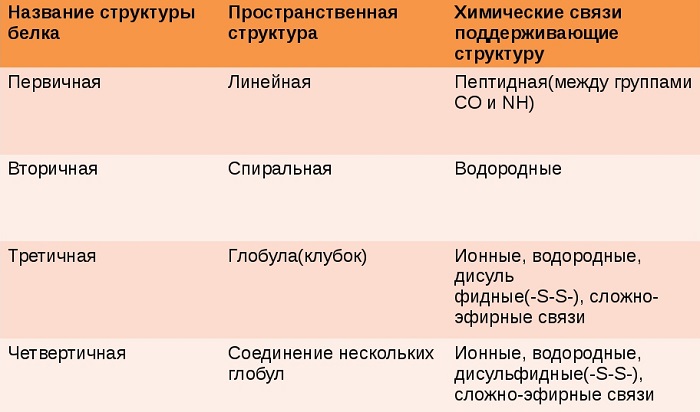
Строение белков. Структуры белков
Структуры белков: первичная, вторичная, третичная и четвертичная
Белки
Название «белки» происходит от способности многих из них при нагревании становиться белыми. Название «протеины» происходит от греческого слова «первый», что указывает на их важное значение в организме. Чем выше уровень организации живых существ, тем разнообразнее состав белков.
Белки образуются из аминокислот, которые соединяются между собой ковалентной – пептидной связью: между карбоксильной группой одной аминокислоты и аминогруппой другой. При взаимодействии двух аминокислот образуется дипептид (из остатков двух аминокислот, от греч. пептос – сваренный). Замена, исключение или перестановка аминокислот в полипептидной цепи вызывает возникновение новых белков. Например, при замене лишь одной аминокислоты (глутамина на валин) возникает тяжелая болезнь – серповидно-клеточная анемия, когда эритроциты имеют другую форму и не могут выполнять свои основные функции (перенос кислорода). При образовании пептидной связи отщепляется молекула воды. В зависимости от количества аминокислотных остатков выделяют:
– олигопептиды (ди-, три-, тетрапептиды и т. п.) – содержат до 20 аминокислотных остатков;
– полипептиды – от 20 до 50 аминокислотных остатков;
– белки – свыше 50, иногда тысячи аминокислотных остатков
По физико-химическим свойствам различают белки гидрофильные и гидрофобные.
Существуют четыре уровня организации белковой молекулы – равноценные пространственные структуры (конфигурации, конформации) белков: первичная, вторичная, третичная и четвертичная.
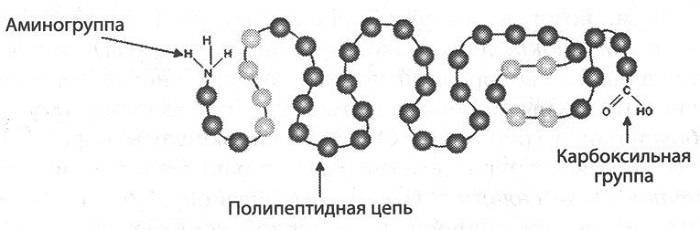
Первичная структура
Первичная структура белков является простейшей. Имеет вид полипептидной цепи, где аминокислоты связаны между собой прочной пептидной связью. Определяется качественным и количественным составом аминокислот и их последовательностью.
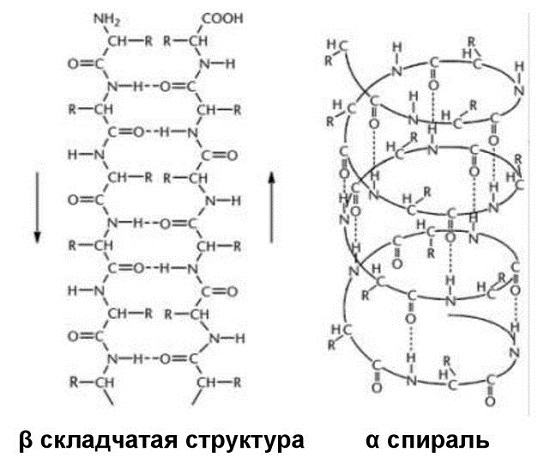
Вторичная структура
Вторичная структура образована преимущественно водородными связями, которые образовались между атомами водорода NH-группы одного завитка спирали и кислорода СО-группы другого и направлены вдоль спирали или между параллельными складками молекулы белка. Белковая молекула частично или целиком скручена в α-спираль или образует β-складчатую структуру. Например, белки кератина образуют α-спираль. Они входят в состав копыт, рогов, волос, перьев, ногтей, когтей. β-складчатую имеют белки, которые входят в состав шелка. Извне спирали остаются аминокислотные радикалы (R-группы). Водородные связи значительно более слабые, чем ковалентные, но при значительном их количестве образуют довольно прочную структуру.
Функционирование в виде закрученной спирали характерно для некоторых фибриллярных белков – миозин, актин, фибриноген, коллаген и т. п.
Третичная структура
Третичная структура белка. Эта структура постоянна и своеобразна для каждого белка. Она определяется размером, полярностью R-групп, формой и последовательностью аминокислотных остатков. Полипептидная спираль закручивается и укладывается определенным образом. Формирование третичной структуры белка приводит к образованию особой конфигурации белка – глобулы (от лат. globulus – шарик). Его образование обуславливается разными типами нековалентных взаимодействий: гидрофобные, водородные, ионные. Между остатками аминокислоты цистеина возникают дисульфидные мостики.
Гидрофобные связи – это слабые связи между неполярными боковыми цепями, которые возникают в результате взаимного отталкивания молекул растворителя. При этом белок скручивается так, что гидрофобные боковые цепи погружены вглубь молекулы и защищают ее от взаимодействия с водой, а снаружи расположены боковые гидрофильные цепи.
Третичную структуру имеет большинство белков – глобулины, альбумины и т. п.
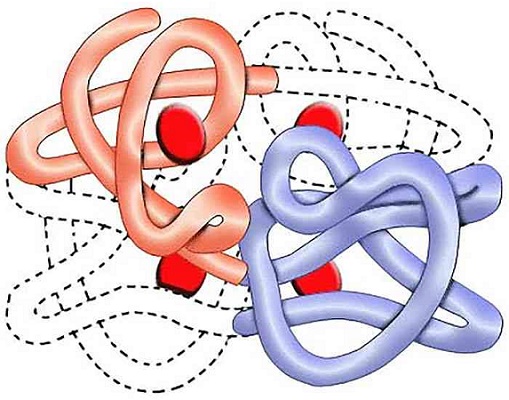
Четвертичная структура
Четвертичная структура белка. Образуется в результате объединения отдельных полипептидных цепей. В совокупности они составляют функциональную единицу. Типы связей разные: гидрофобные, водородные, электростатические, ионные.
Электростатические связи возникают между электроотрицательными и электроположительными радикалами аминокислотных остатков.
Для одних белков характерно глобулярное размещение субъединиц – это глобулярные белки. Глобулярные белки легко растворяются в воде или растворах солей. К глобулярным белкам принадлежит свыше 1000 известных ферментов. К глобулярным белкам относятся некоторые гормоны, антитела, транспортные белки. Например, сложная молекула гемоглобина (белка эритроцита крови) является глобулярным белком и состоит из четырех макромолекул глобинов: двух α-цепей и двух β-цепей, каждая из которых соединена с гемом, содержащим железо.
Для других белков характерно объединение в спиральные структуры – это фибриллярные (от лат. fibrilla – волоконце) белки. Несколько (от 3 до 7) α–спиралей свиваются вместе, подобно волокнам в кабеле. Фибриллярные белки нерастворимы в воде.
Белки делят на простые и сложные.
Простые (протеины)
Состоят только из остатков аминокислот. К простым белкам относят глобулины, альбумины, глутелины, проламины, протамины, пистоны. Альбумины (например, альбумин сыворотки крови) растворимы в воде, глобулины (например, антитела) нерастворимы в воде, но растворимы в водных растворах некоторых солей (хлорид натрия и т. п.).
Сложные (протеиды)
Включают в состав, кроме остатков аминокислот, соединения другой природы, которые называются простетическою группой. Например, металлопротеиды – это белки, содержащие негеминовое железо или связанные атомами металлов (большинство ферментов), нуклеопротеиды – белки, соединенные с нуклеиновыми кислотами (хромосомы и т. п.), фосфопротеиды –белки, в состав которых входят остатки фосфорной кислоты (белки яичного желтка и т. п.), гликопротеиды –белки в соединении с углеводами (некоторые гормоны, антитела и т. п.), хромопротеиды – белки, содержащий пигменты (миоглобин и т. п.), липопротеиды – белки, содержащие липиды (входят в состав мембран).
Структура белка необычайно важна для соединений, так как все функции они выполняют, принимая определённую пространственную конфигурацию.
Белки – это природные полимеры, молекулы которых состоят из остатков аминокислот, соединенных амидными (пептидными) связями.
Мономерами для образования макромолекулы служат α-аминокислоты. Это соединения, содержащие аминогруппу у первого атома углерода, не считая углерод карбоксильной группы.
Таких аминокислот известно 20. Из этого количества создаётся всё многообразие белков. Некоторые аминокислоты могут образовываться в организме, их называют заменимыми. Те, которые поступают только с пищей – незаменимые. В зависимости от состава, белки делят на полноценные, содержащие незаменимые аминокислоты, и неполноценные, не содержащие незаменимые аминокислоты.
Состав, строение и функции белков очень сложные, изучает эти вопросы биология. Рассматриваются природные полимеры и в курсе химии. Состав их можно выразить формулой:
В природные полимеры входят химические элементы: углерод, кислород, водород, азот, сера. В состав некоторых соединений включены фосфор, селен железо, медь и прочие элементы.
Первичная структура белка
Последовательно соединенные друг с другом аминокислотные остатки в цепь образуют первичную структуру. Цепь образована пептидной химической связью. Этот уровень организации самый важный. Случайная замена одной аминокислоты вызывает тяжелое генетическое заболевание.
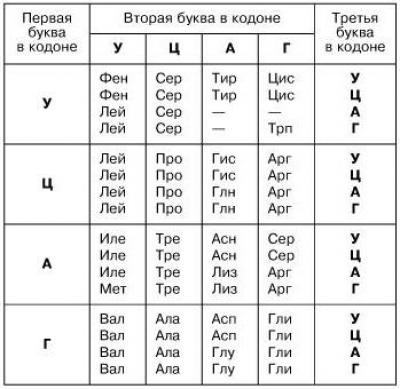
Белковые молекулы образуются в процессе биосинтеза на рибосомах. Здесь реализуется наследственная информация. Последовательность аминокислотных остатков определяется последовательностью нуклеотидов в и-РНК. Зависимость триплетов и аминокислот записана в таблице генетического кода.
Если первичный уровень организации белка задаётся правильно, остальные структуры макромолекула принимает самопроизвольно.
Вторичная структура белка
Свёрнутая в спираль одна или 2 полипептидные цепи образуют вторичную структуру. Её поддерживают водородные связи.
Большинство белковых молекул имеют вторичный уровень.
Третичная структура белка
Упаковка вторичной структуры в клубок образует третичный уровень организации.
Поддерживают данную структуру дисульфидные, солевые, сложноэфирные мостики, силы электростатического взаимодействия.
Четвертичная структура белка
Некоторые белковые единицы формируют сложные агрегаты в пространстве. Несколько упакованных в клубок белков, ориентированных относительно друг друга, создают четвертичную структуру.
Удерживаются такие агрегаты водородными связями, электростатическими и прочими взаимодействиями.
Денатурация и ренатурация белка
Природные соединения проявляют разные свойства. Одно из важнейших свойств – денатурация белка. Это разрушение пространственной организации белковых молекул. Последовательность соединения аминокислот, а значит и химический состав, не изменяется.
Пространственная конфигурация может разрушаться в результате действия разных факторов:
солей тяжёлых металлов;
механических и иных факторов.
Если первичный уровень организации белка не нарушен, может идти обратная реакция – ренатурация. Это восстановление пространственного строения молекулы. Не все природные полимеры способны к восстановлению пространственной организации.
Иногда денатурация протекает необратимо, хотя первичная структура не разрушается. Функции белки способны выполнять, находясь в определенной пространственной конфигурации.
Протеины – простые белки
К простым белкам относят высокомолекулярные соединения, состоящие только из остатков аминокислот. В них содержатся незаменимые и заменимые аминокислоты.
Протеины применяются в спортивной среде для восполнения белковой массы в организме. Используют протеиновый порошок для приготовления коктейля, в качестве добавки к пище.
Протеиновый порошок получают в результате переработки продуктов животного происхождения: молока, мяса, яиц, рыбы. Организм будет получать протеины, если просто употреблять в пищу указанные продукты. Усвоение их будет идти медленнее.
Протеиды – сложные белки
Сложными называют белки, содержащие небелковые по природе вещества. Так называемые простетические группы.
В соответствии с химическим составом и наличием групп их классифицируют:
гликопротеиды и другие.
В состав протеидов входят элементы: магний, железо, медь и другие. Примером протеидов являются гемоглобин и миоглобин. Они выполняют важнейшие функции, принимают участие в обменных процессах.
Функции белков
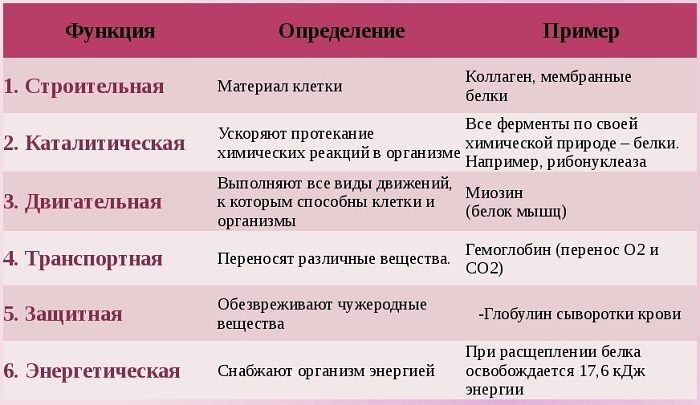
Белки выполняют в клетках организмов важные функции:
Состав и структура белков
Вопрос 1. Какие вещества называются белками или протеинами?
Белки (протеины) — это гетерополимеры, состоящие из 20 различных мономеров — природных альфа-аминокислот. Белки — нерегулярные полимеры.
Общее строение аминокислоты может быть представлено следующим образом:
R—С(NH2)—СООН. Все аминокислоты имеют аминогруппу (—МН2) и карбоксильную группу (—СООН) и различаются строением и свойствами радикалов. Аминокислоты в белке связаны пептидной
связью —N(Н)—С(=О), поэтому белки ещё называют пептидами.
Вопрос 2. Что такое первичная структура белка?
В молекуле белка аминокислоты связаны друг с другом пептидной связью между атомами углерода и азота. В строении молекулы белка различают первичную структуру — последовательность аминокислотных остатков.
Вопрос 3. Как образуются вторичная, третичная и четвертичная структуры белка?
Вторичная структура белка — как правило, это спиральная структура (альфа-спираль), которая удерживается множеством водородных связей, возникающих между находящимся близко друг от друга С=О и NН-группами. Другой тип вторичной структуры — это бета-слой, или складчатый слой; это две параллельные полипептидные цепи, связанные водородными связями, перпендикулярными цепям.
Третичная структура белковой молекулы — это пространственная конфигурация, напоминающая компактную глобулу. Она поддерживается ионными, водородными и дисульфидными (S=S) связями, а также гидрофобными взаимодействиями.
Четвертичная структура белка образуется при взаимодействии нескольких глобул, которые объединяются в комплекс (например, молекула гемоглобина состоит из четырех таких субъединиц).
Вопрос 4. Что такое денатурация белка?
Утрата белковой молекулой своей структуры называется денатурацией; она может быть вызвана повышением температуры, обезвоживанием, облучением и т.д. Если при денатурации первичная структура не нарушается, то при восстановлении нормальных условий полностью воссоздается структура белка. Если же действие фактора нарастает, разрушается и первичная структура белка — полипептидная цепь. Это уже необратимый процесс — восстановить структуру белок не может. Например, при высокой температуре (выше 42oС) в организме человека многие белки денатурируют необратимо.
Вопрос 5. По какому признаку белки делятся на простые и сложные?
Простые белки (протеины) состоят исключительно из аминокислот (альбумины, глобулины, кератин, коллаген, гистон и другие). В состав сложных белков могут входить другие органические вещества: углеводы (тогда они называются гликопротеидами), жиры (липопротеиды), нуклеиновые кислоты (нуклеопротеиды), фосфорная кислота (фосфопротеиды), при сочетании белка с каким-либо окрашенным веществом образуются так называемые хромопротеиды. Из хромопротеидов наиболее изучен гемоглобин – красящее вещество красных кровяных шариков (эритроцитов).
Белки
теория по биологии 🌿 цитология
Строение белков
Аминокислоты ассоциируются с генетическим кодом, так как последовательности нуклеотидов кодируют триплеты нуклеотидов. Такие задачи изучаются в школе и встречаются в ЕГЭ. Всем, кто сталкивался с генетикой, хорошо знакома таблица
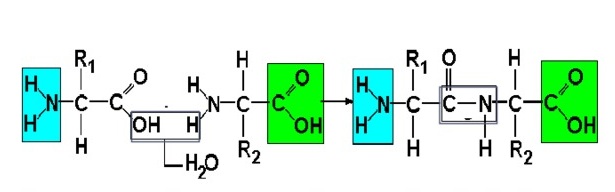
В один белок может входить много аминокислот. Они соединяются в цепь посредством образования пептидных связей: азот одной аминокислоты связывается с углеродом другой аминокислоты:
Строение белка. Зеленым цветом обозначена карбоксильная группа аминокислоты, голубым цветом — аминогруппа аминокислоты
Некоторые аминокислоты животный
Классификация белков
Протеины –
Протеиды – белки, в состав которых, кроме белковых молекул, входят небелковые молекулы.
Для того чтобы не путаться в понятиях, нужно вспомнить, что принимают спортсмены для того, чтобы скорее нарастить мышечную массу, то есть протеиновые коктейли, батончики и т.д. Именно протеиновые, это слово на слуху, пусть теперь оно ассоциируется с этой классификацией.
Уровни организации белковой молекулы
Структура белка именуется просто по счету, в зависимости от сложности укладки.
Первичная структура белка представляет собой прямую цепь из аминокислот. Она является главной и определяющей свойства, форму и функции белка.
Вторичная структура белка – уже две цепи. Однако эти цепи не идут параллельно друг другу. Они скручены в спираль и связаны водородными связями, которые их удерживают за счет того, что их много.
Третичная структура белка – глобула. Глобула означает шар, что и является описанием структуры белка. В этом случае прочность обусловлена тремя видами связей: водородными, ионными и дисульфидными.
Четвертичная структура белка – это как бы глобула из глобул. Она встречается не у всех белков. Белок крови
Регенерация — восстановление организмом утраченных или повреждённых органов и тканей, а также восстановление целого организма из его частей.
Денатурация и ренатурация
Функции белков
Белки входят в состав всего в клетке: мембраны и органоиды. Кроме того, есть белки, которые очень важно знать:
Ферменты – катализаторы (= ускорители химических реакций) белковой природы. С ферментами происходит тесное знакомство в разделе «пищеварение». Есть одно важное правило, которое нужно обязательно запомнить: все ферменты – белки, но не все белки – ферменты.
Белки-транспортеры осуществляют перенос веществ через мембрану клетки. Очень наглядным примером транспорта белками является белок-переносчик гемоглобин, благодаря которому мы дышим. В мышцах существует аналог этого белка – миоглобин (приставка мио- означает «сокращение», тем самым называя месторасположение белка).
Кроме оборонительной и атакующей функции во благо защиты организма, есть и латающая. При порезе и кровопотере молекулы белка тромбина объединяются для того, чтобы закрыть поврежденный сосуд, а тем временем, тонкие нити белка фибрина переплетаются на поверхности раны, образуя тоненькую пленочку. Если порез был несерьезным, то кровотечение успешно остановлено.
Некоторые белки являются гормонами. Они отвечают за регуляцию физиологических процессов организма. Наиболее известным примером белкового
Как и углеводы с жирами, белки тоже могут быть расщеплены для получения энергии. Однако, чаще всего, аминокислоты, полученные в результате распада белка, снова используются организмом для построения других белков. Это делает для экономии энергии и биологического материала, ведь в случае повторного использования, не нужно тратиться на синтез новых соединений. При расщеплении 1 г белка высвобождается 17,6 кДж энергии.
Задание EB11693 Установите соответствие между классами органических веществ и выполняемыми ими функциями в клетке.
| ОСОБЕННОСТИ СТРОЕНИЯ И СВОЙСТВ ВЕЩЕСТВА | ВЕЩЕСТВА |
| A) запасание энергии B) хранение генетической информации Д) входит в состав клеточных стенок и мембран Е) реализация генетической информации (синтез белка) 2) нуклеиновые кислоты (ДНК, РНК) |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
| А | Б | В | Г | Д | Е |
Для начала вспомним какие вообще есть классы органических веществ в клетке.
Это белки, жиры, углеводы и нуклеиновые кислоты. Белки, жиры и углеводы являются источниками энергии, но у них есть и более локальные функции:
| Белки | Жиры | Углеводы | Нуклеиновые кислоты |
| Структурная | + | + | |
| Энергетическая | + | + | + |
| Защитная | + | + | |
| Ферментативная | + | ||
| Двигательная | + | ||
| Транспортная | + | ||
| Регуляторная | + | ||
| Рецепторная | + | ||
| Хранение и передача ген.информации | + | ||
| Биосинтез белка | + |
Выберем вначале то,что относится к нуклеиновым кислотам: биосинтез белка и хранение генетической информации.
PS: сигнальная и рецепторная функция — одно и то же.
pазбирался: Ксения Алексеевна | обсудить разбор | оценить
На данной схеме изображена реакция между двумя аминокислотами, что известно из вопроса. Между ними действуют пептидные связи.
Пептидная связь — это химическая связь, возникающая между двумя молекулами в результате реакции конденсации между карбоксильной группой (-СООН) одной молекулы и аминогруппой (-NH2) другой молекулы, при выделении одной молекулы воды (H2O).
pазбирался: Ксения Алексеевна | обсудить разбор | оценить