Фиброин
Свойства
Фиброин является гетеродимером, образованным двумя белковыми цепями. Его первичная структура состоит из повторяющейся аминокислотной последовательности (Gly-Ser-Gly-Ala-Gly-Ala) n.
В свою очередь, повторяющиеся аминокислотные последовательности образуют антипараллельные складчатые β-слои, связанные водородными связями. Эта структура обуславливает высокий предел прочности нитей паутин и шелка. Более прочный, чем кевлар, фиброин вдобавок ещё и высоко эластичен. Эти качества делают его материалом, применяемым в различных областях, включая биомедицину и текстильное производство.
Структуры
Структура белка
По вторичной структуре белка семейство кератинов разделяется на две группы:
Для первичной структуры α-кератинов характерно большое содержание цистеина и множество дисульфидных связей.
В отличие от α-кератинов поперечные дисульфидные связи между соседними полипептидными цепями у β-кератинов отсутствуют. В полипептидной цепи каждый второй элемент — глицин. Характерно повторение последовательности «GSGAGA».
Для α-кератинов основным структурным компонентом являются цилиндрические микрофибриллы диаметром 75 А, состоящие из спирализованных, скрученных попарно протофибрилл.
Биология. 11 класс
§ 4. Структура и свойства белков
Белки *(протеины)* — это полипептиды, в состав молекул которых входит множество остатков аминокислот (до нескольких тысяч). * Белки — нерегулярные биополимеры.* Они различаются количеством аминокислотных звеньев, их составом и последовательностью расположения. При этом каждый белок имеет особый, присущий только ему порядок чередования аминокислот.
Уровни структурной организации белковых молекул. Для того чтобы белок мог выполнять свою биологическую функцию, его молекула должна иметь определенную пространственную конфигурацию. Различают четыре основных уровня организации белковых молекул — первичную, вторичную, третичную и четвертичную структуры (рис. 4.1).
Первичная структура белка — это строго определенная последовательность аминокислотных остатков в линейной полипептидной цепи. Каждый белок обладает уникальной первичной структурой. Ее существование обусловлено наличием прочных пептидных связей между остатками аминокислот. Все последующие, более сложные структуры формируются на основе первичной. Поэтому изменение первичной структуры (например, замена одних аминокислотных остатков на другие) приводит к изменению формы молекулы, свойств и функций белка.
Вторичная структура белка формируется за счет образования многочисленных водородных связей между атомами водорода NH-групп и атомами кислорода CO-групп разных аминокислотных остатков. Несмотря на то что эти связи слабее ковалентных, их количество обеспечивает стабильность вторичной структуры.
Чаще всего водородные связи возникают внутри одной полипептидной цепи между близко расположенными остатками аминокислот, что приводит к закручиванию этой цепи в так называемую α-спираль.
Иногда водородные связи возникают между относительно удаленными друг от друга участками полипептидной цепи (или нескольких разных цепей). *Данные участки могут располагаться параллельно (если полипептидные цепи идут в одном направлении, например, от N-конца к C-концу) либо антипараллельно (если цепи имеют противоположное направление: одна идет от N-конца к С-концу, а соседняя наоборот).* При этом формируется складчатая структура, напоминающая гармошку. Такой тип вторичной структуры получил название β-складчатый слой (см. рис. 4.1).
*α-спиральные и β-структурные участки белковой молекулы могут взаимодействовать друг с другом и между собой, образуя упорядоченные структуры (ансамбли). Например, α-спиральные фрагменты могут объединяться в двойные или тройные спирали. На основе β-участков часто образуются структуры, имеющие вид шпилек, арок, зигзагов и др. Участки, имеющие α- и β- строение, могут формировать ансамбли состава αβ, βαβ, βαβαβ и т. п. Эти пространственные конфигурации представляют собой так называемую сверхвторичную структуру белка.
Ансамбли сверхвторичной структуры являются основой для формирования в молекулах белков доменов. Это структурно и функционально обособленные области, соединенные друг с другом короткими фрагментами полипептидной цепи — шарнирными участками.
Например, молекулы мембранных белков-рецепторов чаще всего состоят из трех доменов. Надмембранный домен обеспечивает прием внешних сигналов, внутримембранный закрепляет белок в мембране, подмембранный осуществляет передачу сигнала внутрь клетки. Другим примером может служить сывороточный альбумин — белок плазмы крови, способный связываться с высшими карбоновыми кислотами, билирубином, некоторыми токсинами и другими соединениями и доставлять их в те или иные органы. Молекула этого белка содержит три домена, каждый из которых отвечает за избирательное связывание с определенными веществами.*
Многие белки способны выполнять свои биологические функции, обладая третичной структурой. Но некоторым белкам для этого необходимо объединение в единый комплекс двух или более молекул, имеющих третичную структуру. Так возникает четвертичная структура белка. Молекулы, входящие в ее состав *(их называют субъединицами или протомерами)*, могут быть одинаковыми или разными. Они удерживаются вместе благодаря различным видам нековалентных связей — водородным, ионным, гидрофобным взаимодействиям и др. В некоторых белках, например иммуноглобулинах, к множеству таких связей добавляются несколько ковалентных дисульфидных. Примером белка, имеющего четвертичную структуру, может служить гемоглобин (рис. 4.3).
Строение белков. Структуры белков
Структуры белков: первичная, вторичная, третичная и четвертичная
Белки
Название «белки» происходит от способности многих из них при нагревании становиться белыми. Название «протеины» происходит от греческого слова «первый», что указывает на их важное значение в организме. Чем выше уровень организации живых существ, тем разнообразнее состав белков.
Белки образуются из аминокислот, которые соединяются между собой ковалентной – пептидной связью: между карбоксильной группой одной аминокислоты и аминогруппой другой. При взаимодействии двух аминокислот образуется дипептид (из остатков двух аминокислот, от греч. пептос – сваренный). Замена, исключение или перестановка аминокислот в полипептидной цепи вызывает возникновение новых белков. Например, при замене лишь одной аминокислоты (глутамина на валин) возникает тяжелая болезнь – серповидно-клеточная анемия, когда эритроциты имеют другую форму и не могут выполнять свои основные функции (перенос кислорода). При образовании пептидной связи отщепляется молекула воды. В зависимости от количества аминокислотных остатков выделяют:
– олигопептиды (ди-, три-, тетрапептиды и т. п.) – содержат до 20 аминокислотных остатков;
– полипептиды – от 20 до 50 аминокислотных остатков;
– белки – свыше 50, иногда тысячи аминокислотных остатков
По физико-химическим свойствам различают белки гидрофильные и гидрофобные.
Существуют четыре уровня организации белковой молекулы – равноценные пространственные структуры (конфигурации, конформации) белков: первичная, вторичная, третичная и четвертичная.
Первичная структура
Первичная структура белков является простейшей. Имеет вид полипептидной цепи, где аминокислоты связаны между собой прочной пептидной связью. Определяется качественным и количественным составом аминокислот и их последовательностью.
Вторичная структура
Вторичная структура образована преимущественно водородными связями, которые образовались между атомами водорода NH-группы одного завитка спирали и кислорода СО-группы другого и направлены вдоль спирали или между параллельными складками молекулы белка. Белковая молекула частично или целиком скручена в α-спираль или образует β-складчатую структуру. Например, белки кератина образуют α-спираль. Они входят в состав копыт, рогов, волос, перьев, ногтей, когтей. β-складчатую имеют белки, которые входят в состав шелка. Извне спирали остаются аминокислотные радикалы (R-группы). Водородные связи значительно более слабые, чем ковалентные, но при значительном их количестве образуют довольно прочную структуру.
Функционирование в виде закрученной спирали характерно для некоторых фибриллярных белков – миозин, актин, фибриноген, коллаген и т. п.
Третичная структура
Третичная структура белка. Эта структура постоянна и своеобразна для каждого белка. Она определяется размером, полярностью R-групп, формой и последовательностью аминокислотных остатков. Полипептидная спираль закручивается и укладывается определенным образом. Формирование третичной структуры белка приводит к образованию особой конфигурации белка – глобулы (от лат. globulus – шарик). Его образование обуславливается разными типами нековалентных взаимодействий: гидрофобные, водородные, ионные. Между остатками аминокислоты цистеина возникают дисульфидные мостики.
Гидрофобные связи – это слабые связи между неполярными боковыми цепями, которые возникают в результате взаимного отталкивания молекул растворителя. При этом белок скручивается так, что гидрофобные боковые цепи погружены вглубь молекулы и защищают ее от взаимодействия с водой, а снаружи расположены боковые гидрофильные цепи.
Третичную структуру имеет большинство белков – глобулины, альбумины и т. п.
Четвертичная структура
Четвертичная структура белка. Образуется в результате объединения отдельных полипептидных цепей. В совокупности они составляют функциональную единицу. Типы связей разные: гидрофобные, водородные, электростатические, ионные.
Электростатические связи возникают между электроотрицательными и электроположительными радикалами аминокислотных остатков.
Для одних белков характерно глобулярное размещение субъединиц – это глобулярные белки. Глобулярные белки легко растворяются в воде или растворах солей. К глобулярным белкам принадлежит свыше 1000 известных ферментов. К глобулярным белкам относятся некоторые гормоны, антитела, транспортные белки. Например, сложная молекула гемоглобина (белка эритроцита крови) является глобулярным белком и состоит из четырех макромолекул глобинов: двух α-цепей и двух β-цепей, каждая из которых соединена с гемом, содержащим железо.
Для других белков характерно объединение в спиральные структуры – это фибриллярные (от лат. fibrilla – волоконце) белки. Несколько (от 3 до 7) α–спиралей свиваются вместе, подобно волокнам в кабеле. Фибриллярные белки нерастворимы в воде.
Белки делят на простые и сложные.
Простые (протеины)
Состоят только из остатков аминокислот. К простым белкам относят глобулины, альбумины, глутелины, проламины, протамины, пистоны. Альбумины (например, альбумин сыворотки крови) растворимы в воде, глобулины (например, антитела) нерастворимы в воде, но растворимы в водных растворах некоторых солей (хлорид натрия и т. п.).
Сложные (протеиды)
Включают в состав, кроме остатков аминокислот, соединения другой природы, которые называются простетическою группой. Например, металлопротеиды – это белки, содержащие негеминовое железо или связанные атомами металлов (большинство ферментов), нуклеопротеиды – белки, соединенные с нуклеиновыми кислотами (хромосомы и т. п.), фосфопротеиды –белки, в состав которых входят остатки фосфорной кислоты (белки яичного желтка и т. п.), гликопротеиды –белки в соединении с углеводами (некоторые гормоны, антитела и т. п.), хромопротеиды – белки, содержащий пигменты (миоглобин и т. п.), липопротеиды – белки, содержащие липиды (входят в состав мембран).
Строение и функции белков
Белки (протеины) составляют 50% от сухой массы живых организмов.
Белки состоят из аминокислот. У каждой аминокислоты есть аминогруппа и кислотная (карбоксильная) группа, при взаимодействии которых получается пептидная связь, поэтому белки еще называют полипептидами.
Структуры белка
Первичная – цепочка из аминокислот, связанных пептидной связью (сильной, ковалентной). Чередуя 20 аминокислот в разном порядке, можно получать миллионы разных белков. Если поменять в цепочке хотя бы одну аминокислоту, строение и функции белка изменятся, поэтому первичная структура считается самой главной в белке.
Вторичная – спираль. Удерживается водородными связями (слабыми).
Третичная – глобула (шарик). Четыре типа связей: дисульфидная (серный мостик) сильная, остальные три (ионные, гидрофобные, водородные) – слабые. Форма глобулы у каждого белка своя, от нее зависят функции. При денатурации форма глобулы меняется, и это сказывается на работе белка.
Четвертичная – имеется не у всех белков. Состоит из нескольких глобул, соединенных между собой теми же связями, что и в третичной структуре. (Например, гемоглобин.)
Денатурация
Это изменение формы глобулы белка, вызванное внешними воздействиями (температура, кислотность, соленость, присоединение других веществ и т.п.)
Функции белков
Их очень много, например:
Еще можно почитать
Задания части 1
Выберите один, наиболее правильный вариант. Водородные связи между СО- и NН-группами в молекуле белка придают ей форму спирали, характерную для структуры
1) первичной
2) вторичной
3) третичной
4) четвертичной
Выберите один, наиболее правильный вариант. Четвертичная структура молекулы белка образуется в результате взаимодействия
1) участков одной белковой молекулы по типу связей S-S
2) нескольких полипептидных нитей, образующих клубок
3) участков одной белковой молекулы за счет водородных связей
4) белковой глобулы с мембраной клетки
Выберите один, наиболее правильный вариант. Последовательность и число аминокислот в полипептидной цепи – это
1) первичная структура ДНК
2) первичная структура белка
3) вторичная структура ДНК
4) вторичная структура белка
Выберите один, наиболее правильный вариант. Первичная структура белка образована связью
1) водородной
2) макроэргической
3) пептидной
4) ионной
Выберите один, наиболее правильный вариант. В основе образования пептидных связей между аминокислотами в молекуле белка лежит
1) принцип комплементарности
2) нерастворимость аминокислот в воде
3) растворимость аминокислот в воде
4) наличие в них карбоксильной и аминной групп
БЕЛКИ
1. Выберите три варианта. Белки в организме человека и животных
1) составляют бо́льшую часть организма по массе
2) начинают расщепляться в ротовой полости
3) не содержат фосфора в составе молекулы
4) могут откладываться в запас
5) в качестве ферментов ускоряют химические реакции
6) служат основным строительным материалом
2. Выберите три верных ответа из шести и запишите цифры, под которыми они указаны. Выберите только особенности строения белковой молекулы.
1) содержит атомы фосфора
2) состоит из аминокислот
3) мономеры удерживаются пептидными связями
4) состоит из одинаковых по строению мономеров
5) изменяет форму под действием температуры
6) четвертичная структура состоит из нескольких молекул
3. Выберите три верных ответа из шести и запишите цифры, под которыми они указаны. Какие из перечисленных ниже признаков относятся к характеристикам молекул белков?
1) состоят из нуклеотидов
2) выполняют только структурную и двигательную функции
3) могут иметь форму глобулы
4) содержат в составе азот и серу
5) всегда нерастворимы в воде
6) являются нерегулярными полимерами
Выберите три верных ответа из шести и запишите цифры, под которыми они указаны. Какие из перечисленных ниже веществ относятся к белкам?
1) крахмал
2) коллаген
3) фибриноген
4) тестостерон
5) гемоглобин
6) сахароза
БЕЛКИ КРОМЕ
1. Все перечисленные признаки, кроме двух, можно использовать при описании яичного белка альбумина. Определите два признака, «выпадающие» из общего списка, и запишите цифры, под которыми они указаны.
1) состоит из аминокислот
2) пищеварительный фермент
3) денатурирует обратимо при варке яйца вкрутую
4) мономеры связаны пептидными связями
5) молекула образует первичную, вторичную и третичную структуры
2. Все перечисленные ниже признаки, кроме двух, можно использовать для описания молекулы белка. Определите два признака, «выпадающих» из общего списка, и запишите цифры, под которыми они указаны.
1) состоит из нуклеотидов
2) может иметь форму глобулы
3) имеет третичную и четвертичную структуры
4) образуется в ядре
5) бывают глобулярные и фибриллярные
БЕЛКИ КРОМЕ РИС
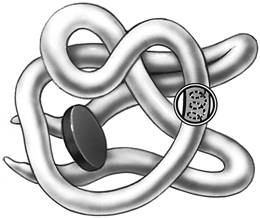
1. Перечисленные ниже признаки, кроме двух, используются для описания строения, функций изображенного органического вещества. Определите два признака, «выпадающие» из общего списка, и запишите цифры, под которыми они указаны.
1) имеет структурные уровни организации молекулы
2) входит в состав клеточных стенок
3) является биополимером
4) служит матрицей при трансляции
5) состоит из аминокислот

2. Все перечисленные ниже признаки, кроме двух, используются для описания изображённой на рисунке структуры. Определите два признака, «выпадающие» из общего списка, и запишите цифры, под которыми они указаны.
1) вторичная структура молекулы белка
2) удерживается только пептидными связями
3) определяется методом рентгеноструктурного анализа
4) представляет собой глобулу
5) может выполнять ферментативные функции

3. Все перечисленные ниже характеристики, кроме двух, используют для описания изображенной на рисунке молекулы органического вещества клетки. Определите две характеристики, «выпадающие» из общего списка, и запишите цифры, под которыми они указаны.
1) денатурация
2) репликация
3) транскрипция
4) аминокислоты
5) водородные связи
СТРУКТУРЫ БЕЛКА
Установите соответствие между характеристикой и структурой белка: 1) первичная, 2) третичная. Запишите цифры 1 и 2 в порядке, соответствующем буквам.
А) молекула в форме глобулы или фибриллы
Б) строгая последовательность аминокислотных остатков
В) аминокислотные остатки соединены только пептидными связями
Г) имеет дисульфидные мостики между радикалами аминокислот
Д) при ее разрушении наступает необратимая денатурация
Е) пространственная конфигурация полипептидной цепи
ФЕРМЕНТАТИВНАЯ
1. Все приведенные ниже признаки, кроме двух, можно использовать для описания ферментов. Определите два признака, «выпадающих» из общего списка, и запишите цифры, под которыми они указаны.
1) входят в состав клеточных мембран и органоидов клетки
2) играют роль биологических катализаторов
3) имеют активный центр
4) оказывают влияние на обмен веществ, регулируя различные процессы
5) специфические белки
2. Выберите три верных ответа из шести и запишите цифры, под которыми они указаны. Ферменты – это вещества, которые
1) вырабатываются в железах внутренней секреции
2) являются белками
3) поступают в организм, как правило, вместе с пищей
4) являются в организме источником энергии
5) ускоряют протекание химических реакций
6) у человека выполняют свои функции при температуре около 36 градусов
ФУНКЦИИ БЕЛКОВ
Выберите три верных ответа из шести и запишите цифры, под которыми они указаны. Функциями белков в организме человека являются
1) строительная
2) передача наследственных признаков
3) защитная
4) запасающая
5) ферментативно-каталитическая
6) хранение генетической информации
ФУНКЦИИ БЕЛКОВ КРОМЕ
Все перечисленные характеристики используют для описания функций белков. Определите две характеристики, «выпадающие» из общего списка, и запишите цифры, под которыми они указаны.
1) регуляторная
2) двигательная
3) рецепторная
4) образуют клеточные стенки
5) служат коферментами

Рассмотрите рисунок с изображением полипептида и укажите (А) уровень его организации, (Б) форму молекулы и (В) вид взаимодействия, поддерживающий эту структуру. Для каждой буквы выберите соответствующий термин или соответствующее понятие из предложенного списка.
1) первичная структура
2) вторичная структура
3) третичная структура
4) взаимодействия между нуклеотидами
5) металлическая связь
6) гидрофобные взаимодействия
7) фибриллярная
8) глобулярная

Рассмотрите схему химического вещества. Укажите (А) название класса органических веществ, (Б) уровень организации полимерной молекулы и (В) название мономеров, из которых состоит данная молекула. Для каждой буквы выберите соответствующий термин из предложенного списка.
1) ДНК
2) белок
3) альфа-спираль
4) вторичная структура
5) третичная структура
6) аминокислоты
7) нуклеотиды
8) рибоза

Рассмотрите рисунок с изображением полипептида. Укажите (А) уровень его организации, (Б) мономеры, которые его образуют, и (В) вид химических связей между ними. Для каждой буквы выберите соответствующий термин или соответствующее понятие из предложенного списка.
1) первичная структура
2) водородные связи
3) двойная спираль
4) вторичная структура
5) аминокислота
6) альфа-спираль
7) нуклеотид
8) пептидные связи

Проанализируйте таблицу «Уровни организации белка». Для каждой ячейки, обозначенной буквой, выберите соответствующий термин из предложенного списка.
1) глобула
2) двойная спираль
3) эфирные
4) гидрофильные
5) пептидные
6) нитчатая
7) вторичная
8) четвертичная
Известно, что белки – нерегулярные полимеры, имеющие высокую молекулярную массу, строго специфичны для каждого вида организма. Выберите из приведенного ниже текста три утверждения, по смыслу относящиеся к описанию этих признаков, и запишите цифры, под которыми они указаны. (1) В состав белков входит 20 различных аминокислот, соединенных пептидными связями. (2) Белки имеют различное количество аминокислот и порядок их чередования в молекуле. (3) Низкомолекулярные органические вещества имеют молекулярную массу от 100 до 1000. (4) Они являются промежуточными соединениями или структурными звеньями – мономерами. (5) Многие белки характеризуются молекулярной массой от нескольких тысяч до миллиона и выше, в зависимости от количества отдельных полипептидных цепей в составе единой молекулярной структуры белка. (6) Каждый вид живых организмов имеет особый, только ему присущий набор белков, отличающий его от других организмов.
§ 4. Структура и свойства белков
| Сайт: | Профильное обучение |
| Курс: | Биология. 11 класс |
| Книга: | § 4. Структура и свойства белков |
| Напечатано:: | Гость |
| Дата: | Пятница, 24 Декабрь 2021, 09:29 |
Оглавление
Белки *(протеины)* — это полипептиды, в состав молекул которых входит множество остатков аминокислот (до нескольких тысяч). * Белки — нерегулярные биополимеры.* Они различаются количеством аминокислотных звеньев, их составом и последовательностью расположения. При этом каждый белок имеет особый, присущий только ему порядок чередования аминокислот.
Уровни структурной организации белковых молекул. Для того чтобы белок мог выполнять свою биологическую функцию, его молекула должна иметь определенную пространственную конфигурацию. Различают четыре основных уровня организации белковых молекул — первичную, вторичную, третичную и четвертичную структуры (рис. 4.1).
Первичная структура белка — это строго определенная последовательность аминокислотных остатков в линейной полипептидной цепи. Каждый белок обладает уникальной первичной структурой. Ее существование обусловлено наличием прочных пептидных связей между остатками аминокислот. Все последующие, более сложные структуры формируются на основе первичной. Поэтому изменение первичной структуры (например, замена одних аминокислотных остатков на другие) приводит к изменению формы молекулы, свойств и функций белка.
Вторичная структура белка формируется за счет образования многочисленных водородных связей между атомами водорода NH-групп и атомами кислорода CO-групп разных аминокислотных остатков. Несмотря на то что эти связи слабее ковалентных, их количество обеспечивает стабильность вторичной структуры.
Чаще всего водородные связи возникают внутри одной полипептидной цепи между близко расположенными остатками аминокислот, что приводит к закручиванию этой цепи в так называемую α-спираль.
Иногда водородные связи возникают между относительно удаленными друг от друга участками полипептидной цепи (или нескольких разных цепей). *Данные участки могут располагаться параллельно (если полипептидные цепи идут в одном направлении, например, от N-конца к C-концу) либо антипараллельно (если цепи имеют противоположное направление: одна идет от N-конца к С-концу, а соседняя наоборот).* При этом формируется складчатая структура, напоминающая гармошку. Такой тип вторичной структуры получил название β-складчатый слой (см. рис. 4.1).
*α-спиральные и β-структурные участки белковой молекулы могут взаимодействовать друг с другом и между собой, образуя упорядоченные структуры (ансамбли). Например, α-спиральные фрагменты могут объединяться в двойные или тройные спирали. На основе β-участков часто образуются структуры, имеющие вид шпилек, арок, зигзагов и др. Участки, имеющие α- и β- строение, могут формировать ансамбли состава αβ, βαβ, βαβαβ и т. п. Эти пространственные конфигурации представляют собой так называемую сверхвторичную структуру белка.
Ансамбли сверхвторичной структуры являются основой для формирования в молекулах белков доменов. Это структурно и функционально обособленные области, соединенные друг с другом короткими фрагментами полипептидной цепи — шарнирными участками.
Например, молекулы мембранных белков-рецепторов чаще всего состоят из трех доменов. Надмембранный домен обеспечивает прием внешних сигналов, внутримембранный закрепляет белок в мембране, подмембранный осуществляет передачу сигнала внутрь клетки. Другим примером может служить сывороточный альбумин — белок плазмы крови, способный связываться с высшими карбоновыми кислотами, билирубином, некоторыми токсинами и другими соединениями и доставлять их в те или иные органы. Молекула этого белка содержит три домена, каждый из которых отвечает за избирательное связывание с определенными веществами.*
Многие белки способны выполнять свои биологические функции, обладая третичной структурой. Но некоторым белкам для этого необходимо объединение в единый комплекс двух или более молекул, имеющих третичную структуру. Так возникает четвертичная структура белка. Молекулы, входящие в ее состав *(их называют субъединицами или протомерами)*, могут быть одинаковыми или разными. Они удерживаются вместе благодаря различным видам нековалентных связей — водородным, ионным, гидрофобным взаимодействиям и др. В некоторых белках, например иммуноглобулинах, к множеству таких связей добавляются несколько ковалентных дисульфидных. Примером белка, имеющего четвертичную структуру, может служить гемоглобин (рис. 4.3).
Многообразие и свойства белков. В зависимости от состава различают простые и сложные белки. Молекулы простых белков построены только из аминокислотных остатков *(кератин, коллаген, фибрин, альбумины крови и др.)*. В состав сложных белков, кроме того, входит какой-либо компонент неаминокислотной природы *— так называемая простетическая группа. Более подробная информация о сложных белках приведена в таблице 4.1.*
*Таблица 4.1. Основные группы сложных белков
Название
Простетическая группа
Примеры
ДНК-полимераза (содержит Mg 2+ ),
трансферрин (содержит Fe 3+ )
Казеин молока, вителлин яичного желтка
Антитела ( иммуноглобулины ), муцин слюны
Тромбопластин, липопротеины клеточных мембран
Окрашенный небелковый компонент (пигмент)
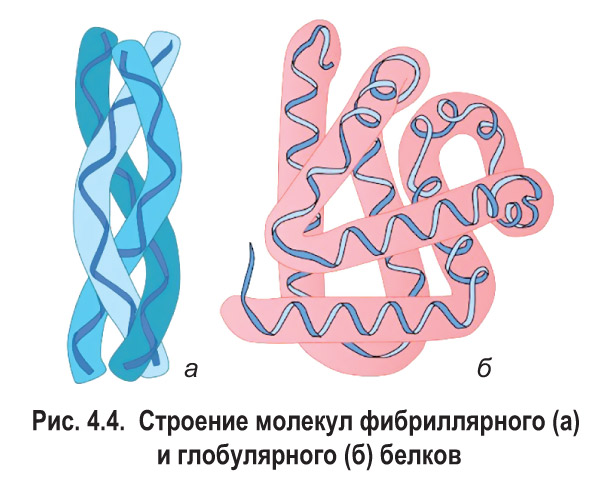
Многие белки хорошо растворяются в воде, однако среди них есть и нерастворимые — кератин, фибрин и др. Известно, что глобулярные белки в основном являются водорастворимыми, а фибриллярные, как правило, в воде не растворяются.
Белки чувствительны к внешним воздействиям: изменение химического состава среды, температуры и других факторов вызывает изменение их структуры и свойств. Действие высоких и низких температур, сильных кислот и щелочей, ионов тяжелых металлов, ультрафиолетового излучения, радиации ведет к разрушению связей, стабилизирующих пространственную конфигурацию белков. Вследствие разрыва водородных, ионных, дисульфидных и других связей белок может последовательно утратить свою четвертичную, третичную и даже вторичную структуру. Процесс нарушения природной структуры белка под влиянием внешних факторов без разрушения его первичной структуры называется денатурацией (рис. 4.5).

Пространственная структура белка определяет его физико-химические свойства и биологические функции. Поэтому денатурация приводит не только к изменению размеров и формы молекул белка, но и его свойств, например растворимости. Неполярные гидрофобные группы, которые располагались внутри молекулы, оказываются на ее поверхности, и белок становится менее гидрофильным. Важно то, что в результате денатурации белки теряют способность выполнять свои функции.
Степень денатурации белка зависит от силы воздействия на него различных факторов: чем интенсивнее их действие, тем глубже денатурация. В ряде случаев она становится необратимой. Однако если фактор, вызвавший денатурацию, действовал непродолжительно, то после прекращения его воздействия белок может восстановить свою природную структуру, свойства и функции. Такое явление называется ренатурацией. Развернутая полипептидная цепь способна самопроизвольно восстановить вторичную структуру, а затем уложиться в третичную. Это означает, что пространственная конфигурация белка определяется его первичной структурой, т. е. последовательностью аминокислотных остатков. Если же воздействие на белок было слишком жестким и привело к разрыву пептидных связей, возвращение белковой молекулы к исходной структуре становится невозможным.
*Большинство белков денатурирует при нагревании выше 50—60 °С. Но, например, денатурация сократительных белков мышц начинается уже при 45—50 °С, а яичный белок денатурирует при температуре 60—70 °С. Белки некоторых термофильных бактерий, обитающих в горячих источниках, могут полноценно функционировать при температурах выше 90 °С!
Явление денатурации широко используется в медицине, биохимических исследованиях, пищевой промышленности и других сферах деятельности человека.
Применение таких антисептиков, как спирт, хлорамин, формалин и т. п., основано на том, что они вызывают денатурацию белков и, вследствие этого, гибель микроорганизмов. То же самое происходит под действием высоких температур при стерилизации медицинских инструментов и материалов. Ультрафиолетовое излучение используется в качестве денатурирующего агента для дезинфекции помещений, промышленного обеззараживания воды и т. д.
Денатурацию белков может вызвать и присоединение к ним ионов тяжелых металлов. При этом они прочно связываются с выпадающим в осадок денатурированным белком. Поэтому при пищевом отравлении соединениями ртути, свинца, меди пострадавшему как можно быстрее дают выпить молоко или раствор яичного белка для того, чтобы ограничить дальнейшее всасывание токсичных веществ.
Осаждение белков при денатурации также применяется в лабораторной практике. Оно позволяет удалять белки из различных жидкостей биологического происхождения (например, плазмы крови, ликвора), что облегчает процессы выделения и анализа других веществ, входящих в состав таких жидкостей. Кроме того, осаждение белков используется для определения их количественного содержания в биологическом материале.
*Радикалы ряда аминокислот, входящих в состав белковой молекулы, содержат оснóвные и кислотные функциональные группы. Поэтому белки, как и аминокислоты, являются амфотерными соединениями. Амфотерность придает белкам буферные свойства.
Снижение кислотности среды усиливает диссоциацию групп —СООН. При этом высвобождаются дополнительные ионы водорода и заряд белковой молекулы становится отрицательным. Таким образом, белки способны в определенной степени поддерживать уровень рН среды. Например, альбумины и глобулины участвуют в поддержании слабощелочной реакции плазмы крови (совместно с другими буферными системами).*
*При определенном значении pH количество положительно и отрицательно заряженных групп в молекуле белка становится одинаковым, и его суммарный электрический заряд оказывается равным нулю. Такое значение pH называют изоэлектрической точкой белка (см. рис. 4.6). Каждый белок имеет определенное значение изоэлектрической точки, которое определяется аминокислотным составом. Изоэлектрические точки белков, в составе которых преобладают остатки кислых аминокислот, располагаются в области pH 7.
У большинства белков значение изоэлектрической точки находится в пределах 5,5—7,0. Но, например, для пепсина (фермента желудочного сока) величина изоэлектрической точки равна 1, а для сальмина (белка, содержащегося в молóках семги) — почти 12.
Чем больше значение рН среды отличается от изоэлектрической точки, тем больший заряд имеет белок. Из-за этого между белковыми молекулами существует электростатическое отталкивание, препятствующее их слипанию (агрегации). В изоэлектрической точке силы отталкивания минимальны. Из-за этого белки наименее устойчивы в растворе, их молекулы легко слипаются и выпадают в осадок.*
 | 1. Охарактеризуйте уровни структурной организации белков. Какие химические связи обусловливают существование и стабильность первичной, вторичной, третичной и четвертичной структур белков? 2. Чем простые белки отличаются от сложных? Фибриллярные от глобулярных? Приведите примеры фибриллярных и глобулярных белков. 3. Как называется процесс нарушения природной структуры белка, при котором сохраняется его первичная структура? Действие каких факторов может приводить к нарушению структуры белковых молекул? 4. За счет чего белки обладают буферными свойствами? Каким образом они участвуют в поддержании определенной кислотности среды? 5*. Докажите, что пространственная структура белка определяет его физико-химические свойства и биологические функции. Наблюдение денатурации белкаВспомните, как тепловая обработка влияет на цвет яичного белка и его растворимость в воде. Очевидно, что свойства белка изменяются вследствие его денатурации под действием высокой температуры.Налейте в стакан немного молока и добавьте в него 1—2 мл уксуса (лимонного сока или раствора лимонной кислоты).● Как изменилась растворимость казеина — основного молочного белка? ● Как вы думаете, что произошло с молекулами казеина? ● Подобное явление происходит и при обычном скисании молока. Вспомните, под воздействием каких микроорганизмов происходит этот процесс. Какое вещество является денатурирующим агентом? |









