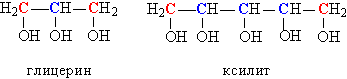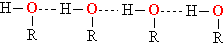Спирты
Классификация спиртов
Одноатомные спирты также подразделяются в зависимости от положения OH-группы: первичные (OH-группа у первичного атома углерода), вторичные (OH-группа у вторичного атома углерода) и третичные (OH-группа у третичного атома углерода).
Номенклатура и изомерия спиртов
Названия спиртов формируются путем добавления суффикса «ол» к названию алкана с соответствующим числом атомов углерода: метанол, этанол, пропанол, бутанол, пентанол и т.д.
Для спиртов характерна изомерия углеродного скелета (начиная с бутанола), положения функциональной группы и межклассовая изомерия с простыми эфирами, которых мы также коснемся в данной статье.
Получение спиртов
Присоединения молекулы воды (HOH) протекает по правилу Марковникова. Атом водорода направляется к наиболее гидрированному атому углерода, а гидроксогруппа идет к соседнему, наименее гидрированному, атому углерода.
В результате восстановления альдегидов и кетонов получаются соответственно первичные и вторичные спирты.
Синтез газом в промышленности называют смесь угарного газа и водорода, которая используется для синтеза различных химических соединений, в том числе и метанола.
В ходе брожения глюкозы выделяется углекислый газ и образуется этанол.
Химические свойства спиртов
Щелочные металлы (Li, Na, K) способны вытеснять водород из спиртов с образованием солей: метилатов, этилатов, пропилатов и т.д.
Необходимо особо заметить, что реакция с щелочами (NaOH, KOH, LiOH) для предельных одноатомных спиртов невозможна, так как образующиеся алкоголяты (соли спиртов) сразу же подвергаются гидролизу.
Реакция с галогеноводородами протекают как реакции обмена: атом галогена замещает гидроксогруппу, образуется молекула воды.
В результате реакций спиртов с кислотами образуются различные эфиры.
Дегидратация спиртов (отщепление воды) идет при повышенной температуре в присутствии серной кислоты (водоотнимающего) компонента.
Качественной реакцией на спирты является взаимодействие с оксидом меди II. В ходе такой реакции раствор приобретает характерное фиолетовое окрашивание.
Замечу, что в обычных условиях третичные спирты окислению не подвергаются. Для них необходимы очень жесткие условия, при которых углеродный скелет подвергается деструкции.
Вторичные и третичные спирты определяются другой качественной реакцией с хлоридом цинка II и соляной кислотой. В результате такой реакции выпадает маслянистый осадок.
Такой реакцией является взаимодействие многоатомного спирта со свежеприготовленным гидроксидом меди II. В результате реакции раствор окрашивается в характерный синий цвет.
Важным отличием многоатомных спиртов от одноатомных является их способность реагировать со щелочами (что невозможно для одноатомных спиртов). Это говорит об их более выраженных кислотных свойствах.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
СПИРТЫ
СПИРТЫ (алкоголи) – класс органических соединений, содержащих одну или несколько группировок С–ОН, при этом гидроксильная группа ОН связана с алифатическим атомом углерода (соединения, у которых атом углерода в группировке С–ОН входит в состав ароматического ядра, называются фенолами)
Классификация спиртов разнообразна и зависит от того, какой признак строения взят за основу.
1. В зависимости от количества гидроксильных групп в молекуле спирты делят на:
а) одноатомные (содержат одну гидроксильную ОН-группу), например, метанол СН3ОН, этанол С2Н5ОН, пропанол С3Н7ОН
б) многоатомные (две и более гидроксильных групп), например, этиленгликоль
Соединения, в которых у одного атома углерода 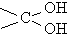
Спирты, содержащие три группы ОН у одного атома углерода 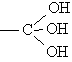
2. По типу атома углерода, с которым связана группа ОН, спирты делят на:
а) первичные, у которых ОН-группа связана с первичным атомом углерода. Первичным называют атом углерода (выделен красным цветом), связанный всего с одним углеродным атомом. Примеры первичных спиртов – этанол СH3–CH2–OH, пропанол СH3–CH2–CH2–OH.
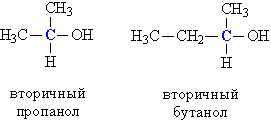
б) вторичные, у которых ОН-группа связана с вторичным атомом углерода. Вторичный атом углерода (выделен синим цветом) связан одновременно с двумя атомами углерода, например, вторичный пропанол, вторичный бутанол (рис. 1).
Рис. 1. СТРОЕНИЕ ВТОРИЧНЫХ СПИРТОВ
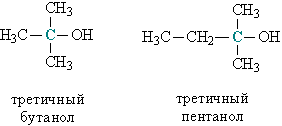
в) третичные, у которых ОН-группа связана с третичным атомом углерода. Третичный углеродный атом (выделен зеленым цветом) связан одновременно с тремя соседними атомами углерода, например, третичный бутанол и пентанол (рис. 2).
Рис. 2. СТРОЕНИЕ ТРЕТИЧНЫХ СПИРТОВ
В соответствии с типом углеродного атома присоединенную к нему спиртовую группу также называют первичной, вторичной или третичной.
У многоатомных спиртов, содержащих две или более ОН-групп, могут присутствовать одновременно как первичные, так и вторичные НО-группы, например, в глицерине или ксилите (рис. 3).
Рис. 3. СОЧЕТАНИЕ В СТРУКТУРЕ МНОГОАТОМНЫХ СПИРТОВ ПЕРВИЧНЫХ И ВТОРИЧНЫХ ОН-ГРУПП.
3. По строению органических групп, связанных ОН-группой, спирты подразделяют на предельные (метанол, этанол, пропанол), непредельные, например, аллиловый спирт СН2=СН–СН2–ОН, ароматические (например, бензиловый спирт С6Н5СН2ОН), содержащие в составе группы R ароматическую группу.
Непредельные спирты, у которых ОН-группа «примыкает» к двойной связи, т.е. связана с атомом углерода, участвующим одновременно в образовании двойной связи (например, виниловый спирт СН2=СН–ОН), крайне нестабильны и сразу же изомеризуются (см. ИЗОМЕРИЗАЦИЯ) в альдегиды или кетоны:
Номенклатура спиртов.
Для распространенных спиртов, имеющих простое строение, используют упрощенную номенклатуру: название органической группы преобразуют в прилагательное (с помощью суффикса и окончания «овый») и добавляют слово «спирт»:
| СН3ОН | метиловый спирт |
| С2Н5ОН | этиловый спирт |
| (Н3С)2СНОН | изопропиловый спирт |
| С4Н9ОН | бутиловый спирт |
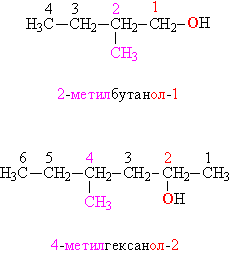
В том случае, когда строение органической группы более сложное, используют общие для всей органической химии правила. Названия, составленные по таким правилам, называют систематическими. В соответствии с этими правилами, углеводородную цепь нумеруют с того конца, к которому ближе расположена ОН-группа. Далее используют эту нумерацию, чтобы указать положение различных заместителей вдоль основной цепи, в конце названия добавляют суффикс «ол» и цифру, указывающую положение ОН-группы (рис. 4):
Рис. 4. СИСТЕМАТИЧЕСКИЕ НАЗВАНИЯ СПИРТОВ. Функциональные (ОН) и замещающие (СН3) группы, а также соответствующие им цифровые индексы выделены различающимися цветами.
Систематические названия простейших спиртов составляют по тем же правилам: метанол, этанол, бутанол. Для некоторых спиртов сохранились тривиальные (упрощенные) названия, сложившиеся исторически: пропаргиловый спирт НС є С–СН2–ОН, глицерин HO–СH2–СН(ОН)–CH2–OH, пентаэритрит С(СН2ОН)4, фенетиловый спирт С6Н5–CH2–CH2–OH.
Физические свойства спиртов.
Спирты растворимы в большинстве органических растворителей, первые три простейших представителя – метанол, этанол и пропанол, а также третичный бутанол (Н3С)3СОН – смешиваются с водой в любых соотношениях. При увеличении количества атомов С в органической группе начинает сказываться гидрофобный (водоотталкивающий) эффект, растворимость в воде становится ограниченной, а при R, содержащем свыше 9 атомов углерода, практически исчезает.
Благодаря наличию ОН-групп между молекулами спиртов возникают водородные связи.
Рис. 5. ВОДОРОДНЫЕ СВЯЗИ В СПИРТАХ (показаны пунктиром)
В результате у всех спиртов более высокая температура кипения, чем у соответствующих углеводородов, например, Т. кип. этанола +78° С, а Т. кип. этана –88,63° С; Т. кип. бутанола и бутана соответственно +117,4° С и –0,5° С.
Химические свойства спиртов.
Спирты отличаются разнообразными превращениями. Реакции спиртов имеют некоторые общие закономерности: реакционная способность первичных одноатомных спиртов выше, чем вторичных, в свою очередь, вторичные спирты химически более активны, чем третичные. Для двухатомных спиртов, в том случае, когда ОН-группы находятся у соседних атомов углерода, наблюдается повышенная (в сравнении с одноатомными спиртами) реакционная способность из-за взаимного влияния этих групп. Для спиртов возможны реакции, проходящие с разрывом как С–О, так и О–Н – связей.
1. Реакции, протекающие по связи О–Н.
При взаимодействии с активными металлами (Na, K, Mg, Al) спирты проявляют свойства слабых кислот и образуют соли, называемые алкоголятами или алкоксидами:
Алкоголяты химически не стабильны и при действии воды гидролизуются с образованием спирта и гидроксида металла:
Эта реакция показывает, что спирты в сравнении с водой представляют собой более слабые кислоты (сильная кислота вытесняет слабую), кроме того, при взаимодействии с растворами щелочей спирты не образуют алкоголяты. Тем не менее, в многоатомных спиртах (в том случае, когда ОН-группы присоединены к соседним атомам С) кислотность спиртовых групп намного выше, и они могут образовывать алкоголяты не только при взаимодействии с металлами, но и со щелочами:
Когда в многоатомных спиртах НО-группы присоединены к не соседствующим атомам С, свойства спиртов близки к одноатомным, поскольку взаимовлияние НО-групп не проявляется.
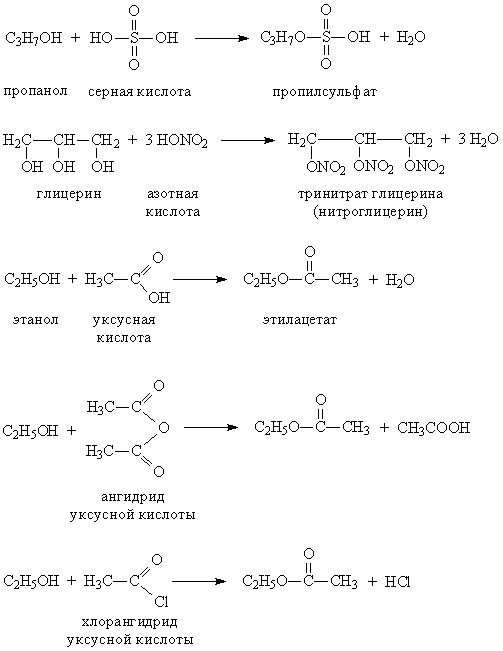
При взаимодействии с минеральными или органическими кислотами спирты образуют сложные эфиры – соединения, содержащие фрагмент R–O–A (А – остаток кислоты). Образование сложных эфиров происходит и при взаимодействии спиртов с ангидридами и хлорангидридами карбоновых кислот (рис. 6).
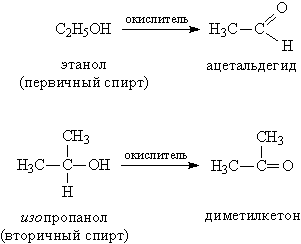
При действии окислителей (К2Cr2O7, KMnO4) первичные спирты образуют альдегиды, а вторичные – кетоны (рис.7)
Рис. 7. ОБРАЗОВАНИЕ АЛЬДЕГИДОВ И КЕТОНОВ ПРИ ОКИСЛЕНИИ СПИРТОВ
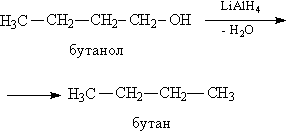
Восстановление спиртов приводит к образованию углеводородов, содержащих то же количество атомов С, что молекула исходного спирта (рис.8).
Рис. 8. ВОССТАНОВЛЕНИЕ БУТАНОЛА
2. Реакции, протекающие по связи С–О.
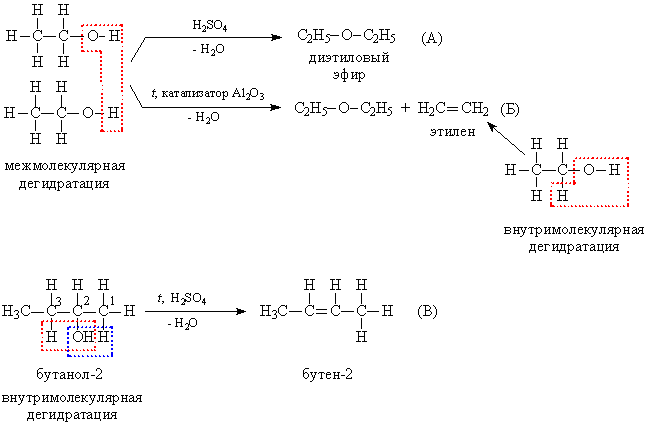
В присутствии катализаторов или сильных минеральных кислот происходит дегидратация спиртов (отщепление воды), при этом реакция может идти в двух направлениях:
а) межмолекулярная дегидратация с участием двух молекул спирта, при этом связи С–О у одной из молекул разрываются, в результате образуются простые эфиры – соединения, содержащие фрагмент R–О–R (рис. 9А).
В случае вторичных спиртов при образовании алкена возможны два направления реакции (рис. 9В), преимущественное направление то, при котором в процессе конденсации отщепляется водород от наименее гидрогенизированного атома углерода (отмечен цифрой 3), т.е. окруженного меньшим количеством атомов водорода (в сравнении с атомом 1). Показанные на рис. 10 реакции используют для получения алкенов и простых эфиров.
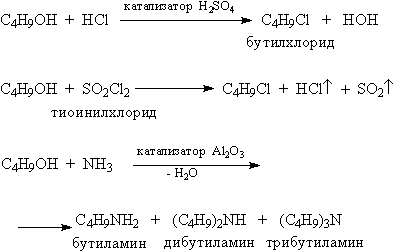
Разрыв связи С–О в спиртах происходит также при замещении ОН-группы галогеном, или аминогруппой (рис. 10).
Рис. 10. ЗАМЕНА ОН-ГРУППЫ В СПИРТАХ ГАЛОГЕНОМ ИЛИ АМИНОГРУППОЙ
Реакции, показанные на рис. 10, используют для получения галогенуглеводородов и аминов.
Получение спиртов.
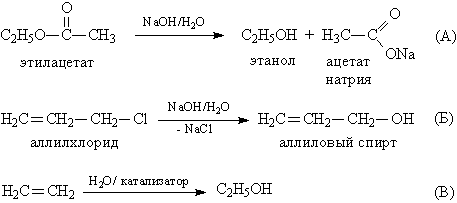
Некоторые из показанных выше реакций (рис. 6,9,10) обратимы и при изменении условий могут протекать в противоположном направлении, приводя к получению спиртов, например при гидролизе сложных эфиров и галогенуглеводородов (рис.11А и Б, соответственно), а также гидратацией алкенов – присоединением воды (рис.11В).
Рис. 11. ПОЛУЧЕНИЕ СПИРТОВ ГИДРОЛИЗОМ И ГИДРАТАЦИЕЙ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Реакция гидролиза алкенов (рис. 11, схема В) лежит в основе промышленного производства низших спиртов, содержащих до 4 атомов С.
Этанол образуется и при так называемом спиртовом брожении сахаров, например, глюкозы С6Н12О6. Процесс протекает в присутствии дрожжевых грибков и приводит к образованию этанола и СО2:
Брожением можно получить не более чем 15%-ный водный раствор спирта, поскольку при более высокой концентрации спирта дрожжевые грибки погибают. Растворы спирта более высокой концентрации получают перегонкой.
Метанол получают в промышленности восстановлением монооксида углерода при 400 ° С под давлением 20–30 МПа в присутствии катализатора, состоящего из оксидов меди, хрома, и алюминия:
Если вместо гидролиза алкенов (рис. 11) проводить окисление, то образуются двухатомные спирты (рис. 12)
Рис. 12. ПОЛУЧЕНИЕ ДВУХАТОМНЫХ СПИРТОВ
Применение спиртов.
Способность спиртов участвовать в разнообразных химических реакциях позволяет их использовать для получения всевозможных органических соединений: альдегидов, кетонов, карбоновых кислот простых и сложных эфиров, применяемых в качестве органических растворителей, при производстве полимеров, красителей и лекарственных препаратов.
Этанол С2Н5ОН – исходное соединение для получения ацетальдегида, уксусной кислоты, а также для производства сложных эфиров карбоновых кислот, используемых в качестве растворителей. Кроме того, этанол – основной компонент всех спиртных напитков, его широко применяют и в медицине как дезинфицирующее средство.
Бутанол используют как растворитель жиров и смол, кроме того, он служит сырьем для получения душистых веществ (бутилацетата, бутилсалицилата и др.). В шампунях он используется как компонент, повышающий прозрачность растворов.
Фенетиловый спирт С6Н5–CH2–CH2–OH обладает запахом розы, содержится в розовом масле, его используют в парфюмерии.
Этиленгликоль HOCH2–CH2OH используют в производстве пластмасс и как антифриз (добавка, снижающая температуру замерзания водных растворов), кроме того, при изготовлении текстильных и типографских красок.
Диэтиленгликоль HOCH2–CH2OCH2–CH2OH используют для заполнения тормозных гидравлических приспособлений, а также в текстильной промышленности при отделке и крашении тканей.
Глицерин HOCH2–CH(OH)–CH2OH применяют для получения полиэфирных глифталевых смол, кроме того, он является компонентом многих косметических препаратов. Нитроглицерин (рис. 6) – основной компонент динамита, применяемого в горном деле и железнодорожном строительстве в качестве взрывчатого вещества.
Пентаэритрит (HOCH2)4С применяют для получения полиэфиров (пентафталевые смолы), в качестве отвердителя синтетических смол, как пластификатор поливинилхлорида, а также в производстве взрывчатого вещества тетранитропентаэритрита.
Многоатомные спирты ксилит НОСН2–(СНОH)3–CН2ОН и сорбит НОСН2– (СНОН)4–СН2OН имеют сладкий вкус, их используют вместо сахара в производстве кондитерских изделий для больных диабетом и людей страдающих от ожирения. Сорбит содержится в ягодах рябины и вишни.
Спирты
Карточка контроля знаний (скачать PDF 255КБ)
Спирты – производные углеводородов, в молекулах которых есть одна или несколько гидроксильных групп (ОН-), непосредственно связанных с атомом углерода в углеводородном радикале.
Классификация спиртов
Спирты классифицируются по разным структурным признакам:
1) По числу гидроксильных групп:
— одноатомные спирты – спирты, у которых имеется одна гидроксильная группа;
— многоатомные – спирты, имеющие несколько гидроксильных групп: например, двухатомные спирты (гликоли), трёхатомные спирты (глицерины) и т.д.;
2) В зависимости от насыщенности углеводородного заместителя:
— предельные (насыщенные) спирты, содержащие в молекуле лишь предельные углеводородные радикалы, например: метанол СН3ОН, этанол CH3 – CH2OH.
— непредельные (ненасыщенные) спирты, содержащие в молекуле кратные (двойные и тройные) связи между атомами углерода, например:
пропен-2-ол-1 (аллиловый спирт) CH2 = СН – CH2OH.
— ароматические спирты, содержащие в молекуле бензольное кольцо и гидроксильную группу, связанные друг с другом не непосредственно, а через атомы углерода, например:
3) В зависимости от наличия или отсутствия цикла в углеводородном заместителе:
— ациклические (алифатические) спирты (этанол);
— алициклические спирты (циклогексанол).
4) В зависимости от числа заместителей при α-углеродном атоме:
Номенклатура
CH3ОН метанол (метиловый спирт)
CH2OH – CH3 этанол (этиловый спирт)
В том случае, когда строение органической группы более сложное, используют общие для всей органической химии правила: углеводородную цепь нумеруют с того конца, к которому ближе расположена ОН-группа. Далее используют эту нумерацию, чтобы указать положение различных заместителей вдоль основной цепи, в конце названия добавляют суффикс «ол» и цифру, указывающую положение ОН-группы:
Изомерия спиртов
1) Структурная изомерия
а) Положения функциональной группы (начинается с третьего члена гомологического ряда)
пропанол-1 (пропиловый спирт) пропанол-2 (изопропиловый спирт)
б) Изомерия углеродного скелета (начинается с четвертого члена гомологического ряда)
бутанол- 1 2-метилпропанол-1
в) Межклассовая изомерия (начинается со второго члена гомологического ряда) – спирты изомерны простым эфирам:
этанол (этиловый спирт) диметиловый эфир
2) Пространственная изомерия – оптическая (зеркальная).
Например, бутанол-2 СH3 – CH(OH) – СH2 – CH3, в молекуле которого второй атом углерода (выделен цветом) связан с четырьмя различными заместителями, существует в форме двух зеркальных изомеров.
Физические свойства спиртов
Низшие и средние члены ряда предельных одноатомных спиртов, содержащие от одного до одиннадцати атомов углерода, – жидкости. Высшие спирты (начиная с С12Н25ОН) при комнатной температуре – твёрдые вещества. Низшие спирты имеют характерный алкогольный запах и жгучий вкус, хорошо растворимы в воде. Растворимость в воде зависит от молекулярной массы, чем она выше, тем спирт хуже растворяется воде. Так, низшие спирты (до пропанола) смешиваются с водой в любых пропорциях, а высшие практически не растворимы в ней. Например, октанол-1 растворяется лишь в пропорции 1 мл в 2 л воды. Температура кипения также возрастает с увеличением атомной массы, например, tкип.СН3ОН 65°С, а tкип.С2Н5ОН 78°С. Чем выше температура кипения, тем ниже летучесть, т.е. вещество плохо испаряется. Данные физические свойства насыщенных спиртов с одной гидроксильной группой можно объяснить возникновением межмолекулярной водородной связи между отдельными молекулами самого соединения или спирта и воды.
При всей пользе этиленгликоля нужно учитывать, это очень сильный яд!
Глицерин представляет собой вязкую бесцветную жидкость, сладковатую на вкус. Он очень хорошо растворим в воде, кипит при температуре 220 0 C. Его химическая формула CH2OH–СНОН–CH2OH – это трёхатомный спирт.
Строение спиртов
Что такое Спирт?
Спирт представляет собой гомологичный ряд, в котором соединения содержат функциональную группу, называемую гидроксильной группой (-ОН). Общая молекулярная формула для спиртов: CnH2n+1OH. Спирты — это все производные углеводородов, в которых один или несколько атомов водорода в углеводороде замещены гидроксильной группой. Гидроксильная группа также отвечает за придание соединению определенных химических и/или физических свойств.
Спирты — это органические соединения, которые характеризуются наличием одной, двух или более гидроксильных групп (- OH), которые присоединены к атому углерода в алкильной группе или углеводородной цепи. Спирты рассматриваются как производные воды, где один из атомов водорода заменяется алкильной группой. Спирты также имеют различные структуры и формы. Они являются одним из наиболее часто встречающихся органических соединений. Спирты используются в различных отраслях промышленности, например в пищевой из этилового спирта производят алкогольные напитки, в медицине из этилового спирта и изопропилового спирта производят антисептики.
Содержание
Четырьмя наиболее распространенными спиртами, которые также являются простейшими, являются метанол (CH3OH), этанол (C2H5OH), пропанол (C3H7OH) и бутанол (C4H9OH).

Далее, по порядку, спирты идут следующие: Пентанол (C5H11OH), Гексанол (C6H13OH), Гептанол (C7H15OH), Октанол ( C8H17 OH), Нонанол (C9H19OH), Деканол (C10H21OH)
Названия спиртов имеют в соответствии с алкановой основой. Если гидроксильная (-ОН) группа присоединена к основной цепи метана, соединение называется метанолом или метиловым спиртом. Если основой является бутан, образующийся спирт является бутанолом. Таким образом, чтобы получить название спирта, берётся название углеводородного основы и добавляется «ол».
Спирты подразделяются на различные группы в зависимости от того, где в молекуле находится гидроксильная группа. это приводит к некоторым различиям в химических свойствах.
Первичные спирты. В первичном спирте углерод с гидроксильной группой присоединен только к одной алкильной группе. Некоторые примеры первичных спиртов:

Метанол является исключением из этого. Это все еще первичный спирт, даже если углерод, к которому присоединена гидроксильная группа, не имеет другой алкильной группы, присоединенной к нему.
Вторичные спирты. Во вторичном спирте углерод с гидроксильной группой присоединен к двум алкильным группам. Некоторые примеры вторичных спиртов:
Третичные спирты. В третичном спирте углерод с гидроксильной группой присоединен к трем другим алкильным группам. Некоторые примеры третичных спиртов:
Наиболее распространенные спирты:
| Химическая формула | Химическое название | Распространенное название |
| Одноатомные спирты | ||
| CH3OH | Метанол | Метиловый спирт |
| C2H5OH | Этанол | Этиловый Спирт |
| C3H7OH | Пропанол-2 | Изопропиловый спирт |
| C4H10O | 2-метилпропанол-1 | Изобутиловый спирт |
| C5H11OH | Пентанол | Амиловый спирт |
| C16H33OH | Гексадеканол-1 | Цетиловый спирт |
| Многоатомные спирты | ||
| C2H4(OH)2 | Этандиол-1,2 | Этиленгликоль |
| C3H5(OH)3 | Пропантриол-1,2,3 | Глицерин |
| C4H6(OH)4 | Бутантетраол-1,2,3,4 | Эритритол |
| C5H7(OH)5 | Пентанпентол-1,2,3,4,5 | Ксилит |
| C6H8(OH)6 | Гексангексол-1,2,3,4,5,6 | Маннит, сорбит |
| C7H9(OH)7 | Гептангептол-1,2,3,4,5,6,7 | Волемитол |
| Ненасыщенные алифатические спирты | ||
| C3H5OH | Пропен-2-ол-1 | Аллиловый спирт |
| C10H17OH | α: (2E)-3,7-диметил-2,7-октадиен-1-ол β: (2E)-3,7-диметил-2,6-октадиен-1-ол | Гераниол |
| C3H3OH | 2-пропин-1-ол | Пропаргиловый спирт |
| Алициклические спирты | ||
| C6H6(OH)6 | Циклогексан-1,2,3,4,5,6-гексол | Инозитол |
| C10H19OH | 2-(2-пропил)-5-метилциклогексан-1-ол | Ментол |
Свойства спиртов
Физические свойства
Растворимость в воде. Спирты растворимы в воде. Это связано с гидроксильной группой в спирте, которая способна образовывать водородные связи с молекулами воды. Спирты с меньшей углеводородной цепью хорошо растворимы. По мере увеличения длины углеводородной цепи растворимость в воде уменьшается. С четырьмя атомами углерода в углеводородной цепи и выше, снижение растворимости становится видимым, когда смесь образует два несмешивающихся слоя жидкости. Причина, по которой растворимость уменьшается с увеличением длины углеводородной цепи, заключается в том, что для преодоления водородных связей между молекулами спирта требуется больше энергии, поскольку молекулы более плотно упаковываются вместе по мере увеличения размера и массы.
Точка кипения. Этот график показывает сравнение температур кипения метана с метанолом, этана с этанолом, пропана с пропанолом и бутана с бутанолом.
Из графика видно, что температура кипения спирта всегда намного выше, чем температура кипения соответствующего алкана с той же углеводородной цепью. Температура кипения спиртов также увеличивается с увеличением длины углеводородной цепи.
Причина, по которой спирты имеют более высокую температуру кипения, чем алканы, заключается в том, что межмолекулярные силы спиртов представляют собой водородные связи, в отличие от алканов с ван-дер-ваальсовыми силами в качестве их межмолекулярных сил.
Спирты превращаются из жидкости в твердое вещество при комнатной температуре и давлении по мере увеличения длины углеводородной цепи в спирте.

Факторами, влияющими на температуры кипения/плавления спиртов, являются не только водородные связи, но также и дисперсионные силы Ван-дер-Ваальса и диполь-дипольные взаимодействия. Водородные связи и диполь-дипольные взаимодействия остаются относительно одинаковыми во всем ряду спиртов. Дисперсионные силы Ван-дер-Ваальса увеличиваются с увеличением длины углеводородной цепи. Это связано с увеличением числа электронов в молекулах, что, в свою очередь, увеличивает силу и размер временно индуцированного диполь-дипольного притяжения. Следовательно, для преодоления межмолекулярных сил требуется больше энергии, что приводит к увеличению температур кипения/плавления.
Вязкость. Вязкость — это свойство жидкости, которая противостоит силе, стремящейся заставить жидкость течь. Вязкость спиртов увеличивается с увеличением размера молекул. Это потому, что сила межмолекулярных сил увеличивается, сильнее удерживая молекулы на месте.
Полярность. Амид> кислота> Алкоголь> Кетон
Альдегид> Амин> Сложный эфир> Эфир> Алкан
Амид является наиболее полярным, в то время как алкан является наименее полярным. Спирты занимают третье место по полярности благодаря своим возможностям водородной связи и присутствию одного атома кислорода в молекуле спирта. Карбоновые кислоты являются более полярными, чем спирты, поскольку в молекуле карбоновой кислоты присутствуют два атома кислорода.
Воспламеняемость. Воспламеняемость спиртов уменьшается с увеличением размера и массы молекул. Сгорание разрушает ковалентные связи молекул, поэтому, когда размер и масса молекул увеличиваются, появляется больше ковалентных связей, чтобы разжечь этот спирт. Следовательно, для разрушения связей требуется больше энергии, поэтому воспламеняемость спиртов уменьшается с увеличением размера и массы молекул.
Химические свойства
Горение. Спирты сгорают в кислороде с образованием углекислого газа и воды. Спирты горят чисто и легко и не дают сажи. С увеличением количества молекул сжигать спирты становится все труднее. Общее молекулярное уравнение реакции:
CnH2n+1OH + (1.5n)O2 → (n+1)H2O + nCO2
Реакция сжигание этанола: C2H5OH (l) + 3 O2 (g) → 2 CO2 (g) + 3 H2O (g); (ΔHc = −1371 кДж/моль)
Дегидратация. Дегидратация спирта происходит до алкена.
Дегидратация спиртов осуществляют путем нагревания с концентрированной серной кислотой, которая действует как дегидратирующий агент, при 180 °C. Эту реакцию спиртов используют для получения соответствующих алкенов и воды в качестве побочного продукта, например, для дегидратации этанола.
Окисление. Окисление — спирта происходит до карбоновой кислоты. Спирты могут окисляться в карбоновые кислоты.
например, реакция окисление этанола выглядит следующим образом: C2H5OH + [O] → CH3COOH + H2O
Окисление можно проводить с использованием окислителей, таких как подкисленный дихромат калия (VI), подкисленный марганат калия (VII) или атмосферный кислород.
Этанол, если его оставить на воздухе, может окислиться и стать этановой кислотой. Например, вино становится кислым, так как содержание алкоголя в этаноле окисляется кислородом воздуха.
Этерификация. Спирты могут реагировать с карбоновой кислотой с образованием сложных эфиров. Подробнее об этом будет рассказано в разделе Формирование сложных эфиров.
Получение спиртов
Ферментация. Спирты могут быть получены с помощью процесса ферментации (брожения). Ферментация обычно осуществляется с помощью дрожжей, которые воздействуют на углеводы и производят этанол и углекислый газ. Для реакции с дрожжами обычно используются картофель, зерно, рис, солод и фрукты, которые являются богатыми источниками углеводов. Например, реакция превращения глюкозы в этанол выглядит следующим образом: C6H12O6 → 2C2H5OH + 2CO2
Условия для ферментации должны быть следующие:
Гидратация от алкенов. Спирты могут образовываться при взаимодействии алкенов с водой. Гидратация является реакцией сложения, т.е. осуществляется с помощью присоединения молекул воды к молекулам вещества или его ионам. Например, реакция гидратации этена до этанола выглядит следующим образом: C2H4 + H2O → C2H5OH

Условия для гидратации должны быть следующие:
Примечание: для получения чистого этанола после гидратации используется фракционная перегонка для отделения фосфорной кислоты, которая имеет температуру кипения 158 °C, и этанола, который имеет температуру кипения 78 °C.
Использование спирта
Использование в алкогольных напитках. Этиловый спирт используется в качестве ингредиента в алкогольных напитках, например, в вине и пиве.

Используется для производства метилированного спирта. Метилированный спирт — это этанол, смешанный с небольшим количеством метанола, который ядовит, что делает его непригодным для употребления. Кроме того метилированный спирт является горючим, поэтому его можно используют в лампах и горелках, например в горелках для кемпинга. Ещё одно применение метилированного спирта, это использование его для удаления чернил с непористых поверхностей. Например, удаление чернил с металлических и пластмассовых поверхностей. Метилированный спирт чато используется в качестве компонента в бытовых чистящих средствах, а также в стеклоочистителях.
Используется в качестве топлива. Этанол сгорает в чистом виде с образованием диоксида углерода и воды. Использование этанола в качестве топлива вносит большой вклад в защиту от загрязнения окружающей среды. Для получения экологичного топлива этанол смешивают с бензином, в котором содержание этанола составляет около 10-20%. Использование этанола в качестве топлива снижает нашу зависимость от природных ископаемых углеводородов, используемых для производства бензина и дизельного топлива.
Используется в качестве растворителя. Этанол является хорошим растворителем и очень часто он используется для растворения органических соединений, которые нерастворимы в воде. Например, он используется в косметике, такой как парфюмерия; используется в медикаментах, таких как дезинфицирующие средства; используется в туалетных принадлежностях, таких как лосьоны после бритья. Преимущества этанола в качестве растворителя в том, что он летуч, бесцветен и имеет относительно высокую температуру кипения — 78 °С. Кроме того, он смешивается как с водой, так и с другими органическими растворителями.