О Спутник Лайт
О «Спутник Лайт»
«Спутник Лайт» является первым компонентом (рекомбинантный аденовирус человека 26 серотипа (rАd26)) вакцины «Спутник V» — первой в мире зарегистрированной вакцины против коронавируса.
Вакцина «Спутник Лайт», как и «Спутник V» создана на проверенной и хорошо изученной платформе аденовирусных векторов человека, которые вызывают обычную простуду и с которыми человечество мирно сосуществует тысячелетиями.
Безопасность вакцины «Спутник Лайт», первого компонента «Спутника V», подтверждена реальными данными по вакцинации в ОАЭ, Бахрейне, Аргентине, России, Мексике, Сербии, Сан-Марино, Филиппинах, Ливии, Парагвае, Венгрии, Азербайджане и Беларуси.
доказанная эффективность против заражения,
выше, чем у большинства зарубежных двухдозных вакцин
Эффективность против госпитализации и тяжелых случаев еще выше
«Спутник Лайт» — идеальный бустер:
«Спутник Лайт», как отдельная вакцина, высокоэффективен против Дельта и других новых штаммов COVID-19
эффективность против
заражения штаммом Дельта
эффективность для
возрастной группы до 60 лет
выше, чем у большинства зарубежных двухдозных вакцин
В качестве бустера защита «Спутника Лайт» против штамма Дельта приближается к защите Спутник V
эффективность
против заражения
эффективность
против госпитализации
«Спутник Лайт» обеспечивает длительную защиту, которая даже увеличивается в течение 4-6 месяцев после вакцинации.
В течение того же периода эффективность других зарубежных вакцин против штамма Дельта значительно снижается до уровня ниже 50%.
Безопасность и эффективность «Спутник Лайт» подтверждена реальными данными по вакцинации во многих странах, а также более чем 20 публикациями в ведущих международных научных изданиях.
«Спутник Лайт», первый компонент Спутник V – одна из ключевых вакцин в рамках программы иммунизации в Аргентине
Источник: JHU CSSE COVID-19 Data
Фаза I/II исследования безопасности и иммуногенности «Спутник Лайт» продемонстрировала следующие результаты:




Находясь на настоящем сайте, пользователь принимает
и присоединяется к положениям политики конфиденциальности
О Спутник V
О Спутник V
«Спутник V» — первая в мире зарегистрированная вакцина на основе хорошо изученной платформы вектора аденовируса человека. Она одобрена в 71 стране с общим населением 4 млрд человек.
Вакцина названа в честь первого советского космического спутника. Запуск «Спутника-1» в 1957 году дал новый импульс космическим исследованиям во всем мире, создав так называемый «момент Спутника» для мирового сообщества.
Эффективность вакцины составляет 97,6% по результатам анализа данных о заболеваемости коронавирусом среди россиян, привитых обоими компонентами препарата в период с 5 декабря 2020 года по 31 марта 2021 года.
Фаза 1 и 2 клинических испытаний вакцины были завершены 1 августа 2020 года. Итоги третьей фазы клинических испытаний в России опубликованы в журнале Lancet 2 февраля 2021 года. Клинические испытания третьей фазы «Спутник V» также успешно проходят в ОАЭ, Индии, Венесуэле и Беларуси.
Вакцина «Спутник V» создана на проверенной и хорошо изученной платформе аденовирусных векторов человека, которые вызывают обычную простуду и с которыми человечество сталкивалось на протяжении тысячелетий.
В вакцине «Спутник V» впервые среди вакцин против коронавируса был применен подход гетерогенного бустирования, в основе которого лежит применение двух разных векторов для двух уколов в процессе вакцинации. Такой подход формирует более стойкий иммунитет по сравнению с вакцинами, которые используют одинаковый механизм доставки для обоих уколов.
Безопасность, эффективность и отсутствие долгосрочных негативных последствий у аденовирусных вакцин доказаны в более чем 250 клинических исследованиях на протяжении двух десятилетий.
«Спутник V» не вызывает сильной аллергии.
Температура хранения на уровне +2+8 градусов Цельсия позволяет хранить вакцину в обычном холодильнике без необходимости инвестиций в дополнительную инфраструктуру холодовой цепи.
Как работают вакцины на основе аденовирусного вектора
«Векторы» являются носителями, которые могут доставить генетический материал из другого вируса в клетку. При этом генетический материал аденовируса, который вызывает инфекцию, удаляется и вставляется материал с кодом белка от другого вируса, в данном случае от шипа коронавируса. Этот новый элемент безопасен для организма, но он помогает иммунной системе реагировать и вырабатывать антитела, которые защищают от инфекции.
Технологическая платформа векторов на основе аденовирусов упрощает и ускоряет создание новых вакцин путем модификации исходного вектора-носителя генетическим материалом из новых появляющихся вирусов, что позволяет получать новые вакцины в сжатые сроки. Такие вакцины вызывают сильный ответ со стороны иммунной системы человека.
Человеческие аденовирусы считаются одними из самых простых для модификации, поэтому они стали очень популярными в качестве векторов.
Преимущества прайм-буст иммунизации

Безопасность и эффективность
После начала пандемии российские исследователи извлекли фрагмент генетического материала нового коронавируса SARS-COV-2, кодирующий информацию о структуре S белка шипа вируса (белок формирующего «корону» вируса и отвечающий за его связывание с клетками человека), и вставили его в уже знакомый им аденовирусный вектор для доставки в человеческую клетку, создав, таким образом, первую в мире вакцину против коронавируса SARS-COV-2.
Чтобы обеспечить длительный иммунитет, российские ученые предложили использовать два разных типа аденовирусных векторов для первой и второй вакцинации, усиливая действие вакцины.
Использование аденовирусов человека в качестве векторов безопасно, так как данные вирусы, вызывающие ОРВИ, не являются новыми и существуют уже тысячи лет.
Эффективность против новых штаммов
Вакцинация препаратом вырабатывает защитные нейтрализующие титры антител против новых штаммов, включая Alpha B.1.1.7 (впервые выявлен в Великобритании), Beta B.1.351 (впервые выявлен в ЮАР), Gamma P.1 (впервые выявлен в Бразилии), Delta B.1.617.2 и B.1.617.3 (впервые выявлены в Индии) и выявленных в Москве вариантов B.1.1.141 и B.1.1.317 с мутациями в рецептор-связывающем домене (RBD).Методология исследования основана на оценке вируснейтрализующей активности (ВНА) с применением живого вируса, что позволяет получить наиболее достоверные данные и является «золотым» стандартом. В ходе исследования сравнивалась ВНА сыворотки крови людей после вакцинации препаратом «Спутник V» на образцах штаммов, имеющих международное распространение, с ВНА против исходного штамма B.1.1.1. Сыворотка крови была собрана у лиц, иммунизированных обоими компонентами «Спутника V».
Полученные данные демонстрируют, что «Спутник V» сохраняет защитные свойства против новых штаммов. Снижение уровня вируснейтрализующей активности у препарата «Спутник V» к ряду штаммов оказалось значительно меньшим по сравнению с данными, опубликованными производителями других вакцин, которые ранее подтвердили эффективность своих препаратов против новых мутаций коронавирусной инфекции.
Названы различия между двумя компонентами «Спутника V»
Фото: Александр Подгорчук / «Коммерсантъ»
Вакцина от коронавируса «Спутник V» состоит из двух компонентов, поэтому прививка проходит в два этапа. Молекулярный биолог, ведущий научный сотрудник МГУ имени Ломоносова Максим Скулачев объяснил, в чем заключаются различия между первым и вторым компонентом вакцины. Его слова передает радио Sputnik.
«В этих компонентах используются разные аденовирусы, поэтому иммунный ответ на вирус-носитель не мешает при втором уколе, и развивается полноценный иммунный ответ на коронавирусный антиген. Два укола на основе разных вирусов-носителей, аденовирусов — оптимальный вариант, который дает самую лучшую защиту от коронавируса», — рассказал Скулачев.
По словам биолога, при вакцинации «Спутником V» ген белка коронавируса, вызывающий иммунный ответ, доставляется в организм другим вирусом — вектором, которым является аденовирус человека. В «природном» состоянии аденовирус вызывает ОРВИ, но для изготовления вакцины его специальным образом обрабатывают, чтобы он не мог размножаться в клетках и не приводил к заболеванию, добавил Скулачев.
Также он объяснил, что произойдет, если пройти только первый этап вакцинации или повторно получить первый компонент вакцины. «Ничего страшного не будет, он [один укол] тоже дает защиту. Если врач перепутает и случайно второй укол сделает еще раз первым компонентом, в худшем случае у вас просто не будет усиления иммунитета, вся защита будет обеспечена первым уколом», — сказал он.
Ранее были названы отличия между тремя российскими вакцинами от коронавируса. «Спутник V» считается универсальной и защищает от новых штаммов коронавируса. «ЭпиВакКорона» безопасна для пожилых и людей, склонных к аллергии и имеющих проблемы со здоровьем и иммунитетом. «КовиВак» неприхотлива, ее легче хранить и транспортировать.
Названы главные особенности вакцины «Спутник V» Как она действует, какие имеет побочные эффекты и чем отличается от зарубежных аналогов?
Фото: Виталий Аньков / РИА Новости
«Спутник V» создан в короткие сроки и в августе был зарегистрирован как первая в мире вакцина от COVID-19. Это стало возможно потому, что ничего революционного в ней нет, только проверенные алгоритмы.
Препарат представляет собой векторную вакцину на основе аденовируса человека — такие разработки существуют в России с середины 90-х годов.
Научно-исследовательский центр эпидемиологии и микробиологии имени Гамалеи — создатели «Спутника» — работали, например, над вакциной от лихорадки Эбола.
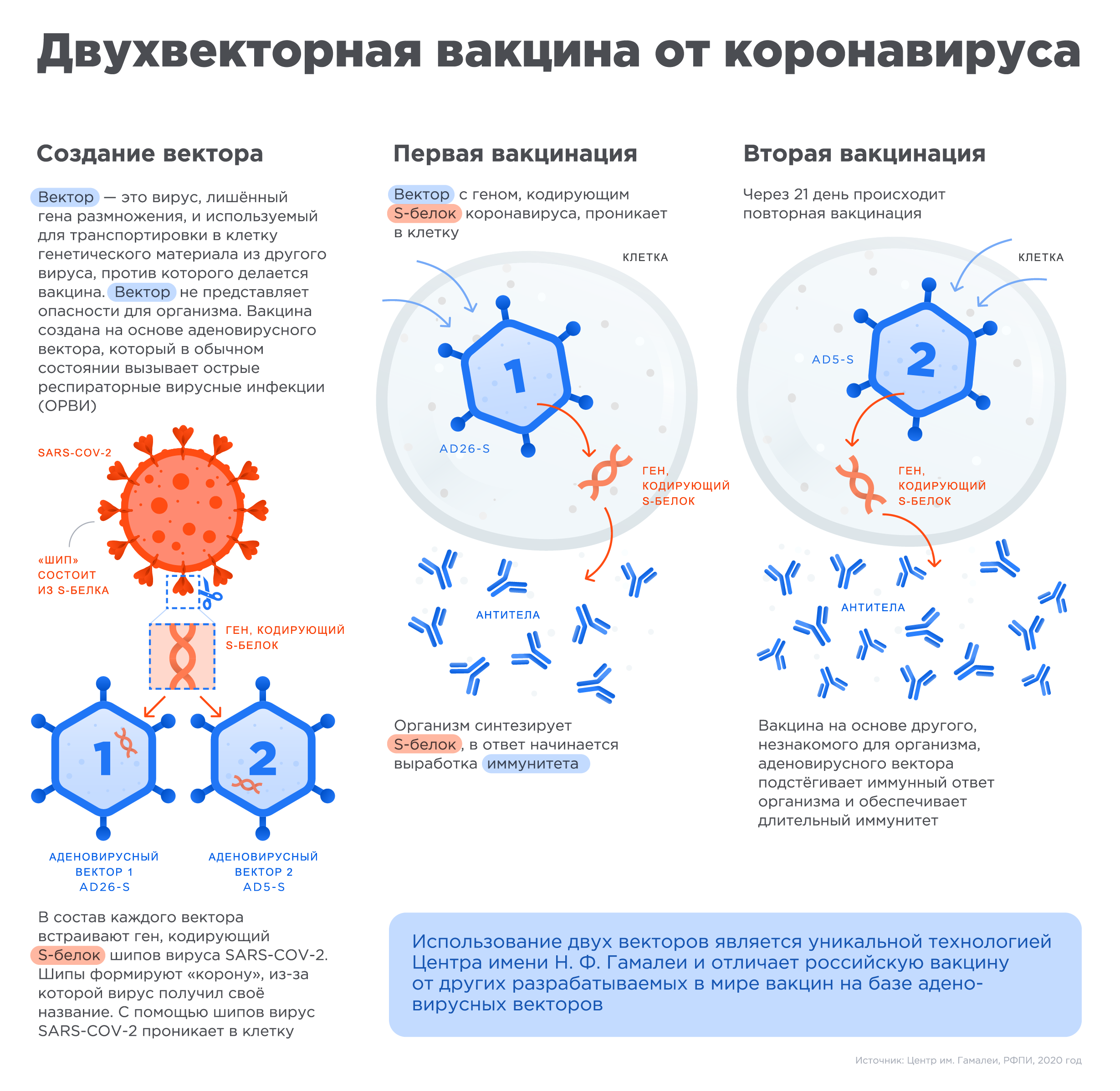
Термин «векторная вакцина» означает, что векторы, созданные на основе другого вируса (в данном случае — аденовируса), выступают в роли носителей генетического материала, доставляя его в клетку. При этом генетический материал аденовируса, который вызывает инфекцию, удаляется и вставляется материал с кодом белка от другого вируса, в данном случае от шипа коронавируса.
Последний безопасен для организма, в то же время он помогает иммунной системе реагировать и вырабатывать антитела, которые защищают от инфекции. Человеческие аденовирусы считаются одними из самых простых для модификации, поэтому они стали очень популярными в качестве векторов.
При введении первой части вакцины вектор с геном, кодирующим S-белок, проникает в клетку. Организм синтезирует S-белок и начинает вырабатывать иммунитет. После второго укола препарат на основе другого, еще не знакомого организму аденовирусного вектора, подстегивает иммунный ответ и обеспечивает длительный иммунитет.
По словам исследователей, это проверенная схема. Британская компания AstraZeneca уже заявила, что будет испытывать «Спутник V» в качестве второго компонента своей вакцины. Сейчас она обеспечивает эффективность в 60 процентов после первого укола. Ученые хотят добавить «Спутник V» в качестве второй дозы препарата — технология у этих вакцин схожая.
«Если не брать во внимание политику, с точки зрения биологии это очень разумное предложение», — прокомментировала идею объединить два препарата доктор биологических наук, профессор Школы системной биологии университета Джорджа Мэйсона (США), главный научный сотрудник медико-генетического научного центра РАН Анча Баранова.
Помимо нашей страны, где в пострегистрационном клиническом исследовании «Спутник V» согласились участвовать 40 тысяч добровольцев, испытания российской вакцины объявлены в ОАЭ, Индии, Венесуэле и Беларуси.
Согласно полученным данным, недомогание наблюдалось примерно у каждого 20-го человека. Однако ничего серьезного отмечено не было — немного повышенная температура и легкое недомогание, которое проходит через день-два. Аналогичные симптомы из года в год встречаются у людей, делающих прививку от гриппа.
Ряд зарубежных вакцин действуют по иному принципу, нежели «Спутник V». В частности, американские препараты Pfizer и Moderna представляют собой так называемые РНК-вакцины. Специалисты относят их к препаратам генной терапии. При этом опыта применения таких прививок у человека раньше никогда не было.
РНК-вакцины могут вызвать редкие побочные эффекты, которые пока до конца не исследованы. Среди них ученые называют аутоиммунные реакции и образование тромбов. Выявить полную картину можно будет только после тестирования препаратов на большом количестве добровольцев.
В начале декабря американское Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) сообщило, что у четверых добровольцев, получивших вакцину Pfizer, развился паралич Белла. При этом расстройстве наблюдается временная неработоспособность лицевого нерва. Среди других побочных явлений ученые зафиксировали лихорадку, утомляемость, головную боль и мышечную боль.
По словам врача и телеведущего Александра Мясникова, принципы вакцинации от коронавируса были разработаны в 2002 году, когда возникла вспышка вируса SARS-1. Тогда стало понятно, что вакцина должна быть направлена на нейтрализацию «шипов» коронавируса (spike-protein), с помощью которых он прикрепляется к рецепторам легких и проникает в клетки, как и любой другой вирус.
Он пояснил, что вакцина «Спутник V» работает на основе аденовирусов, вызывая иммунный ответ из-за сходного белка «шипов». Вырабатывающиеся антитела в свою очередь работают против «шипов» коронавируса. Специалист уточнил, что по схожему принципу работает вакцина от университета Оксфорда и компании AstraZeneca. Подобный процесс запускается в препаратах, где используются «живые», но ослабленные вирусы, неопасные для человека.
Вторая российская вакцина от COVID-19, «ЭпиВакКорона» — рекомбинантный белковый препарат, в котором «шип» коронавируса синтезируется искусственно, но идентичен натуральному. На него в итоге вырабатываются антитела. Похожий принцип работы у американской вакцины «Новавакс», написал врач.
Еще один принцип работы вакцин — «кодировка» белкового «шипа» с помощью гена РНК, который доставляется в протеин в липидной наночастице. Ген перекодирует «шип», делая его мишенью для собственных иммунных сил. Мясников уточнил, что такой препарат работает эффективнее у молодых. Такие препараты разрабатывают Pfizer и BioNTech, а также Moderna.
В Китае разработаны вакцины Sinovac и Sinopharm, они действуют на основе инактивированного нового коронавируса. На подобном принципе разрабатываются вакцины в Индии и Казахстане, добавил Мясников. В стадии разработки также препараты, позволяющие интраназальное введение и дающие местный иммунитет — такой способ более перспективен в случае, если коронавирус проникает в дыхательные пути.
С самого начала к российской вакцине специалисты были настроены скептически. В частности, Еврокомиссия заявляла, что не считает российский «Спутник V» безопасным препаратом. После того как власти Венгрии сообщили о намерении приобрести российскую разработку, представитель Еврокомиссии Эрик Мамер пригрозил ввести против этой страны административные меры.
Он обратил внимание, что вакцины не из ЕС смогут попасть на рынок Европы только, если Брюссель их одобрит.
При этом с разработкой вакцин за рубежом есть свои проблемы. Так, в ходе испытаний вакцины Pfizer скончались шесть добровольцев. Однако это не помешало начать вакцинацию этим препаратом в США.
В декабре в Российском фонде прямых инвестиций (РФПИ) заявили об информационной атаке на «Спутник V» за границей как по конкурентным, так и по политическим причинам. Представители организации отметили, что в СМИ периодически появляются несоответствующие действительности сведения о характеристиках средства и его производстве. Также отмечается, что о ходе переговоров фонда с потенциальными партнерами и контрагентами иногда публикуется недостоверная информация.
Российскую вакцину от коронавируса «Спутник V» планируется дискредитировать из-за рубежа — якобы ведется информационная кампания, финансируемая иностранными государствами. Об этом заявил официальный представитель Минобороны России генерал-майор Игорь Конашенков.
«В социальных сетях и финансируемых на зарубежные гранты русскоязычных интернет-ресурсах готовится серия псевдоаналитических «расследований» и лжесвидетельств «очевидцев» о якобы опасности российской вакцины или поголовных «отказах» от вакцинирования», — предупредил Конашенков.
Он заявил, что российский препарат отличается высокой эффективностью, а вбросы против вакцины не сделают зарубежные аналоги лучше. Среди военнослужащих, по его словам, отказов от вакцинации нет, а до конца года прививку получат еще около 100 тысяч человек.
Миллиарды людей по всему миру, скорее всего, не получат вакцину от коронавируса в ближайшее время, поскольку богатые страны раскупили большинство самых многообещающих препаратов. Согласно прогнозам, в наиболее бедных государствах девять из десяти человек не смогут сделать вакцину в 2021 году.
Богатые страны, где проживает 14 процентов населения мира, обеспечили себя 53 процентами наиболее многообещающих вакцин. Больше всего доз на душу населения купила Канада: их хватит, чтобы вакцинировать каждого канадца пять раз.
Почти все вакцины Pfizer — 96 процентов доз — купили западные страны. Похожая картина наблюдается и с препаратом Moderna. Обе вакцины стоят дорого, и доступ для стран с низкими доходами будет затруднен также и из-за сверхнизких температур, при которых их необходимо хранить.
Подобного мнения придерживается директор программы Всемирной организации здравоохранения (ВОЗ) по чрезвычайным ситуациям Майкл Райан, который предрек миру дефицит вакцин от коронавируса. По его словам, людям необходимо осознать факт того, что в мире не будет достаточной вакцинации для предотвращения нового роста числа случаев заболевания по меньшей мере в течение трех-шести месяцев.
Число заражений коронавирусом в мире составило почти 73 миллиона, свидетельствуют данные мониторингового проекта университета Джонса Хопкинса.
Наибольшее число инфицированных было зарегистрировано в США — 16,5 миллиона человек. На втором месте Индия с 9,9 миллиона пациентов, на третьем — Бразилия с 6,9 миллиона заболевших. Россия находится на четвертом месте с 2,6 миллиона подтвержденных случаев коронавируса.
Вакцина Спутник Лайт
Вакцина «Спутник Лайт» защищает от инфекций:
Стоимость прививки Спутник Лайт в Москве составляет 2500 руб. В цену включён осмотр врача перед вакцинацией.
Похожие вакцины (аналоги Спутник Лайт):
| Вакцина | Цена |
|---|---|
| КовиВак ФГБНУ «ФНЦИРИП» им. М. П. Чумакова РАН, Россия | 3000 ₽ |
| Спутник V «НИЦЭМ им. Н. Ф. Гамалеи» Минздрава России | 1500 ₽ |
Торговое наименование:
Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Лекарственная форма:
раствор для внутримышечного введения
Состав на 1 дозу (0,5 мл):
Действующее вещество: рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (1,0±0,5)×10 11 частиц/доза.
Вспомогательные вещества: трис(гидроксиметил)аминометан – 1,21 мг, натрия хлорид – 2,19 мг, сахароза – 25,0 мг, полисорбат 80 – 250 мкг, магния хлорида гексагидрат – 102,0 мкг, ЭДТА динатриевая соль дигидрат – 19,0 мкг, этанол 95 % – 2,5 мкл, вода для инъекций – до 0,5 мл.
Описание
Раствор замороженный – плотная затвердевшая беловатого цвета масса. После размораживания – однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Характеристика
Вакцина получена биотехнологическим путем, при котором не используется патогенный для человека вирус SARS-CoV-2. В состав препарата входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S вируса SARS-CoV-2.
Фармакотерапевтическая группа:
Код АТХ:
Фармакологические свойства
Новая редакция от 19 августа 2021 года.
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологические свойства и безопасность вакцины изучали в различных клинических исследованиях у взрослых добровольцев обоего пола в возрасте старше 18 лет. Промежуточный анализ иммуногенности показал, что вакцина формирует гуморальный иммунный ответ у добровольцев. На 28 день сероконверсия обнаружена у 96,88% здоровых добровольцев.
У лиц с предсуществующим иммунитетом к коронавирусу отмечен выраженный рост титра антител на 10 день после вакцинации, что может указывать на возможность применения препарата для вакцинации ранее переболевших COVID-19 после снижения титра антител с целью предотвращения повторных случаев заболевания.
С учетом рекомендаций Всемирной организации здравоохранения для достижения уровня коллектннного иммунитета населения, следует проводить вакцинацию против новой коронавирусной инфекции COVID- 19 по эпидемическим показаниям спустя 6 месяцев после перенесенного заболевания (в том числе у ранее вакцинированных лиц) или спустя 6 месяцев после предыдущей первичной вакцинации.
В результате однократной иммунизации 100% здоровых добровольцев (все 30 человек у которых изучены показатели клеточного иммунитета) сформировали клеточный иммунный ответ против S белка SARS-Cov2.
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Показания к применению
Новая редакция от 19 августа 2021 года.
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых старше 18 лет.
Противопоказания
С осторожностью
Новая редакция от 19 августа 2021 года.
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и сахарном диабете в стадии декомпенсации), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
Категориям населения старше 60 лет, ранее не прошедшим иммунизацию от COVID-19, и не болевшим COVID-19, иммунокомпрометированным лицам независимо от возраста, для формирования иммунитета не рекомендовано применение препарата Спутник Лайт в связи со снижением функции иммунной системы, для формирования иммунного ответа показана вакцинация двухкомпонентной вакциной Гам-Ковид-Вак.
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Применение при беременности и в период грудного вскармливания
Препарат противопоказан при беременности и в период грудного вскармливания, так как его эффективность и безопасность в этот период не изучались.
Способ применения и дозы
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу – препарат вводят в латеральную широкую мышцу бедра.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Замороженный препарат
Перед вакцинированием флакон, ампулу или шприц с препаратом достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон, ампулу или шприц снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона, ампулы или шприца!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Вскрывают ампулу по кольцу и/или точке излома. Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту из ампулы или флакона.
Внимание! Доза, вводимая пациенту, не должна превышать 0,5 мл!
Препарат в шприцах готов к применению без дополнительных манипуляций.
Применение вакцины производства ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России) (флаконы) и АО «Биннофарм» (ампулы, шприцы):
Не допускается хранение размороженного препарата более 30 минут!
Повторное замораживание не допускается!
Применение вакцины производства АО «ГЕНЕРИУМ» (флаконы), ОАО «Фармстандарт-УфаВИТА» (флаконы, ампулы), ЗАО «ЛЕККО» (флаконы):
Внимание! Повторное замораживание флакона или ампулы с раствором не допускается!
Суммарное время хранения размороженного раствора при комнатной температуре не должно превышать 2 часов. Неиспользованная вакцина подлежит уничтожению.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого или невскрытого флакона не более 2 часов при комнатной температуре.
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение вакцины при комнатной температуре: вскрытой ампулы, закрытой стерильной салфеткой, не более 1 часа, невскрытой ампулы – не более 2 часов.
ВНИМАНИЕ! Одна ампула содержит две дозы вакцины. Объем одной дозы составляет 0,5 мл. Одному пациенту вводить 1 дозу (0,5 мл).
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение невскрытой ампулы при комнатной температуре не более 2 часов.
Применение вакцины производства ЗАО «БИОКАД» (флаконы), АО «Р-Фарм» (флаконы):
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона по 3 мл не более 2 часов при комнатной температуре.
Не допускается хранение размороженного препарата во флаконах по 0,5 мл более 30 минут!
Повторное замораживание не допускается!
Жидкий препарат
Применение вакцины производства ООО «БиоИнтегратор» (флаконы):
Внимание! Замораживание флакона с раствором не допускается!
Флакон достают из холодильника и выдерживают при комнатной температуре, допускается слегка нагреть препарат, например, подержав его в руках. Не следует нагревать препарат выше 37 °С.
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона или ампулы не более 2 часов при комнатной температуре.
Внимание! К использованию непригоден препарат (жидкий и/или замороженный) с дефектами укупорочной системы и/или нарушенной маркировкой флакона или ампулы,, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата путем внесения информации в соответствующий раздел информационной системы ЕГИСЗ.
Побочное действие
Нежелательные явления, характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Часто и очень часто могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции.
Нежелательные явления, представленные ниже, перечислены по системам организма и в соответствии с частотой встречаемости. Частота встречаемости определяется следующим образом: очень часто (≥1/10), часто (≥1/100 и При производстве ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России):
по 0,5 мл (1 доза) препарата – во флаконы, укупоренные пробками из резины, обжатые алюминиевыми или алюмопластиковыми колпачками.
1 флакон препарата с инструкцией по применению в пачку картонную или в пачку из картона коробочного.
При производстве АО «Биннофарм»:
по 0,5 мл (1 доза) препарата – в ампулы из бесцветного стекла с точкой излома или в стерильном одноразовом шприце.
По 5 ампул препарата в контурную ячейковую упаковку из пленки поливинилхлоридной, или по 1 или 3 шприца с препаратом помещают в контурную ячейковую упаковку из пленки поливинилхлоридной, покрытую пленкой полиэтиленовой, или без покрытия.
По 1 контурной ячейковой упаковке вместе с инструкцией по применению в пачку из картона.
При производстве на АО «ГЕНЕРИУМ»:
по 3,0 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
1 флакон препарата вместе с инструкцией по медицинскому применению – в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «ЛЕККО»:
по 3 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 1 флакону вместе с инструкцией по применению – в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ОАО «Фармстандарт-УфаВИТА»:
по 0,5 мл (1 доза) или по 1,0 мл (2 дозы) препарата в ампулы из бесцветного стекла.
По 5 ампул помещают в контурную ячейковую упаковку из пленки поливинилхлоридной.
По 1 или 2 контурные ячейковые упаковки вместе с инструкцией по применению – в пачку из картона.
По 3 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 1 флакону вместе с инструкцией по применению в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «БИОКАД»:
по 0,5 мл (1 доза) или по 3,0 мл (5 доз) препарата во флаконы из нейтрального стекла I гидролитического класса (типа 2R, 6R), герметично укупоренные резиновыми пробками, с обкаткой алюминиевыми колпачками с пластиковой крышкой типа «flip-off».
На флаконы препарата наклеивают этикетку самоклеящуюся.
1 флакон 6R препарата с инструкцией по применению в пачку картонную.
1 флакон 2R препарата в контурной ячейковой упаковке из ПВХ пленки с инструкцией по применению в пачку картонную.
При производстве на АО «Р-Фарм»:
по 0,5 мл (1 доза) препарата во флаконы, герметично укупоренные пробками из резины и обжатые алюмопластиковыми колпачками.
По 1, 2, 5 или 10 флаконов вместе с инструкцией по применению в пачку из картона.
При производстве на ООО «БиоИнтегратор»:
по 0,5 мл (1 доза) препарата – во флаконы, укупоренные пробками из резины, обжатые алюминиевыми или алюмопластиковыми колпачками.
1 флакон препарата с инструкцией по применению в пачку картонную или в пачку из картона коробочного.
Условия хранения
Хранить в защищенном от света месте, при температуре не выше минус 18 °С. Повторное замораживание не допускается.
Хранить в недоступном для детей месте.
Хранить в защищенном от света месте, при температуре от 2 до 8 °С. Не замораживать.
Хранить в недоступном для детей месте.
Условия транспортирования
Транспортирование препарата при температуре не выше минус 18 °С.
Транспортирование препарата при температуре от 2 до 8 °С. Не замораживать.
Срок годности
6 месяцев. Не применять по истечении срока годности.
1 месяц. Не применять по истечении срока годности.
Условия отпуска:
для лечебно-профилактических учреждений.
Производитель
Наименования и адреса производственных площадок производителя лекарственного препарата:
1) ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия, 123098, г. Москва, улица Гамалеи, д. 18 (все стадии производства).
2) АО «Р-Фарм», Россия, 150061, Ярославская обл., г.о. г. Ярославль, г. Ярославль, ул. Громова, д. 15 (производство готовой формы, первичная и вторичная (потребительская) упаковка).
3) АО «Биннофарм», Россия, 124460, г. Москва, г. Зеленоград, ул. Конструктора Гуськова, д. 3, стр. 1 (производство готовой формы, первичная и вторичная (потребительская) упаковка).
4) ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, п. Стрельна, ул. Связи, д. 38, стр. 1 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
5) АО «ГЕНЕРИУМ», Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 263 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
6) ЗАО «ЛЕККО», Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 277; 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 279 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
7) ОАО «Фармстандарт-УфаВИТА», Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, д. 28 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
8) ООО «БиоИнтегратор», Россия, 141401, Московская область, г.о. Химки, г. Химки, ул. Рабочая, д. 2А, стр. 1 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
Выпускающий контроль качества
ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России). Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Владелец регистрационного удостоверения/организация, принимающая претензии потребителя:
ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия
Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Узнать наличие вакцины Спутник Лайт и записаться на прививку можно по телефонам центра:
«Диавакс» на Таганке
Если хотите пригласить определённого специалиста, оставьте заявку и мы вам перезвоним!
А еще мы отвечаем на интересующие вас вопросы в специальном разделе! Чаще всего это вопросы индивидуального характера в отношении вакцинации, иммунитета и тому подобного.