Плавление
Из Википедии — свободной энциклопедии
Плавле́ние — это процесс перехода тела из кристаллического твёрдого состояния в жидкое, то есть переход вещества из одного агрегатного состояния в другое. Плавление происходит с поглощением теплоты плавления и является фазовым переходом первого рода, которое сопровождается скачкообразным изменением теплоёмкости в конкретной для каждого вещества температурной точке превращения — температура плавления.
Способность плавиться относится к физическим свойствам вещества [1]
При нормальном давлении, наибольшей температурой плавления среди металлов обладает вольфрам (3422 °C), среди простых веществ — углерод (по разным данным 3500 — 4500 °C [2] ) а среди произвольных веществ — карбид тантала-гафния Ta4HfC5 (3942 °C). Можно считать, что самой низкой температурой плавления обладает гелий: при нормальном давлении он остаётся жидким при сколь угодно низких температурах.
Многие вещества при нормальном давлении не имеют жидкой фазы. При нагревании они путём сублимации сразу переходят в газообразное состояние.
ПЛАВЛЕНИЕ
П. предшествуют интенсивное разупорядочивание кристаллов в-ва (т. наз. предплавление) и проявление жидких микроучастков на пов-сти кристаллов и вблизи межкристал-литных границ. По мере нагревания микроучастки укрупняются и сливаются, формируя жидкую фазу, а кристаллы рассыпаются на фрагменты и уменьшаются в размерах до полного исчезновения. Теплота, подводимая к в-ву при П., расходуется в осн. на разрыв межатомных связей, а не на его нагревание. Поэтому чистые крупнокристаллич. в-ва в течение П. не изменяют свою т-ру (рис. 1). Для таких в-в т-ра П. служит идентифицирующей характеристикой и критерием их чистоты. П. в-в со сходной кристаллич. структурой описывается эмпирич. ф-лой Линдемана:
Т-ра П. большинства чистых в-в (за исключением т. наз. аномальных-Bi, Ga, Sb, льда и др.) возрастает с увеличением давления. Для давлений, меньших 10 5 Па, зависимость Т пл от давления pприближенно выражается эмпирич. ф-лой Симона:
ПАРАМЕТРЫ ПЛАВЛЕНИЯ НЕКОТОРЫХ ВЕЩЕСТВ
При p >10 5 Па ф-ция Т пл (р)может иметь максимумы (рис. 2). Разница между т-рами П. полиморфных модификаций одного и того же в-ва достигает 270 К (напр., две кубич. модификации KCl), а кристаллов с разл. изотопным составом-5 К (напр., водород и дейтерий). Крупные кристаллы чистого в-ва плавятся при более высокой т-ре, чем мелкие. При размерах кристаллов d >10 нм т-ра их П. определяется по ф-ле:
Переход мелкокристаллич. полидисперсных в-в в жидкое состояние происходит не при постоянной т-ре, а в интервале т-р (до неск. градусов): начинается при т-ре П. самых мелких, а завершается при т-ре П. наиб. крупных кристаллов. Твердые р-ры также плавятся в температурном интервале, к-рый может достигать десятков градусов и в соответствии с диаграммой состояния зависит от состава этих р-ров. Уд. энтальпия П. большинства в-в находится в пределах 10-300 кДж/кг и значительно уступает энтальпии парообразования. Возрастание при П. энтропии составляет 3-60 Дж/(моль
Смотреть что такое ПЛАВЛЕНИЕ в других словарях:
ПЛАВЛЕНИЕ
переход вещества из кристаллического (твёрдого) состояния в жидкое; происходит с поглощением теплоты (Фазовый переход I рода). Главными характе. смотреть
ПЛАВЛЕНИЕ
плавление ср. Процесс действия по знач. глаг.: плавить (1*), плавиться (1*).
ПЛАВЛЕНИЕ
плавление с.melting точка плавления — melting-point
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ, переход вещества из кристаллич. (твёрдого) состояния в жидкое; происходит с поглощением теплоты (фазовый переход 1 рода). Гл. характеристи. смотреть
ПЛАВЛЕНИЕ
переход в-ва из кристаллич. (твёрдого) состояния в жидкое, происходит с поглощением теплоты (фазовый переход I рода). Гл. хар-ками П. чистых в-. смотреть
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
[fusion, melting] — процесс перехода вещества из кристаллического (твердого) состояния в жидкое с поглощением теплоты (фазовый переход I рода). Главные характеристики плавления чистых веществ: температура плавления (Tпл) и необходимая теплота (Qпл, Дж/моль).Температура плавления зависит от внешнего давления; на диаграмме состояния чистого вещества эта зависимость изображена кривой плавления (кривой сосуществования твердой и жидкой фаз). Плавление сплавов и твердых растворов происходит, как правило, в интервале температур (исключение составляют эвтектики с постоянной Tпл). Зависимость температуры начального и окончательного плавление сплава от его состава при определенном давлении изображено на диаграме состояния кривыми ликвидуса и солидуса. Среди чистых металлов самая высокая tпл = 3410 °С у W, а самая низкая — у Hg-38,9 °С. У особо тугоплавких соединений tпл: 3200 °С-TiN, 3580 °С-HfN, 3805 °С-ZrC, 4070 °С-ТаС, 4160 °С-HfC и др. Для веществ с высокой tпл, как правило, характерны более высокие mQпл. Примеси в кристаллических веществах снижают их tпл. Это используют для получения легкоплавких сплавов и охлаждающих смесей.
Смотри также:
— окислительное плавление
. смотреть
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
1) Орфографическая запись слова: плавление2) Ударение в слове: плавл`ение3) Деление слова на слоги (перенос слова): плавление4) Фонетическая транскрипц. смотреть
ПЛАВЛЕНИЕ
• плавление n english: melting, fusion, melt-down deutsch: Schmelzen n français: fusion Синонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
переход в-ва из кристаллич. состояния в жидкое, происходящий с поглощением теплоты. При пост. внеш. давлении П. происходит при определ. темп-ре, наз. т. смотреть
ПЛАВЛЕНИЕ
ПЛА́ВЛЕНИЕ (-ье), я, ср.Действ. по гл. плавить1 и плавиться1 (1).Руд плавление розное и подобает по рудѣ исправляти. Кн. горн. 42. Металлурги при плавл. смотреть
ПЛАВЛЕНИЕ
переход тв. кристаллич. в-ва в жидкое состояние (фазовый переход первого рода). При постоянном внеш. давлении П. чистого в-ва происходит при постоянной. смотреть
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ, переход твердого кристаллического вещества в жидкое состояние (фазовый переход первого рода). При постоянном внешнем давлении плавление чистого вещества происходит при постоянной температуре (tпл), называется температурой плавления; tпл при атмосферном давлении называется точкой плавления вещества. Аморфные твердые тела не имеют точки плавления. Они переходят в жидкое состояние постепенно, размягчаясь при повышении температуры.
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ, переход твердого кристаллического вещества в жидкое состояние (фазовый переход первого рода). При постоянном внешнем давлении плавление чистого вещества происходит при постоянной температуре (tпл), называется температурой плавления; tпл при атмосферном давлении называется точкой плавления вещества. Аморфные твердые тела не имеют точки плавления. Они переходят в жидкое состояние постепенно, размягчаясь при повышении температуры. смотреть
ПЛАВЛЕНИЕ
— переход твердого кристаллического вещества в жидкое состояние(фазовый переход первого рода). При постоянном внешнем давлении плавлениечистого вещества происходит при постоянной температуре (tпл), называетсятемпературой плавления; tпл при атмосферном давлении называется точкойплавления вещества. Аморфные твердые тела не имеют точки плавления. Онипереходят в жидкое состояние постепенно, размягчаясь при повышениитемпературы. смотреть
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
сeritme; erimeто́чка плавле́ния — erime noktasıтемперату́ра плавле́ния — erime ısısıСинонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
Rzeczownik плавление n topnienie odczas. n topienie odczas. n stapianie odczas. n
ПЛАВЛЕНИЕ
colliquation, fusing, fusion, melt, melting, (чугуна, электростали, цветных металлов, ферросплавов) smelting* * *плавле́ние с.fusion, melting* * *smelt. смотреть
ПЛАВЛЕНИЕ
-я, ср. Действие по знач. глаг. плавить 1; действие и состояние по знач. глаг. плавиться 1. Температура плавления. Точка плавления.Синонимы: купеляц. смотреть
ПЛАВЛЕНИЕ
Плавление – переход вещества из твердого состояния в жидкое, т. е. переход от дальнего порядка к ближнему порядку. [Блюм Э. Э. Словарь основных м. смотреть
ПЛАВЛЕНИЕ
Нева Напев Налив Нал Липа Лина Лиеп Ливан Лена Лен Лев Лал Илл Иена Иван Ение Елена Еле Евина Ева Вне Вип Виллан Нелли Непал Вилл Нива Нил Павел Павлин Паление Пан Пани Пеан Вилен Вие Пелена Виан Пена Пенал Вена Валин Пие Пилав Пинаев Вале Вал Аллен План Плевание Плена Алле Алл Алин Алиев Ален Аил Авил Плие Плевел Плавление Плав Пила Пиан Пение. смотреть
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
процесс перехода материала из твердой в жидкую фазу при повышении температуры до точки плавления (зависит от давления).Источник: Справочник дорожных те. смотреть
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
с.fonte f, fusion fточка плавления — degré m (extrême) de fusionСинонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
с. fonte f, fusion f точка плавления — degré m (extrême) de fusion
ПЛАВЛЕНИЕ
Ударение в слове: плавл`ениеУдарение падает на букву: еБезударные гласные в слове: плавл`ение
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
сSchmelzen nточка плавления — Schmelzpunkt mСинонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
плавлениеהַתָכָה נ’; הִיתוּך ז’* * *המסההפשרההתכההתמוגגותנתיכהСинонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ плавления, мн. нет, ср. (спец.). Состояние по глаг. плавиться, процесс перехода из твердого состояния в жидкое под воздействием высокой температуры. Точка плавления (температура, при к-рой вещество начинает плавиться).
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
с.fusión fточка плавления — punto de fusión
ПЛАВЛЕНИЕ
(2 с), Пр. о плавле/нииСинонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
n.melting, fusionСинонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
Á сущ; 32 иск см. _Приложение IIСинонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
сущ. ср. родадействие/процессплавлення
ПЛАВЛЕНИЕ
с.melting, fusion- анизотропное локальное плавление- поверхностное плавление
ПЛАВЛЕНИЕ
• lydymasis (-osi) (1)• tirpimas (2)
ПЛАВЛЕНИЕ
плавление с Schmelzen n 1 точка плавления Schmelzpunkt m 1Синонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
сfusão fСинонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
1) dissolving2) fluxxing3) liquefactionСинонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
плавле́ниеСинонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
плавле’ние, плавле’ния, плавле’ния, плавле’ний, плавле’нию, плавле’ниям, плавле’ние, плавле’ния, плавле’нием, плавле’ниями, плавле’нии, плавле’ниях
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
с. fusione f точка плавления — punto di fusione Итальяно-русский словарь.2003. Синонимы: купеляция, плавка, топка, топление
ПЛАВЛЕНИЕ
(руды) Einschmelzen, Schmelzarbeit, Schmelzen
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
ПЛАВЛЕНИЕ
ср. эрүү, эрий турган абалга келүү; точка плавления эрүү точкасы (эрий турган убагына жетүү).
Температура плавления: от чего зависит, как характеризуется и другое
Содержание:
Температура плавления – состояние, при котором твердое кристаллическое тело приобретает свойства жидкости. Она представляет собой границу между жидкостью и твердым веществом. Обозначение температуры плавления – t. При дальнейшем нагревании системы вещество переходит в жидкость, а при охлаждении – в твердое вещество.
От чего зависит температура плавления?
Как определить температуру плавления?
Существует несколько методов экспериментального определения температуры плавления.
Формула определения температуры плавления по методу «мгновенного плавления»:
Для определения температуры плавления твердых веществ, которые быстро превращаются в порошок, используют методы №1 и №3, а для аморфных веществ, плавящихся при температуре ниже 100°С, — метод №2.
Температуру плавления нельзя определить теоретическим путем с помощью формул. Ознакомиться с ней можно в специальном химическом справочнике.
Температура плавления и кипения
Рекордсмены по температуре плавления
Наиболее высокую температуру плавления имеет вещество графит – аллотропная модификация углерода. Он начинается плавиться при +3000°С. Другое аллотропное состояние углерода – алмаз. Это твердое вещество начинает плавиться при 3500°С.
Фазовые переходы и уравнение теплового баланса
теория по физике 🧲 термодинамика
Фазовые переходы — это термодинамические процессы, приводящие к изменению агрегатного состояния вещества.
Плавление и отвердевание
Для расчета количества теплоты, необходимого для процесса плавления, следует применять формулу:
m — масса вещества, λ (Дж/кг) — удельная теплота плавления.
Плавление каждого вещества происходит при определенной температуре, которую называют температурой плавления. Все проводимое тепло идет на разрушение кристаллической решетки, при этом увеличивается потенциальная энергия молекул. Кинетическая энергия остается без изменения и температура в процессе плавления не изменяется.
Удельная теплота плавления показывает, какое количество теплоты необходимо сообщить 1 кг данного вещества, чтобы перевести его из твердого состояния в жидкое при условии, что оно уже нагрето до температуры плавления. В процессе отвердевания 1 кг данной жидкости, охлажденной до температуры отвердевания, выделится такое же количество теплоты.
Внимание! Удельная теплота плавления — табличная величина.
Определение Отвердевание, или кристаллизация — переход состояния из жидкого состояния в твердое (это процесс, обратный плавлению).
Отвердевание происходит при той же температуре, что и плавление. В процессе отвердевания температура также не изменяется. Количество теплоты, выделяемое в процессе отвердевания:
Парообразование и конденсация
Количество теплоты, необходимое для процесса кипения, вычисляют по формуле:
m — масса вещества, r (Дж/кг) — удельная теплота парообразования.
Парообразование происходит при определенной температуре, которую называют температурой кипения. В отличие от испарения, процесс парообразования идет со всего объема жидкости. Несмотря на то, что к кипящему веществу подводят тепло, температура не изменяется. Все затраты энергии идут на увеличение промежутком между молекулами. Температура кипения зависит от рода вещества и внешнего атмосферного давления.
Удельная теплота парообразования показывает, какое количество теплоты необходимо затратить, чтобы перевести в пар 1 кг жидкости, нагретой до температуры кипения. Такое же количество теплоты выделится в процессе конденсации 1 кг пара, охлажденного до температуры конденсации.
Внимание! Удельная теплота парообразования — табличная величина.
Определение Конденсация — процесс, обратный кипению. Это переход вещества из газообразного состояния в жидкое.
Конденсация происходит при температуре кипения, которая также не изменяется во время всего процесса. Количество теплоты, выделяемое в процессе конденсации:
Тепловые процессы при нагревании и охлаждении
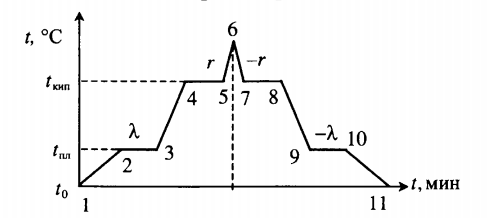
Все фазовые переходы, а также процессы нагревания и остывания вещества можно отобразить графически. Посмотрите на график фазовых переходов вещества:
Он показывает зависимость температуры вещества от времени в процессе его нагревания и остывания. Опишем процессы, отображаемые на графике, в таблице.
| Процесс | Что происходит | Количество выделенной теплоты | ||||||||||||||||||||||||||||||||||||||||||
| 1–2 | Нагревание твердого тела | |||||||||||||||||||||||||||||||||||||||||||
| 6–7 | Охлаждение пара |
| Что происходит | График | Формула количества теплоты | |||||||||||||||||||||||||||||||
| Полностью растопили лед, имеющий отрицательную температуру. | 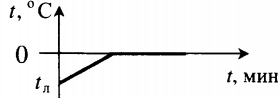 | ||||||||||||||||||||||||||||||||
| Лед, взятый при отрицательной температуре, превратили в воду при комнатной температуре. | 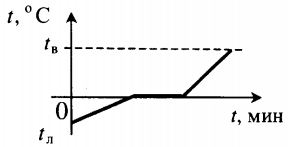 | ||||||||||||||||||||||||||||||||
| Взяли лед при температуре 0 о С и полностью испарили. | 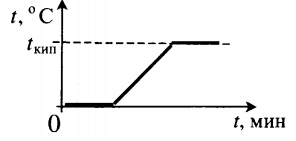 | ||||||||||||||||||||||||||||||||
| Взяли воду при комнатной температуре и половину превратили в пар. | 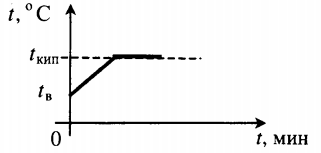 |
| Единицы измерения | Температуру можно оставлять в градусах Цельсия, так как изменение температуры в градусах Цельсия равно изменению температуры в Кельвинах. |
| Кипяток | Вода, которая при нормальном атмосферном давлении имеет температуру в 100 о С. |
| Объем воды 5 л | m = 5 кг, так как: m = ρ V =10 3 · 5 · 10 − 3 м 3 = 5 к г Внимание! Равенство V (л) = m (кг) справедливо только для воды. |
Пример №1. Какое количество теплоты нужно сообщить льду массой 2 кг, находящемуся при температуре –10 о С, чтобы превратить его в воду и нагреть ее до температуры +30 о С?
Можно выделить три тепловых процесса:
Поэтому количество теплоты будет равно сумме количеств теплоты для каждого из этих процессов:
Q = c л m ( 0 − t 1 ) + λ m + c в m ( t 2 − 0 )
Удельные теплоемкости и удельную теплоту плавления смотрим в таблицах:
Уравнение теплового баланса
Суммарное количество теплоты, которое выделяется в теплоизолированной системе равно количеству теплоты (суммарному), которое в этой системе поглощается.
Математически уравнение теплового баланса с учетом знаков количества теплоты записывается так:
Отданное количество теплоты меньше нуля (Qотд 0).
Подсказки к задачам на уравнение теплового баланса
| Теплообмен происходит в калориметре | Потерями энергии можно пренебречь. |
| Жидкость нагревают в некотором сосуде | Начальные и конечные температуры жидкости и сосуда совпадают. |
| В жидкость опускают термометр | Через некоторое время он покажет конечную температуру жидкости и термометра. |
| Мокрый снег | Содержит воду и лед при 0 о С. Учтите, что лед плавится, если он находится при температуре 0 о С и получает энергию от более нагретого тела. Вода кристаллизируется при температуре 0 о С, если она отдает энергию более холодному телу. Если лед и вода находятся при температуре 0 о С, то никаких агрегатных переходов между ними не происходит. |
Частные случаи теплообмена
| В воду комнатной температуры бросили ком снега, содержащий некоторое количество воды, после чего установилась некоторая положительная температура. | 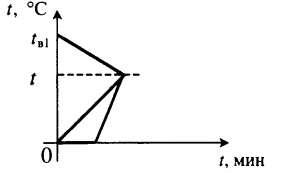 Уравнение теплового баланса: Уравнение теплового баланса: c в m в 1 ( t − t в 1 ) + c в m в 2 ( t − 0 ) + λ m л + c в m л ( t − 0 ) = 0 | ||||||||
| Для получения некоторой положительной температуры воды используют горячую воду и лед, имеющий отрицательную температуру. | 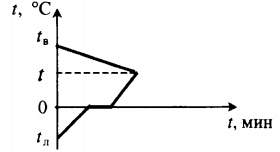 Уравнение теплового баланса: Уравнение теплового баланса: c в m в ( t − t в ) + c л m л ( 0 − t л ) + λ m л + c в m л ( t − 0 ) = 0 | ||||||||
| В воду комнатной температуры бросают раскаленное твердое тело, в результате часть воды испаряется. | 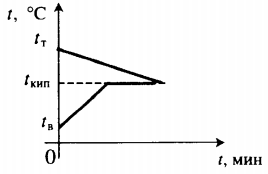 Уравнение теплового баланса: Уравнение теплового баланса: c т m т ( 100 − t т ) + c в m в ( 100 − t в ) + r m п = 0 | ||||||||
| Воду комнатной температуры нагревают до кипения, вводя пар при t = 100 о С. | 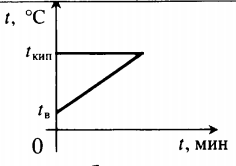 Уравнение теплового баланса: Уравнение теплового баланса: − r m п + c в m в ( 100 − t в ) = 0 | ||||||||
| Лед, имеющий температуру плавления, нагревают до положительной температуры, вводя пар при t = 100 о С. | 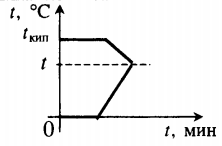 Уравнение теплового баланса: Уравнение теплового баланса: − r m п + c в m п ( t − t к и п ) + λ m л + c в m л ( t − t п л ) = 0 Пример №2. В кастрюлю, где находится вода объемом 2 л при температуре 25 о С, долили 3 л кипятка. Какая температура воды установилась? Количество теплоты, отданное кипятком, равно количеству теплоты, принятому более прохладной водой. Поэтому: c m 1 ( t − t 0 ) = − c m 2 ( t − t к и п ) m 1 ( t − t 0 ) = − m 2 ( t − t к и п ) m 1 t + m 2 t = m 1 t 0 + m 2 t к и п ( m 1 + m 2 ) t = m 1 t 0 + m 2 t к и п Взаимные превращения механической и внутренней энергииЕсли в тексте задачи указан процент одного вида энергии, перешедший в другой, то он указывается в виде десятичной дроби перед этой энергией, которой тело обладало вначале. Частные случаи закона сохранения энергии
|



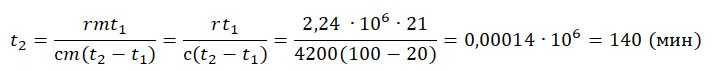
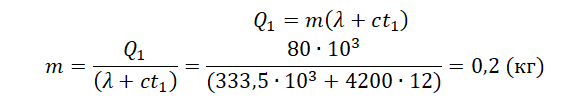
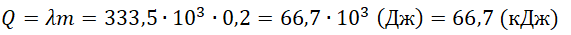
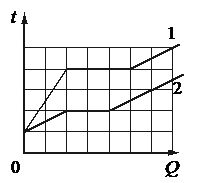 На рисунке представлены графики зависимости температуры t двух тел одинаковой массы от сообщённого им количества теплоты Q. Первоначально тела находились в твёрдом агрегатном состоянии.
На рисунке представлены графики зависимости температуры t двух тел одинаковой массы от сообщённого им количества теплоты Q. Первоначально тела находились в твёрдом агрегатном состоянии.


