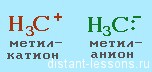Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии
Содержание:
Органическая химия вызывает страх при виде формул из этого раздела, но давайте перестанем бояться и углубимся в изучение взаимодействия веществ.
Что же из себя представляют механизмы реакций?
Это детальное разъяснение процесса перехода субстрата в продукт. В органике выделяются два типа механизмов химических реакций, ионный и радикальный.
Ионный механизм
Типичными представителями ионных реакций отмечают взаимодействия электролитов в растворах, которые знакомы нам с первых шагов познания неорганической химии, реакции присоединения к непредельным углеводородам, дегидрирование спиртов и замещение гидроксильной группы в спиртах.
Правило Владимира Васильевича Марковникова
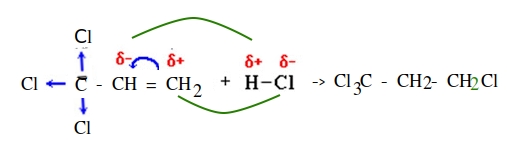
Формулировка гласит следующим образом: при присоединении протонных кислот или воды к несимметричным алкенам или алкинам, атом водорода присоединяется к наиболее гидрогенизированному атому углерода. Проще говоря, атом водорода присоединяется к тому атому углерода, у которого наименьшее количество связей с водородом, рассмотрим это заключение на примере гидрогалогенирования пропена:
Но также существуют и исключения из этого правила, когда заместитель при двойной связи оттягивает электронную плотность на себя
или при присоединении в присутствии пероксидов
Радикальный механизм
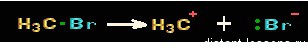
Происходит деление общей пары электронов между атомами, приводя к образованию нейтрально заряженных частиц (радикалов), которые имеют неспаренные электроны. Будучи гомолитическим, такой разрыв возможен при малополярной ковалентной связи.
Реакции, проходящие по этому механизму, происходят в газовой фазе с огромной скоростью, зачастую сопровождаясь взрывом. Сами радикальные взаимодействия возникают между образовавшимися в ходе взаимодействия нейтрально заряженными частицами и молекулами.
Весьма немалое количество органических реакций протекают по радикальному механизму, например: галогенирование алканов, полимеризация этилена и синтез аммиака.
1.4.10 Ионный и радикальный механизмы реакций в органической химии
Видеоурок: Классификация реакций: ионные и радикальные реакции
Лекция: Ионный и радикальный механизмы реакций в органической химии
На предыдущих уроках мы рассматривали различные типы неорганических реакций, классифицируемых по тепловому эффекту, обратимости, изменению степени окисления и др. На данном уроке пойдет речь о типах органических химических реакций, которые классифицируются по механизму разрыва существующих химических связей и образования новых. Выделяют радикальный и ионный механизмы реакций.

Если общая электронная пара делится между атомами, образуются радикалы – нейтральные частицы, имеющие неспаренные электроны. Такой разрыв возможен при неполярной или малополярной ковалентной связи, называется радикальным и является гомолитическим:
Химические реакции с участием радикалов происходят в газовой фазе при большой скорости. Чаще всего со взрывом. Радикальные реакции проходят между появившимися в ходе реакции радикалами и молекулами.
Такие реакции называются цепными.
Инициация галогенирования, обычно, происходит под действием облучения:
Радикальными являются большое количество реакций горения органических и неорганических веществ. Сюда можно отнести: синтез воды, аммиака, полимеризацию этилена.

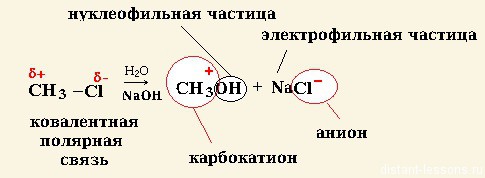
Если при разрыве связи общая электронная пара остается у одного атома образуются ионы (катионы и анионы). Такой разрыв возможен при полярной ковалентной связи, называется ионным и является гетероциклическим:
В результате такого разрыва образовались:
Ионными являются реакции электролитов в растворе (неорганическая химия). А из органической химии – реакции присоединения к алкенам, окисление, дегидрирование спиртов, замещение спиртовой группы.
Механизмы реакций в органической химии
Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии.
Механизмы разрыва химических связей в органических реакциях
| Гомолитический разрыв связи – это такой разрыв химической связи, когда каждый атом получает при разрыве связи по одному электрону из общей электронной пары. |
Образующиеся при этом частицы — это свободные радикалы.
| Свободные радикалы – это частицы, каждая из которых содержит один неспаренный электрон. A:B → A∙ + ∙B Гомолитический разрыв связи характерен для слабо полярных или неполярных связей. Условия протекания радикальных реакций: То есть реакция протекает как цепь последовательных превращений с участием свободных радикалов. Свободные радикалы R∙ – это атомы или группы связанных между собой атомов, которые содержат один или несколько неспаренных электронов. Свободные радикалы – очень активные частицы, которые стремятся образовать связь с каким-либо другим атомом. Этапы радикально-цепного процесса: Стадия 1. Инициирование цепи. Под действием кванта света или при нагревании молекула галогена распадается на радикалы: Cl:Cl → Cl⋅ + ⋅Cl Стадия 2. Развитие цепи. Радикалы взаимодействуют с молекулами с образованием новых молекул и радикалов. Радикал галогена взаимодействует с молекулой алкана и отрывает от него водород. При этом образуется промежуточная частица – алкильный радикал, который в свою очередь взаимодействует с молекулой хлора: CH4 + ⋅Cl → CH3⋅ + HCl Стадия 3. Обрыв цепи. При протекании цепного процесса рано или поздно радикалы сталкиваются с радикалами. При этом образуются молекулы, т.е. радикальный процесс обрывается. Могут столкнуться разные радикалы, в том числе два метильных радикала:
При гетеролитическом разрыве связи образуются ионы – положительно заряженный катион и отрицательно заряженный анион. A:B → A: – + B +
Гетеролитический (ионный) механизм характерен для полярных и легко поляризуемых связей. Условия протекания ионных реакций: Присоединение галогеноводородов (гидрогалогенирование). Например, этилен взаимодействует с бромоводородом: Реакция протекают по механизму электрофильного присоединения в несколько стадий. II стадия. Карбокатион взаимодействует с анионом Br – : При присоединении галогеноводородов и других полярных молекул к симметричным алкенам образуется одно вещество. При присоединении полярных молекул к несимметричным алкенам образуется смесь изомеров. При этом выполняется правило Марковникова.
В некоторых случаях присоединение к двойным связям происходит против правила Марковникова. Исключения из правила Марковникова: 1) Если в молекуле присутствует заместитель, который оттягивает на себя электронную плотность двойной связи. 2) Если в реакционной системе присутствуют свободные радикалы или источники свободных радикалов, то реакция присоединения полярных молекул вида НХ к двойной связи протекает по радикальному механизму против правила Марковникова. Химия, Биология, подготовка к ГИА и ЕГЭИонный и радикальный механизмы |