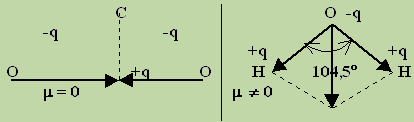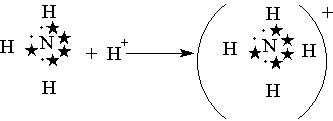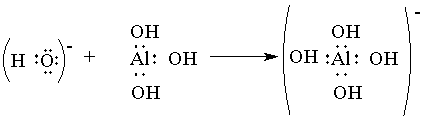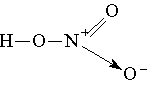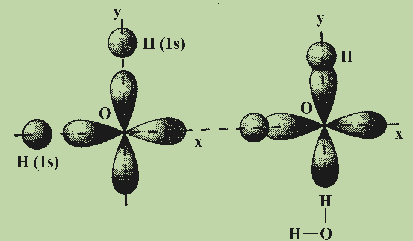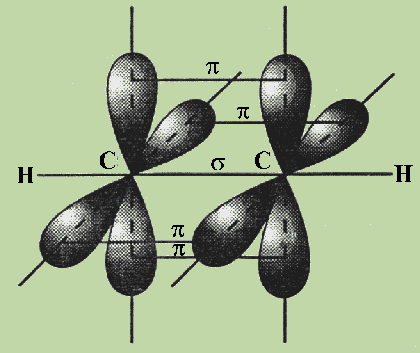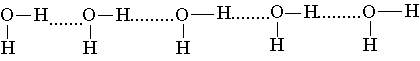Атомы и электроны
Атомно-молекулярное учение
Описываемая модель атома называется «планетарной» и была предложена в 1913 году великими физиками: Нильсом Бором и Эрнестом Резерфордом
Запомните, что в невозбужденном состоянии атом содержит одинаковое число электронов и протонов. Так у кальция (порядковый номер 20) в ядре находится 20 протонов, а вокруг ядра на электронных орбиталях 20 электронов.
Я еще раз подчеркну эту важную деталь. На данном этапе будет отлично, если вы запомните простое правило: порядковый номер элемента = числу электронов. Это наиболее важно для практического применения и изучения следующей темы.
Электронная конфигурация атома
Электроны атома находятся в непрерывном движении вокруг ядра. Энергия электронов отличается друг от друга, в соответствии с этим электроны занимают различные энергетические уровни.
Состоит из s-подуровня: одной «s» ячейки (2s 2 ) и p-подуровня: трех «p» ячеек (2p 6 ), на которых помещается 6 электронов
Состоит из s-подуровня: одной «s» ячейки (3s 2 ), p-подуровня: трех «p» ячеек (3p 6 ) и d-подуровня: пяти «d» ячеек (3d 10 ), в которых помещается 10 электронов
Состоит из s-подуровня: одной «s» ячейки (4s 2 ), p-подуровня: трех «p» ячеек (4p 6 ), d-подуровня: пяти «d» ячеек (4d 10 ) и f-подуровня: семи «f» ячеек (4f 14 ), на которых помещается 14 электронов
Зная теорию об энергетических уровнях и порядковый номер элемента из таблицы Менделеева, вы должны расположить определенное число электронов, начиная от уровня с наименьшей энергией и заканчивая к уровнем с наибольшей. Чуть ниже вы увидите несколько примеров, а также узнаете об исключении, которое только подтверждает данные правила.
Подуровни: «s», «p» и «d», которые мы только что обсудили, имеют в определенную конфигурацию в пространстве. По этим подуровням, или атомным орбиталям, движутся электроны, создавая определенный «рисунок».
Правила заполнения электронных орбиталей и примеры
Должно быть, вы обратили внимание на некоторое несоответствие: после 3p подуровня следует переход к 4s, хотя логично было бы заполнить до конца 4s подуровень. Однако природа распорядилась иначе.
Запомните, что, только заполнив 4s подуровень двумя электронами, можно переходить к 3d подуровню.
Теперь мы располагаем указанное количество электронов на энергетических уровнях, руководствуясь правилами заполнения.
Обращаю ваше особе внимание: на 2p-подуровне углерода мы расположили 2 электрона в разные ячейки, следуя одному из правил. А на 3p-подуровне у серы электронов оказалось много, поэтому сначала мы расположили 3 электрона по отдельным ячейкам, а оставшимся одним электроном дополнили первую ячейку.
Внешний уровень и валентные электроны
Тренировка
Потренируйтесь и сами составьте электронную конфигурацию для магния и скандия. Определите число электронов на внешнем (валентном) уровне и число неспаренных электронов. Ниже будет дано наглядное объяснение этой задаче.
Химия
ОСНОВЫ ТЕОРЕТИЧЕСКОЙ ХИМИИ
5. Химическая связь
Согласно теории химической связи, наибольшей устойчивостью обладают внешние оболочки из двух или восьми электронов (электронные группировки благородных газов). Атомы, имеющие на внешней оболочке менее восьми (или иногда двух) электронов, стремятся приобрести структуру благородных газов. Такая закономерность позволила В. Косселю и Г. Льюису сформулировать положение, которое является основным при рассмотрении условий образования молекулы: “При образовании молекулы в ходе химической реакции атомы стремятся приобрести устойчивую восьмиэлектронную (октет) или двухэлектронную (дублет) оболочки”.
Образование устойчивой электронной конфигурации может происходить несколькими способами и приводить к молекулам (и веществам) различного строения, поэтому различают несколько типов химической связи. Таковы ионная, ковалентная и донорно-акцепторная (координационная) связи. Кроме этих видов связей существуют другие, не относящиеся непосредственно к электронным оболочкам. Таковы водородная и металлическая связи.
Валентность элементов в соединениях. Современные представления о природе химической связи основаны на электронной (спиновой) теории валентности (наибольший вклад в развитие этой теории внесли Г. Льюис и В. Коссель), в соответствии с которой атомы, образуя связи, стремятся к достижению наиболее устойчивой (т. е. имеющей наименьшую энергию) электронной конфигурации. При этом электроны, принимающие участие в образовании химических связей, называются валентными.
Согласно спиновой теории, валентность атома определяется числом его неспаренных электронов, способных участвовать в образовании химических связей с другими атомами, поэтому валентность всегда выражается небольшими целыми числами.
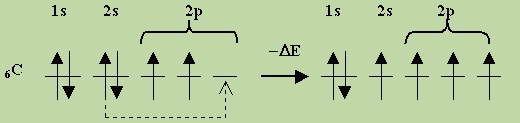
Рассмотрим электронную конфигурацию атома углерода. В свободном состоянии он имеет два неспаренных электрона и два спаренных электрона в состоянии 2s. В определенных условиях (при затрате некоторого количества энергии извне) эту пару электронов 2s 2 можно разъединить (“распарить”) путем перевода одного электрона из состояния 2s в состояние 2р и сделать эти электроны также валентными:
В таком состоянии атом углерода может образовывать соединения, где он будет четырехвалентен.
Процесс распаривания электронов требует определенной затраты энергии ( D E), и, казалось бы, он не выгоден. Но для учета энергетических соотношений нужно рассмотреть весь баланс образования связей. Дело в том, что при переходе одного из электронов 2s в состояние 2р получается состояние атома, в котором он может образовать уже не две, а четыре связи. При образовании химической связи обычно выделяется энергия, поэтому появление двух новых валентностей приводит к выделению дополнительной энергии, которая превосходит энергию D E затраченную на распаривание 2s-электронов.
Опыты доказали, что энергия, затраченная на распаривание электронов в пределах одного энергетического уровня, как правило, полностью компенсируется энергией, выделенной при образовании дополнительных связей.
Чтобы таким же образом получить, например, четырехвалентный кислород, трехвалентный литий, двухвалентный неон, необходима очень большая затрата энергии D E связанная с переходом 2р ® 3s (кислород). 1s ® 2р (литий), 2р ® 3s (неон). В этом случае затрата энергии настолько велика, что не может быть компенсирована энергией, выделяющейся при образовании химических связей. Поэтому и не существует соединений с переменной валентностью кислорода, лития или неона.
Энергия связи. Существенной характеристикой химической связи является ее прочность. Для оценки прочности связей обычно пользуются понятием энергии связей.
Ионная связь. Ионная связь — это электростатическое взаимодействие между ионами с зарядами противоположного знака.
Валентность элементов в соединениях с ионными связями очень часто характеризуют степенью окисления, которая, в свою очередь, соответствует величине заряда иона элемента в данном соединении.
Использование понятия степени окисления для атомов элементов, образующих другие виды химической связи, не всегда корректно и требует большой осторожности.
Представим себе, что мы имеем два отдельных изолированных атома водорода Н’ и Н». При сближении этих атомов между собой силы электростатического взаимодействия — силы притяжения электрона атома Н’ к ядру атома Н» и электрона атома Н» к ядру атома Н’ — будут возрастать: атомы начнут притягиваться друг к другу. Однако одновременно будут возрастать и силы отталкивания между одноименно заряженными ядрами атомов и между электронами этих атомов. Это приведет к тому, что атомы смогут сблизиться между собой настолько, что силы притяжения будут полностью уравновешены силами отталкивания. Расчет этого расстояния ( длины ковалентной связи ) показывает, что атомы сблизятся настолько, что электронные оболочки, участвующие в образовании связи, начнут перекрываться между собой. Это, в свою очередь, приведет к тому, что электрон, двигавшийся ранее в поле притяжения только одного ядра, получит возможность перемещаться и в поле притяжения другого ядра. Таким образом, в какой-то момент времени то вокруг одного, то вокруг другого атома будет возникать заполненная оболочка благородного газа (такой процесс может происходить только с электронами, обладающими противоположно направленными проекциями спина). При этом возникает общая пара электронов, одновременно принадлежащая обоим атомам.
Область перекрытия между электронными оболочками имеет повышенную электронную плотность, которая уменьшает отталкивание между ядрами и способствует образованию ковалентной связи.
Таким образом, связь, осуществляемая за счет образования электронных пар, в одинаковой мере принадлежащих обоим атомам, называется ковалентной.
Полярность связи. Ковалентная связь может возникать не только между одинаковыми, но и между разными атомами. Так, образование молекулы НСl из атомов водорода и хлора происходит также за счет общей пары электронов, однако эта пара в большей мере принадлежит атому хлора, нежели атому водорода, поскольку неметаллические свойства у хлора выражены гораздо сильнее, чем у водорода.
Разновидность ковалентной связи, образованной одинаковыми атомами, называют неполярной, а образованной разными атомами — полярной.
Дипольный момент является величиной векторной и направлен по оси диполя от отрицательного заряда к положительному. Следует различать дипольные моменты (полярность) связи и молекулы в целом. Так, для простейших двухатомных молекул дипольный момент связи равен дипольному моменту молекулы.
Напротив, в молекуле оксида углерода (IV) каждая из связей полярна, а молекула в целом неполярна ( m =0), так как молекула О==С==О линейна, и дипольные моменты связей С==О компенсируют друг друга (см. рис.). Наличие дипольного момента в молекуле воды означает, что она нелинейна, т. е. связи О—Н расположены под углом, не равным 180° (см. рис.).
Электроотрицательность. Наряду с дипольными моментами для оценки степени ионности (полярности) связи используют и другую распространенную характеристику, называемую электроотрицательностью.
Электроотрицательность — это способность атома притягивать к себе валентные электроны других атомов. Электроотрицательность (ЭО) не может быть измерена и выражена в единицах каких-либо физических величин, поэтому для количественного определения ЭО предложены несколько шкал, наибольшее признание и распространение из которых получила шкала относительных ЭО, разработанная Л. Полингом.
По шкале Полинга ЭО фтора (наиболее электроотрицательного из всех элементов) условно принята равной 4,0;на втором месте находится кислород, на третьем — азот и хлор. Водород и типичные неметаллы находятся в центре шкалы; значения их ЭО близки к 2. Большинство металлов имеют значения ЭО, приблизительно равные 1,7 или меньше. ЭО является безразмерной величиной.
Шкала ЭО Полинга в общих чертах напоминает периодическую систему элементов. Эта шкала позволяет дать оценку степени ионностй (полярности) связи. Для этого используют зависимость между разностью ЭО и степенью ионности связи.
Чем больше разность ЭО, тем больше степень ионности. Разность ЭО, равная 1,7, соответствует 50%-ному ионному характеру связей, поэтому связи с разностью ЭО больше 1,7 могут считаться ионными, связи с меньшей разностью относят к ковалентным полярным.
Энергия ионизации. Энергия ионизации — это энергия, необходимая для отрыва наиболее слабо связанного электрона от атома. Она обычно выражается в электрон-вольтах. При отрыве электрона от атома образуется соответствующий катион.
Энергия ионизации для элементов одного периода возрастает слева направо с возрастанием заряда ядра. В подгруппе она уменьшается сверху вниз вследствие увеличения расстояния электрона от ядра.
Энергия ионизации связана с химическими свойствами элементов. Так, щелочные металлы, имеющие небольшие энергии ионизации, обладают ярко выраженными металлическими свойствами. Химическая инертность благородных газов связана с их высокими значениями энергии ионизации.
Сродство к электрону. Атомы могут не только отдавать, но и присоединять электроны. При этом образуется соответствующий анион. Энергия, которая выделяется при присоединении к атому одного электрона, называется сродством к электрону. Обычно сродство к электрону, как и энергия ионизации, выражается в электрон-вольтах. Значения сродства к электрону известны не для всех элементов; измерять их весьма трудно. Наиболее велики они у галогенов, имеющих на внешнем уровне по 7 электронов. Это говорит об усилении неметаллических свойств элементов по мере приближения к концу периода.
Понятие степени окисления было введено в предположении о полном смещении пар электронов к тому или другому атому (показывая при этом заряд ионов, образующих ионное соединение). Поэтому в полярных соединениях степень окисления означает число электронов, лишь смещенных от данного атома к атому, связанному с ним.
Совсем формальным понятие “степень окисления” становится, когда оно используется при рассмотрении ковалентного соединения, поскольку степень окисления — это условный заряд атома в молекуле, вычисленный исходя из предположения, что молекула состоит только из ионов. Ясно, что в действительности никаких ионов в ковалентных соединениях нет.
Таким образом, нужно помнить, что степень окисления — условное, формальное понятие и, чаще всего не характеризует реальное валентное состояние атома в молекуле.
Донорно-акцепторная связь. Помимо механизма образования ковалентной связи, согласно которому общая электронная пара возникает при взаимодействии двух электронов, существует также особый до-норно-акцепторный механизм. Он заключается в том, что ковалентная связь образуется в результате перехода уже существующей электронной пары донора (поставщика электронов) в общее пользование донора и акцептора. Донорно-акцепторный механизм хорошо иллюстрируется схемой образования иона аммония (звездочками обозначены электроны внешнего уровня атома азота):
Аналогично происходит образование связей и во многих других молекулах, даже в таких “простых”, как молекула НNО 3 :
Атом азота при этом отдает свою электронную пару атому кислорода, который ее принимает: в результате как вокруг атома кислорода, так и вокруг азота достигается полностью завершенная восьмиэлектронная оболочка, но поскольку атом азота отдал свою пару и поэтому владеет ею совместно с другим атомом, он приобрел заряд “+”, а атом кислорода — заряд “-”. C тепень окисления азота в HNO 3 равна 5+, тогда как валентность равна 4.
Пространственное строение молекул. Представления о природе ковалентных связей с учетом типа орбиталей, участвующих в образовании химической связи, позволяют делать некоторые суждения о форме молекул.
Рассмотрим примеры, которые позволяют понять общие закономерности в направленности химических связей. Обсудим образование связей в молекуле воды H 2 O. Молекула H 2 O образуется из атома кислорода и двух атомов водорода. Атом кислорода имеет два неспаренных электрона, которые занимают две орбитали, расположенные под углом 90° друг к другу. Атомы водорода имеют неспаренные 1s-электроны. Ясно, что углы между двумя связями О—Н, образованными р-электронами атома кислорода с s-электронами атомов водорода, должны быть прямыми или близкими к нему (см. рис.).
Увеличение валентных углов (> 90°) вполне объяснимо взаимным отталкиванием не связанных друг с другом атомов, которое мы не учитывали при предсказании углов между связями. Так, взаимное отталкивание атомов водорода в молекуле H 2 S слабее, чем в молекуле Н 2 О (так как радиус атома серы больше радиуса атома кислорода), поэтому и валентные углы Н—S—Н ближе к 90°, чем углы Н—О—Н.
Таким образом, двухвалентный атом неметалла с двумя валентными р-орбиталями образует изогнутую (угловую, с углом, близким к 90°) молекулу, а трехвалентный атом с тремя валентными р-орбиталями образует молекулу, имеющую форму пирамиды.
Рассуждая как в случае H 2 O, можно было бы предполагать, что атом углерода будет образовывать три связи С—Н, направленные под прямым углом друг к другу (р-электроны), и одну связь, образованную s-электроном, направление которой было бы произвольным, поскольку s-орбиталь имеет сферическую симметрию.
Следовательно, можно было ожидать, что три связи С—Н в СН 4 являются направленными p-связями и совершенно одинаковы, а четвертая связь есть ненаправленная s—s-связь и отличается от первых трех.
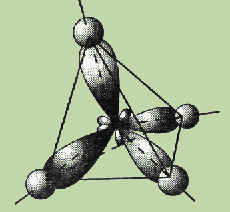
Однако экспериментальные данные показали, что все четыре связи С—Н в молекуле метана СН 4 одинаковы и направлены к вершинам тетраэдра (угол между ними составляет 109,5°).
Ввиду относительной близости значений энергии 2s- и 2p-электронов эти электроны могут взаимодействовать между собой в ходе образования химической связи с электронами другого атома, давая четыре новых равноценных гибридных электронных облака.
Это обусловливает более сильное перекрывание таких орбиталей с орбиталями электронов других атомов по сравнению с перекрыванием s- и р-орбиталей и приводит к образованию более прочных связей.
Гибридизация оказывается характерной не только для соединений атома углерода. Гибридизация орбиталей может происходить в том случае, когда в образовании связей одновременно участвуют электроны, которые принадлежат к различным типам орбиталей.
Водородная связь. Само название этого типа связи подчеркивает, что в ее образовании принимает участие атом водорода. Водородные связи могут образовываться в тех случаях, когда атом водорода связан с электроотрицательным атомом, который смещает на себя электронное облако, создавая тем самым положительный заряд d + на водороде.
Водородная связь, как и другие рассмотренные нами типы связей, обусловлена электростатическим взаимодействием, но это взаимодействие осуществляется уже не между атомами, а между молекулами. Таким образом, водородная связь — пример межмолекулярной связи.
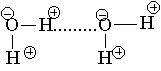
Водородная связь обычно схематично изображается точками.
поскольку атом кислорода имеет две неподеленные пары электронов.
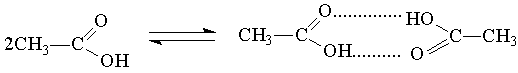
Водородные связи могут возникать как между различными молекулами, так и внутри молекулы, если в этой молекуле имеются группы с донорной и акцепторной способностями. Например, именно внутримолекулярные водородные связи играют основную роль в образовании пептидных цепей, которые определяют строение белков. По-видимому, наиболее важным и, несомненно, одним из наиболее известных примеров влияния внутримолекулярной водородной связи на структуру является дезоксирибонуклеиновая кислота (ДНК). Молекула ДНК свернута в виде двойной спирали. Две нити этой двойной спирали связаны друг с другом водородными связями.
Металлическая связь. Большинство металлов обладает рядом свойств, имеющих общий характер и отличающихся от свойств других простых или сложных веществ. Такими свойствами являются сравнительно высокие температуры плавления, способность к отражению света, высокая тепло- и электропроводность. Эти особенности обязаны существованию в металлах особого вида связи — металлической связи.
В соответствии с положением в периодической системе атомы металлов имеют небольшое число валентных электронов. Эти электроны достаточно слабо связаны со своими ядрами и могут легко отрываться от них. В результате этого в кристаллической решетке металла появляются положительно заряженные ионы и свободные электроны. Поэтому в кристаллической решетке металлов существует большая свобода перемещения электронов: одни из атомов будут терять свои электроны, а образующиеся ионы могут принимать эти электроны из “электронного газа”. Как следствие этого, металл представляет собой ряд положительных ионов, локализованных в определенных положениях кристаллической решетки, и большое количество электронов, сравнительно свободно перемещающихся в поле положительных центров. В этом состоит важное отличие металлических связей от ковалентных, которые имеют строгую направленность в пространстве. В случае металлов невозможно говорить о направленности связей, так как валентные электроны распределены по кристаллу почти равномерно. Именно этим и объясняется, например, пластичность металлов, т. е. возможность смещения ионов и атомов в любом направлении без нарушения связи.
Электронная конфигурация атомов и ионов. Основное и возбужденное состояние атомов
Содержание:
Электронная конфигурация атомов
Записать распределение электронов по энергетическим уровням можно несколькими способами.
Запись по электронным оболочкам (схема электронного строения)
Показывает заряд ядра и количество электронов на каждом энергетическом уровне.
Легче всего начинать с неё, потому что она показывает структуру атома «крупным планом».
Запись с обозначением энергетических уровней и подуровней
Каждая орбиталь обозначается квадратной ячейкой. Электрон обозначается стрелкой. Различное направление стрелок указывает на противоположные спины.Под ячейкой подписывают номер энергетического уровня, буквенное обозначение орбитали и количество электронов на ней.
Буквенно-числовое обозначение такого «адреса» электрона – это электронная формула. Электронная конфигурация – это электронная формула, которая показывает распределение электронов по энергетическим уровням.
Электронная конфигурация атомов 1 и 2 периодов
Электронная конфигурация атомов 3 периода
Электронная конфигурация атомов 4 периода
Заполнение орбиталей атомов 4 периода имеет свои особенности.
На движение электрона влияют поле ядра и поле других электронов. Поэтому в атомах с большим количеством электронов энергия электрона определяется главным и орбитальным квантовыми числами.
Здесь уже надо смотреть на сумму обоих квантовых чисел (n+l). Если для двух подуровней эта сумма равна: 3d, 4p, 5s (n+l=5), то сначала заполняются уровни с меньшими значениями n. То есть последовательность заполнения будет следующей: 3d – 4p – 5s.
Поэтому в 4 периоде сначала заполняется подуровень 4s, а потом подуровень 3d.
Есть ещё одна особенность, которая появляется в 4 периоде. Хром и медь имеют на 4s-орбитали по одному электрону. Всё дело в заполнении d-оболочек. Полузаполненные или заполненные d-оболочки устойчивее частично заполненных. В атоме хрома на каждой из 5 3d-орбиталей есть по одному электрону. В атоме меди на каждой на каждой 3d-орбитали есть по два электрона.
Алгоритм записи электронной конфигурации атома
Электронная конфигурация ионов
Электронная конфигурация ионов составляется по тем же принципам. Нужно учитывать изменения количества электронов на внешнем энергетическом уровне.
Атом электронейтрален, то есть сколько протонов ядре, столько же электронов в атоме. Если атом принимает электроны, он становится отрицательно заряженным ионом (анионом), если отдаёт электроны – положительно заряженным ионом (катионом).
Атому легче всего отдать электроны внешнего энергетического уровня, «чужие» электроны он тоже примет на внешний энергетический уровень. На внешнем энергетическом уровне не может находиться более 8 электронов. Теория «октета» была предложена в 1916 году Гилбертом Ньютоном Льюисом и Вальтером Косселем
Атом «стремится» добрать электроны на внешний уровень или избавиться от них, поэтому и становится ионом. Полное заполнение s- и p-подуровней внешнего уровня придаёт атому стабильность. Только атом гелия имеет на единственном внешнем энергетическом уровне 2 электрона, а не 8, потому что первый энергетический уровень состоит только из одной s-орбитали.
Количество электронов на внешнем энергетическом уровне определяется по таблице Менделеева. У элементов главных подгрупп номер группы – это и есть количество электронов на внешнем уровне. У элементов побочных подгрупп количество электронов на внешнем уровне не больше двух.
Основное и возбуждённое состояния атома
На первый взгляд кажется, что атом хлора может образовывать только одну связь и соединения одного типа – например, хлориды. Но откуда берутся хлорная, хлорноватая, хлористая и хлорноватистая кислоты?
Дело в том, что атом можно перевести из основного состояния в возбуждённое.
Основное состояние – это состояние атома с наименьшей энергией. Атом обладает наименьшей энергией в основном состоянии. Но если ему передать дополнительную энергию, он перейдёт в возбуждённое состояние. Электроны перейдут на уровень или подуровень с большей энергией.
Сначала разрываются электронные пары на 3p-подуровне, электроны переходят на 3d-подуровень. Если атом хлора получит ещё больше энергии, спаренный электрон покинет даже 3s-орбиталь и перейдёт на 3d-подуровень.
Благодаря этому атом хлора может образовывать больше химических связей. Затраты энергии, потраченные на распаривание электронов, окупаются при образовании новых химических связей.
Но в возбуждённое состояние могут перейти атомы, у которых есть неспаренные электроны и свободные орбитали. Длится возбуждённое состояние недолго: атом отдаст энергию и вернётся в основное состояние. Хотя если сообщить атому слишком много энергии, электрон покинет его и атом станет ионом.