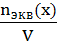Классификация растворов



Растворимость. Способы выражения концентрации растворов. Растворение как физико-химический процесс.
Цели:
− Сформировать представление о понятиях: «раствор», «растворение», «растворимость», «концентрация».
− Рассмотреть физическую, химическую и современную теорию растворов.
− Показать значение растворов в жизни человека.
− Закрепить знания, умения и навыки учащихся по решению задач на тему растворы.
− Развитие у студентов навыков наблюдения, логического мышления, умений делать выводы и заключения.
Ход лекции
I. Организационный момент. Проверка знаний по скорости химической реакции.
II. Объяснение нового материала.
Учитель: Растворы играют важную роль в природе, технике и науке.
Где используются растворы? (ответы учащихся)
Учитель: Велика роль растворов в возникновении и развитии жизни на Земле. Одной из теорий возникновения организмов является теория зарождения жизни в первичном океане, который представлял собой воду с растворенными в ней веществами. Из этого раствора организмы получали необходимые для роста и развития ионы и молекулы.
В организме человека находятся физиологически важные растворы. Какие? (кровь, желудочный сок и др.)
Раствор – это гомогенная система, состоящая из двух или более компонентов, содержание которых можно изменять в определенных пределах без нарушения однородности.
Раствор – гомогенная (однородная) система, состоящая из частиц растворенного вещества, растворителя и продуктов их взаимодействия.
Классификация растворов
• по агрегатному состоянию:газовые(воздух), жидкие(морская вода), твердые (сплавы)
• по составу растворителя (водные, аммиачные, бензольные и др.)
По размеру частиц или по степени измельченности (дисперстности):
Приведите примеры природных грубодисперсных систем?
Коллоидные растворы отличаются тем, что их частицы сильно рассеивают проходящий через них свет и делают заметным путь пропущенного светового луча (эффект Тиндаля).
Концентрация насыщенного раствора наз. растворимостью с указанием температуры, при которой она определена.
n Растворимость — число моль растворенного в-ва в одном литре раств-ля (в состоянии насыщения)
Раствори́мость — способность вещества образовывать с другими веществами однородные системы — растворы, в которых вещество находится в виде отдельных атомов, ионов, молекул или частиц. Растворимость выражается концентрацией растворённого вещества в его насыщенном растворе либо в процентах, либо в весовых или объёмных единицах Растворимость газов в жидкости зависит от температуры и давления. Растворимость жидких и твёрдых веществ — практически только от температуры.
Истинные растворы – термодинамически устойчивые системы, неограниченно стабильные во времени.
Движущими силами образования растворов являются энтропийный и энтальпийный факторы. При растворении газов в жидкости энтропия всегда уменьшается ΔS 0). Чем сильнее взаимодействие растворенного вещества и растворителя, тем больше роль энтальпийного фактора в образовании растворов. Знак изменения энтальпии растворения определяется знаком суммы всех тепловых эффектов процессов, сопровождающих растворение, из которых основной вклад вносят разрушение кристаллической решетки на свободные ионы (ΔH > 0) и взаимодействие образовавшихся ионов с молекулами растворителя (сольтивация, ΔH 
Лекция 5: Растворы. Свойства растворов. Способы выражения концентрации растворов
Лекция 5: Растворы. Свойства растворов. Способы выражения концентрации растворов.
1. Понятие о растворах. Классификация растворов.
2. Растворимость веществ. Факторы, влияющие на растворимость веществ.
3. Сущность процесса растворения. Термодинамика процесса растворения.
4. Способы выражения концентрации растворов.
5. Коллигативные свойства растворов.
1.Растворы. Классификация растворов.
Раствором называется гомогенная (однородная) система, состоящая из двух или более независимых компонентов (растворенное вещество и растворитель), а также продуктов их взаимодействия. Компонент, количество которого преобладает в данной системе, называют растворителем.
По агрегатному состоянию растворы делятся:
- газообразные растворы: воздух – это раствор кислорода, паров воды, углекислого газа СО2 и благородных газов в азоте; твердые растворы: сплавы металлов; жидкие растворы в свою очередь делятся: растворы твердых веществ в жидкостях: соль+Н2О, сахар+Н2О, йод+Н2О растворы газообразныхых веществ в жидкостях: лимонады, нашатырный спирт
3. растворы жидких веществ в жидкостях: уксус, водка (спирт + вода)
Наибольшее значение для химии имеют растворы, в которых растворителем является жидкость. Относительное содержание компонентов в растворе может быть любым, оно ограничено лишь взаимной растворимостью веществ, которая зависит от их химической природы, их сродства друг к другу, а также от условий приготовления растворов – температуры, давления (в случае растворения газов), присутствия других растворенных веществ.
По относительным количествам растворенного вещества и растворители растворы бывают: разбавленные и концентрированные.
По соотношению преобладания частиц, переходящих в раствор и удаляющихся из раствора, различают растворы насыщенные, ненасыщенные и перенасыщенные.
Раствор концентрация которого ниже концентрации насыщенного раствора называется ненасыщенным. В таком растворе можно при тех же условиях растворить дополнительное количество того же самого вещества.
Если раствор, насыщенный при нагревании, осторожно охладить до комнатной температуры так, чтобы не выделялись кристаллы соли, то образуется перенасыщенный раствор. Таким образом, перенасыщенным называется раствор, в котором при данной температуре содержится большее количество растворенного вещества, чем возможно в насыщенном растворе. Перенасыщенный раствор нестабилен, и при изменении условий (например при энергичном встряхивании или внесении кристаллика соли – затравки для кристаллизации) образуется насыщенный раствор и осадок кристаллов соли.
2. Растворимость веществ. Факторы, влияющие на растворимость веществ.
Количественной характеристикой соотношения компонентов насыщенного раствора является растворимость. Наиболее распространенными способами такой характеристики служат:
· коэффициент растворимости вещества (Р) – наибольшая масса вещества, способная при данной температуре раствориться в 100 г растворителя. Например, при 20ْ С в 100 г воды с образованием насыщенного раствора растворяется 36,0 г NaCI, значит Р(NaCI) = 36.
· молярная растворимость вещества (S) — число молей вещества, способное при данной температуре раствориться в 1 л указанного растворителя с образованием насыщенного раствора. Так, S(NaCI) = 6,154 моль\л
· коэффициент поглощения газа –наибольший объем газа, который может раствориться в единице объема растворителя при данной температуре и парциальном давлении газа 1 атм. Так при 20ْ С коэффициенты поглощения водой азота и кислорода, молекулы которых неполярны, составляют соответственно 0,016 и 0,031. Для газов, молекулы которых полярны, коэффициент их поглощения водой значительно выше, например для HCI – 500, NH3 – 1300.
Растворимость веществ существенно зависит от природы растворяемого вещества и растворителя, температуры и давления.
Зависимость от природы реагирующих веществ
Наибольшая растворимость достигается тогда, когда эти силы межмолекулярного взаимодействия имеют подобный характер: «подобное растворяется в подобном». Так вещества с ионным типом химической связи (соли, щелочи) или, полярные (спирты, альдегиды) хорошо растворимы в полярных растворителях, например в воде. И наоборот малополярные соединения, например оксид углерода (II) хорошо растворимы в неполярных соединениях, например в сероуглероде.
Зависимость от температуры.
Так как растворение процесс обратимый, значит к нему применим принцип Ле-Шателье: если растворение вещества происходит с поглощением теплоты, то повышение температуры приводит к увеличению растворимости.
Для большинства твердых веществ повышение температуры способствует увеличению растворимости.
3. Сущность процесса растворения. Термодинамика процесса растворения.
Процесс растворения можно выразить схемой:
растворенное вещество + растворитель ó вещество в растворе ± ∆ Н.
Тепловой эффект, сопровождающий процесс растворения, относящийся к 1 молю растворенного вещества называется молярной теплотой растворения ∆ Н раств.
∆Н 1 > 0 — количество теплоты, затраченной на распределение частиц растворяемого вещества среди молекул растворителя (процесс эндотермический).
∆Н 2 0 — энергия необходимая для разрушения кристаллической решетки и энергия необходимая для разрыва связей между молекулами растворителя (процесс эндотермический).
В зависимости от того преобладает первая или вторая составляющие, процесс растворения может быть экзотермический или эндотермический:
если │ ∆Н2 │> │∆ Н1│, процесс экзотермический и ∆Н 0.
4. Способы выражения состава растворов.
Состав растворов количественно принято выражать через безразмерные количественные величины – доли (массовую, объемную, молярную) и размерные величины – концентрации.
W (NaOH) = 5% или 0,05 означает, что
5 г NaOH находится в 100г раствора,
5 г NaOH находится в 95 г воды
Молярная доля N – отношение числа молей растворенного вещества к сумме числа молей растворенного вещества и растворителя.
Концентрация показывает отношение массы или количества вещества к объему раствора.
Молярная концентрация (молярность) См (моль/л) – показывает число молей растворенного вещества в одном литре раствора, выражается отношением количества растворенного вещества к объему раствора.
См-молярная концентрация раствора.
Ma – молярная масса вещества в г/моль
V – объем раствора в литрах
Для обозначения молярной концентрации применяются символы:
1М-одномолярный раствор См = 1 моль/л
0,1М-децимолярный раствор См = 0,1 моль/л
Раствор в котором содержится 1 моль растворенного вещества называется одномолярным.
2М раствор NaOH означает, что 2 моля NaOH содержится в 1 литре раствора, т. е 2* 40 = 80 г NaOH.
Нормальная концентрация (нормальность раствора) или молярная концентрация эквивалента, Сн (экв/л) – показывает число эквивалентов растворенного вещества, содержащихся в одном литре раствора.
Сн — нормальная концентрация [моль/л]
М эква – эквивалентная масса вещества в г/моль
V – объем раствора в литрах
Эквивалентом вещества называется реальная или условная частица вещества, которая может замещать, присоединять, высвобождаться или быть каким-либо образом эквивалентна (равнозначна) одному катиону H водорода в кислотно-основных растворах или одному электрону в окислительно-восстановительных реакциях. Число, показывающее, какая доля реальной частицы вещества эквивалентна одному катиону H или одному электрону называется фактором эквивалентности ( f экв ). Количество эквивалента (n экв) также как и количество вещества измеряется в молях. Масса одного моля эквивалента называется молярной массой эквивалента (Мэкв) также как и молярная масса измеряется в г/моль. Между собой эти две массы связаны следующим соотношением:
n(Н ) – число ионов водорода, способных замещаться на металл (основность кислоты)
n(ОН ) – число ионов гидроксогрупп (кислотность основания)
f экв = число атомов металла * заряд иона металла
С учетом фактора эквивалентности:
Титр раствора Т – показывает массу растворенного вещества, содержащуюся в 1 мл раствора.
Коллигативные свойства растворов.
Свойства растворов, которые зависят только от концентрации частиц в растворе и не зависят от природы растворенного вещества, называются коллигативными.
Растворы, образованные частицами строго одинакового размера, между которыми действуют примерно одинаковые силы межмолекулярного взаимодействия, не происходит химического взаимодействия, изменения температуры и объема называются идеальными. К идеальным растворам стремятся очень разбавленные растворы.
Коллигативные свойства разбавленных растворов могут быть описаны количественно и выражены в виде законов. К ним относятся:
· давление насыщенного пара растворителя над раствором
· температура кристаллизации раствора
· температура кипения раствора
Осмос. Осмотическое давление.
Растворы однородны по всем частям объема. Если в один сосуд поместить концентрированный раствор, а сверху разбавленный, то через некоторое время эта неоднородная масса вновь станет однородной. Такой самопроизвольный процесс перемешивания вещества, приводящий к выравниванию его концентрации называется диффузией.
Если между двумя растворами поместить полупроницаемую перегородку (мембрану), то выравнивание концентраций будет проходить только вследствие перемещения молекул воды. Такая односторонняя диффузия называется осмосом.
Осмос – односторонняя самопроизвольная диффузия молекул растворителя через полупроницаемую перегородку из раствора с низкой концентрацией в раствор с более высокой концентрацией.
Полупроницаемые перегородки способны пропускать только молекулы растворителя, но не пропускают молекулы растворенного вещества.
искусственные полупроницаемые перегородки – целлофан, пергамент, пленки из желатина.
Количественной характеристикой осмоса является осмотическое давление раствора.
Осмотическим давлением (Pосм.) называют избыточное гидростатическое давление, возникающее в результате осмоса и приводящее к выравниванию скоростей взаимного проникновения молекул растворителя сквозь мембрану с избирательной проницаемостью.
В 1887 г Вант-Гоффом в результате исследований была установлена такая зависимость:
См –молярная концентрация растворенного вещества, моль/л
R – универсальная газовая постоянная, 8,314 Дж/моль* К
Осмотическое давление разбавленного идеального раствора неэлектролита равно тому давлению, которое производило бы растворенное вещество, если бы при той же температуре находилось бы в газообразном состоянии и занимало бы объем, равный объему раствора.
Однако это уравнение справедливо только для растворов, в которых отсутствует взаимодействие частиц, т. е. для идеальных растворов. В реальных растворах имеют место межмолекулярные взаимодействия между молекулами вещества и растворителя, которые могут приводить или к диссоциации молекул растворенного вещества на ионы, или к ассоциации молекул растворенного вещества с образованием из них ассоциатов.
Диссоциации молекул растворенного вещества в водном растворе на ионы характерна для электролитов. В результате диссоциации число частиц в растворе увеличивается.
Ассоциация наблюдается, если молекулы вещества лучше взаимодействуют между собой, чем с молекулами растворителя. Это характерно для коллоидных растворов, что приводит к уменьшению числа частиц в растворе.
Для учета межмолекулярных взаимодействий в реальных растворах Вант-Гофф предложил использовать изотонический коэффициент i. Для молекул растворенного вещества физический смысл изотонического коэффициента:
i = число частиц растворенного вещества / число частиц исходного вещества.
Для растворов неэлектролитов, молекулы которых не диссоциируют и мало склонны к ассоциации, i =1.
Для водных растворов электролитов, вследствие диссоциации i > 1, причем максимальное его значение (i max) для данного электролита равно числу ионов в его молекуле:
Для растворов, в которых вещество находится в виде ассоциатов, i 1 для электролитов.
Изотонические растворы – имеют равное осмотическое давление. Гипертонические растворы– имеют большее осмотическое давление по сравнению с другим раствором. Гипотонические растворы – имеют меньшее осмотическое давление по сравнению с другим раствором.
Понижение давление пара растворов. Законы Рауля.
Над любой жидкостью устанавливается определенное давление пара, насыщающего пространство. В отличии от поверхности растворителя, поверхность раствора частично занята молекулами растворенного вещества. Именно поэтому испарение с поверхности растворов всегда меньше, чем с поверхности растворителя, и при одной и той же температуре давление насыщенного пара над раствором всегда будет ниже давления пара над чистым растворителем.
. Давление пара раствора, содержащего нелетучее растворенное вещество, прямо пропорционально мольной доле растворителя в данном растворе
• p — давление пара над раствором, Па;
• p0 — давление пара над чистым растворителем, Па;
• χр-ль — мольная доля растворителя.
• nв-ва и nр-ля – соответственно количество растворенного вещества и растворителя, моль.
• относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества:
• При этом принимаем, что χв-ва + χр-ль = 1
• Для растворов электролитов данное уравнение приобретает несколько иной вид, в его состав входит изотонический коэффициент i:
• Δp = i · p0 · χв-ва, где
• Δp — изменение давления паров раствора по сравнению с чистым растворителем;
• χв-ва — мольная доля вещества в растворе
• i – изотонический коэффициент.
i =1 для неэлектролитов, i > 1 для электролитов.
Изотонический коэффициент (или фактор Вант-Гоффа) — это параметр, не имеющий размерности, который характеризует поведение какого – либо вещества в растворе. То есть, изотонический коэффициент показывает, разницу содержания частиц в растворе электролита по сравнению с раствором неэлектролита такой же концентрации. Он тесно связан связан с процессом диссоциации, точнее, со степенью диссоциации и выражается следующим выражением:
n – количество ионов, на которые диссоциирует вещество.
α – степень диссоциации.
С понижением давления насыщенного пара растворителя над раствором связано повышение температуры кипения раствора и понижение температуры его замерзания. Любая жидкость кипит, когда давление насыщенного пара над ней становится равным атмосферному. Так как согласно I закону Рауля давление пара над раствором меньше, чем над раствором растворителя, то для того, чтобы раствор закипел, его нужно нагреть до более высокой температуры, чем растворитель. Таким образом, растворы кипят при более высокой температуре, а замерзают при более низкой температуре, чем чистый растворитель.
Разность температур кипения раствора и растворителя называется повышением температуры кипения.
Разность температур замерзания раствора и растворителя называется понижением температуры замерзания.
Понижение температуры замерзания и повышение температуры кипения не зависят от природы растворенного вещества и прямопропорциональны моляльной концентрации раствора.
Кэб – эбулиоскопическая константа
Ккр – криоскопическая константа
Cm – моляльная концентрация раствора [моль/кг растворителя]
i- изотонический коэффициент, i =1 для неэлектролитов, i > 1 для электролитов.
Кэб – эбулиоскопическая константа
Ккр – криоскопическая константа
Физический смысл:
Эбулиоскопическая константа (Кэб) – показывает повышение температуры кипения одномоляльного раствора по сравнению с чистым растворителем.
Криоскопическая константа (Ккр) – показывает понижение температуры замерзания одномоляльного раствора по сравнению с чистым растворителем.
Все одномоляльные растворы неэлектролитов будут
кипеть при температуре: t кип = 100 С + 0,52 С = 100,52 С
Пример. Вычислить температуру кипения и температуру замерзания 4,6% раствора глицерина (С3 Н5 (ОН)3) в воде.
В 100г воды содержится 4,6г глицерина и 95,4г воды.
Классификация растворов



Раствор как гомогенная система. Растворитель, растворенное вещество. Классификация растворов по степени дисперсности, по растворимости в воде, по способности к диссоциации.
Раствор— находящаяся в состоянии равновесия гомогенная система переменного состава из двух или более веществ.
Под переменным составом раствора понимают то простое обстоятельство, что соотношение смешанных друг с другом веществ может непрерывно изменяться в определенных пределах.
Растворитель — компонент, агрегатное состояние которого не изменяется при образовании раствора. (В случае же растворов, образующихся при смешении газа с газом, жидкости с жидкостью, твёрдого вещества с твёрдым, растворителем считается компонент, количество которого в растворе преобладает)
Любой раствор состоит из растворенных веществ и растворителя. Вещества, составляющие раствор, называются компонентами раствора.
Растворенное вещество — Компонент жидкого или твердого раствора, который присутствует в меньшем или незначительном количестве; компонент растворяется в Растворителе.
Классификация растворов
по растворимости в воде:
В лабораторной практике различают концентрированные растворы (содержание растворенного вещества соизмеримо с содержанием растворителя) и разбавленные растворы (содержание растворенного вещества мало по сравнению с содержанием растворителя).
А ниже это уже про растворимость веществ, не нужно здесь.
по способности к диссоциации:
по степени дисперсности:
| Грубодисперсные системы (взвеси) | Коллоидные системы (кровь, лимфа, слюна, белки) | Истинные растворы (раствор соли в воде) |
| Размер частиц дисперсной фазы | ||
| Больше 100 нм 10 –7 –10 –5 м | 1-100 нм 10 –9 –10 –7 | меньше 1 нм |
I. Взвеси – это дисперсные системы, в которых размеры распределённых частиц сравнительно велики (10 –7 –10 –5 м). Взвеси делятся на суспезии и эмульсии; в первых распределённое вещество твёрдое, во вторых – жидкое. Частицы взвеси видны простым глазом или в обычный оптический микроскоп. Взвеси – системы мутные и непрозрачные. Взвеси неустойчивы, частицы диспергированного вещества выпадают в осадок (песок + вода), а если плотность диспергированного вещества меньше плотности среды, то диспергированное вещество всплывает (глина + масло). Процесс разделения взвесей называется седиментацией (для суспензий) и расслоением(для эмульсий).
II. Коллоидные системы – это такие дисперсные системы, в которых частицы распределённого вещества имеют размеры порядка 10 –9 –10 –7 м. Каждая такая частица может содержать большое число атомов или молекул. Такие частицы невидимы через обычный микроскоп, но видимы в ультрамикроскоп, где свет падает сбоку или сзади, в результате чего в поле зрения видны светлые точки, возникающие в результате рассеяния света диспергированными частицами.
III. Истинные растворы или просто растворы – это дисперсные системы, в которых диспергированное вещество распределено в среде в виде молекул или ионов; частицы имеют размеры порядка 10 –10 –10 –7 м. Растворы системы однородные, устойчивые.
Способ выражении концентрации растворов: массовая доля вещества в растворе, молярная концентрация, молярная концентрация эквивалента(или нормальная концентрация), массовая концентрация или титр.
Концентрацией вещества называют величину, измеряемую количеством растворенного вещества, содержащегося в определенной массе или объеме раствора или растворителя.

ω (х)=
Численно массовая доля равна числу граммов вещества, растворенного в 100г раствора.
См=
1моль/л = 1М раствор – одномолярный раствор (в 1 л раствора содержится 1 моль растворенного вещества);
0,1М – децимолярный раствор;
0,01М – сантимолярный раствор;
0,001М – милимолярный раствор.
3. Нормальная концентрация (молярная концентрация эквивалента, СN)- количество моль- эквивалентов вещества, содержащегося в 1 л раствора.
СN=
Единица измерения моль-экв/л, Сокращенно обозначается буквой N. Например, 0.1N HCL означает, что в 1 литре такого раствора содержится 0,1моль- эквивалент НСl.
3. Массовая концентрация или титр раствора T(Х) измеряют в кг/см^3, г/см^3, г/мл,
Титр (Т)— масса растворенного вещества, содержащаяся в 1 мл раствора, выраженная в граммах. Определятся по формуле:
Раствор с известным титром называется титрованным раствором.