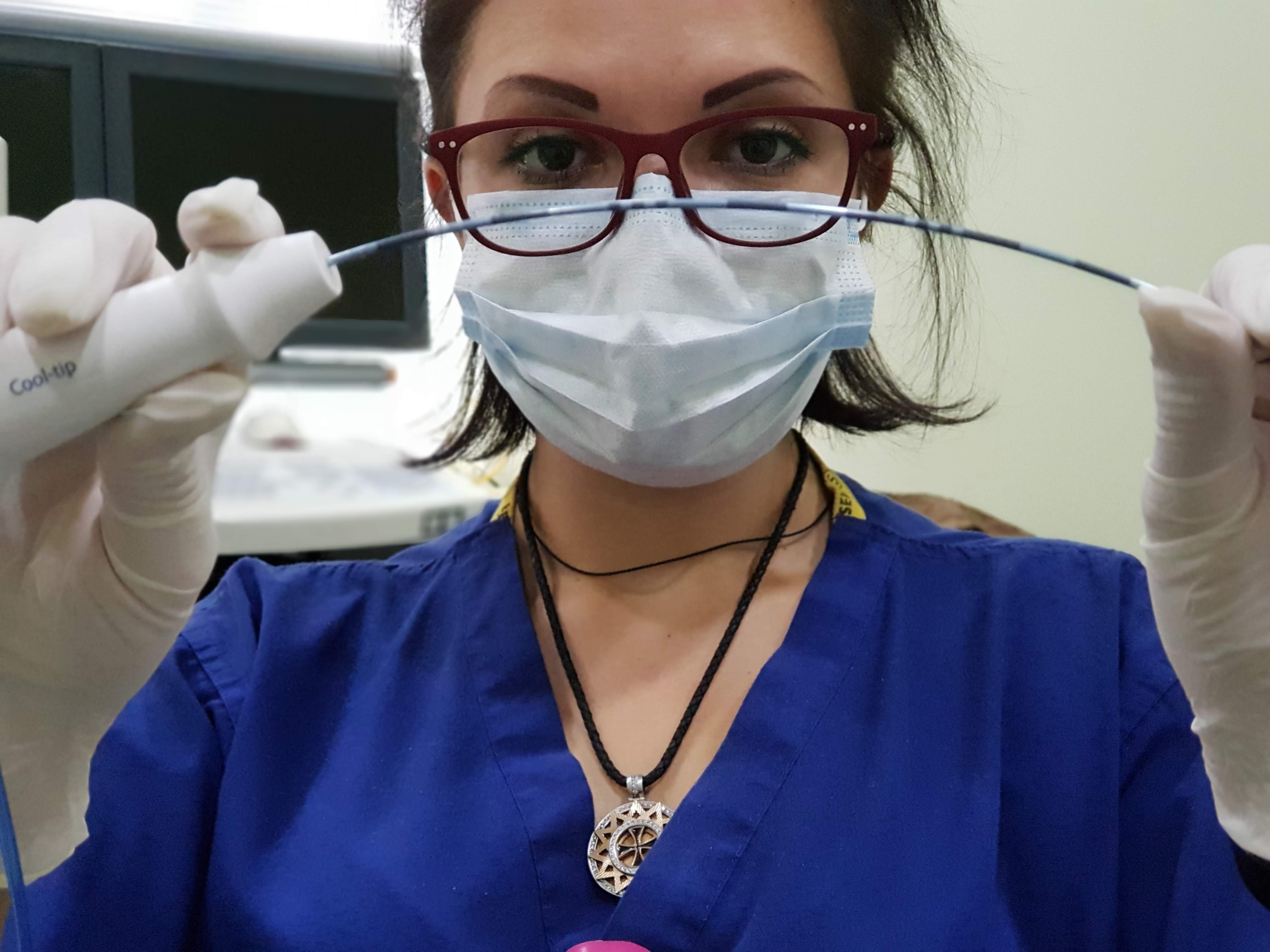
Радиочастотная абляция против рака

Абляция опухолей и метастазов является хорошим выходом для больных, состояние здоровья которых, не позволяет провести химиотерапевтическое или хирургическое лечение.
Преимущества метода абляции в зарубежных клиниках
Отличительной особенностью метода радиочастотного разрушения раковых клеток является:
Важным преимуществом радиочастотной абляции опухолей является возможность проведения повторных процедур по мере надобности. Существует несколько разновидностей данного метода. Таких, как инъекция алкоголя, воздействие лазером и микроволновое воздействие. Новый метод радиочастотного воздействия завоевал репутацию безопасного, действенного и считается на сегодняшний день ведущим. Зарубежная методика главным образом применима при первичных опухолях печени и единичных метастазах в печень (рак толстого кишечника, нейроэндокринные опухоли). Также, абляция рака применима при небольших единичных опухолях почек, лёгких и надпочечников.
Процент осложнений данной процедуры крайне низок и не требует госпитализации.
Процесс проведения абляции
В клиниках за границей абляция опухолей и метастазов выполняется под местной или общей анестезией в стерильных условиях. Под контролем ультразвукового сканера или компьютерного томографа производится введение иглы-электрода в центр опухолевой ткани. Энергия воздействия вырабатывается специальным генератором. Вокруг иглы наблюдается повышение температуры до 50 о С и выше, что влечёт за собой разрушение опухолевых клеток. Во время процедуры производится непрерывный мониторинг показателей напряжения, температуры и сопротивления тканей.
Размеры участка поражения определяются заранее и соответствуют величине опухоли. Внутреннее охлаждение иглы постоянно циркулирующим через неё физиологическим раствором, позволяет предотвратить нежелательный эффект распространения высокой температуры.
Новый метод точечной радиочастотной абляции рака за рубежом является безопасным и действенным для лечения первичных и вторичных новообразований.
Предлагаем Вам более подробно ознакомиться со следующей информацией:
Компания «МедЭкспресс» предлагает широкий спектр услуг по организации лечения за рубежом:
СМОТРИТЕ ЕЩЁ КЛИНИКИ
Профессиональное объединение в составе 12 медицинских учреждений.
В клинике активно используется роботизированная система da Vinci, отличающаяся щадящим.
Ведущая мировая клиника, оборудованная в соответствии с самыми высокими технологическими.
Уважаемые клиенты, компания «МедЭкспресс» качественно, конфиденциально и быстро поможет для каждого из Вас и Ваших близких организовать диагностику, лечение и реабилитацию в клиниках:
Для консультации со специалистами www.medical-express.ru, среди которых врач, кандидат медицинских наук, по вопросам лечения за рубежом заполните заявку прямо сейчас либо позвоните нам по телефону:
+7 (863) 29-888-08 (круглосуточно).
Считаете материал полезным? Поделитесь статьей о лечении за рубежом с друзьями:
Оставить заявку
КОММЕНТАРИИ И ОТЗЫВЫ
Если у Вас есть что добавить по теме, или Вы можете поделиться своим опытом, расскажите об этом в комментарии или отзыве.
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ, ТРЕБУЕТСЯ КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА
Работая в сфере медицинского туризма с 2009 года, компания «МедЭкспресс» наладила партнёрские отношения с лучшими медицинскими центрами Европы, Азии, США. За прошедшее время нам удалось открыть для тысяч пациентов доступ к достижениям хирургии в Италии, акушерства в США, кардиологии в Германии, нейрохирургии в Швейцарии, реабилитации в Китае, ортопедии в Южной Корее и многое другое. По-прежнему очень востребовано направление онкологии. Например, благодарные отзывы о лечении рака влагалища в Израиле упоминают мастерство пластических хирургов, выполняющих реконструкцию органа после противораковой терапии. Это помогает женщинам справиться с психологическим надломом, а для некоторых сохраняется возможность естественных родов. Болезнь будет побеждена, главное вовремя обратить на неё внимание грамотного доктора.
Радиочастотная абляция злокачественных опухолей
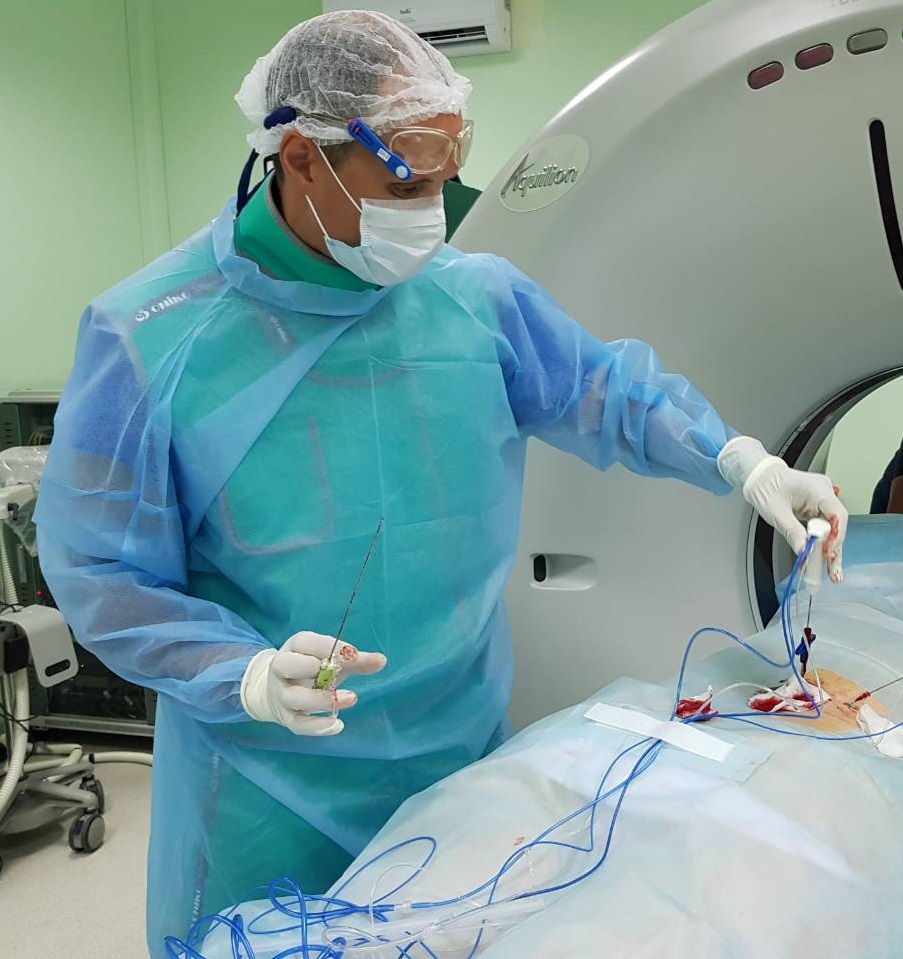
Мир развивается. Развивается стремительно. То, что казалось еще несколько лет назад фантастикой, в настоящее время становится абсолютно реальным. Раньше все удивлялись, что телефон можно носить в кармане. Сейчас весь мир помещается на ладони. Автомобили стали «умнее», чем их хозяева, а ходить за покупками можно не вставая из-за компьютера. Эти изменения не прошли и мимо медицины. То, что казалось невозможным, теперь абсолютно реально.
Ранее «4 стадия рака» звучало как приговор. Сейчас мы не просто лечим таких пациентов, а делаем это успешно.
Не секрет, что большое число людей обращается к врачу, когда дела совсем уж плохи. Время упущено. Опухоль распространилась по всему организму. Даже с такой, казалось бы, безвыходной ситуацией можно попытаться справиться.
Прогресс в медицине существенный: созданы препараты, которые эффективно противостоят росту опухоли, лучевая терапия стала более точной, мощной и направленной. Тем не менее основы лечения больных раком за последнее время значительно не изменились. Единственным радикальным методом избавления от большинства злокачественных образований является их хирургическое удаление, эффективность которого дополняется лучевой, химиотерапией и т.д. Но радикальное вмешательство удается выполнить, к сожалению, не во всех случаях.
Все это не могло оставить равнодушными ни ученых, ни врачей. Постоянно велись разработки методов локальной деструкции опухолей. Локальная деструкция – это как высокоточное оружие: бьет в цель минимально повреждая окружающие ткани. Одной из таких методик является абляция.
Абляция – это метод прямого направленного разрушения тканей, которая достигается путем физического или химического/электрохимического воздействия. Преимуществами являются малая инвазивность, сравнительно недорогое оборудование, хороший объективный терапевтический эффект, малый койко-день и практически отсутствие противопоказаний. Радиочастотная абляция (РЧА) является одним из вариантов абляции. Она привлекает простотой выполнения и кратковременностью процедуры, малым количеством осложнений и низкой летальностью, большим объемом коагулируемой ткани.
РЧА не заменяет и не исключает применение других методов лечения в онкологии и часто выполняется на ряду с химио- и лучевой терапией. Также как хирургическая операция, она может быть, как промежуточным (подготовительным), так и единственным этапом лечения злокачественных опухолей.
Абляция является безопасным способом воздействия в нерезектабельных (когда опухоль нельзя удалить) случаях или может быть дополнением к резекции органа. Данный метод лечения можно использовать повторно в случае появления новых опухолевых очагов или при продолжении роста уже обработанных в результате предыдущей манипуляции. Редко встречающиеся при РЧА осложнения часто не требуют дополнительных манипуляций. А вероятность летального исхода в результате абляции не превышает 1%.
Принцип физического действия РЧА основан на использовании токов высокой частоты (450-500 КГц). При этом возникает ионная стимуляция биологической ткани, которая приводит к ее нагреву до температуры 55-70С° и гибели опухолевых клеток. Вокруг электрода формируется зона коагуляционного некроза (омертвения) тканей.
Игольчатые электроды вводят в опухоль как чрезкожно под контролем УЗИ, КТ или МРТ, так и во время операции под УЗ-наведением. Во время открытой операции абляция часто применяется при удалении основной опухоли и наличии метастазов в печени, когда их резекция невозможна или приведет к увеличению объема послеоперационной травмы и утяжелению послеоперационного периода. Сочетание резекции печени с абляцией позволяет во многих случаях повысить операбельность при множественном полисегментарном поражении. У пациентов с высокой степенью операционного риска РЧА является альтернативой хирургического лечения.
Показаниями к РЧА являются единичные метастазы в печень, легкие и др. паренхиматозные органы, мягкие ткани и кости размером до 4-5 см (в некоторых случаях возможно воздействие на очаги большего диаметра), количество метастазов до 4-5 (в некоторых случаях метод лечения можно использовать и при большем количестве опухолей).
Контроль полноты РЧА и выявления показаний для повторных сеансов проводится с помощью КТ или МРТ с внутривенным контрастированием, а также ПЭТ/КТ для обнаружения участков жизнеспособной опухоли. Исследования проводят через месяц, три, полгода, год после вмешательства. С целью оценки эффективности лечения определяют уровень опухолевых маркеров в крови непосредственно до и через 21 день после лечения.
При РЧА костных опухолей отличительной особенностью является возможность не резецировать участок кости, избежать больших и травматичных операций при остеобластокластомах, остеоидных остеомах и метастазов в кости. Применение абляции приводит к хорошему обезболивающему эффекту при костных метастазах.
При опухолях почек и легких большого размера РЧА можно выполнять за несколько сеансов. Показаниями может являться непереносимость радикальных операций больными из-за общего состояния, возраста, наличие тяжелых сопутствующих заболеваний, а также невозможность резекции из-за функциональной недостаточности остающегося органа (опухоли единственной почки, одного легкого и т.д.).
Перспективными направлениями являются абляция опухолей предстательной железы, надпочечников, узлов щитовидной железы и опухолей паращитовидных желез, молочной железы и фибромиомах матки.
В институте медицинской радиологии мы применяем радиочастотную абляцияю при опухолях различной локализации с апреля 2016 года. Полученные результаты показали высокую эффективность метода. При лечении опухолей до 3 см в диаметре по эффективности РЧА может конкурировать с хирургическим вмешательством. При этом сокращается длительность пребывания человека в стационаре вплоть до одних суток, уменьшается период полного восстановления, значительно ниже риск развития послеоперационных осложнений.
Наши специалисты проходили обучение по проведению радиочастотной абляции в ведущих клиниках Германии, Франции, Италии и Японии, принимали участие в международных конференциях посвященных данной теме.
Все интересующие Вас вопросы, касающиеся этого метода лечения, Вы можете задать по телефонам и электронной почте указанным в разделе «Контакты». Перезвоните или напишите нам и мы постараемся ответить на все Ваши вопросы.
С результатами лечения наших пациентов можно ознакомиться в разделе Истории наших пациентов.
Радиочастотная абляция опухолей легких
Общая информация
Краткое описание
Одобрено
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения и социального развития Республики Казахстан
от «29» ноября 2016 года
Протокол №16
Приложение 1
к клиническому протоколу диагностики и лечения
Лечение
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Цель проведения процедуры/вмешательства: целью радиочастотной абляции (РЧА) является полный некроз злокачественного новообразования легких с возможностью длительной безрецидивной выживаемости.
Радиочастотная абляция – это метод разрушения опухолевой ткани с помощью высокоэнергетических радиоволн, в процессе которого происходит нагревание клеток опухоли до высоких температур и, как следствие, их гибель. Радиочастотная абляция способствует как частичному, так и полному удалению опухоли.
Показания и противопоказания для проведения процедуры/ вмешательства:
Показания к проведению РЧА злокачественных опухолей легких:
· больные НМРЛ I–II стадий, не подлежащие хирургическому лечению по следующим причинам:
— сопутствующие заболевания;
— отказ пациента от хирургического лечения.
· отсутствие внелегочных проявлений заболевания;
· рецидив опухоли менее чем через 6 мес. после резекции легкого;
· удаленная первичная опухоль (при метастазах в легких);
· больные, имеющие несколько метастазов (всего не более 6) в разных долях легких;
· менее 3 метастазов в каждом легком;
· диаметр опухоли до 4 см;
· опухоли, визуализируемые при РКТ;
· локализация опухоли не ближе 1 см от прикорневых структур;
· согласие больного на проведение лечения.
Противопоказания к РЧА злокачественных опухолей легких:
Абсолютные:
· некоррегируемая коагулопатия;
· сепсис;
· метастатический плеврит.
Относительные:
· наличие у пациента искусственного водителя ритма;
· опухолевые узлы прилежат к диафрагме либо располагаются ближе 1 см к прикорневым структурам;
· расположение опухоли рядом с крупными сосудами (аорта, легочные артерии), пищеводом, грудной стенкой, диафрагмой;
· близость сосудов > 3 мм в диаметре;
· первичная опухоль не удалена;
· более 3 метастазов в каждом легком;
· общее количество метастазов более 6.
Перечень основных и дополнительных диагностических мероприятий (отдельно перечислить основные/обязательные и дополнительные обследования, консультации специалистов с указанием цели и показаний):
Основные (обязательные) диагностические обследования:
· ОАК с тромбоцитами;
· ОАМ;
· группа крови и резус-фактор;
· биохимический анализ крови: общий белок с фракциями, АЛТ, АСТ, общий/прямой билирубин, ЩФ, ГГТП, ЛДГ, креатинин, мочевина, амилаза, глюкоза;
· электролиты: калий, натрий;
· микрореакция;
· коагулограмма: протромбиновое время, МНО, АЧТВ, фибриноген;
· маркеры вирусных гепатитов: HBsAg, anti-HCV, ВИЧ;
· альфа-фетопротеин, специфические опухолевые маркеры;
· ЭКГ, спирометрия;
· УЗИ органов брюшной полости;
· рентгенография органов грудной клетки;
· КТ/МРТ торакального сегмента с контрастированием;
· биопсия до РЧА: морфологическое подтверждение злокачественного характера опухоли легкого является обязательным до ее термодеструкции. Биопсия может выполняться непосредственно перед РЧА, однако предпочтительнее проводить ее заранее, чтобы избежать возможных связанных с ней осложнений и сдвинуть сроки проведения РЧА. Кроме того, могут быть выявлены особенности при морфологическом исследовании, способные повлиять на тактику лечения.
Особенности подготовки больного к РЧА злокачественных опухолей легких:
· решение о проведении РЧА как первичных, так и метастатических опухолей легких должна принимать мультидисциплинарная комиссия;
· при сборе анамнеза необходимо уточнить:
− наличие геморрагического диатеза;
− наличие бронхолегочных заболеваний и/или ранее перенесенные хирургические вмешательства на легких, в том числе пульмонэктомии (описаны единичные клинические наблюдения РЧАопухолей в единственном легком);
− наличие пэйсмейкера сегодня не является абсолютным противопоказанием к выполнению РЧА, однако рекомендуется его деактивировать перед вмешательством либо располагать электрод не ближе 5 см от водителя ритма;
− следует иметь в виду, что имплантированные мелкие металлические фрагменты могут нагреваться во время РЧА.
· факторы, оказывающие влияние на эффективность воздействия:
− размеры узлов [при размерах опухолевых узлов менее 3 см отмечены лучшие результаты как для первичных (в виде увеличения частоты полных некрозов и локальной безрецидивной выживаемости), так и для метастатических опухолей легких (увеличение общей выживаемости);
− локализация узлов (ограниченная возможность выполнения РЧА опухолей прикорневой зоны, опухолей, прилежащих к крупным сосудам, бронхам).
Требования к соблюдению мер безопасности и к санитарно-противоэпидемическому режиму: меры безопасности и противоэпидемический режим согласно Санитарным правилам «Санитарно-эпидемиологические требования к объектам здравоохранения», утвержденным приказом и.о. Министра национальной экономики Республики Казахстан от 24 февраля 2015 года №127.
Требования к оснащению, расходным материалам, лекарственным средствам: согласно приказа и.о. Министра здравоохранения Республики Казахстан от 12 августа 2011 года № 540 «Об утверждении Положения о деятельности организаций здравоохранения, оказывающих онкологическую помощь населению Республики Казахстан».
Требования к оснащению, расходным материалам, медикаментам:
· любая сертифицированная система для РЧА опухолей: одноигольчатые электроды с максимальным диаметром воздействия 3 см, выдвигающиеся электроды с максимальным диаметром воздействия 5см и др.;
· система лучевой навигации: РКТ,УЗИ, МРТ;
· анестезиологическое оборудование (аппарат для искусственной вентиляции легких, монитор для контроля сердечной деятельности, артериального давления, сатурации и др.);
· динамический контроль: КТ с внутривенным контрастным усилением, ПЭТ/КТ, МРТ с внутривенным контрастным усилением. Критерии оценки результатов: mRECIST, EASL.
Основные расходные материалы:
· набор белья для инвазивных процедур;
· комплект кластерных или 1-3 одиночных электродов для РЧА;
· генератор;
· насос и система охлаждения;
· емкость для воды;
· ножной выключатель;
· ультразвуковой аппарат.
Дополнительные расходные материалы:
· внутривенные катетеры;
· система одноразовая для инфузий;
· скальпель одноразовый;
· марля медицинская;
· шприцы 20 мл;
· шприцы 10 мл;
· перчатки стерильные;
· перчатки нестерильные;
· шапочки одноразовые;
· маски хирургические;
· бахилы одноразовые;
· одноразовые электроды для ЭКГ.
Требования к подготовке пациента:
· вечером накануне операции легкий ужин до 20:00 часов;
· в день операции – голод;
· побрить операционное поле накануне операции;
· провести перед операцией все гигиенические процедуры: прополоскать полость рта, почистить зубы, снять съемные зубные протезы, очистить полость носа, мужчинам побриться;
· обработка операционного поля препаратами бактерицидного действия;
Методика проведения процедуры/вмешательства:
· собрать систему для радиочастотной абляции по инструкции;
· положение больного – лежа на животе, на боку или на спине в зависимости от доступа;
· возвратные электроды пациента зафиксировать на бедрах пациента;
· процедура проводится, как правило, под внутривенной анестезией или интубационным наркозом;
· выбор электрода определятся размером очага и удаленностью от поверхности кожи;
· пункция очага производится под контролем КТ. Необходимо, чтобы абляционная часть иглы располагалась в центре опухоли. При выявлении эксцентрического расположения электрода необходимо произвести повторную пункцию очага с предварительной термообработкой старого пункционного канала во избежание кровотечения или опухолевой диссеминации, либо введение дополнительных электродов в очаг и обработка его из нескольких точек;
· можно ввести несколько электродов одномоментно при наличии несколько рядом расположенных очагов во избежание «потери» очага после РЧА соседнего;
· удостоверившись в правильном расположении электрода, начинается воздействие на опухоль током частотой 450-500 кГц. В результате опухолевая ткань разогревается до температуры (60-90°С), при которой происходят необратимые изменения в клетках. Опухолевая масса некротизируется. Время воздействия на опухоль 8-12 минут, если опухоль до 3см. Для очень крупных опухолей игольчатые электроды группируют по три в одной рукоятке (электрод-кластер) на расстоянии 0,5 см параллельно друг другу. Именно такие охлаждаемые инструменты позволяют быстро коагулировать опухоли 5-7 см в диаметре и больше. В конце 12-минутного сеанса лечения электрод извлекается при работающем генераторе и коагулирует пункционный канал.
Индикаторы эффективности процедуры/вмешательства:
· отсутствие в послеоперационный период выявляемого всеми доступными визуализационными методами роста резидуальных опухолевых очагов в зоне выполненной абляции;
· отсутствие послеоперационных осложнений (осложнений, связанных с доступом и процедурой);
· снижение количества инвалидизирующих оперативных вмешательств;
· возможность многократного миниинвазивного проведения РЧА деструкции;
· повышение ожидаемой продолжительности жизни;
· повышение качества жизни.
Информация
Источники и литература
Информация
Список разработчиков протокола с указанием квалификационных данных:
1) Боровский Сергей Петрович – доктор медицинских наук, АО «Национальный научный центр онкологии и трансплантологии», заведующий отделением интервенционной рентгенохирургии.
2) Шаназаров Насрулла Абдуллаевич – доктор медицинских наук, профессор, онколог высшей категории, заведующий курсом онкологии кафедры «Хирургических болезней №2» АО «Медицинский университет Астана».
3) Малаев Нияз Бейсенович – MSc, MBA., АО «Национальный научный центр онкологии и трансплантологии», врач рентгенохирург высшей категории, отделения «Интервенционной рентгенохирургии».
4) Нурсеитов Ильяс Ержанович – врач интервенционный рентгенохирург, «Казахский национальный научный исследовательский институт онкологии и радиологии».
Указание на отсутствие конфликта интересов: нет
Рецензент:
1) Кузикеев Марат Оразович – доктор медицинских наук, профессор, Руководитель центра абдоминальной онкологии «Казахского научно-исследовательского института онкологии и радиологии».
Указание условий пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Радиочастотные абляции
Через игольчатые электроды к очагу заболевания подводится высокочастотный электрический ток. Электроэнергия на кончике электрода трансформируется в тепловую, клетки разрушаются и уничтожаются. Высушивание тканей предупреждается подачей физраствора на кончик электрода, что делает невозможным лечение опухолей больших размеров. РЧА применяется во время открытой хирургической операции, лапароскопически или чрезкожно. Чаще методика используется при лечении опухолей диаметром до 4 см, поражающих почки, печень. Есть положительный опыт применения РЧА при лечении метастаза колоректального рака размерами до 7 см.
Абляция в онкологии — разрушение, уничтожение, ликвидация патологического образования (чаще злокачественного) нагреванием, заморозкой, химическими веществами или электричеством. Обычно абляция проводится чрезкожно тонкими электродами или иглами под контролем средств томографии или УЗИ. Целью процедуры является разрушение опухолевых тканей и тонкого слоя нормальных клеток. При необходимости абляция может дополняться хирургическим вмешательством.
Чрезкожная абляция — особенности процедуры
Первым этапом лечения чрезкожной абляции является тщательное изучение снимков УЗИ, ПЭТ-КТ, КТ и других радиологических исследований. Выбор вида абляции определяется разновидностью опухоли, количеством и размером, особенность локализации очагов. Для каждого пациента планируется тип абляции, методы визуализации. Одновременно уточняется конкретное место введение иглы или электрода абляции на коже, выбирается метод анестезии. Большинство видов абляции осуществляется с применением успокоительных препаратов или под местной анестезией. Процедура обычно контролируется УЗИ. Лечение опухолей плохо просматриваемых средствами УЗИ проводится под контролем КТ.
Во время абляции возможно одновременное использование томографии и ангиографии. Если опухоли печени плохо просматриваются на УЗИ и КТ, то в печеночные артерии с помощью ангиографии устанавливается катетер. Через катетер вводится лекарственный препарат, и дальнейшее лечение проводится под наблюдением с помощью УЗИ или КТ. Современная медицина использует «Cone Beam CT» — аппарат, сочетающий томографию и ангиографию. Он упрощает осуществление процедуры абляции, биопсию легких и делает эти процедуры безопаснее.
Виды абляции
Существует 3 группы абляций, применяемых для лечения онкологических заболеваний: химическая, термоабляция и необратимая электропорация.
Химическая абляция
Злокачественная опухоль уничтожается введением внутрь ее тканей химических препаратов или спирта. Эффективность методики доказана 20-летним сроком ее применения в клиниках всего мира. Относительно дешевый метод дает минимальное количество побочных эффектов. Курс лечения для полного уничтожения опухоли включает в себя несколько сеансов.
Химическая абляция обычно применяется для лечения первичного рака печени. Реже методика используется при раке щитовидной железы, метастазах в лимфоузлах.
Термальная абляция — высокотемпературная или заморозка
Разрушение тканей злокачественного новообразования и их уничтожение осуществляется сжиганием или замораживанием путем введения в опухоль электродов, игл.
Высокотемпературные (сжигающие) методы: радиофреканс, лазер и микроволновая абляция. Самой популярной является методика радиофреканса. Игла радиофреканса, введенная в ткани опухоли, преобразует поток высокочастотной электроэнергии в поток ионов. Ионный поток трансформируется в тепловой поток, разрушающий структуру тканей новообразования.
Микроволновая абляция занимает второе место по популярности. От радиофреканса методика отличается способом выработки тепла — используется не электрический поток, а электромагнитные волны. Электромагнитные волны высокой частоты заставляют двигаться находящиеся в тканях опухоли молекулы воды. Процесс сопровождается выделением большого количества тепла, уничтожающего опухоль.
Криоабляция — глубокое замораживание
В новообразование вводится специальная игла (prob). Происходит глубокая заморозка тканей, их разрушение и уничтожение.
Методы термальной абляции применяются при лечении злокачественных новообразований печени, мягких тканей. Чаще используется радиофреканс. В случае недостаточной эффективности радиофреканса при воздействии на относительно изолированную костную или легочную ткань допускается применение микроволновой абляции. Микроволновая и радиофрекансная абляции применяются для лечения раковых опухолей почек, легких, мягких тканей и костных структур.
Криоабляция применяется для уничтожения злокачественных опухолей почек, предстательной железы. Реже методика используется при лечении рака легких, молочной железы, печени. Уничтожение опухоли методом криоабляции проводится с обязательным применением средствам УЗИ, МРТ, КТ, позволяющими контролировать точность воздействия.
Необратимая электропорация
Электропорация — постоянное или временное увеличение проницаемости клеточной мембраны под воздействием высоковольтного электропотока. При временной элетропорации (reversible electroporation) проницаемость клеточных стенок увеличивается временно подачей электрического потока в сотни вольт. Внутрь клетки вводятся большие молекулы типа DNA, изменяя ее генетическую структуры (генетический электротрансфер) либо проводится электрохимиотерапия — введение лекарственного препарата.
Временная электропорация применяется онкологией в течение многих лет. Проницаемость клеточных стенок восстанавливается при прекращении подачи электропотока и нормальная жизнедеятельность клетки восстанавливается. Необратимая электропорация в онкологии стала распространяться в последние годы. Подача высокочастотного электрического потока обеспечивает необратимое увеличение проницаемости клеточных стенок, вызывающего гибель клетки.
Применение методов химической и термальной абляции становится причиной быстрого некроза (омертвления) тканей. В этом случае все ткани, включая нервные окончания, сосуды, расположенные в области воздействия, разрушаются и погибают. Результатом необратимой электропорации становится апопитоз тканей (безтравматичное медленное отмирание).
Отмирание клеток не затрагивает нервных окончаний и сосудов, состоящих в основном из соединительных тканей. Поэтому метод необратимой электропорации применяется для уничтожения раковых опухолей, находящихся рядом с желчными и мочевыми путями, кровеносными сосудами.
Абляция — для каких видов опухолей
Химическая абляция используется при лечении гепатоцелюлокарциномы (первичного рака печени). Методика применяется для разрушения, уничтожения злокачественных новообразований щитовидной железы, метастатических поражений лимфатических узлов. Химическая абляция является альтернативой термоабляции при локализации опухоли или очагов метастазов в труднодоступных местах. Усиление лечебного эффекта достигается комбинацией химио- и термоабляции.
Методы термально абляции в настоящее время являются самыми распространенными способами лечения опухолей. Особой популярностью последние 15 лет пользуется абляция радиофреканс. Для лечения раковых опухолей печени чаще применяются другие виды абляции.
Преимуществом термальной абляции является простота техники ее проведения, возможность контроля и прогноза результата, а также минимальный риск побочных эффектов. Термальная абляция направлена на разрушение и сжигание новообразования с 1 см слоем прилегающей к нему здоровой ткани. Полное уничтожение опухолевых структур в месте воздействия термальной абляции подтверждено исследованиями. Поэтому данный метод широко используется для ликвидации злокачественных очагов, удаление которых ранее было возможно только путем оперативного вмешательства.
Виды термальной абляции недостаточно безопасны при необходимости воздействия на участки органов, расположенные вблизи больших сосудов, крупных нервных стволов, моче- и желчевыводящих путей, желудочно-кишечного тракта — высок риск их повреждения. В этих случаях применяются другие методы абляции.
Основное направление применения необратимой электропорации — лечение рака головки поджелудочной железы. Рядом с головкой поджелудочной железы расположены крупные печеночные артерии, артерии двенадцатиперстной кишки и тонкого кишечника. Техника радиофреканса в этом случае используется редко. Методика необратимой электропорации дает возможность уничтожения опухолевых клеток в области воздействия абляции без повреждения артерий и тонкого кишечника.
Необратимая электропорация применяется для лечения злокачественных опухолей печени, находящихся в непосредственной близости к желчным путям, кровеносным сосудам. Применение методов радиофреканс и других видов термальных абляций на таких новообразованиях не практикуется. Это обусловлено высоким риском травм желчных путей и отсутствием возможности оказать должное воздействие на пораженные ткани, расположенные вблизи с крупными кровеносными сосудами. Необратимая электропорация является максимально эффективной и доступной для лечения очагов рака в таких ситуациях. Недостатками метода являются: техническая сложность, большая продолжительность процедуры, необходимость применения общего наркоза и высокая цена.
Каждый метод чрезкожной абляции имеет своими преимуществами и недостатками. Окончательный выбор делается для каждого пациента высококвалифицированным специалистом интервенционной радиологии индивидуально в зависимости от конкретных условий.
Чрезкожная абляция — преимущества и недостатки методов
Чрезкожная абляция — современная техника лечения рака. Традиционное хирургическое вмешательство подразумевает иссечение кожных покровов для доступа к злокачественному очагу, применение общего наркоза, обязательную госпитализацию пациента. Метод радиотерапии — это отсутствие зависимости от типа опухоли активности радиотерапии и возможность многократного повторения при необходимости. Чрезкожная абляция часто применяется в комплексе с хирургическим вмешательством и радиотерапией. Например, часть очагов опухоли метастазов удаляется хирургическим вмешательством, а часть — чрезкожной абляцией и (или) радиотерапией.
Как и все методы лечения, все типы чрезкожной абляции обладают рядом недостатков. Присутствует риск развития раковой опухоли на том же месте. В этом случае возможно повторное проведение абляции. Степень эффективности чрезкожной абляции, успешный исход лечения также во многом зависит от профессионализма и опыта медицинского персонала, технической составляющей.
Методы чрезкожной абляции применяются для:
• лечения небольших метастаз в мягких тканях и костных структурах;
• разрушения и уничтожения неоперабельных злокачественных новообразований в тканях поджелудочной железы без наличия отдаленных метастазов;
• ликвидации первичных опухолей и метастазов печени и легких маленького диаметра (до 3 см).
Для подбора эффективного метода лечения вы можете обратиться за
— методы инновационной терапии;
— возможности участия в экспериментальной терапии;
— как получить квоту на бесплатное лечение в онкоцентр;
— организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.