Реакции обмена
Урок 31. Химия 8 класс
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобрев в каталоге.
Получите невероятные возможности
Конспект урока «Реакции обмена»
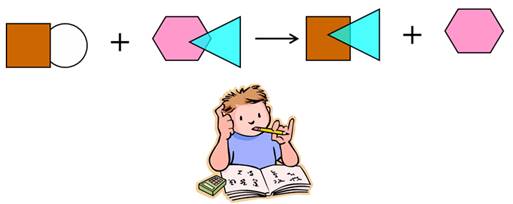
Реакции обмена – это реакции, в результате которых, два сложных вещества обмениваются своими составными частями.
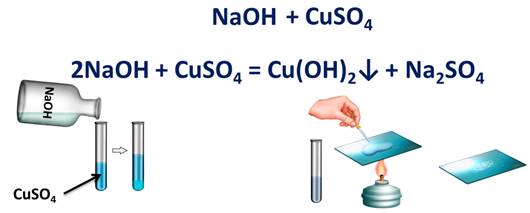
Запишем реакцию взаимодействия двух сложных веществ: гидроксида натрия и сульфата меди (II). Они должны обменяться своими составными частями, т.е. у натрия вместо гидроксид-иона будет сульфат-ион, а у меди вместо сульфат-иона будет гидроксид-ион. Осталось правильно составить формулы продуктов реакции согласно зарядам. Т.е. образуется сульфат натрия – Na2SO4 и гидроксид меди (II) – Cu(OH)2.
Запишем правило: щелочь + соль = основание + соль
Признаком этой реакции является образование осадка голубого цвета. Этот осадок – гидроксид меди (II), поэтому мы ставим после него стрелку, направленную вниз. Еще образуется соль – сульфат натрия. В этом легко убедится, если отфильтровать садок, а на предметное стекло поместить несколько капель раствора и выпарить. После чего на стекле появятся белые кристаллы соли.
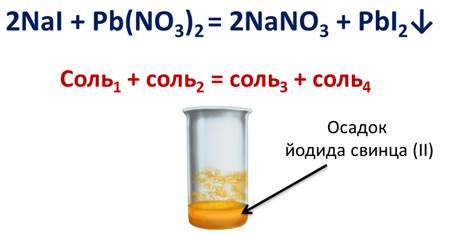
Аналогично обмениваются ионами йодид натрия с нитратом свинца (II). В результате реакции выпадает осадок йодида свинца (II).
Проведем эксперимент. Для этого в пробирку с раствором щелочи добавим несколько капель фенолфталеина. Раствор окрасится в малиновый цвет. Если же к содержимому пробирки добавить кислоты, то малиновая окраска исчезает. Выпарим содержимое полученного раствора. На предметном стекле появляются кристаллы соли. В реакцию у нас вступает щелочь – гидроксид натрия и серная кислота. У гидроксида натрия – гидроксид-ионы, у серной кислоты – сульфат-ионы. Обменяем их ионами, у натрия теперь будут сульфат-ионы, у водорода – гидроксид-ионы. В результате образуется соль – сульфат натрия и вода.
Запишем правило: щелочь + кислота = соль + вода
В каждом из этих растворов была своя седа: у щелочи – щелочная, у кислоты – кислая, а стала нейтральная. Поэтому реакцию обмена между щелочью и кислотой называют реакцией нейтрализации.
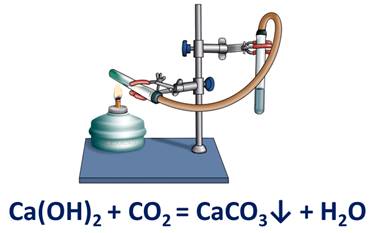
Реакция обмена наблюдается и при взаимодействии известковой воды и углекислого газа. При этом наблюдается помутнение известковой воды вследствие образования осадка – карбоната кальция.
Если в пробирку с карбонатом натрия прилить соляной кислоты, то начинается «вскипание» раствора, вследствие образования углекислого газа. Откуда же углекислый газ, ведь по правилам должна образоваться угольная кислота. Но так как это соединение непрочное, то она распадается на углекислый газ и воду.
Правило: соль + кислота = новая соль + новая кислота
Реакции обмена идут до конца, если в результате их образуется осадок, газ или вода.
Урок+презентация «Реакции обмена» 8 класс
Онлайн-конференция
«Современная профориентация педагогов
и родителей, перспективы рынка труда
и особенности личности подростка»
Свидетельство и скидка на обучение каждому участнику
Выбранный для просмотра документ Презентация.pptx
Описание презентации по отдельным слайдам:
Какая реакция лишняя? 2Cu+O2=2CuO Zn(OH)2=ZnO+H2O Mg+H2SO4=MgSO4+H2 FeS+2HCl=FeCl2+H2S
Художественные образы реакций Реакция разложения Реакция соединения
Лекарь + П Пекарь + Л Реакция замещения
Тема: Реакции обмена Цель: выяснить какие реакции называются реакциями обмена, дать определение, научиться составлять уравнения химических реакций, определить условия их протекания.
Какие из реакций обмена будут протекать до конца? Почему? BaCl2 + 2AgNO3 → Ba(NO3)2 + 2AgCl Cu(NO3)2 + 2NaCl → CuCl2 + 2NaNO3 2НNO3 + К2S → Н2S↑ + 2KNO3 Mg(ОН)2 + Н2SO4 → MgSO4 + 2H2O 2HNO3 + ZnSO4 → H2SO4 + Zn(NO3)2
Выбранный для просмотра документ Технологическая карта открытого урока по химии в 8 классе.docx
Технологическая карта открытого урока по химии в 8 классе
Педагогическая цель : сформировать интерес к изучению нового курса: создать условия для формирования научного мировоззрения у обучающихся о науке химии; продолжить формирование знаний о типах химических реакции, познакомить с реакциями обмена.
Тип, вид урока: урок постановки учебной задачи
— предметные: обучающийся научиться классифицировать химические реакции по числу и составу исходных веществ и продуктов реакции; использовать таблицы растворимости для определения возможности протекания реакции обмена; наблюдать и описывать признаки и условия течения химических реакции; будет знать определения понятий: «реакция обмена», «реакции нейтрализации».
— личностные: формирование умения управлять своей познавательной деятельностью; понимание значимости естественно-научных и математических знаний для решения практических задач; формирование умения грамотного обращения с веществами в химической лаборатории и в быту.
— универсальные учебные действия: Познавательные – использовать знаково-символические средства для раскрытия сущности процессов; создавать обобщения, устанавливать аналогии, осуществлять классификацию, делать выводы, проводить наблюдение; составлять на основе текста таблицы, схемы, опорный конспект, в том числе с применением средств ИКТ; получать информацию из различных источников и интерпретировать её.
Регулятивные – формулировать цель урока и ставить задачи, необходимые для её достижения; планировать свою деятельность и прогнозировать её результаты; работать по плану, сверять свои действия с целью и, при необходимости, корректировать ошибки самостоятельно.
Формы и методы обучения:
Организационная структура урока
Проверка готовности обучающихся к уроку; эмоциональный настрой на урок.
Учитель приветствует обучающихся, просит их проверить готовность к уроку.
Актуализация опорных знаний урока
Активизирует знания, необходимые обучающимся для изучения нового материала. Осуществляет фронтальный контроль:
Учитель: Все, что нас окружает, состоит из веществ. Взаимодействуя друг с другом они изменяют свои свойства и состав. И начать урок я хочу с загадки.
Эти явления знаете вы
В жизни нашей встречаются они,
А отличают эти явления – взаимные превращения,
И образуются всегда – новые вещества.
Что же это за явления? (химические реакции)
Учитель: Кто ответит, что такое химическая реакция?
Учитель: С какими тремя типами хим. Реакций мы уже познакомились?
Учитель: Хорошо, теперь я предлагаю вам немного поиграть. На слайде 4 типа реакций, 3 вам уже знакомы, а одна является лишней т.е. не изученной нами. Вам необходимо определить тип химических реакций, записать уравнения и расставить коэффициенты.
(Один человек работает у доски)
(1 – соединения, 2 – разложения, 3 – замещения)
Мотивация к изучению нового материала. Формулирование темы и целей урока.
Мотивирует обучающихся к определению темы и к постановке познавательной цели урока.
Учитель: Итак, очевидно, что сегодня на уроке мы с вами познакомимся с новым типом химических реакций. (Учитель подходит к ученику и просит у него ручку, а ему отдает карандаш). Вопрос: Что мы сделали? Как выдумаете
к какому типу относится последняя химическая реакция?(ответы учеников)
Это – наша новая тема, то есть эта реакция является реакцией обмена, о которой мы сегодня поговорим. Записываем тему в тетрадь. Давайте попробуем определить цель нашего урока. (ответы учеников)
Наша задача – выяснить что такое реакции обмена, дать определение, выявить их отличие от других типов химических реакций, научиться составлять уравнения реакций обмена. Должны будем понять какие условия или факторы обязательны для выполнения.
Усвоение новых знаний и способов действий.
Учитель: Ребята давайте вернемся к нашей первой реакции обмена, с которой мы сегодня познакомились, посмотрим на нее и попробуем самостоятельно вывести определение реакции обмена. Запись в тетрадь (Реакции обмена – это реакции, протекающие между двумя сложными веществами, результате чего они обмениваются своими составными частями).
Создание проблемной ситуации: французский химик Клод Луи Бертолле сформулировал правило, согласно которому протекают реакции обмена между растворами сложных веществ. «Реакции обмена протекают только тогда, когда образуется малорастворимое соединение (осадок), легколетучее вещество (газ) или малодиссоциирующее соединение (очень слабый электролит в т.ч. вода). Как вы думаете верно ли это утверждение?
Для того чтобы доказать или опровергнуть это утверждение мы должны провести химический эксперимент.
Лабораторный опыт №1. Взаимодействие гидроксида натрия с сульфатом меди ( II )
Для того чтобы определить продукты реакции составим уравнение химической реакции
Какое вещество выпало в осадок? Чтобы ответить на этот вопрос необходимо узнать какое вещество растворяется, а какое нет. Обратимся к таблице растворимости. Вещество Cu ( OH ) 2 – нерастворимо, а следоватеьно выпало в осадок. (гидроксид меди – новое сложное вещество)
Вывод: выпадение осадка одно из условий того, что реакция идет до конца.
Лабораторный опыт №2. Взаимодействие раствора щелочи с раствором кислоты.
Инструкция: В пробирку нальем раствор щелочи и добавим несколько капель ф/ф. Что наблюдаем? (Ф/ф в растворе щелочи приобретает малиновый цвет, это говорит о щелочной реакции среды). К раствору щелочи приливаем раствор соляной кислоты. Что наблюдаем (Восстановление цвета индикатора, что является признаком химической реакции)
Составим уравнение химической реакции
NaOH +ф/ф+ HCl = NaCl + H 2 O
окраска малиновая раствор обесцветился
Вывод: Если в результате реакции образуется вода, то такие реакции
протекают до конца
В результате реакции обмена между растворами щелочи и кислоты образовался раствор с нейтральной средой – такая реакция называется реакцией нейтрализации.
Лабораторный опыт №3. Взаимодействие раствора карбоната натрия с раствором азотной кислоты.
Составим уравнение химической реакции
В таком виде записанное уравнение реакции не показывает образование газа. Угольная кислота в свободном виде не существует, т.к. является нестойкой и легко разлагается на воду и соответствующий оксид. (степень окисления углерода в кислоте и оксиде одинаковая + 4).
Вывод: Если в результате реакции образуется газ, следовательно реакция идет до конца (т.е. практически возможна).
Учитель: Мы с вами выяснили, что химические реакции обмена идут до конца в нескольких случаях. Назовите их. ( ребята отвечают)
Проверка понимания изученного, закрепление знаний
Какие из реакций обмена будут протекать до конца? Почему?
BaCl2 + 2AgNO3 → Ba(NO3)2 + 2AgCl
Cu(NO3)2 + 2NaCl → CuCl2 + 2NaNO3
2НNO3 + К2S → Н2S↑ + 2KNO3
Mg( ОН )2 + Н 2SO4 → MgSO4 + 2H2O
2HNO3 + ZnSO4 → H2SO4 + Zn(NO3)2
2. Реакция обмена протекает между сложными веществами, которые обмениваются своими составными частями.
3. Реакция обмена идет до конца, только когда образуется вода.
4. Реакция обмена идет до конца, когда образуется газ, осадок или вода.
5. Реакция обмена идет до конца, только когда образуется газ.
6. Реакция между кислотой и основанием называется реакцией нейтрализации.
7.Любая реакция обмена является реакцией нейтрализации.
3. Самостоятельная работа:
Закончите уравнения химических реакций и расставьте коэффициенты:
Подведение уроков. Рефлексия
Вернемся к теме сегодняшнего урока.
Какую цель мы поставили в начале урока?
К какому выводу мы пришли?
— Что нового вы узнали на уроке?
— Какие затруднения у вас возникли при работе на уроке?
— Что до сих пор остаётся непонятным?
ДЛЯ УЧЕНИКОВ
Закончите уравнения химических реакций и расставьте коэффициенты:
Закончите уравнения химических реакций и расставьте коэффициенты:
Закончите уравнения химических реакций и расставьте коэффициенты:
Закончите уравнения химических реакций и расставьте коэффициенты:
Закончите уравнения химических реакций и расставьте коэффициенты:
Урок химии в 8-м классе «Реакции обмена»
Разделы: Химия
Тип урока: Урок изучения нового материала.
Основная цель урока: Развитие знаний учащихся о химических реакциях при формировании представлений о реакции обмена.
Задачи урока
Оборудование и реактивы: держатель для пробирок, CuO, растворы HCl, H2SO4, CuSO4, NaOH, Na2SO4, BaCl2, KCl, фенолфталеин, компьютер, проектор, ПСХЭ, таблица растворимости; на партах учеников инструктаж по технике безопасности и р-ры HNO3 и Na2CO3.
Ход урока
1. Организационный момент.
2. Подготовка к основному этапу усвоения учебного материала.
2.1. Проверка домашнего задания: (3 ученика у доски)
Далее слушаем ответы учеников у доски.
Затем учитель предлагает определить типы химической реакции (на слайде записаны):
Идет обсуждение.
Вопрос: Как вы думаете, к какому типу относится последняя химическая реакция?
Ученики затрудняются определить тип 4 реакции.
Учитель: Это-наша новая тема, то есть эта реакция является реакцией обмена, о которой мы сегодня узнаем.
Ученики в тетрадях записывают тему урока:»Реакции обмена».
3. Усвоение новых знаний и способов действий.
Учитель: Ребята, давайте попробуем самостоятельно вывести определение реакции обмена. Запись в тетрадь: Реакции обмена-это реакции, протекающие между двумя сложными веществами, в результате чего они обмениваются своими составными частями.
3.1. а) Демонстрация опыта (NaOH и HCl).
Учитель: Ребята, а какое еще можно дать определение реакции обмена, если реакция протекает между веществами в растворе?
Вывод: Тип реакции-реакция обмена (обмен ионами).
Вид реакции-реакция нейтрализации.
(Ученики сами формулируют понятия).
3.2. б) Демонстрация реакции между нерастворимым основанием и кислотой:
гидроксидом меди (II) и соляной кислотой.
Учитель перед учениками выставляет проблему:
Мы рассмотрели реакцию растворимого основания с кислотой. А будет ли реакция протекать между нерастворимым основанием и кислотой? И будет ли она относится к реакции нейтрализации?
1) Получение нерастворимого основания Cu(OH)2
Запись уравнения реакции учеником:
СuSO4 + 2 NaOH = Na2SO4 + Cu(OH)2 ↓
2) Демонстрация реакции между нерастворимым основанием и кислотой:
гидроксидом меди (II) и соляной кислотой.
На доске ученик записывает уравнение реакции
Cu(OH)2+2HCl=CuCl2+2H2O
Ученики рассуждают и приходят к выводу, что реакция между нерастворимым основанием и кислотой не является реакцией нейтрализации, но нейтрализовать кислотой нерастворимое основание можно.
3.3.Учитель: Назовите в каких классах соединений мы встречаем ионную связь?
(Ответ: ионная связь в солях и основаниях).
Учитель перед учениками выставляет новую проблему.
Вопрос: А будет ли протекать реакция, т.е. обмен ионами а) между солями?
б) солью и кислотой?
Демонстрация:
А) Na2SO4 и BaCl2 Б) Н2SO4 и BaCl2
Уравнения записывают ученики. Работают с таблицей растворимости.
3.4. Лабораторный опыт.
Инструктаж по ТБ
Ученики проводят реакцию между Na2CO3 и HNO3
Записывают уравнение реакции, работают с таблицей растворимости, рассуждают.
Подводится итог этой части урока. Ученики делают вывод: реакции обмена протекают между сложными веществами, т.е. между основаниями и кислотами, солями и щелочами, солями и кислотами, между солями.
3.5. Учитель перед классом ставит проблемный вопрос:
Будет ли протекать реакция между оксидами металлов и кислотами?
Демонстрируется взаимодействие оксида меди(II) с раствором серной кислоты при нагревании.
Ученик на доске записывает уравнение реакции:
CuO + Н2SO4 = CuSO4 + H2O
3.6. Условия течения реакций между растворами до конца.
Эта часть урока дается только на предмет возможности протекания реакций между растворами до конца.
Учитель перед классом ставит проблемный вопрос:
Все ли реакции, протекающие в растворах между двумя сложными веществами, будут протекать до конца?
Правило Бертолле (слайд). Газ, осадок, вода.
3.7. Демонстрация опыта: NaOH и KCl
NaOH + KCl ≠ NaCl + KOH
Ученики фиксируют, что нет признаков реакции, записывают уравнение реакции, работают с таблицей растворимости, делают вывод, что данная реакция не идет до конца, т.к. не происходит связывания ионов.
4. Закрепление и применение полученных знаний.
5. Рефлексия.
Учитель задает вопрос: Что нового вы узнали на уроке?
6. Подведение итогов занятия.
Подведем итоги нашего урока-точно сформулируем понятия:
7. Домашнее задание:
Учебник: О.С.Габриелян. Химия 8 класс. Дрофа 2007.
§32, № 3 (а), № 4(в,г,д), №6(задача).
Открытый урок по химии на тему «Реакция обмена» 8 класс
Онлайн-конференция
«Современная профориентация педагогов
и родителей, перспективы рынка труда
и особенности личности подростка»
Свидетельство и скидка на обучение каждому участнику
Открытый урок по химии в 8 классе
Тип урока : Урок открытия новых знаний, обретения новых умений и навыков.
Вид урока : проблемный урок.
Форма урока : урок – эксперимент.
Используемые технологии : ИКТ, ПДО.
Мотивация учащихся. (слайд 1.)
Сегодня я начну урок необычно. Попрошу карандаш у …, а отдам ей свою ручку. Что мы сделали? ( обменялись предметами ). Попрошу запомнить это.
Сегодня вы будете оценивать свою работу на каждом этапе урока, используя лист рефлексии. Подпишите его.
Начнем с теории (задания на известный материал):
Что изучали последние уроки? ( типы химических реакций ) (слайд 2.)
Перечислите известные типы реакций и дайте им определение (фиксирую на доске типы реакций). ( Реакции соединения, разложения, замещения. Дают определение ) (слайд 3,4,5)
У меня 3 рисунка (прил. 5). Имеют ли они отношение к обсуждаемым вопросам и если да, то какое? ( Да. Это художественные образы реакций, которые нам известны ). (слайд 6, 7)
Кто знает все изученные типы реакций и правильно соотнес образы реакций, тот ставит в оценочную таблицу (колонка1) за теорию 3балла. Кто в чем-то ошибся, количество баллов уменьшает.
Выполните задания на карточках ( слайд 8). Проведите самопроверку (с образцом) (слайд 9.) и выставите в лист рефлексии. (оценочная таблица – колонка2) баллы за задания– максимум 5б.
III . Изучение нового материала.
— Определите тип 4 реакции. ( Na 2 SO 4 + 2 KCl = K 2 SO 4 + 2 NaCl ) ( Испытывают затруднения (проблемная ситуация)).
( Что это за новый тип реакции?) (слайд 10.)
Тема нашего урока «Реакция обмена». Цель: Рассмотреть новый тип реакций и научиться его определять.) (слайд 11.)
— Как мы можем решить данную проблему? ( с помощью учебника, расскажет учитель, провести эксперимент).
-Какой способ поможет лучше понять и приобрести опыт в решении реакций? (эксперимент).
Предлагаю провести опытов в группах по инструктивным карточкам с формулированием выводов: осуществима практически проведенная реакция или нет (прил. 2). (слайд 12.)
Но сначала мы вспомним правила техники безопасности.
Не спеши хватать пробирку,
А инструкцию читай.
Убедись, что ты все понял,
Вот тогда и начинай.
Это, друг, химкабинет,
Для еды условий нет.
Пусть в пробирке пахнет воблой,
В колбе — будто мармелад.
Вещества на вкус не пробуй!
Всякое в опыте может случиться,
Внимательным будь и не оплошай.
Тебе всегда поможет учитель,
Паники только не допускай!
Ты сливал, нагревал реактивы
И отчет подготовил в тетрадке.
Не забудь вымыть руки с мылом,
Чтоб здоровье было в порядке
После проведения опытов. (Введение понятия «реакция нейтрализации».)
— Какой ответ мы можем дать на главный вопрос нашего урока? Что такое реакция обмена? ( Реакции обмена. Дают определение) (слайд 14.)
Демонстрация художественного образа р. обмена (прил. 6). Кто сам сформулировал новый тип реакций и смог дать ему определение – выставляет себе 2б в оценочную таблицу (колонка 3).
— Какой еще возник вопрос при проведении эксперимента? ( Почему одни идут реакции до конца, а другие нет)
— Как на него ответите? ( если в результате выпадает осадок, выделяется газ или вода ) (слайд 15.)
IV . Закрепление новых знаний.
Используя свои новые знания, выполните на листе контроля задание №1 (прил. 3).
Обменяйтесь листами контроля и проверьте у соседа правильность выполненного задания (сверка с образцом). (слайд 16.) Оцените его и выставите в лист рефлексии (колонка 4).
Выполните задание №2 на листе контроля (прил. 3). Проведите самооценку, сверив правильные ответы (с образцом). (слайд 17.) Оцените задание и выставите в лист рефлексии (колонка 5).
В чем испытали затруднение? Причина затруднения?
Урок по химии для 8 класса «Реакции обмена»
Онлайн-конференция
«Современная профориентация педагогов
и родителей, перспективы рынка труда
и особенности личности подростка»
Свидетельство и скидка на обучение каждому участнику
Развернутый план-конспект урока «Реакции обмена».
Учебник: О.С. Габриелян.
Тема урока: Реакции обмена.
Тип урока: изучение нового материала.
Образовательные задачи: познакомить с реакциями обмена, с реакцией нейтрализации и с условиями протекания реакций обмена в растворах до конца; сформировать у учащихся знание о реакциях обмена, о реакциях нейтрализации, о условиях протекания реакций обмена в растворах до конца; начать формировать умения составлять реакции обмена, расставлять коэффициенты.
Воспитательные задачи: продолжить формирование естественнонаучного мировоззрения, представления о единичном и целом.
Развивающие задачи: продолжить формирования умения наблюдать, анализировать, объяснять, делать выводы.
Методы обучения: словесные (объяснение и рассказ учителя ), словесно – наглядные( объяснение с использованием записей на классной доске).
Оборудование: классная доска, таблица Д. И. Менделеева, химические колбы и пробирки.
1.Организационный момент (2-5мин.)
Здравствуйте ребята присаживайтесь. Сегодня на уроке мы с вами должны будем познакомиться еще с одним типом реакций обмена.
2. Объяснение нового материала (20 – 30 мин.)
Прежде чем переходить к новой теме, давайте вспомним, какие реакции называются реакциями замещения.
( Реакции замещения – это такие реакции, в результате которых атомы простого вещества замещают атомы одного из химических элементов в сложном веществе).
По своей способности вытеснять водород из растворов кислот все металлы расположены в особый ряд, что это за ряд, как он правильно называется? (Вытеснительный ряд или ряд активности (напряжений металлов) металлов).
Какие должны быть условия взаимодействия металлов с растворами солей, чтобы реакция протекала? ( Металл должен располагаться в ряду активности металлов левее металла, входящего в соль, т. е. быть активнее металла соли).
Сравните реакции замещения с реакциями разложения и соединения.
А теперь давайте перейдем к новой теме реакции обмена, в конце урока вы должны будете дать определение реакциям обмена.
Для того чтобы разобраться с реакциями обмена проведем несколько опытов.
В демонстрационную пробирку нальем раствор щелочи – гидроксида натрия, а затем добавим к нему раствор соли – сульфат меди (ІІ). Выпадает густой синий осадок нерастворимого в воде гидроксида меди (ІІ). Если небольшую часть содержимого из пробирки, в которой образовался осадок, профильтровать и выпарить несколько капель полученного раствора на часовом стекле, то нетрудно будет заметить появление белых кристалликов соли, образовавшейся в ходе реакции. Запишем уравнение реакции:
Чтобы подчеркнуть, что в результате реакции образуется осадок нерастворимого в воде гидроксида меди (ІІ), рядом с его формулой в уравнении реакции записывают стрелку, направленную вниз.
В результате проведенной реакции два сложных вещества ионного строения – щелочь и соль – обменялись своими ионами, т. е. произошла реакция обмена.
Аналогично обмениваются ионами в результате реакции обмена иодид натрия и нитрат свинца (ІІ) в растворе. В итоге выпадает желтый осадок иодида свинца (ІІ).
Запишем уравнение реакции:
В демонстрационную пробирку нальем раствор щелочи и добавим к нему несколько капель фенолфталеина. Содержимое пробирки окрасится в малиновый цвет, что свидетельствует о щелочной среде раствора. Если же к содержимому пробирки прилить немного раствора кислоты, окраска исчезнет, раствор обесцветится, что является признаком химической реакции. Если несколько капель жидкости, полученной в результате реакции, выпарить на часовом стекле, то на нем образуется, кристаллики соли. Еще одним продуктом проведенной реакции является вода.
Запишем уравнение реакции:
Обратите внимание, взаимодействуют два сложных вещества: щелочь, состоящая из ионов металла и гидроксид – ионов, и кислота – молекулярное соединение, которое в растворе образует ионы водорода и кислотного остатка. В итоге образуется два новых сложных вещества: ионное соединение – соль сульфат натрия и молекулярное – вода.
В каждом из двух взаимодействующих растворов была своя среда, соответственно щелочная и кислотная. В результате реакции среда стала нейтральной. Поэтому реакцию обмена между кислотами и щелочами называют реакциями нейтрализации.
В демонстрационную пробирку нальем прозрачный бесцветный раствор карбоната натрия и добавим к нему немного раствора азотной кислоты. Признаком химической реакции послужит «вскипание» раствора из – за выделившегося углекислого газа т.к угольная кислота – непрочное соединение, которое распадается на углекислый газ и воду.
Запишем уравнение реакции:
Сформулируем правило, согласно которому протекают реакции обмена между растворами веществ.
Реакции обмена, протекающие в растворах, идут до конца только в том случае, если в результате их образуется осадок, газ или вода.
3.Первичное закрепление знаний (10 – 12 мин.)
Сегодня на уроке мы с вами познакомились с реакциями обмена и нейтрализации, а также с условиями протекания реакций обмена в растворах до конца.