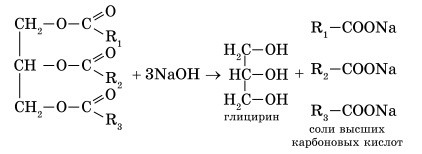Процесс омыления и примеры расчетов.
Каждый, кто уже пытался варить мыло с нуля, наверняка знает, что такое мыльный калькулятор. Но как он работает, и откуда берутся выдаваемые им показатели? В этой статье мы поговорим о базовых принципах мыловарения и расскажем, что такое щелочь, почему без нее никак нельзя изготовить мыло «с нуля», как рассчитывать ее количество и почему нужно разводить ее в воде.
Омыление.
Омылением называется реакция щелочного гидролиза жиров, сущность которой состоит в расщеплении молекула жира (масла) на глицерин и жирные кислоты; последние в щелочной среде образуют соли (которые суть и есть наше мыло):
Однако, если мы просто положим сухие шарики щелочи в твердое или даже жидкое масло, то ровным счетом ничего не произойдет. Жиры гидролизуются и становятся в состоянии реагировать с щелочью только в водной среде.
Таким образом, поскольку щелочь всегда действует в водном растворе, эту формулу можно представить более просто:
Щелочь + Вода + Жир = Мыло + Глицерин
Как видно из этой формулы, обойтись без щелочи в процессе мыловарения никак нельзя. Если же заморачиваться с суровой химией на дому все же не хочется, то ваш выбор – мыло из основы. Основа содержит уже готовые соли жирных кислот, так что проводить омыление самому не придется. Но продолжим про мыло с нуля.
Природные масла представляют собой смесь, содержащую различные по строению и массе молекулы жиров. Чтобы реакция омыления в такой смеси прошла полностью, и при этом не образовался избыток едкой щелочи, необходимо точно подобрать количества взаимодействующих компонентов.
Это можно сделать и самостоятельно, зная состав каждого масла и рассчитав параметры соответствующих химических реакций. Однако, чтобы облегчить мыловарам эту задачу была составлена таблица омыления для наиболее часто используемых масел (см. таблицу в конце статьи).
Кстати, в отличие от мыльного калькулятора, эту таблицу можно распечатать и взять с собой на необитаемый остров, где нет электричества и интернета. Ну, если вы внезапно захотите поварить мыло в совсем полном одиночестве.
Для получения твердого мыла используется NaOH (едкий натр или каустическая сода), тогда как для жидкого рекомендуется применять KOH (едкое кали, оно же каустический поташ).
Чтобы просто и быстро определить, сколько щелочи необходимо для полного омыления нужного количества масла надо умножить массу масла на коэффициент из таблицы. А для приготовления мыла из смеси нескольких масел нужно отдельно посчитать количество щелочи, необходимое для каждого из компонентов, а затем просто сложить полученные веса.
Пример: рассчитаем количество едкого натра, необходимое для полного омыления 0,5 кг масла ши и 0,5 кг кунжутного.
Ши: 500 грамм умножаем на табличный коэффициент масла какао для NaOH, т. е. на 0,1282 и получаем: 500*0,1282 = 64,1 грамма NaOH.
Кунжут: аналогично, 1000*0,1376 = 68,8 грамма NaOH.
Всего потребуется 64,1+ 68,8 = 132,9 грамма щелочи.
Необходимое разведение щелочи.
Не стоит забывать, что масса щелочи считается для твердого порошка (или гранул) 100%-й щелочи, а не для ее водного раствора. Остановимся на этом подробнее. Дело в том, что наиболее часто используемый принцип разбавл ения – брать воду из расчета 33% от веса масел. Это значение стоит «по умолчанию» в большинстве мыльных калькуляторов:
Однако надо понимать, что сама вода как таковая в реакцию не вступает, и уж тем более, никак не реагирует с маслом, а служит реакционной средой, растворителем! Она нужна именно для создания реакционной среды – чтобы щелочь могла полноценно проявить свои свойства, а также для гидролизации жира, т.е. его подготовки к собственно химическому взаимодействию.
Таким образом, главное, на что влияет количество добавленной воды – это по сути скорость затвердевания сваренного мыла. При этом даже правильнее рассчитывать воду не сколько от масла/жира, а от всей реакционной массы. Обычно это требуется при варке совсем небольших объемов мыла или при использовании незнакомых рецептов, где важно не переборщить с водой или подозревается долгое затвердевание:
Пример: разведем щелочь водой в количестве 33% от массы реакционной смеси.
*для 100 граммов кокосового масла это 0,33*(100+18,3) = 39 граммов,
*а для 100 граммов масла жожоба = 0,33*(100+6,6) = 35,2 грамма.
Если по каким-то причинам вам нужно, чтобы мыло сохло помедленнее – разводите щелочь в большем количестве воды. И наоборот, чтобы ускорить процесс, добавьте ее меньше.
Важная деталь! Не стоит разводить щелочь с водой меньше, чем 1:1! То есть масса воды всегда должна быть равна или больше, чем масса щелочи.
Таблица коэффициентов омыления.
Что такое реакция омыления
Растительные и животные жиры
Жиры образуются в организме растений и животных, служат запасным питательным веществом. В строении растительных и животных жиров есть некоторые важные отличия.
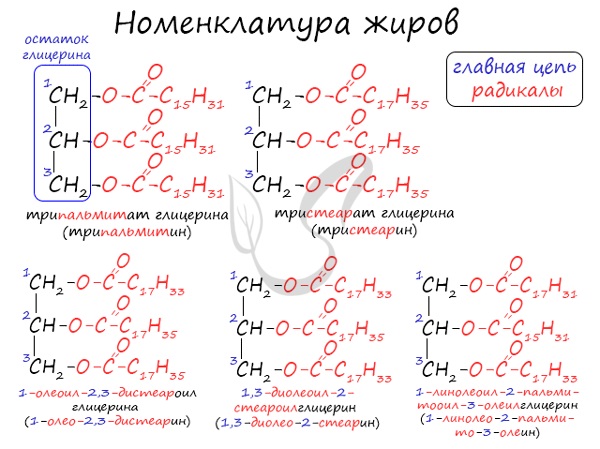
Номенклатура жиров
В соответствии с тривиальной номенклатурой, жиры называют, добавляя окончание «ин» к названию кислоты и приставку, указывая, сколько гидроксогрупп в молекуле глицерина подверглось этерификации. В общем лучше 1 раз увидеть, чем 100 раз услышать 😉
Получение жиров
Жиры (по строению сложные эфиры) получаются в реакции этерификации, протекающей между трехатомным спиртом глицерином и высшими карбоновыми (жирными) кислотами.
В зависимости от того, какие именно кислоты участвуют в реакции, образуются различные жиры.
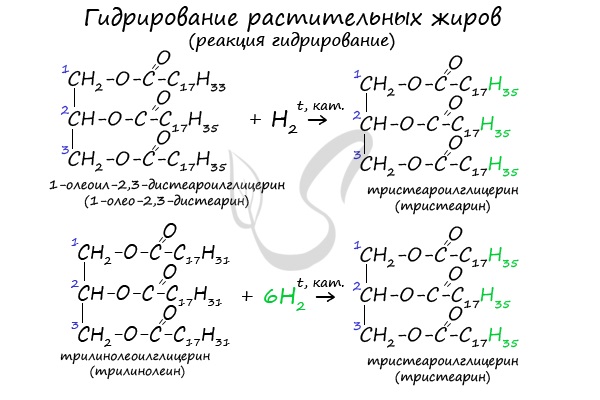
Химические свойства жиров
В состав растительных жиров входят непредельные кислоты, которые поддаются гидрированию и превращаются в предельные. Таким путем в пищевой промышленности получают маргарин.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
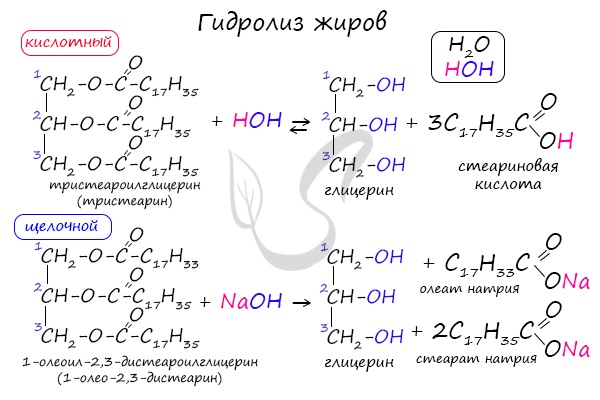
Реакция омыления.

К слову, о температурном режиме. Реакция омыления качественно пройдет при любой температуре. Поместит мыловар смесь в холодильник, оставит ли как есть, или поместит на водяную баню, полностью реакция между щелочью и маслами пройдет непременно, но за разное время. При высоких температурах речь идет о порядке 3-8 часов, а без принудительного подогрева порядка 5-12 часов. И, по мнению того же Кевина Данна, исходя из результатов его экспериментов, в течении суток вся щелочь полностью прореагирует с кислотами. Иными словами, реакция омыления полностью заканчивается в течении суток независимо от способа приготовления мыла. Далее мылу необходим период созревания. Время, в течении которого мылу надо просохнуть, уплотнится, иначе оно будет мягкое и быстро смыливаться. Если мыло приготовлено горячим способом, созревание идет быстро, всего пару дней. Если холодным способом, около месяца (зависит от того, сколько воды использовал мыловар для приготовления щелочного раствора). Если безгелевым способом (при низких температурах), еще дольше, до двух-трех месяцев. Ошибочно утверждают некоторые мыловары, что период созревания нужен мылу для того, чтобы щелочь до конца прореагировала с кислотой. Правдой это становится только тогда, когда в готовом мыле (то есть через сутки после начала его приготовления) остался избыток щелочи. Тогда, по данным Кевина Данна, за период созревания повышенный щелочной уровень должен понизится. Ну а в случае правильно составленного рецепта, и точного его соблюдения, мыло безопасно к использованию уже через сутки.
Вот и все, на что я хотела обратить внимание мыловаров по теме реакции омыления. Выше рассмотрен случай приготовления чистого мыла, без всяких добавок, из масел с помощью водного раствора гидрооксида натрия. А ведь в мыло с нуля чего только не добавляют.
Рассмотрим в следующей части, какие же мифы живут в области дополнительных ингредиентов в мыле с нуля.
ОМЫЛЕНИЕ
ОМЫЛЕНИЕ — обратимая реакция сложного эфира с водой, в результате к-рой образуются спирт и карбоновая к-та. О. сложных эфиров имеет большое значение в обмене веществ животных и растительных организмов, где процесс О. катализируют специфические ферменты — эстеразы (см.). Наибольшее значение в этом отношении среди них имеют липазы (см.), участвующие в процессе О. жиров, эстеразы алифатических эфиров, лецитиназы (см.) и др. Для осуществления функций нервной системы большое значение имеет реакция О. ацетилхолина, протекающая в области синапсов при участии холинэстеразы (см.).
В промышленности широко используется О. природных жиров (см.), являющихся эфирами высших жирных к-т и глицерина. Жиры обрабатывают р-рами щелочей при повышенной температуре, в результате чего образуются соли жирных к-т, или мыла (см.), откуда и произошло название реакции О.
Главными этапами ферментативного О. сложных эфиров являются: взаимодействие эфира с активным центром фермента, содержащим нуклеофильную группировку (либо ими-ногруппу имидазольного кольца остатка гистидина, либо поляризованную соседними функц, группами ОН-группу остатка серина); образование промежуточного соединения; перераспределение в нем электронов и выделение молекулы спирта с образованием ацилированного фермента, к-рый разлагается водой, в результате чего регенерируется молекула нативного фермента и освобождается молекула к-ты.
Библиография: Бендер М. Л. Механизмы катализа нуклеофильных реакций производных карбоновых кислот, пер. с англ., М., 1964; Реутов О. А. Теоретические проблемы органической химии, М., 1956; Степаненко Б. Н. Органическая химия, М., 1980.
ОМЫЛЕНИЕ в гистологической технике
ОМЫЛЕНИЕ в гистологической технике — гистохимическая реакция, осуществляемая с целью выявления в гистол, препаратах калийных, натронных и кальциевых солей жирных к-т (мыл). Калийные и натронные мыла при фиксации ткани в формалине растворяются, поэтому, чтобы наблюдать совершившееся О. в целом, стремятся при фиксации все мыла перевести в нерастворимый жирно-кислый кальций. О. в гистологии применяют также для гистохим, изучения полисахаридов, гликоз-аминпротеогликанов, основных белков, катехинов и др. После О. способность испытуемых веществ к специфическому окрашиванию может полностью или частично восстановиться или не восстановиться совсем в зависимости от хим. строения вещества и от способа проведения реакции О.
Мак-Манус (J. F. A. McManus) и Маури (R. W. Mowry) рекомендуют для О. сложных эфиров уксусной к-ты 0,1 н. р-р KOH в воде. Амиды, получающиеся при ацетилировании NH2-групп, при этом способе О. не реагируют с йодной к-той, что может служить одним из способов идентификации аминогрупп.
Для проведения реакции О. чаще используют обработку срезов 1% р-ром аммиака в 70% спирте (так наз. спиртовый аммиак). Напр., после О. спиртовым аммиаком у ацетили-рованных сахаров почти полностью восстанавливается способность к реакции с шифф-йодной к-той (см. Шиффа реактив), у фенолов — к реакции азосочетания, у катехинов —к восстановлению кислых р-ров AgN03, у основных белков — к окрашиванию кислыми красителями. Метилированные остатки сульфокислот, фосфорной и карбоновых к-т после реакции О., по данным Лилли (R. D. Lillie), хорошо окрашиваются основными красителями. О. спиртовым аммиаком мышечных волокон, ацилированных путем обработки смесью серной к-ты, уксусного ангидрида и ледяной уксусной к-ты, лишь частично восстанавливает их способность воспринимать окраску прочным зеленым и не снимает блокирования специфической окраски гликозаминпротеогликаыов после аци-лирования или гликозаминогликанов после сульфатирования.
Библиография: Лилли Р. Патогистологическая техника и практическая гистохимия, пер. с англ., с. 182 и др., М., 1969; Принципы и методы гистоцитохимического анализа в патологии, под ред. А. П. Авцы-наидр.,М., 1971.
Что такое мыла и как их получают? Какова химическая формула мыла?
Содержание:
Мыло – это вещество, которое используется в качестве косметического средства или средства бытовой химии. Это жидкий или твердый продукт, который содержит поверхностно-активные вещества (ПАВ). Эти вещества снижают поверхностное натяжение и увеличивают смачивающую способность воды.
История открытия мыла
Впервые о мыле в Древнем Риме в 77 г. н.э. говорил Плиний Старший. В Русь из Византийской империи пришло не только православие, но и мыло. Особенно поддерживал мыловарение Петр I.
Формула мыла в химии была определена Мишелем Эжен Шеврёль в XIX веке. Ученый установил, что мыло — это смесь натриевых солей жирных кислот. В нашей столице первое производство мыла было открыто во второй половине XIX века. Мыло стоило одну копейку, поэтому его могли покупать даже бедные люди.
Химическая формула мыла
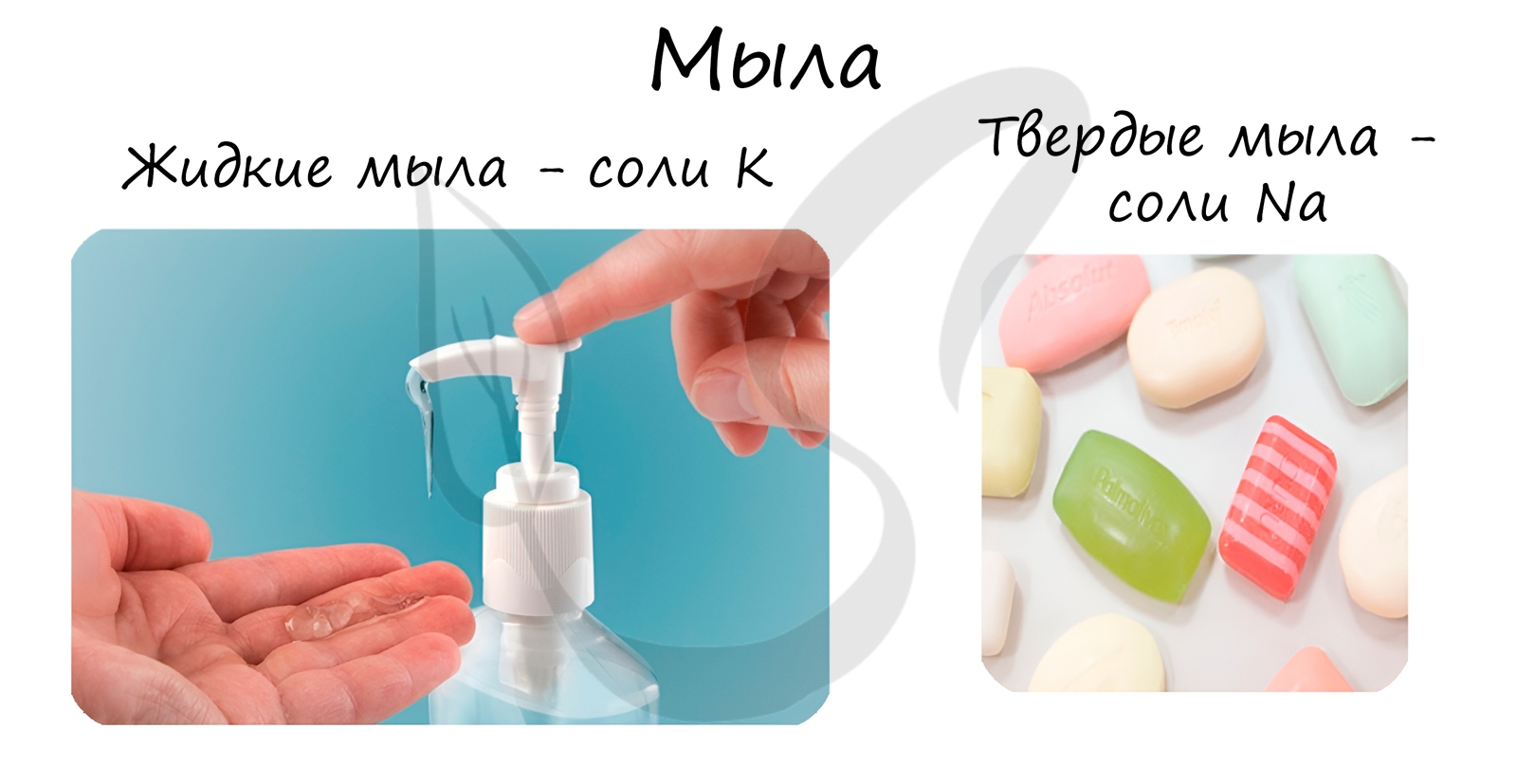
Например, формула твердого мыла C17H35COONa, а жидкого – C17H35COOК. В состав мыла также входят красящие вещества и ароматизаторы.
Особенные свойства мыла
Мыло формирует пену благодаря образованию мицелл и высокой поверхностной активности. Остаток кислоты – гидрофобная часть очищающего средства, карбоксильный ион – гидрофильная.
Грязь растворяется в несколько этапов:
Классификация мыла
I. По особенностям реагирования с водой:
II. По агрегатному состоянию:
III. По сферам применения:
Способы получения мыла
Процесс изготовления мыла
Очищающее средство в промышленных условиях синтезируют в результате двух стадий.
Мыло можно сварить двумя способами.
Как ПАВ влияют на природу
Водоемы могут самоочищаться, что достигается разбавлением, оседанием частичек на дно и созданием отложений, разложением органики до аммиака и солей аммония при помощи микробов. Устранить негативные последствия действия ПАВ сложно, ведь ПАВ в водоемах присутствуют в виде гомологов и изомеров. Если концентрация ПАВ в смеси близка к критической, то вредные свойства всех веществ в смеси суммируются.
ПАВ можно классифицировать на две группы:
ПАВ опасны для природы, т. к. они понижают поверхностное натяжение. Если в водоемах поверхностное натяжение изменяется, то концентрация кислорода в воде снижается. Это приводит к развитию биомассы водных растений и гибели водных животных. Но ПАВ могут быть не только вредными, но и безопасными. Некоторые ПАВ распадаются на углеводы.
В организм человека или животного ПАВ попадают с пищей, водой и через кожу. ПАВ могут вызывать аллергию, которые иногда сопровождаются осложнениями.