Токсические влияния на репродуктивную функцию. Тератогенез
Репродуктивная функция осуществляется как сложноорганизованная последовательность физиологических процессов, протекающих в организме отца, матери, плода. Токсиканты могут оказывать неблагоприятное воздействие на любом этапе реализации функции. Сложность феномена репродукции делает его весьма уязвимым для ксенобиотиков. Трудность познания феномена состоит в том, что нарушение репродукции может быть следствием даже острого токсического действия на различные органы и системы одного из «участников» процесса, в различные временные периоды, а проявляться лишь спустя многие месяцы, а иногда и годы, дефектами зачатия, вынашивания, развития плода и несостоятельностью растущего организма (таблица 1).
Таблица 1. Периоды реализации репродуктивной функции, уязвимые для действия токсикантов.
— формирование половых клеток (гамет)
Рост и развитие ребенка
— развитие половых органов
Трансплацентарный канцерогенез
1. Краткая характеристика анатомо-физиологических особенностей репродуктивных органов
Женская репродуктивная система состоит из 4 анатомических образований, функция которых регулируется гормонами, продуцируемыми гипофизом, яичниками, плацентой.
Мужская репродуктивная система состоит из четырёх органов, функции которых регулируются гормонами, синтезируемыми гипофизом и семенниками (яички).
3. Особенности действия токсикантов на репродуктивные функции
Точно выявить механизм, лежащий в основе репродуктивных нарушений, порой практически невозможно, так как ксенобиотик мог подействовать либо на обоих родителей, либо только на одного из них, либо на мать и плод.
Неблагоприятное действие токсикантов (и их метаболитов) на мужские и женские органы репродуктивной системы может быть обусловлено либо нарушением механизмов физиологической регуляции их функций, либо прямыми цитотоксическими эффектами. Так, нарушение гормональной регуляции функций яичников может быть следствием конкуренции ксенобиотиков с половыми гормонами (андрогены, контрацептивные средства), действия на рецепторы эстрогенов (хлорорганические и фосфорорганические соединения), изменения скорости продукции половых гормонов, их метаболизма и выведения (ДДТ, ТХДД, ПХБ, хлордан). Например, полигалогенированные бифенилы нарушают метаболизм половых гормонов. При введении новорожденным крысам, эти вещества существенно изменяют функции печени, значительно изменяя уровень циркулирующих в крови половых гормонов. В последующем это приводит к нарушению оплодотворяемости животных.
Цитотоксичность, как правило лежит в основе поражения половых клеток отца или матери и клеток эмбриона.
Механизм действия многих токсикантов остается неизвестным (сероуглерод, углеводороды). Некоторые из опасных веществ, способных нарушать репродуктивные функции, представлены в таблице 2.
Таблица 2. Вещества, предположительно нарушающие репродуктивные функции
— андрогены, эстрогены, прогестины
— алкилирующие агенты, антиметаболиты, антибиотики
3. Психоактивные препараты, вещества, действующие на ЦНС
— летучие анестетики (галотан, енфлюран, метоксифлюран, хлороформ)
4. Металлы и микроэлементы
— алюминий*, мышьяк, бор*, бериллий, кадмий, свинец (органические и неорганические соединения), литий, ртуть (органическккие и неорганические соединения), молибден, никель, серебро*, селен, таллий
— гексахлорбензол, карбаматы (карбарил), производные хлорбензола (метоксихлор, ДДТ), альдрин, дильдрин, ФОС (паратион), другие (хлордекон, этиленоксид, мирекс)
— афлатоксины*, циклогексиламин, диметилнитрозамин, глутамат, производные нитрофурана, нитрит натрия
— формальдегид, хлорированные углеводороды (трихлорэтилен, тетрахлорэтилен, ТХДД*, полихлорированные бензофураны*), этилендибромид, этилендихлорид, этиленоксид, этилентиомочевина, этиленхлоргидрин, анилин, мономеры пластмасс (капролактам, стирол, винилхлорид, хлоропрен), эфиры фталиевой кислоты, полициклическкие ароматические углеводороды (бенз(а)пирен), растворители (бензол, сероуглерод, этанол, эфиры гликолей, гексан, толуол, ксилол), оксид углерода, метилхлорид, диоксид азота, цианокетоны, гидразин, анилин
— этанол, компоненты табачного дыма, средства пожаротушения (трис-(2,3-дибромпропил)фосфат), радиация*, гипоксия*
Вещества, вызывающие преимущественное повреждение репродуктивных органов мужчины, представлены в таблице 3.
Таблица 3. Вещества, вызывающие преимущественное повреждение репродуктивных органов мужчины
Добавочные половые железы
Хлогидрин, метилхлорид, этан диметилсульфонат
На репродуктивные характеристики в постнатальном периоде могут оказывать влияние ксенобиотики, попадающие в организм кормящей матери и выделяющиеся с грудным молоком. Такие вещества, как металлы (ртуть, свинец), тетрахлорэтан, галогенированные ароматические углеводороды (дибензофураны, бифенилы, диоксины), пестициды (ДДТ, диэльдрин, гептахлор и т.д.) могут поступать в организм новорожденного этим путем в больших количествах.
Наиболее часто при нарушениях репродуктивной функции сталкиваются с полигенным (действие на различные органы и системы), многофакторным (действие нескольких токсикантов), синергическим (однонаправленное спонтанное и индуцированное токсикантом нарушение развития) действием.
Основными проявлениями токсического действия химических веществ на органы и ткани, ответственные за репродуктивные функции организма, и непосредственно на плод, являются: бесплодие и тератогенез.
Дословный перевод термина «тератогенез» означает «рождение монстров», от греческого teras, означающего «монстр». В древние времена полагали, что рождение деформированного ребенка с аномалиями развития является следствием кровосмешения человека и божества. В средние века, случившийся факт рассматривали как результат происков дьявола, и, как правило, дитя и мать приговаривали к смерти.
Тератогенным называется действие химического вещества на организм матери, отца или плода, сопровождающееся существенным увеличением вероятности появления структурно-функциональных нарушений у потомства. Вещества, обладающие тератогенной активностью, называются тератогенами. Существует представление, согласно которому практически любое химическое вещество, введенное в организм отца или матери, в тот или иной период беременности, в достаточно большой дозе, может вызывать тератогенез. Поэтому тератогенами в узком смысле слова следует называть лишь токсиканты, вызывающие эффект в концентрациях, не оказывающих заметного действия на организм родителей. В ходе лабораторных и эпидемиологических исследований установлено, что многие ксенобиотики имеют достаточно высокий потенциал репродуктивной токсичности. Из обследованных примерно трех тысяч ксенобиотиков около 40% обладают свойствами тератогенов.
Существует четыре типа патологии развития плода: гибель, уродства, замедление роста, функциональные нарушения.
Действие токсиканта, сопровождающееся гибелью эмбриона, чаще обозначается как эмбриотоксическое.
В ходе изучения тератогенеза, удалось выявить ряд закономерностей, среди них основными являются: 1) токсикокинетические; 2) генетической предрасположенности; 3) критических периодов чувствительности; 4) общности механизмов формирования; 5) дозовой зависимости.
Особенности токсикокинетики. Тератогенным действием на плод обладают лишь вещества, хорошо проникающие через плацентарный барьер. Многие тератогены подвергаются в организме матери или плода биоактивации (см. раздел «Метаболизм ксенобиотиков»).
Отчасти этот феномен связан с существенными различиями токсикокинетики ксенобиотиков.
Период наивысшей чувствительности к тератогенам, в котором они оказывают наиболее значимое действие на плод и индуцируют появление грубых морфологических дефектов, это период закладки зародышевых листков и начала органогенеза (первые 12 недель эмбрионального развития). Период органогенеза начинается после дифференциации зародышевых листков и завершается формированием основных органов. За периодом органогенеза следуют периоды гистогенеза и функционального созревания органов и тканей плода (таблица 4).
Таблица 4. Критические периоды эмбриогенеза человека. Примеры веществ, оказывающих патогенное действие на плод (J.V. Aranda, L. Stern, 1983)
Анатомические образования/функции
глаза, мозг, спинной мозг, сердце, дуга аорты, череп,
урогенитальная система, зубы
пальцы, гениталии, брюшная стенка, небо
Функциональное созревание
Внешние половые признаки;
Продолжительность периодов внутриутробного развития у различных видов млекопитающих представлена в таблице 5.
Таблица 5. Продолжительность периодов внутриутробного развития у различных видов млекопитающих (сутки). Последствия действия тератогенов
пренатальная гибель
грубые морфологические дефекты
физиологические и функциональные нарушения
Тип нарушения, вызванный веществом, определяется стадией развития плода и конкретным временем воздействия. Для того, чтобы некий тератоген вызвал повреждение конкретного органа, плод должен быть подвержен действию этого вещества в период формирования данного органа. Для развития различных органов «критические периоды» отмечаются в разное время после зачатия. Гистогенез и функциональное развитие органа начинаются до завершения периода органогенеза и продолжаются в периоде роста плода. Неблагоприятные последствия действия тератогенов в этом периоде это уже не морфологические дефекты органов и систем, но различного рода функциональные нарушения.
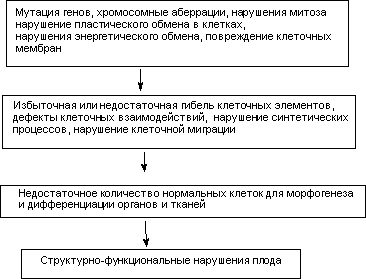
Механизмы формирования. Различные вещества с различным механизмом токсичности, при действии на плод в один и тот же критический период, часто вызывают одинаковые виды нарушений. Из этого следует, что значимым является не столько механизм действия токсиканта, сколько сам факт повреждения клеточных элементов на определенном этапе развития организма, инициирующий во многом одинаковый каскад событий, приводящих к уродствам (рисунок 1)
Рисунок 1. Предполагаемые этапы формирования дефектов развития при действии токсикантов на плод
Таблица 6. Частота случаев дефектов развития у новорожденных мышат линии C57BL/6 после скармливания беременным самкам ТХДД
Двухсторонняя аномалия почек (%)
3.1.2. Особенности токсикокинетики тератогенов
Попав в организм матери, вещества распределяются в соответствии с токсикокинетическими свойствами ксенобиотика. Беременность существенно влияет на характер распределения (снижается связывание токсикантов белками, увеличивается объем распределения) и скорость выведения веществ (увеличивается мощность гломерулярной фильтрации) из организма матери. Активность ферментов I и II фаз метаболизма чужеродных соединений снижается.
Токсический эффект ксенобиотиков может зависеть от действия на структуры-мишени их метаболитов, образующихся в организме матери или/и плода. Основным органом биоактивации является печень матери. Однако, образующиеся в ходе метаболизма высоко активные в химическом отношении продукты, быстро реагируют со структурными элементами печени или органами и тканями матери, и не в состоянии достичь тканей плода. Таким образом, действовать на плод могут лишь более стабильные, те есть более инертные в химическом отношении молекулы, образовавшиеся в организме матери, либо реактивные метаболиты, образующиеся непосредственно в тканях плода. Некоторые вещества метаболизируют в плаценте.
3.1.3. Механизмы действия тератогенов
Тератогенный эффект развивается при действии токсиканта в определенной дозе, на чувствительный орган, в определенный период его формирования. Выявлено множество механизмов, посредством которых ксенобиотики оказывают неблагоприятное воздействие. Понимание этих механизмов помогает предвидеть риск, сопряженный с контактом с веществом, корректно экстраполировать данные, получаемые в экспериментах на животных на человека.
Повреждение механизмов репарации. Нарушение свойств генетического аппарата клетки может быть следствием угнетения активности ферментов, обеспечивающих репарацию спонтанно трансформирующихся молекул ДНК (гидроксимочевина, антагонисты фолиевой кислоты).
Нарушение биосинтеза жизненно важных молекул может стать следствием действия токсикантов. Многие вещества способны нарушать синтез белка, блокируя процессы репликации (синтез ДНК), транскрипции (синтез РНК) и трансляции (собственно синтез белка). К числу таких веществ относятся многие цитостатики и некоторые антибиотики. По большей части, действие этих веществ приводит к гибели плода; уродства отмечаются значительно реже.
Вещества, способные угнетать активность энзимов пластического обмена в клетках плода, нарушают его развитие.
Нарушение энергетического обмена может привести к тератогенезу или гибели плода. Причинами состояния могут стать блокада гликолиза, повреждение цикла трикарбоновых кислот (йод- и фторацетат, 6-аминоникотинамид), блок электрон-транспортной системы и разобщение процессов окисления и фосфорилирования (цианиды, динитрофенол).
Повреждение клеточных мембрран. Нарушение проницаемости мембран клеток эмбриона может сопровождаться их гибелью и нарушением эмбриогенеза глаз, мозга, конечностей. Полагают, что в основе тератогенного действия таких веществ, как диметилсульфоксид (ДМСО) и витамин А, лежит именно этот механизм.
Таким образом, в основе тератогенеза могут лежать практически все известные механизмы токсического действия ксенобиотиков (см. раздел «Механизмы действия»).
4. Характеристика некоторых токсикантов, влияющих на репродуктивные функции
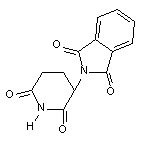
Талидомид (рисунок 2) один из активнейших, известных, тератогенов для человека.
Рисунок 2. Структура талидомида
Это вещество является выраженным тератогеном для экспериментальных животных. Для человека этот вид токсического действия окончательно не доказан. Хлорид ртути вызывает аборты, однако, трансплацентарное поступление неорганических соединений ртути в организм плода не приводит к врожденным аномалиям. Пары ртути, действуя ингаляционно, вызывают нарушения менструального цикла. Элементарная ртуть также обладает способностью проникать через плацентарный барьер. Повышенное содержание ртути в плаценте и тканях плода обнаружено при обследовании женщин стоматологов, имевших контакт с ртутными амальгамами.
Метилртуть вызывает серьёзное поражение мозга плода, сопровождающееся нейрональной дегенерацией и пролиферацией глии, особенно выраженной в коре мозжечка и конечного мозга. Глубина нарушений зависит от сроков беременности. Особенно опасно воздействие токсиканта во втором и третьем триместре беременности. Некоторые проявления патологических изменений выявляются сразу после рождения, другие, спустя несколько месяцев. Основные симптомы поражения: спастичность, гипотония, микроцефалия, нарушение движения глазных яблок (нистагм, стробизм), умственная отсталость, нарушение роста зубов. Отсутствуют данные о дозовой нагрузке, приводящей к патологии.
Дети, подвергшиеся воздействию свинца в утробе матери, требуют длительного и постоянного контроля состояния их здоровья. Необходимо контролировать количество свинца в плазме крови, протопорфиринов в эритроцитах, оценивать неврологический статус.
В лабораторных условиях периодически наблюдаются эффекты, связанные с действия кадмия на репродуктивные функции экспериментальных животных. Эффект зависит от дозы вещества, вида лабораторного животного, периода воздействия. Экстраполяция данных, в этой связи, на человека весьма затруднена. Основываясь на экспериментальных данных, полагают, что тератогенное действие Cd-содержащих веществ может быть связано с ингибированием активности карбоангидразы. Установлено также, что кадмий способен накапливаться в плаценте и вызывать её повреждение.
Данные, полученные при обследовании людей менее убедительны. Только при действии вещества в высоких дозах иногда отмечается повреждение семенников, тератогенез.
4.5. Полигалогенированные бифенилы (ПГБ)
Эта группа химических веществ включает более ста наименований. Соединения используются в качестве изолирующих жидкостей, теплообменников, химических добавок к маслам и т.д. Как правило, коммерческие препараты представляют собой смесь веществ, включая более токсичные дибензофураны.
В условиях опыта на лабораторных животных удается выявить неблагоприятное действие растворителей на репродуктивную функцию. В этой связи органические растворители рассматриваются как тератогены для экспериментальных животных.
С другой стороны отсутствуют убедительные данные, указывающие на неблагоприятное действие цитостатиков (по показателю «увеличение риска тератогенеза») на организм отца до, или в период, зачатия.
5. Выявление действия токсикантов на репродуктивную функцию.
Оценить токсическое действие веществ на репродуктивные функции чрезвычайно сложно, поскольку многообразны и сложны механизмы и условия, приводящие к неблагоприятному эффекту. В настоящее время разработано большое количество протоколов опытов, в рамках которых подобные исследования выполняются. Обычно они осуществляются в четыре этапа:
3. Изучение тератогенной активности веществ;
4. Выявление перинатальной и постнатальной токсичности.
Опыты выполняются на животных, содержащихся в строго контролируемых условиях.
Выраженность токсического действия исследуемого вещества на репродуктивные функции оценивают по следующим показателям:
— морфологические изменения в репродуктивных органах животных;
— продолжительность периода беременности;
— численность приплода и его состояние, соотношение живых и мертвых новорожденных крысят, вес крысят, наличие видимых уродств;
— характеристика развития новорожденных: прибавка в весе, смертность и т.д.
— наличие морфологических дефектов формирования органов и тканей у крысят после завершения выкармливания матерью.
Все показатели оцениваются количественно, обрабатываются статистически и сравниваются с контролями. Существенные, статистически достоверные нарушения хотя бы одного из оцениваемых показателей свидетельствует о репродуктивной токсичности исследуемого вещества.
Значительно более трудоемким является протокол исследования, предполагающий проследить неблагоприятный эффект в нескольких поколениях. Основная сложность состоит в правильном формировании исследуемых групп и групп сравнения. С содержанием таких протоколов можно познакомиться в специальной литературе.
Таблица 7. Типовой протокол исследования тератогенной активности и перинатальной/постнатальной токсичности
Мать и потомство умерщвляют на 20 сутки
Самкам, начиная с 15 дня беременности, вводят токсикант
Введение токсиканта до завершения лактации (21 сутки). Умерщвление матери и потомства
В процессе исследования оценивают структурные нарушения развития плода (таблица 8), величину эмбрио-фетальной летальности.
Таблиц 8. Некоторые аномалии развития, выявляемые входе оценки тератогенности ксенобиотиков
А. Дефекты, выявляемые при общем осмотре
1. Череп, головной и спинной мозг
— увеличение носовых ходов
— отсутствие носовой перегородки
Б. Дефекты внутренних органов
— уменьшение размеров легких
— нарушение формы органа
В. Нарушения скелета
— нарушение формы хвоста
Поскольку практически все выявляемые нарушения встречаются и у интактных животных, а также могут быть вызваны факторами не химической природы, большое внимание необходимо уделять формированию репрезентативных контрольных групп и статистической обработке получаемых результатов.
В качестве дополнения к предлагаемому протоколу рассматривается возможность использования методов оценки функционального состояния животных, родившихся от самок, подвергшихся воздействию исследуемого химического вещества. Постнатальная оценка функционального состояния животных включает определение скорости роста, состояния почек, печени, сердечно-сосудистой, дыхательной систем, ЦНС.
Изучение перинатальной и постнатальной токсичности. Исследование выполняют на беременных самках белых крыс (таблица 7). 20 животным (на каждую исследуемую дозу) вводят исследуемый препарат в течении последней трети беременности и периода лактации. Способы введения и дозы испытываемых веществ подбирают по общим правилам (см. выше). Оценивают продолжительность беременности, число и размеры новорожденных, скорость роста приплода и т.д. Целесообразно использовать морфологические и физиологические методы оценки состояния здоровья крысят. Результаты обрабатывают статистически и сравнивают с контролями.
5.2. Оценка риска поражения
Теоретически оценить риск нарушения репродуктивной функции можно только с учетом дозовых нагрузок ксенобиотика, поскольку, как сказано выше, практически отсутствуют вещества безопасные при любых условиях воздействия и в любых дозах. Однако на практике сделать это применительно к человеку в настоящее время не представляется возможным. Чрезвычайно сложная методология получения данных для построения зависимостей «доза-эффект», применительно к рассматриваемой проблеме, не позволяет накопить необходимую для этого информацию.
В этой связи оценка риска поражения и диагностика действия токсиканта на репродуктивную функцию людей строятся на комплексном изучении состояния здоровья, конкретных обстоятельств жизни и работы обследуемых.
Признаки нарушения репродуктивных функций могут быть различными, но всегда следует брать под контроль любой выявленный случай. Возможны, в частности, обращения к врачу по поводу получения информации об опасности тех или иных токсикантов, с которыми отцу или матери приходится сталкиваться на производстве. При этом, работающий может предъявлять жалобы на состояние здоровья, что, по его мнению, указывает на пагубное действие некоего вещества (веществ). Достаточно часто за консультацией обращаются бесплодные супружеские пары, с просьбой решить не является ли причиной их беды тот или иной токсикант, с которым контактирует один или оба супруга. Наконец, поводом для исследования могут стать просьбы родителей проконсультировать их о возможных причинах дефекта развития их ребенка.
Во всех подобных случаях врачу необходимо обследовать пациента, документировать все предъявляемые жалобы, выявить последовательность появления симптомов, степень их выраженности, продолжительность. Желательно опросить, и в случае необходимости, осмотреть сослуживцев пациента на предмет выявления у них аналогичных проявлений. Следует обращать внимание на возможность действия на женщину «непроизводственных токсикантов» в быту (растворители, моющие средства, косметика, вредные привычки, приём лекарств и т.д.). Важной информацией для принятия решения являются данные о возрасте, профессии пациентов, перенесённых заболеваниях.
Ретроспективная оценка возможного токсического воздействия не всегда разрешимая задача, поскольку информация предъявляемая пациентами, как правило, носит субъективный характер. Лица с нарушением репродуктивной функции значительно чаше вспоминают факт воздействия «вредности», чем лица, без такового. Выявление времени воздействия токсиканта и установление, в каком периоде беременности это произошло, также основывается, как правило, на опросе, и потому весьма затруднено.
При изучении условий труда обследуемых необходимо обращать внимание на перечень потенциально опасных действующих токсикантов, их количественные характеристики на рабочем месте, принимаемые меры защиты (технические, организационные и т.д.).
Важно установить отсутствие генетических дефектов у родителей и родственников обследуемых. Наиболее часто встречающиеся «спонтанные» нарушения у человека это: анэнцефалия, spina bifida, дефекты конечностей, расщепленное небо, заячья губа, врожденный вывих бедра, пилоростеноз.
Медицинское обследование беременной женщины, подвергшейся (подвергающейся) действию токсикантов, должно быть тщательным и включать исследование состояния плода, особенно его подвижность, частоту сердечных сокращений, размер.
Полезными методами оценки репродуктивных функций мужчины являются: вес тела, размеры тестикул, анализ спермы (количество сперматозоидов, их подвижность, морфология), эндокринные функции (фолликулостимулирующий, лютеинизирующий гормоны, тестостерон, гонадотропин). При обследовании женщин оценивают: вес тела, эндокринные функции (гонадотропин, пролактин, хориоидный гонадотропин, эстроген, прогестерон), цитологические свойства цервикальной жидкости, анатомо-морфологические особенности органов половой системы. В ряде случаев возникает необходимость пренатального обследования плода (ультрозвуковая диагностика, лучевая диагностика, фетоскопия, фетография, амниография, амниоцентез, исследование хориона, анализ фетальной крови, биопсия кожи и печени плода).
5.3. Эпидемиология токсического действия
Неблагоприятное действие химических веществ на репродуктивную функцию человека, а также частоту и распространённость нарушений и дефектов развития плода и ребенка, вызываемых токсикантами, изучается и эпидемиологическими методами. В ходе подобных исследований количественные данные получают с помощью специальных приемов.
Таблица 9. Вероятность спонтанных абортов в различные сроки беременности