Что такое резекция 12 перстной кишки
При ее разрыве дефект ушивают двухрядным швом и забрюшинное пространство дренируют широким дренажом, выведенным через контрапертуру. В просвете кишки обязательно оставляют зонд для постоянной аспирации с целью ликвидации дуоденостаза.
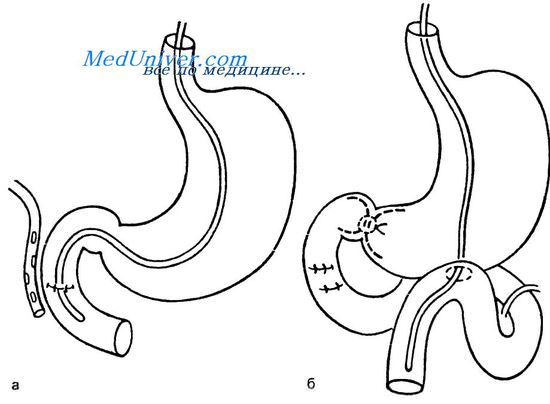
При обширном разрушении двенадцатиперстной кишки, когда ушивание раны невозможно, от кишки отсекают желудок, резецируют его дистальную половину, производят стволовую ваготомию и соединяют культю желудка анастомозом с мобилизованной по Ру тонкой кишкой на значительном расстоянии от связки Трейтца (длина отводящей петли 60—70 см предупреждает антиперистальтическое забрасывание пищевых масс в двенадцатиперстную кишку). Следует, однако, иметь в виду, что резекция желудка увеличивает продолжительность операции и ее травматизм, представляя при тяжелой сочетанной травме существенный риск, поэтому предпочтительнее использовать другие варианты выключения двенадцатиперстной кишки из пассажа желудочного содержимого, основанные на перекрытии просвета привратника. Для этого вскрывают просвет желудка в антральном отделе и, расширив крючками Фарабефа гастротомичсское отверстие, ушивают изнутри слизи стую оболочку привратника непрерывным швом из длительно нерассасывающегося материала (викрил, ПДС). Гастротоми ческое отверстие используют затем для наложения обходного гастроеюноанастомоза. Для декомпрессии кишечникка, а в по следующем для кормления проводят назоеюнальный зонд. Технические сложности ушивания привратника изнут ри привели к разработке методики блокирования привратника снаружи путем прошивания его аппаратом УО-40 или УО-60 с погружением линии скобок серо-серозными швами
Мы с 1985 г. используем собственную наиболее простую методику выключения двенадцатиперстной кишки которая за ключается в наложении на стенку желудка субсерозного кисет ного шва из толстого хромированного кетгута, викрила или полидиоксанона с проведением нити по задней стенке у головки поджелудочной железы, по передней — тотчас ниже пилорической вены.
Умеренным натяжением нити добиваемся перекрытия просвета привратника и нить завязываем. Линию лигирования прикрываем непрерывным серо-серозным швом викрилом 2/0 на атравматичной игле. Наложение обходного гастроеюноанастомоза не занимает много времени При крайне тяжелом состоянии пострадавшего наложение анастомоза может быть отложено на 2—3 сут. В таких случаях приходится ограничиваться наложением гастростомы или установкой назогастрального зонда для аспирации содержимого желудка. Пассаж содержимого желудка по двенадцатиперстной кишке восстанавливается через 2—3 мес после операции. Еслиазрыв локализуется не в самом начальном отделе двенадцатиперстной кишки, то культю ее ушивают, а в рану вводят силиконовый (лучше двухпросветный) дренаж и фиксируют его швом к краю раны кишки. Зону повреждения двенадцатиперстной кишки отгораживают от свободной брюшной полости марлевыми тампонами, которые вместе с дренажем выводят наружу через относительно узкую контрапертуру. Для утилизации пищеварительных соков, которые в послеоперационном периоде получают по дренажной трубке, находящейся в двенадцатиперстной кишке, проводят назоеюнальную интубацию или накладывают еюностому.
Тонкая кишка. Небольшие субсерозные гематомы после рассечения погружают в стенку кишки серозно-мышечными узловыми швами из нерассасывающегося материала в поперечном по отношению к ходу кишки направлении. Десерозированные участки ушивают такими же швами. Разрывы тонкой кишки после экономного иссечения имбибированных кровью краев ушивают в поперечном направлении двухрядными швами. При наличии на одной петле нескольких разрывов, при отрыве кишки от брыжейки на протяжении более 5 см, а также при сомнительной ее жизнеспособности после перевязки поврежденного сосуда необходима резекция петли с наложением анастомоза.
Анастомоз конец в конец является более надежным в плане кровоснабжения и более физиозогичным. Немаловажно и то, что на его наложение уходит меньше времени, чем на анастомоз бок в бок, так как при анастомозе конец в конец исключается ушивание обеих культей пересеченной кишки. Однако при несоответствии диаметров приводящей и отводящей петли анастомоз конец в конец выполнить технически сложнее, поэтому предпочтение в таких случаях следует отдавать анастомозу бок в бок.
Использование аппаратов для механического шва намного ускоряет выполнение резекции кишки и наложение анастомоза. При этом сначала бранши аппаратов НЖКА, GIA-55, GIA-60, Endo GIA-30 помещают внутрь фиксированных концов приводящей и отводящей петель и после их смыкания прошивают стенки этих отрезков четырьмя рядами скобок. Одновременно между двумя рядами происходит рассечение стенок кишки Операцию заканчивают наложением аппаратов типа УО-60 на открытые концы обеих петель и их прошиванием. Анастомоз выполняют очень быстро, хотя выглядит он достаточно грубо, но в критической ситуации аппаратный метод сберегает много времени и потому имеет все преимущества при тяжелой сочетанной травме.
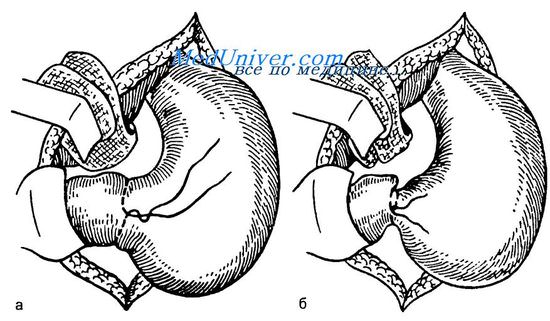
При резекции подвздошной кишки, если терминальный (отводящий) участок кишки не превышает 5—8 см, анастомоз в этом месте накладывать не следует из-за опасности нарушения кровоснабжения. Оставшийся короткий отводящий конец ушивают наглухо, а приводящий анастомозируют с восходящей ободочной кишкой по типу конец в бок.
В условиях распространенного гнойного перитонита кишку в месте повреждения пересекают вместе с брыжейкой и оба конца кишки выводят наружу через контрапертуры в передней брюшной стенке. Если при этом на одной петле имеется несколько разрывов, а также при отрыве гонкой кишки от брыжейки выполняют резекцию поврежденного участка кишки и оба конца кишки выводят наружу.
Органосохраняющие операции при опухолях поджелудочной железы и двенадцатиперстной кишки
Количество операций на этих органах увеличивается, но в подавляющем большинстве случаев вмешательства стандартны и сводятся к удалению правой половины поджелудочной железы с 12-перстной кишкой (панкреатодуоденальная резекция, ПДР, операция Уипла), или к удалению левой половины поджелудочной железы (дистальная резекция поджелудочной железы). Реже необходимо полное удаление поджелудочной железы. Эти операции могут быть направлены на радикальное удаление как собственно опухолей поджелудочной железы или двенадцатиперстной кишки (первичные опухоли), так и метастазов (дочерних опухолей) других злокачественных новообразований в поджелудочной железе (вторичные опухоли). Например, в поджелудочную железу чаще всего матастазирует рак почки.
При резекции значительной части поджелудочной железы или её полном удалении страдают обе её главные функции.
Избежать этих проблем и сохранить высокое качество жизни позволяют органосохраняющие операции.
При раке поджелудочной железы или двенадцатиперстной кишки, даже при опухоли небольших размеров, возможно ее скрытое распространение по лимфатическим путям, нервным волокнам, вдоль сосудов и в толще органа. Необходимость радикального удаления опухоли в этих случаях делает невозможными органосохраняющие вмешательства, и даже наоборот требует расширения границ резекции, в т.ч. за счет резекции сосудов. Такая же ситуация встречается при большинстве других злокачественных опухолей этих органов, если они достигают значительных размеров.
Имеющиеся в настоящее время данные о биологии ряда опухолей поджелудочной железы и двенадцатиперстной кишки позволяют с очень высокой долей вероятности утверждать, что некоторые кистозные опухоли поджелудочной железы являются облигатными предраками (т.е. станут злокачественными через некоторое время), но существует период и признаки, свидетельствующие о том, что озлокачествления нет с очень высокой долей вероятности. Их способность метастазировать (т.е. давать отсевы) в лимфатические узлы и другие органы чрезвычайно мала при малых размерах этих опухолей, например, нейроэндокринных, солидно-псевдопапиллярных, гастроинтестинальных стромальных опухолях, т.е. при опухолях с низким злокачественным потенциалом. Именно в этих случаях могут использоваться органосохраняющие вмешательства.
Сохранение двенадцатиперстной кишки при резекции или удалении поджелудочной железы.
Удаление или резекция двенадцатиперстной кишки с сохранением поджелудочной железы (с реплантацией желчного и панкреатического протоков или без).
Удаление центральной части поджелудочной железы с сохранением её головки и хвоста, а также двенадцатиперстной кишки.
Удаление головки и хвоста поджелудочной железы с сохранением её центральной части (с сохранением селезенки и двенадцатиперстной кишки или без).
Удаление тела и/или хвоста поджелудочной железы с сохранением селезенки.
Удаление тела и/или хвоста поджелудочной железы с сохранением селезенки и резекцией селезеночных сосудов.
Энуклеация – удаление небольших опухолей из ткани поджелудочной железы с оступом 1 мм и сохранением всей оставшейся ткани железы (чаще всего при инсулиномах).
Чаще всего органосохраняющие резекции выполняются при нейроэндокринных опухолях, тубуло-папиллярных, муцинозных цистаденомах, солидно-псевдопапиллярных опухолях, внутрипротоковых паппилярно-муцинозных опухолях поджелудочной железы и при некоторых других опухолях поджелудочной железы.
При некоторых опухолях двенадцатиперстной кишки – например, при гастроинтестинальных стромальных опухолях, при больших полипах, при виллёзных аденомах, при диффузном семейном полипозе, когда ещё нет озлокачествления, может выполняться панкреассохраняющая резекция двенадцатиперстной кишки. Т.е. может быть удалена либо верхняя часть двенадцатиперстной кишки, либо нижняя часть, либо вся двенадцатиперстная кишка целиком. При этом поджелудочная железа будет полностью сохранена.
Органосохраняющие операции выполняются при особой форме хронического панкреатита – кистозной дистрофии стенки двенадцатиперстной кишки, которую еще называют бороздчатым (groove pancreatitis) или парадуоденальным панкреатитом. Опыт хирургов Ильинской больницы в отношении системного успешного применения панкреассохраняющих резекций при этом заболевании был неоднократно представлен в специализированной печати, на международных конгрессах и в средствах массовой информации. В 2019 году исполнилось 10 лет с момента внедрения этой органосохраняющей операции, которая показала свою высокую надежность и эффективность.
Операции могут выполняться как традиционным, так и малоинвазивным (лапароскопически или с использованием хирургического робота) доступом. Все зависит от анатомических особенностей, расположения опухоли и оценки рисков. В любом случае отдаленные результаты органосохраняющих операций, выполненных по показаниям, не отличаются от обширных резекций в онкологическом смысле и принципиально лучше в отношении сохранения функций органов ЖКТ и пациента в целом. После операции пациент наблюдается вначале оперирующим хирургом, а затем возвращается под наблюдение семейного врача. Динамическое наблюдение, адаптация к новым специфическим особенностям жизни, выполнение послеоперационных профилактических мероприятий и т.д. – все это компетенция и ответственность врача общей практики.
К июлю 2020 года врачами Ильинской больницы проведено более 600 органосохраняющих операций на поджелудочной железе и двенадцатиперстной кишке.
Что такое резекция 12 перстной кишки
ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» РАМН
Российский онкологический научный центр им. Н.Н. Блохина РАМН, Москва
Российский онкологический научный центр им. Н.Н. Блохина РАМН, Москва
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина» Минздрава России, Москва, Россия
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина» Минздрава России, Москва, Россия
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина» Минздрава России, Москва, Россия; ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, Москва, Россия
Дистальная дуоденальная резекция: новый способ хирургического лечения при опухолевом поражении двенадцатиперстной кишки
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2019;(9): 5-12
Стилиди И. С., Неред С. Н., Никулин М. П., Егенов О. А., Петросян А. П., Архири П. П. Дистальная дуоденальная резекция: новый способ хирургического лечения при опухолевом поражении двенадцатиперстной кишки. Хирургия. Журнал им. Н.И. Пирогова. 2019;(9):5-12.
Stilidi I S, Nered S N, Nikulin M P, Egenov O A, Petrosyan A P, Arkhiri P P. Distal duodenectomy: a new option of surgical treatment for duodenal tumors. Khirurgiya. 2019;(9):5-12.
https://doi.org/10.17116/hirurgia20190915
ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» РАМН
Гастропанкреатодуоденальная резекция (ГПДР) — стандартный объем хирургического вмешательства при опухолевом поражении двенадцатиперстной кишки. Послеоперационные осложнения после ГПДР развиваются у 30—70% больных. По данным литературы, при неэпителиальных опухолях (за исключением лимфом) оправданы экономные операции. Обязательными требованиями к хирургическому вмешательству являются отрицательные края резекции и сохранение целостности капсулы опухоли. Цель исследования — оценка переносимости, безопасности и функциональности дистальной резекции двенадцатиперстной кишки, методика которой разработана в НМИЦ онкологии им. Н.Н. Блохина. Материал и методы. В НМИЦ онкологии им. Н.Н. Блохина с 2006 по 2018 г. выполнено 10 дистальных резекций двенадцатиперстной кишки по поводу ее опухолевого поражения, в том числе по поводу первичной опухоли у 8 больных, по поводу вторичной опухолевой инвазии извне у 2. В раннем послеоперационном периоде осложнения I—II степени (по классификации Clavien—Dindo) развились у 4 (40%) больных. Хирургическое осложнение II степени отмечено у 1 (10%) больного в виде панкреатического свища, который закрылся на фоне консервативного лечения. Несостоятельности культи двенадцатиперстной кишки и дуоденоеюноанастомоза, нарушения билиодинамики и/или стеноза анастомоза с замедлением эвакуации из желудка, а также летальных исходов во всех случаях не наблюдалось. Выводы. Дистальная резекция двенадцатиперстной кишки ассоциируется с низкой послеоперационной морбидностью, хорошей функциональностью и качеством жизни больных и является методом выбора у больных неэпителиальными и нейроэндокринными опухолями, а также при вторичной опухолевой инвазии двенадцатиперстной кишки извне.
ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» РАМН
Российский онкологический научный центр им. Н.Н. Блохина РАМН, Москва
Российский онкологический научный центр им. Н.Н. Блохина РАМН, Москва
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина» Минздрава России, Москва, Россия
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина» Минздрава России, Москва, Россия
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина» Минздрава России, Москва, Россия; ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, Москва, Россия
Первичные злокачественные новообразования тонкой кишки — относительно редко встречаемые опухоли, в структуре опухолей желудочно-кишечного тракта (ЖКТ) занимают всего 2% [1]. Чаще всего они локализуются в двенадцатиперстной кишке (ДПК) и составляют более 50% всех новообразований тонкой кишки и 0,3% всех опухолей ЖКТ.
Аденокарцинома — наиболее часто встречаемая около 80% — злокачественная опухоль ДПК [2, 3]. Реже встречаются саркомы, нейроэндокринные опухоли и лимфомы — 7, 5 и 3% соответственно. Среди сарком наиболее распространены гастроинтестинальные стромальные опухоли (ГИСО) — 4,5% всех злокачественных опухолей ДПК [4, 5].
Первичные злокачественные опухоли чаще всего локализуются в нисходящем отделе ДПК, реже — в нижнегоризонтальном сегменте и в дуоденоеюнальном переходе. В начальном отделе ДПК злокачественные опухоли встречаются крайне редко [6—8].
Гастропанкреатодуоденальная резекция (ГПДР) — стандартный объем хирургического вмешательства при опухолевом поражении ДПК. Однако послеоперационные осложнения после ГПДР развиваются у 30—70% больных [9]. Наиболее частым осложнением является несостоятельность панкреатоеюно- и билиодигестивного анастомозов — 30 и 9% соответственно. Послеоперационная летальность, по разным источникам [10—13], достигает 5%. Панкреатические свищи после ГПДР развиваются в 10—15% случаев [14].
По данным литературы [15—17], при неэпителиальных опухолях (за исключением лимфом) оправданы экономные операции при отсутствии элементов опухоли по линии резекции (R0). В результате выполнения экономных резекций значительно улучшаются непосредственные результаты и качество жизни больных. При этом показатели общей выживаемости не отличаются от результатов после расширенных хирургических вмешательств [15—17]. Обязательными требованиями к хирургическому вмешательству являются отрицательные края резекции и сохранение целостности капсулы опухоли [14, 16, 18].
Аналогичные сведения приводятся и в отношении больных с аденокарциномой ДПК. По данным многих авторов [15, 19, 20], сравнивших результаты хирургического лечения больных с аденокарциномой ДПК, различий в отдаленных результатах после экономных резекций и ГПДР не установлено.
Таким образом, экономные резекции оправданы у больных с неэпителиальными опухолями и рассматриваются как альтернатива расширенным операциям при аденокарциноме ДПК. К экономным резекциям ДПК относятся атипичная резекция, дистальная сегментарная резекция и панкреатосохранная тотальная дуоденэктомия.
Цель исследования — оценка переносимости, безопасности и функциональности дистальной резекции ДПК, методика которой разработана в НМИЦ онкологии им. Н.Н. Блохина.
Материал и методы
В НМИЦ онкологии им. Н.Н. Блохина с 2006 по 2018 г. выполнено 10 дистальных резекций (ДР) ДПК по поводу ее опухолевого поражения. Среди больных было 6 мужчин и 4 женщины. Средний возраст больных составил 56 лет (от 28 до 74 лет). У 8 больных ДР ДПК выполнили по поводу первичной опухоли ДПК (у 1 лейомиосаркома ДПК, у 7 ГИСО ДПК). У 3 пациентов с ГИСО ДПК проводили неоадъювантную терапию иматинибом в дозе 400 мг/сут с частичной регрессией опухоли, что позволило выполнить R0-резекции (без элементов опухолевого роста по краю резекции ДПК). В 2 случаях ДР ДПК выполнили по поводу опухолевой инвазии извне — рака поперечной ободочной кишки (1) и забрюшинной неорганной опухоли (1).
Технические хирургические аспекты
Для выполнения ДР ДПК применяют срединный лапаротомный доступ. После тщательной ревизии брюшной полости начинают мобилизацию ДПК по Кохеру с применением приема Cattell—Braasch. Пересекают передний листок брюшины от уровня гепатодуоденальной связки по ходу подпеченочного пространства, правого латерального канала до уровня купола слепой кишки. Далее разрез брюшины продолжают влево и краниально до уровня связки Трейтца. Острым и тупым путем проводят мобилизацию правой половины ободочной кишки и всей тонкой кишки с брыжейкой и отводят влево и кверху. В результате этого маневра ДПК обнажается на всем протяжении.
Технически ограничивающим критерием выполнения ДР ДПК являлось расстояние от макроскопически видимой границы опухолевой инфильтрации до дуоденального сосочка. При близком расположении опухолевой инфильтрации к дуоденальному сосочку необходимо выполнить интраоперационное эндоскопическое исследование для определения возможной границы резекции ДПК. Минимальное расстояние, при котором нами выполнена резекция ДПК (у больной ГИСО после неоадъювантной терапии иматинибом с выраженным положительным эффектом), составило 3 см (рис. 1). 
После определения проксимальной границы резекции ДПК приступают к мобилизации дуоденоеюнального перехода, для чего пересекают связку Трейтца. Для большей мобильности тощую кишку пересекали на расстоянии 10—15 см от связки Трейтца между первой и второй артериями тощей кишки с помощью сшивающего аппарата. Далее рассекали брыжейку начального отдела тощей кишки и дистальной части ДПК с перевязкой ветвей первой тонкокишечной артерии и сопровождающих их вен (рис. 2, 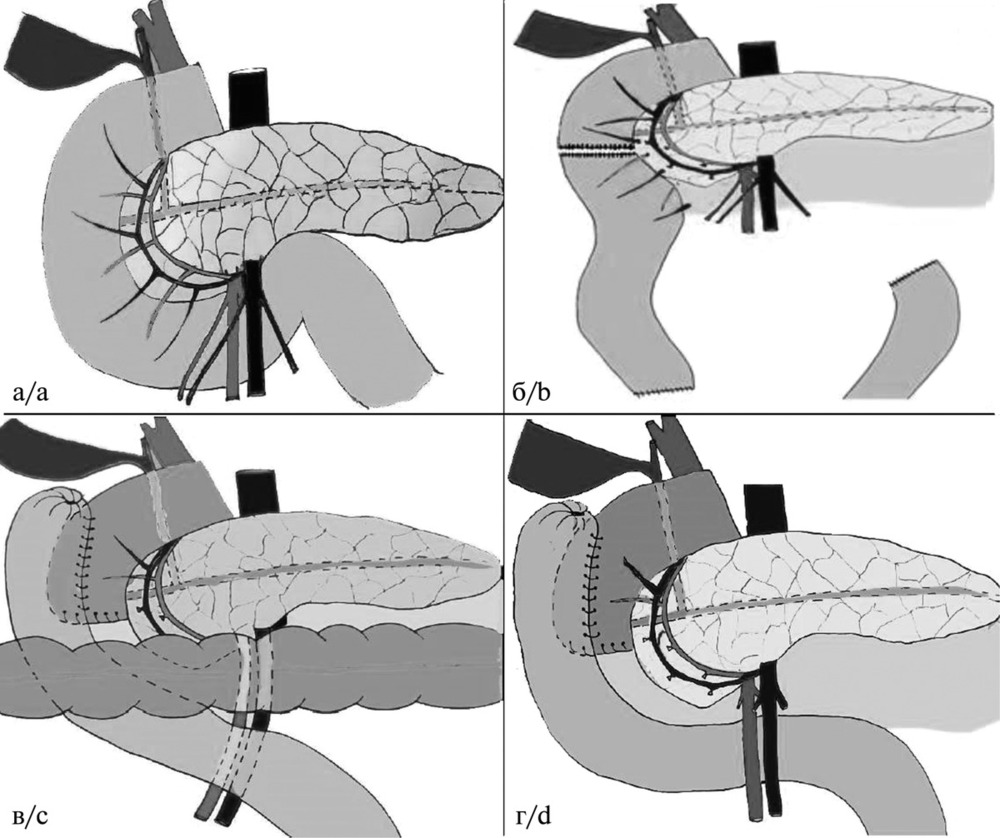

Следующий, наиболее деликатный этап операции — выделение нисходящей части и нижнего угла ДПК от ткани головки поджелудочной железы. Чтобы минимизировать ее повреждение, мобилизацию ДПК следует проводить с учетом анатомических особенностей кровоснабжения нисходящей и нижнегоризонтальной частей ДПК.
Эти отделы ДПК кровоснабжаются из верхней и нижней панкреатодуоденальных артерий. Каждая из них делится на 2 ствола — передний и задний, которые идут навстречу друг к другу, анастомозируют и формируют переднюю и заднюю артериальные дуги. Передняя и задняя артериальные панкреатодуоденальные дуги располагаются в борозде между головкой поджелудочной железы и ДПК. От передней артериальной дуги отходят короткие дуоденальные стволы, питающие переднюю стенку ДПК, от задней дуги — заднюю стенку (см. рис. 2, а). Венозный отток идет по венам, которые следуют по ходу одноименных артерий, вливаясь в систему воротной вены [21]. В процессе мобилизации дистального отдела нисходящей части и нижнего угла ДПК отдельно перевязывают передние и задние дуоденальные ветви панкреатодуоденальных сосудов с сохранением соответствующих сосудистых дуг (см. рис. 2, в).
Линейным степлерным аппаратом пересекали двенадцатиперстную кишку (см. рис. 2, в и 3, в). Механический шов культи тощей кишки погружали в кисетный шов. Культю нисходящей части ДПК с учетом ограниченного расстояния до дуоденального сосочка укрывали отдельными узловыми серозно-мышечными швами, что позволяет избежать образования инвагината больших размеров.
С нашей точки зрения и по данным литературы [22], наиболее надежным способом восстановления непрерывности кишечного тракта является выполнение дуоденоеюноанастомоза по типу бок в бок. Во всех 10 случаях сформированы анастомозы по типу бок-в-бок между передненаружной стенкой оставшейся нисходящей части ДПК и дистальной культей тощей кишки (см. рис. 2, в, г и 3, в, г). В 9 (90%) случаях сформированы изоперистальтические анастомозы, в 1 (10%) — антиперистальтический. Тощую кишку для формирования анастомоза лучше всего подводить позадиободочно (через окно в брыжейке поперечной ободочной кишки) и кпереди от верхнебрыжеечных сосудов. В некоторых случаях удобнее располагать тощую кишку позади верхнебрыжеечных сосудов (в ложе удаленной нижнегоризонтальной и вертикальной части ДПК). Такой вид реконструкции использован у 1 (10%) пациента.
Продолжительность операции в среднем составила 250 мин (150—300 мин), интраоперационная кровопотеря — 300 мл (150—600 мл) (см. таблицу). 
С учетом возможности развития в послеоперационном периоде панкреатического свища необходимо адекватное дренирование брюшной полости с обязательным подведением дренажа к крючковидному отростку и нижнему краю головки поджелудочной железы.
Послеоперационная морбидность оценена по классификации Clavien—Dindo [23]. В раннем послеоперационном периоде осложнения I—II степени развились у 4 (40%) больных. Осложнения II степени отмечены у 2 пациентов, из них у 1 в виде панкреатического свища, который закрылся на фоне консервативного лечения. У 1 пациента диагностирована полисегментарная пневмония.
На 5—7-е сутки всем пациентам выполнили дуоденографию с пероральным контрастированием с оценкой функции анастомоза. Несостоятельности швов культи ДПК и дуоденоеюноанастомоза не наблюдали.
В результате выполненных операций нарушения билиодинамики и/или стеноза дуоденоеюноанастомоза с замедлением эвакуации из желудка не отмечено. Летальных исходов в послеоперационном периоде не было. Послеоперационное пребывание в стационаре составило в среднем 13 сут (10—16 сут).
Обсуждение
На основании доступных мировых и собственных данных основным методом лечения больных опухолевым поражением ДПК (за исключением лимфомы) является хирургический. Актуальным вопросом является выбор объема хирургического вмешательства. Выполнение экономных резекций в первую очередь необходимо рассматривать у больных с неэпителиальными опухолями. Наиболее часто среди неэпителиальных опухолей ЖКТ (до 80% случаев) встречаются ГИСО [24], в 18—19% — лимфомы, в 1—2% — саркомы. При неэпителиальных опухолях ДПК отдаленные результаты после расширенных и экономных резекций не различаются, что оправдывает выполнение последних [4, 14, 25]. Более того, они ассоциируются с более низкой послеоперационной морбидностью, лучшими функциональностью и качеством жизни больных. Метастазирование в регионарных лимфатических узлах при ГИСО встречается редко (2—3%) и лимфаденэктомия выполняется только в случае наличия подозрительных лимфатических узлов [26]. Поэтому экономные резекции являются методом выбора у больных с неэпителиальными опухолями ДПК.
Экономные резекции рассматриваются как метод выбора и у больных с нейроэндокринной опухолью. Нейроэндокринная опухоль ДПК встречается редко и составляет всего 2—3% всех желудочно-кишечных нейроэндокринных опухолей [5]. В некоторых исследованиях [27, 28] экономные резекции ДПК приводили к хорошим отдаленным результатам даже при метастатическом поражении регионарных лимфатических узлов.
Нами оценены переносимость, безопасность и функциональность дистальной дуоденальной резекции у 10 пациентов с неэпителиальной опухолью ДПК или вторичной инвазией ДПК извне. Хирургические осложнения после ДР ДПК развились только у 1 (10%) пациента в виде панкреатического свища. В результате адекватного интраоперационного дренирования и послеоперационного консервативного лечения панкреатический свищ закрылся в течение 20 сут без дополнительных интервенционных манипуляций.
Несостоятельности швов культи ДПК и дуоденоеюноанастомоза, а также летальных исходов не отмечено ни в одном случае. У всех больных в ранние и отдаленные сроки отмечалась хорошая функциональность ЖКТ без нарушения эвакуации из желудка. В отдаленные сроки при динамическом наблюдении локального интрамурального или системного рецидива не наблюдали.
Послеоперационные непосредственные результаты и летальность после ГПДР несопоставимо выше, чем после экономной резекции. Несостоятельность панкреатоеюно- и билиодигестивного анастомозов развивается в 30 и 9% случаев соответственно [9], а панкреатический свищ — в 10—15% случаев, в то время как послеоперационная летальность достигает 5% [12, 13].
Актуальным и спорным остается проблема эффективности экономных резекций у больных аденокарциномой ДПК. Наиболее значимыми критериями, влияющими на прогноз для жизни и выздоровления этих больных, являются отрицательные края резекции (R0) и метастатическое поражение регионарных лимфатических узлов [29—31]. По данным многих авторов, достижение R0-резекции при выполнении экономной резекции не приводит к ухудшению отдаленных результатов. J. Cloyd и соавт. [32] на основании ретроспективного сравнительного анализа результатов хирургического лечения (ГПДР и ДР ДПК) 1611 пациентов с аденокарциномой ДПК показали, что несмотря на то что при ГПДР удаляли большее количество лимфатических узлов, показатели общей выживаемости не различались. С учетом сопоставимой общей выживаемости, лучших непосредственных результатов и качества жизни больных экономные резекции можно рассматривать как альтернативу и у больных с аденокарциномой ДПК.
Таким образом, ДР ДПК ассоциируются с низкой послеоперационной морбидностью, хорошей функциональностью и удовлетворительным качеством жизни больных, а также с меньшей продолжительностью пребывания в стационаре по сравнению с расширенными операциями. С учетом отсутствия различий в отдаленных результатах экономная резекция ДПК является методом выбора у больных неэпителиальными (за исключением лимфомы), нейроэндокринными опухолями и вторичной опухолевой инвазией ДПК извне. Проблема эффективности экономной резекции при аденокарциономе ДПК в настоящее время не решена. По данным многих авторов, при аденокарциноме ДПК отдаленные результаты не различаются как после расширенных, так и после экономных резекций, однако рандомизированных исследований, подтверждающих данный факт, пока нет.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflict of interest.




