Что такое секреторный иммуноглобулин а
Известно, что степень защиты от локальных вирусных инфекций респираторного и желудочно-кишечного трактов прежде всего зависит от содержания в организме специфического секреторного IgA, а не от наличия сывороточного IgG к энтеропатогенным или пневмотропным вирусам.
Стабильная структура, выраженный аффинитет к поверхности слизистых оболочек, преобладающее содержание в секрете молочной железы обусловливают биологическую роль секреторного IgA в защите организма от неблагоприятного воздействия различных патогенных агентов, в том числе вирусов.
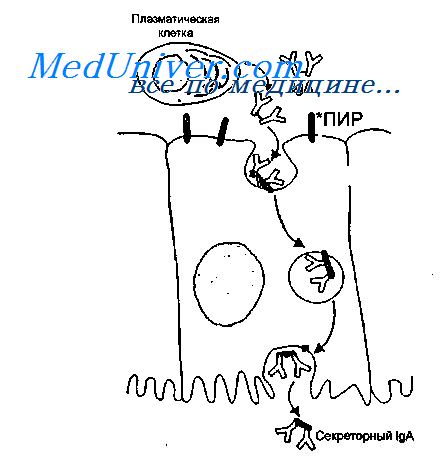
IgA синтезируется в димерной форме в клетках lamina propria и после связывания с иммуноглобулиновым рецептором, синтезированным в эпителиальных клетках, транспортируется на поверхность слизистой оболочки. В момент выхода IgA в просвет кишечника рецептор частично расщепляется, в результате чего в составе IgA остается фрагмент рецептора, который называют секреторным компонентом.
Таким образом, секреторный IgA является продуктом кооперации двух типов клеток — плазматических и эпителиальных.
Секреторный IgA образуется не только в димерной, но и в тетрамерной форме, что усиливает его вируснейтрализующую способность. Секреторный компонент предохраняет IgA от расщепления протеолитическими ферментами, что обусловливает его значительные преимущества перед антителами других классов. Секреторный IgA нейтрализует вирус не только в просвете кишечника, но и при транспортировке его внутрь клетки. Димер IgA может нейтрализовать вирус в подслизистой оболочке кишечника, а затем, связавшись с рецептором, транспортировать его в просвет кишечника.
Димерные иммуноглобулины класса A (US IgA), соединенные посредством j-цепи в единую структуру с секреторным компонентом, представляют собой уникальный пример эволюционной адаптации иммуноглобулинов на слизистых покровах для эффективного функционирования в условиях постоянного воздействия антигенов различной природы.
Исходя из способности к локальному синтезу молекул секреторного компонента, а также димерной формы IgA-местно расположенными плазматическими клетками, ткани слизистых покровов можно разделить на три основных класса.
В слизистых оболочках индуктивная и продуктивная фазы гуморального иммунного ответа разобщены пространственно в большей степени, чем в других отделах иммунной системы.
Клеточные и гуморальные превращения, связанные с появлением IgA во внешних секретах, представлены на рисунке.
В молоко и, по-видимому, в другие внешние секреты молекулы IgA поступают из двух главных источников. Большая часть IgA, выделяемого со слюной, секретами слезной и молочной желез, а также пищеварительного и респираторного трактов, образуется плазматическими клетками. Однако IgA, обнаруживаемые в различных внешних секретах, могут иметь и системное происхождение. Продуцируясь клетками слизистых оболочек одних органов, они поступают в кровь и переносятся в слизистые покровы других органов.
Антиген после проникновения внутрь пейеровой бляшки активирует Т- и В-лимфоциты, которые по лимфатическому протоку поступают в мезентериальный лимфатический узел, а затем в кровь, селезенку, снова в кровь и селективно локализуются в лимфатических образованиях всех слизистых оболочек и экзокринных секреторных железах — молочных, слюнных и слезных. При этом Т-лимфоциты локализуются преимущественно между эпителиальными клетками слизистой оболочки, обеспечивая клеточный иммунный ответ, а В-лимфоциты — в lamina propria, где они дифференцируются в плазматические клетки и синтезируют IgA.
Около 90% плазматических клеток в lamina propria продуцируют IgA, в то время как в лимфатических узлах доля таких клеток составляет всего 2—5%.
Уникальна в этом отношении роль печени. Имеются убедительные данные, свидетельствующие о том, что гепатоциты избирательно связывают и в последующем транспортируют IgA в желчь, тем самым усиливая систему секреторного IgA кишечника.
Секреторные иммуноглобулины А – «главная скрипка» мукозального иммунитета
В полости рта и ротоглотке наибольшее протективное значение имеют sIgA слюны, а в носовых ходах и носоглотке – sIgA назального секрета.
Доминирование секреторного иммуноглобулина А среди других антител в слизистой оболочке дыхательных путей и ротоглотки
В полости рта и ротоглотке наибольшее протективное значение имеют sIgA слюны, а в носовых ходах и носоглотке – sIgA назального секрета. Помогают этим антителам в нейтрализации вирусов и бактерий секреторные IgM (sIgM), но их защитное значение существенно ниже.
Помимо sIgA и sIgM, в верхних отделах дыхательных путей и ротоглотке обнаруживаются в небольших количествах и все другие известные изотипы Ig. Появление IgG и мономерного («сывороточного») IgA в слюне и назальном секрете обусловлено транссудацией этих молекул из плазмы крови. При патологических (например, воспалительных) процессах увеличивается транссудация IgG, мономерного IgA и более крупных полимерных молекул IgM. В секретах слизистых оболочек дыхательных путей выявляют еще и IgD, который тоже участвует в противоинфекционном ответе.
Особенности выработки sIgA и sIgM
Вначале плазматические клетки слизистых оболочек синтезируют димерный IgA, в котором два мономера IgA соединены между собой J-цепью. После этого димерный IgA захватывается рецептором к полимерным иммуноглобулинам на базальной поверхности эпителиальных клеток и подвергаются транспорту к апикальной поверхности эпителиоцитов. Здесь происходит распад транспортирующего рецептора, в результате которого внеклеточная часть этого рецептора (так называемый «секреторный компонент») остается связанной с димерным IgA, который высвобождается в окружающую среду (слюну, слизь, другие биологические жидкости). Именно такой димерный IgA, связанный с секреторным компонентом, называют sIgA.
Как уже упоминалось, существуют еще и секреторный IgM (sIgM). Выработка sIgM напоминает таковую sIgA. Все начинается с синтеза плазматическими клетками в слизистой оболочке пентамерного IgM, который захватывается рецептором к полимерным иммуноглобулинам на базальной поверхности эпителиальных клеток и подвергаются трансэпителиальному транспорту. На апикальной поверхности эпителиоцитов пентамерный IgM вместе с секреторным компонентом высвобождается во внешнюю среду, превращаясь в sIgM.
Секреторные компоненты в составе sIgA и sIgM стабилизируют соответственно димерную или пентамерную структуру этих Ig и обеспечивают их длительное функционирование в биологических жидкостях.
Где происходит индукция выработки sIgA в слюне и назальном секрете?
Появление sIgA в слюне и назальном секрете происходит как следствие первичного контакта с антигенами патогенов в разных индуктивных зонах в верхних отделах респираторного и пищеварительного трактов. Главными индуктивными зонами при этом являются небные и носоглоточные миндалины, а также протоки слюнных (особенно малых, поднижечелюстных и подъязычных) желез, открытые для прямого воздействия антигенов. К индуктивным зонам относятся и другие участки слизистой оболочки полости рта, глотки, верхних и нижних дыхательных путей.
Все перечисленные индуктивные зоны доступны для стимулирующего действия топических бактериальных лизатов ИРС®19 и Имудон®.
Еще одной индуктивной зоной, антигенная стимуляция которой может привести к выработке антител в слюне и дыхательных путях, является лимфоидная ткань, ассоциированная с кишечником (Gut-Associated Lymphoid Tissue – GALT). Эта зона также доступна для действия топических бактериальных лизатов, компоненты которых неминуемо попадают в желудочно-кишечный тракт в результате проглатывания.
При раннем назначении топических бактериальных лизатов адаптивные антибактериальные механизмы (локальная продукция sIgA) включаются как раз тогда (4–5-е сутки), когда наиболее высок риск развития вторичной бактериальной инфекции.
Таким образом, ИРС®19 и Имудон® не только предотвращают развитие вторичных бактериальных осложнений вирусной инфекции, но и неспецифически усиливают противовирусную и антибактериальную защиту уже в первые часы терапевтического применения. Препараты обладают целым рядом фармакологических свойств, которые принципиально отличают их от иммуностимуляторов с системным действием, связанных со сложными маршрутами миграции иммунокомпетентных клеток. ИРС®19 и Имудон® действуют нацелено на стимуляцию противоинфекционной защиты в месте их первичного введения в организм т.е. во входных воротах для болезнетворных вирусов и бактерий и арене ключевых патогенетических событий.
Материал разработан при поддержке компании abbott в целях повышения осведомлённости пациентов о состоянии здоровья. информация в материале не заменяет консультацию специалиста здравоохранения.обратитесь к лечащему врачу.
Что такое секреторный иммуноглобулин а
Одним из иммуноглобулинов играющим важную роль в желудочно-кишечном тракте является секреторный иммуноглобулин А (sIgA) [1,2,3]. Секреторный иммуноглобулин А непосредственно обеспечивая «первую линию защиты» слизистой оболочки кишечника от воздействия чужеродных антигенов, является «главным чистильщиком» кишечника. По данным Маковецкой А.К. и соавт., (2005) снижение sIgА может указывать на недостаточность функции местного иммунитета, а его повышенное количество – на дисбаланс в иммунной системе [4]. Вместе с тем, в ряде исследований показано, что при снижении местного иммунитета, и в частности sIgA, формируется хроническая патология. В исследовании Calvo M. с соавт. (1990) показано, что у здоровых детей, имеющих нормальный уровень sIgA, риск развития хронической легочной патологии, в том числе и бронхиальной астмы, составляет 46 %, а при низком уровне sIgA повышается до 86 % [1]. У часто болеющих детей с бронхиальной астмой отмечается снижение sIgA в секрете ротоглотки [5]. Принимая ограниченность результатов исследований по изучению роли sIgA при лямблиозной инфекции мы считаем актуальным изучение гуморального иммунитета в кишечнике.
Цель исследования – изучить особенности клинической картины и содержание секреторного иммуноглобулина А при лямблиозе.
Материалы и методы исследования
Основную группу составили 87 пациентов в возрасте от 18 до 60 лет, группу сравнения составили 22 пациента сопоставимые по поло-возрастному признаку и наличию сопутствующей патологии.
Диагноз был верифицирован на основании клинико-анамнестических и лабораторных (копроскопия кала, результат дуоденального зондирования, ПЦР-диагностика). Вегетативные формы лямблий были обнаружены в дуоденальном содержимом и жидких испражнениях, цистированные формы – в нативных фекалиях в течение 2-х часов после сбора анализа.).
Кроме того, у всех пациентов подтвержден лямблиоз кишечника, преимущественно с многолетним рецидивирующим течением
У обследованных нами больных выявлены сопутствующие заболевания, среди которых преобладали: пищевая аллергия на облигатные аллергены, хроническая патология со стороны ЛОР-органов (хронический тонзиллит, аденоидит), нормохромная анемия легкой степени. По совокупности клинико-анамнестических данных, результатов объективного осмотра и копрологического исследования, у всех пациентов имелись проявления дисбактериоза кишечника в той или иной степени.
С целью изучения состояния гуморального иммунитета в кишечнике нами определен его основной маркер – секреторный иммуноглобулин А (sIgA) в кале.
Для исследования иммуноглобулина А в копрофильтрате использован твердофазный хромогенный иммуноферментный анализ с использованием коммерческого набора производства «Вектор-Бест» на оборудовании Bio-Rad в соответствии с инструкциями, прилагаемыми к наборам в формате 96- луночного планшета.
Статистическую обработку результатов исследования проводили с использованием метода математической статистики. Достоверность различий средних величин оценивали с помощью критериев Стьюдента.
Результаты исследования и их обсуждение
Клиническая картина лямблиоза среди обследованных пациентов характеризовалась различными симптомами. У значительной части пациентов отмечались проявления болевого абдоминального синдрома. Локализация боли имела различное расположение, но чаще она располагалась в правом подреберье, в точке проекции желчного пузыря и в области выше пупка. На отсутствие боли указывало 12,5±9,6 (P
Что такое секреторный иммуноглобулин а
Антитела класса IgA, основной функцией которых является местная гуморальная защита слизистых оболочек.
Иммуноглобулины (антитела) класса А.
Синонимы английские
Immunoglobulin A; IgA, total, Serum.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Иммуноглобулины класса А – гликопротеины, которые синтезируются в основном плазматическими клетками слизистых оболочек в ответ на местное воздействие антигена.
В организме человека IgA существует в двух формах – сывороточной и секреторной. Время их полужизни – 6-7 суток. Секреторный IgA обладает димерной структурой и устойчив к воздействию ферментов благодаря особенностям строения. Секреторный IgA находится в слезах, поте, слюне, молоке и молозиве, секретах бронхов и желудочно-кишечного тракта и защищает слизистые оболочки от инфекционных агентов. 80-90 % циркулирующих в крови IgA состоят из сывороточной мономерной формы данного класса антител. IgA входят во фракцию гамма-глобулинов и составляют 10-15 % от всех иммуноглобулинов крови.
Антитела класса IgA являются важным фактором местной защиты слизистых оболочек. Они связываются с микроорганизмами и предотвращают их проникновение с внешних поверхностей вглубь тканей, усиливают фагоцитоз антигенов путем активации комплемента по альтернативному пути. Достаточный уровень IgA в организме препятствует развитию IgЕ-зависимых аллергических реакций. IgA не проникают через плаценту, но поступают в организм ребенка с молоком матери при кормлении.
Селективный дефицит IgA является одним из наиболее распространенных иммунодефицитов в популяции. Частота – 1 случай на 400-700 человек. Данная патология часто протекает бессимптомно. Дефицит IgA может проявиться аллергическими заболеваниями, рецидивирующими респираторными или желудочно-кишечными инфекциями, нередко ассоциируется с аутоиммунной патологией (сахарным диабетом, системной красной волчанкой, ревматоидным артритом, пернициозной анемией). Дефицит IgA иногда сочетается с недостаточным уровнем IgG-2 и IgG-4, что приводит к более выраженным клиническим признакам иммунодефицита.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Возраст
Референсные значения
Причины понижения уровня IgА в сыворотке и состояния, ассоциированные с дефицитом данного класса антител:
Что может влиять на результат?
Факторы, повышающие уровни иммуноглобулинов в крови:
Факторы, снижающие уровни IgA в крови:
Кто назначает исследование?
Иммунолог, инфекционист, гематолог, онколог, ревматолог.
Что такое секреторный иммуноглобулин а
Ротовая полость обладает как твердой (зубы), так и мягкой (слизистая) тканями. Зубы можно описать как неизменяемую твердую поверхность, которая имеет много разных мест для адгезии и колонизации бактерий ниже (сабгингивиал) и выше (супрагингивиал) гингивиального края. Напротив, слизистая оболочка характеризуется сплошной (непрерывной) десквамацией ее поверхностных эпителиальных клеток, которые способствуют быстрой элиминации адгезирующих бактерий. Слизистая оболочка полости рта, которая покрывает щеки, язык, десны, небо, а также полости рта, в зависимости от ее анатомической локализации существенно отличается. Например, эпителиальные клетки в слизистой могут быть кератинизированными (небо), некератинизированными (гингивиальная щель). Язык с его сосковидной поверхностью благоприятствует колонизации микроорганизмов на отдельных местах, при этом сосковидные структуры предохраняют от механического удаления бактерий.
Гингивиальная жидкость является транссудат экссудатом, происходящим из плазмы, которая проходит через гингивиа (соединяющие эпителии) в гингивиальную щель и далее течет вдоль зубов. Диффузия гингивиальной жидкости у здоровых десен происходит медленно, а в период воспаления она увеличивается. Состав гингивиальной жидкости одинаков с таковой у плазмы: он содержит протеины, альбумины, лейкоциты, иммуноглобулины, а также комплемент [4,5,6].
Слюна помогает поддерживать целостность зубов, обеспечивая такими ионами, как кальций фосфат, магнезиум, фтор. Также в составе слюны содержатся иммуноглобулины (А, М, G). Между микробной флорой челюстно-лицевой области и факторами организма существует постоянное равновесие. Однако эти факторы часто подвергаются атаке как вследствие размножения и ускоренного развития микробов (зубные отложения), так и из-за ослабления самих факторов общей и особенно местной иммунной защиты.
Специфическим иммунитетом является способность микроорганизма избирательно реагировать на попавшие в него антигены. Главным фактором специфической антимикробной защиты являются иммуноглобулины.
Секреторный IgA представляет собой один из основных иммуноглобулиновых изотипов слюны и всех других секретов слизистых оболочек организма. SIgA состоит из двух пар полипептидных цепей, соединенных дисульфидными связями.
Секреторный IgA устойчив к действию различных протеолитических ферментов. Существует предположение, что чувствительные к действию ферментов пептидные связи в молекулах секреторного IgA закрыты вследствие присоединения секреторного компонента. Эта устойчивость к протеолизу имеет важное биологическое значение. SIgA секретируются плазмоцитами подслизистого слоя миндалин и клетками Lamino propra. В слюне содержится гораздо больше секреторного IgA, чем других иммуноглобулинов: например, в слюне, выделяемой околоушными железами, соотношение IgA/IgG в 400 раз превышает таковое в сыворотке крови.
Одним из важных вопросов, имеющих отношение к роли секреторного IgA в микробной экологии полости рта, и в частности, патологии ротовой полости, является вопрос о влиянии этих иммуноглобулинов на местную микрофлору. Несмотря на присутствие высокого уровня секреторного IgA в слюне, местная бактериальная микрофлора все еще персистирует в полости рта. Отсюда можно предположить, что выжившей в полости рта микробиоте свойственна пониженная чувствительность к секретору IgA, а также способность избегать действия иммунных механизмов. По мнению некоторых авторов [2, 4], аутохтонные бактерии не иммуногенны в организме хозяина, и поэтому эти микроорганизмы в период продолжительной эволюционной адаптации достигли симбиоза с организмом хозяина. Вместе с тем другие микроорганизмы резисдентной микробиоты, которые потенциально патогенны, могут индуцировать протективную ответную реакцию и элиминироваться из организма или же сохраняться в небольшом количестве при нормальных условиях. Некоторые экспериментальные исследования подтверждают гипотезу о том, что иммунная система относительно толерантна к аутохтанным микроорганизмам [7, 8, 9, 10]. Правомерно считать, что подобная толерантность может быть результатом клональной элиминации (гибель клеток), клональной энергии (функциональной инактивации клеток без их гибели) или активной супрессии антиген-реактивных В- и Т-клеток. Предполагается также, что местные резисдентные бактерии со своими поверхностными антигенами, имея сходство с тканевыми хозяина или покрываясь молекулами тканевой природы, могут не восприниматься иммунной системой как чужеродные [9, 10].
Изучению формирования SIgA антительного ответа к оральной микрофлоре у людей посвящено много работ. Так, Смит и коллеги подчеркивают, что появление IgA антител к стрептококкам (S.salivaris и S.mitis) у новорожденных и детей старшего возраста непосредственно коррелирует с колонизацией этими бактериями полости рта у детей. При этом показано, что секреторные антитела, продуцируемые иммунной системой слизистых полости рта против стрептококков в период колонизации слизистой ротовой полости, могут повлиять на степень и продолжительность колонизации, способствуя при этом специфической элиминации этих микроорганизмов [11].
Можно предположить, что эти естественно обнаруживаемые SIgA антитела могут играть важную роль в гомеостазе резидентной микрофлоры полости рта, а также в профилактике кариесов и периодонтальных, а также челюстно-лицевых заболеваний (актиномикоз, флегмоны, абсцессы и др.). Эти антитела были определены к S.mutans, A.actinomysetemcomitans и Porphyromonas gingivalis, которые строго ассоциировали с патологическими процессами в ротовой полости. Также известно, что при возникновении болезней ротовой полости и челюстно-лицевой области (особенно актиномикотических патологических) немаловажную роль играют именно актиномицеты, такие, как Act.israelii, Act.odontolyticus, и так называемые «сопутствующие микроорганизмы» (бактерии и грибы) [16, 17, 18, 19, 20]. Надо отметить, что у больных, особенно с актиномикотическими патологиями, у которых были выделены актиномицеты, отмечаются существенные изменения состояния иммунных механизмов защиты ротовой полости, проявляющиеся местными изменениями, особенно в составе слюны SIgA. У больных, у которых выделены актиномицеты, концентрация SIgA относительно понижена [17].
Таким образом, надо отметить, что в возникновении инфекционной патологии полости рта и челюстно-лицевой области значительную роль в местной иммунной защите слизистых оболочек играет концентрация секреторного IgA.